Tecnologia do DNA recombinante Engenharia Gentica DNA Recombinante

Tecnologia do DNA recombinante (Engenharia Genética)

DNA Recombinante Molécula de DNA construída com segmentos de DNA de diferentes origens.

Processo básico para estudar o DNA Separação do material genético dos outros constituintes da célula Propriedades do DNA que viabilizam o estudo da molécula • Desnaturação -separação temporária das pontes de hidrogênio -aquecimento ou ação química • Renaturação -processo inverso a desnaturação
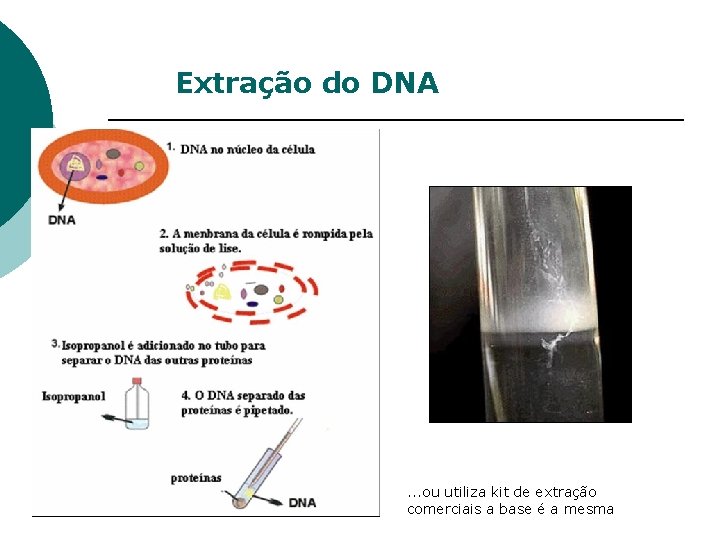
Extração do DNA . . . ou utiliza kit de extração comerciais a base é a mesma

Usos da tecnologia do DNA recombinante Pesquisa básica – isolar um gene particular, parte de um gene ou região do genoma Análise de mutações no diagnóstico doenças, ciência forense. . . Aumentar a eficiência de produção de drogas e enzimas de interesse (produção de vacinas, proteínas. . . em larga escala) Modificação de organismos vivos de maneira a expressarem uma característica em particular (produção de plantas e animais geneticamente modificados) Correção de defeitos genéticos (TERAPIA GENICA)

A construção da molécula de DNA recombinante -enzimas -DNA “doador” -vetores
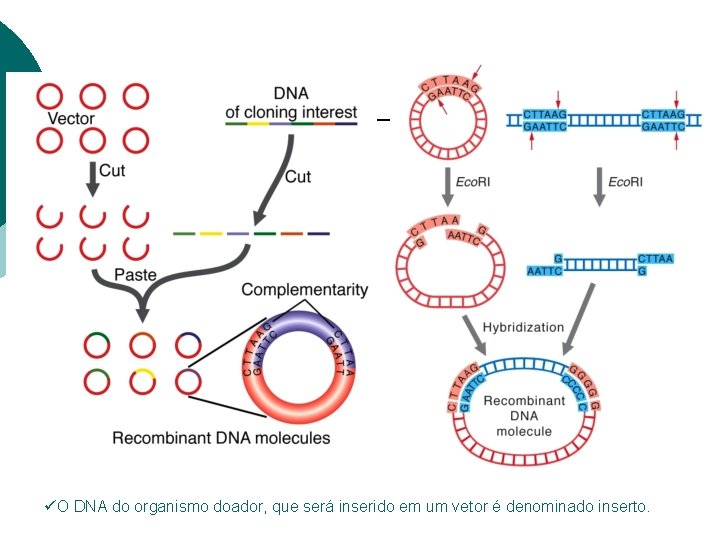
üO DNA do organismo doador, que será inserido em um vetor é denominado inserto.

ENZIMAS DE RESTRIÇÃO • São endonucleases (tipo I, II ou III) • Isoladas de bactérias (mecanismo de defesa de bactérias) • ~400 tipos • Reconhecem sequências específicas de 4 a 8 bases • Geram fragmentos de restrição de extremidade cega ou coesivas • Frequência de corte depende da composição da sequência

Enzimas de Restrição Tipo II (mais utilizadas) ü reconhecem uma sequência específica e cortam precisamente as duas fitas de DNA ü sequências que possuam simetria inversa – sequência palindrômica (leitura sentido 5’ 3’) Ex: produção de extremidades coesivas (overhangs) 5' GAATT C 3' 3' C TTAAG 5' Eco. RI 5' G AATTC 3' 3' CTTAA G 5’ Ex: produção de extremidades cegas (blunt end) 5’ GGCC 3’ Hae. III 5’ GG CC 3’ 3’ CCGG 5’ 3’ CC GG 5’

Nomenclatura de enzimas de restrição

Vetores de clonagem • Transportadores de DNA • Replicação independente – origem de replicação • Presença de um único sítio de restrição • Presença de um marcador de seleção Vetores de expressão • Contém todos os requisitos de um vetor de clonagem, além de conter requisitos para expressão, como por exemplo um promotor.

Capacidade de inserto dos vetores VETOR TAMANHO MÁXIMO DO INSERTO (Kb) Plasmídeo até 10 Fago 20 Cosmídeo 30 – 45 PAC 130 -150 BAC até 300 YAC 300 - >1500

Plasmídios DNA extra cromossômico em forma circular Poucos genes Região polylinker (múltiplos cortes) Presença de genes de resistência a antibióticos

Clonagem CLONAGEM DO DNA “IN VIVO” • Produção dos fragmentos de DNA • Inserção do fragmento de DNA em estudo no vetor • Transformação • Seleção
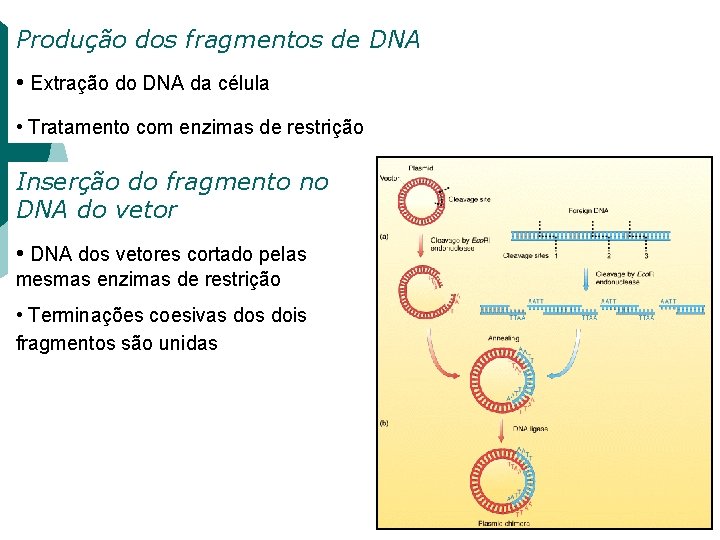
Produção dos fragmentos de DNA • Extração do DNA da célula • Tratamento com enzimas de restrição Inserção do fragmento no DNA do vetor • DNA dos vetores cortado pelas mesmas enzimas de restrição • Terminações coesivas dois fragmentos são unidas
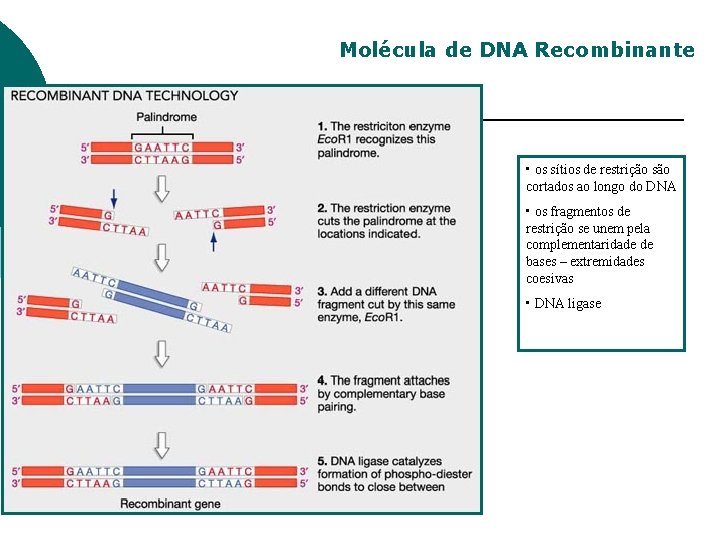
Molécula de DNA Recombinante • os sítios de restrição são cortados ao longo do DNA • os fragmentos de restrição se unem pela complementaridade de bases – extremidades coesivas • DNA ligase
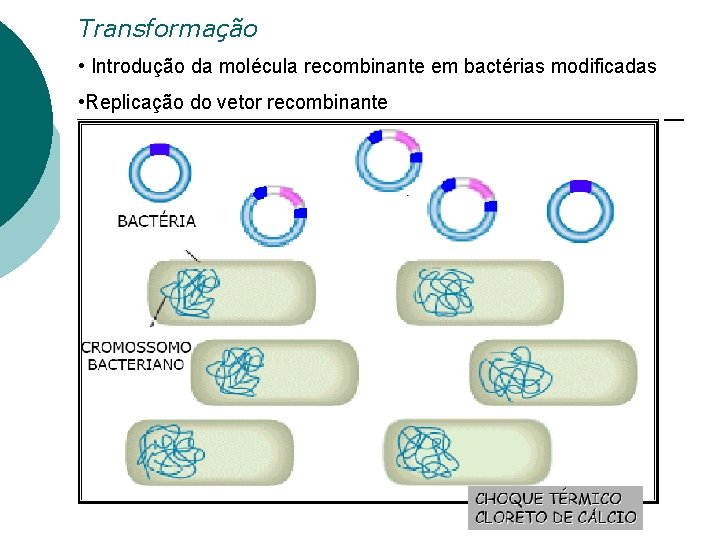
Transformação • Introdução da molécula recombinante em bactérias modificadas • Replicação do vetor recombinante
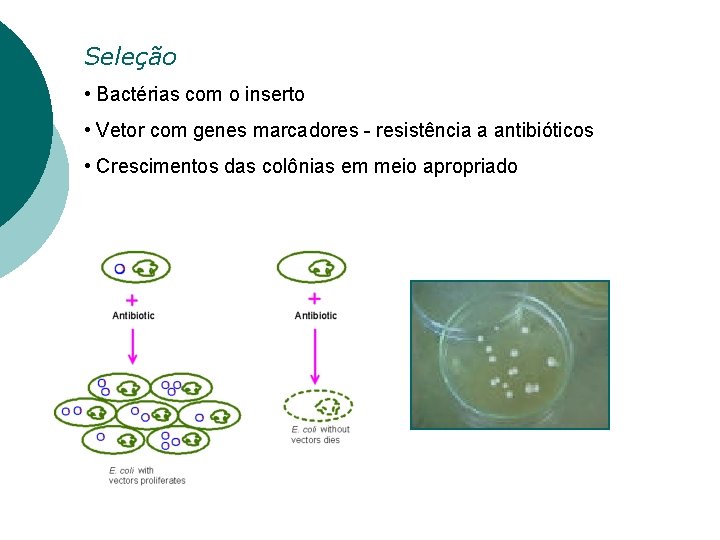
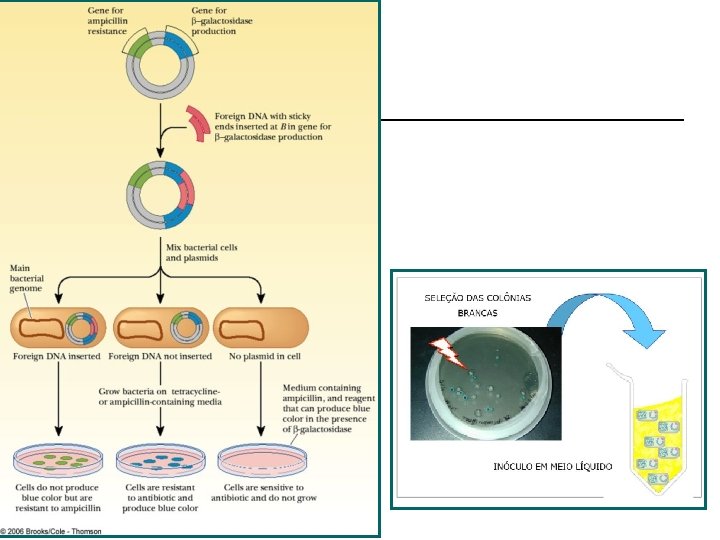
Seleção • Bactérias com o inserto • Vetor com genes marcadores - resistência a antibióticos • Crescimentos das colônias em meio apropriado

AMPLIFICAÇÃO DO DNA IN VITRO PCR

PCR (polimorfism chain reaction) ou reação em cadeia da polimerase Desenvolvida nos anos 80 por Kary Mullis Amplificação enzimática in vitro de uma sequência específica de DNA O processo pode ser utilizado para amplificar sequências de DNA de qualquer fonte: bacteriana, viral, vegetal ou animal São utilizados dois “primers” ou inicadores (pequenas seqüências de nucleotídeos sintéticos) - Isso delimita o segmento amplificado e determina o crescimento exponencial do número de moléculas de DNA A dupla fita é separada e serve como molde para a síntese das fitas complementares Uma enzima DNA polimerase termoestável catalisa a adição de nucleotídeos de acordo com a fita molde A polimerização segue a orientação 5’ > 3’
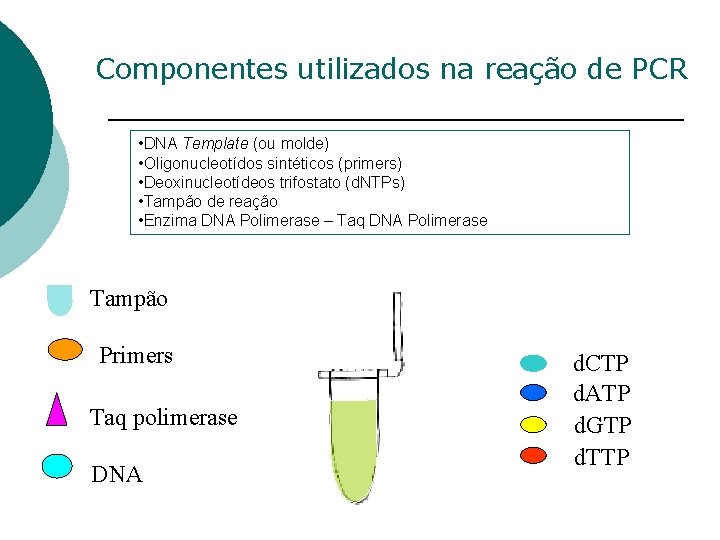
Componentes utilizados na reação de PCR • DNA Template (ou molde) • Oligonucleotídos sintéticos (primers) • Deoxinucleotídeos trifostato (d. NTPs) • Tampão de reação • Enzima DNA Polimerase – Taq DNA Polimerase Tampão Primers Taq polimerase DNA d. CTP d. ATP d. GTP d. TTP

Algumas condições tem extrema importância no sucesso da reação de PCR: • A solução tem que ser totalmente livre de DNases • Condições específicas de concentrações de sais e p. H devem ser obedecidas • Ciclos específicos de temperatura devem ser obedecidos • Os Primers utilizados tem que ser complementares a região alvo que se deseja amplificar • A enzima DNA polimerase utilizada deve ser termoestável

Os primers são utilizados na reação de PCR para permitir a ação da enzima DNA polimerase e devem obedecer alguns princípios que garantam sua eficiência: • Preferencialmente devem ter de 20 a 35 nucleotídeos • Preferencialmente devem ser ricos em bases G-C • Não podem ser complementares entre si

Protocolo Padrão de Amplificação Etapa Etapa 1. 2. 3. 4. 5. 6. 1 minuto a 92°C 30 segundos a 92°C -Denaturação 30 segundos a 55°C -Anelamento 60 segundos a 72°C -Extensão 10 minutos a 72°C 4 -12°C 30 ciclos
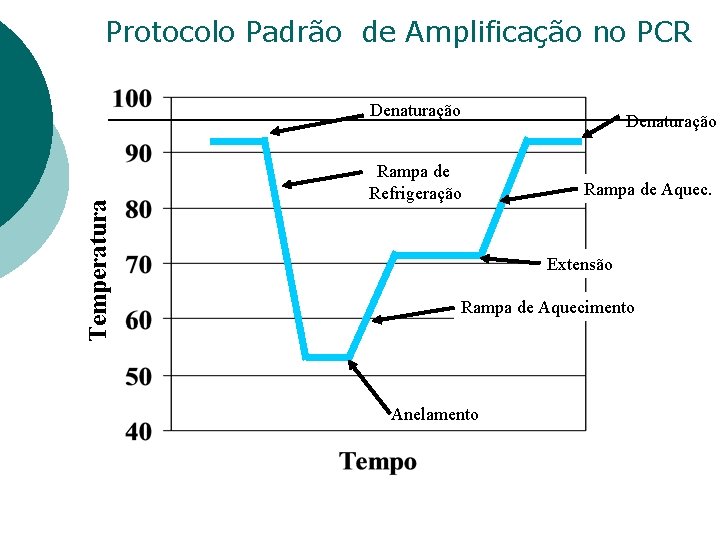
Protocolo Padrão de Amplificação no PCR Temperatura Denaturação Rampa de Refrigeração Rampa de Aquec. Extensão Rampa de Aquecimento Anelamento

Como é a reação de amplificação de DNA? PCR — Reação em Cadeia da Polimerase C T G T T CGAT G C TT A T C CC A G C T G A G T A T C C A AGCT A C G AA T A G GG T C A CAT A GG
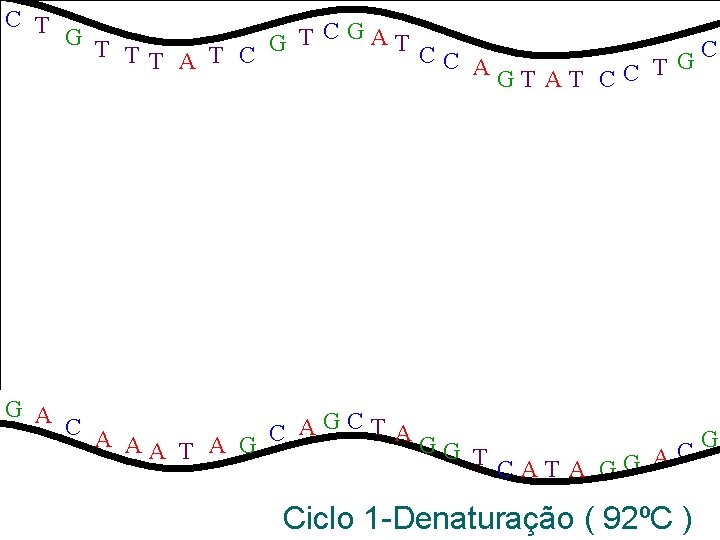
C T G A G T T CGAT G C TT A T C CC G AGT AT CC T C A AGCT A C AA T A G GG T CAT A GG G C A Ciclo 1 -Denaturação ( 92ºC )
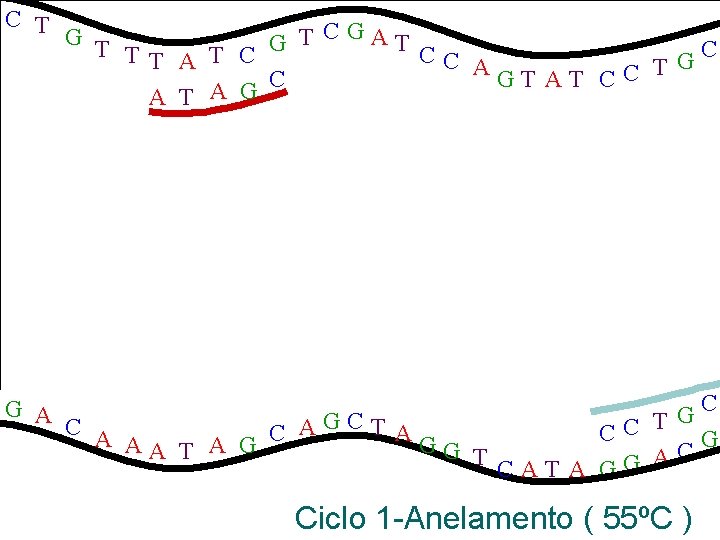
C T G A G T T CGAT G C TT A T C CC G AGT AT CC T C A T A G C A AGCT A CC T G C AA T A G GG T C A G CAT A G Ciclo 1 -Anelamento ( 55ºC )
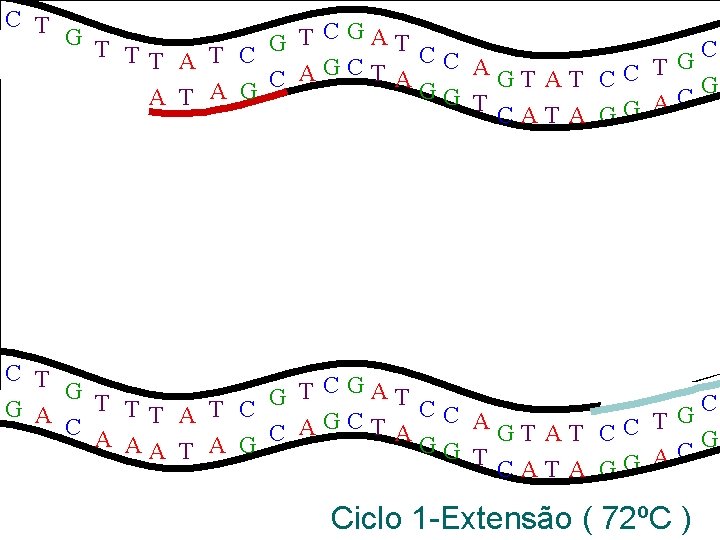
C T G T T CGAT G C G A TT A T C C G C AGT AT CC T C A AGCT A C G AA T A G GG C T CAT A GG A C T G T T CGAT G C TT A T C CC G AGT AT CC T C A AGCT A C G AA T A G GG T C A CAT A GG Ciclo 1 -Extensão ( 72ºC )
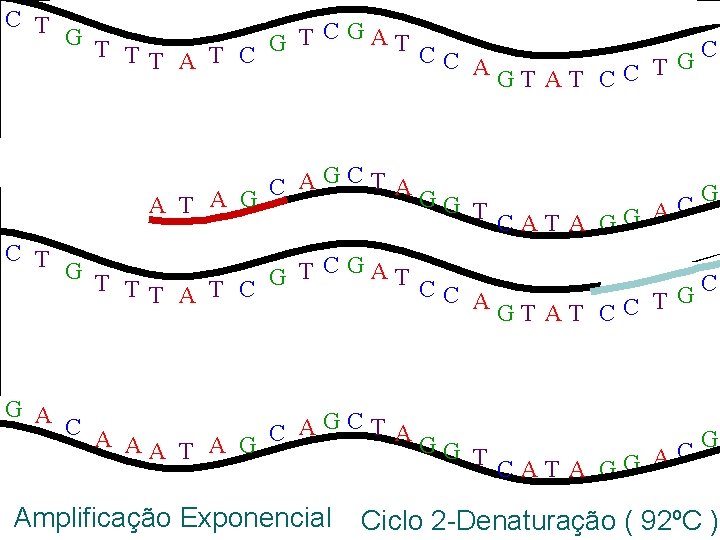
C T G T T CGAT G C TT A T C CC G AGT AT CC T G A C A AGCT A C G AA T A G GG C T CAT A GG A C T G T T CGAT G C TT A T C CC A G GT AT CC T G A C A AGCT A C AA T A G GG T Amplificação Exponencial CAT A GG G C A Ciclo 2 -Denaturação ( 92ºC )
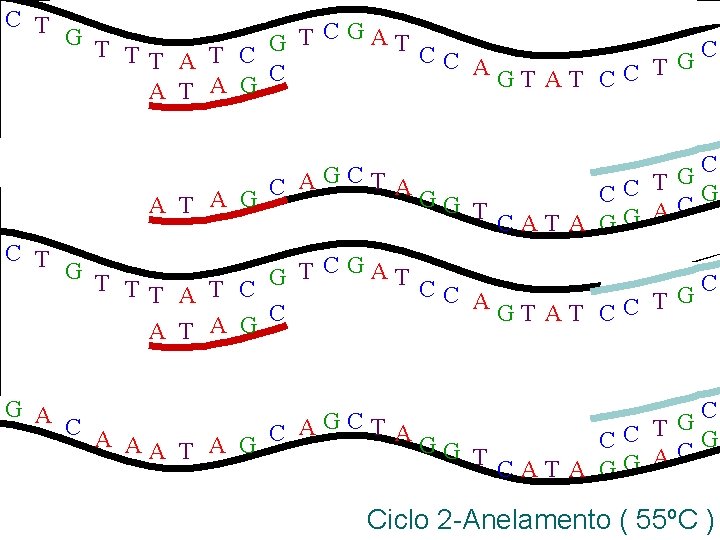
C T G T T CGAT G C TT A T C CC G AGT AT CC T C A T A G G A C G C A A TA T G C C C AA T A G GG T CAT A GG AC C T G T T CGAT G C TT A T C CC A G C T C G T A T C A T A G G A C A AGCT A C AA T A G GG T C G CC T CG A CAT A GG Ciclo 2 -Anelamento ( 55ºC )
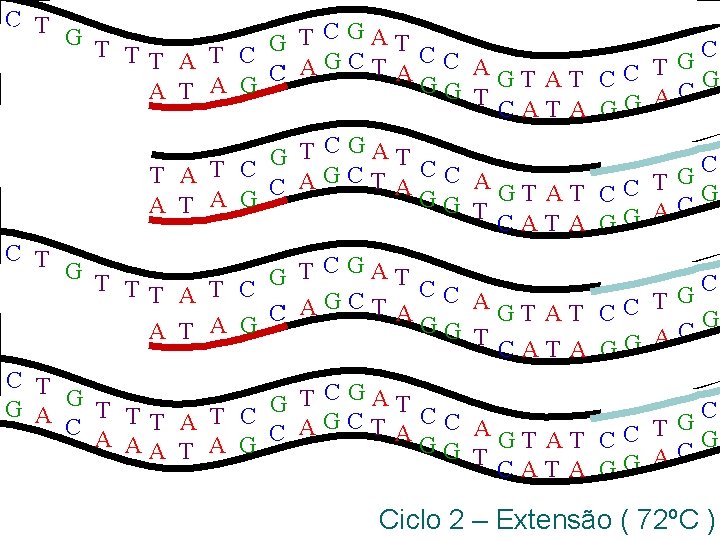
C T CGA G T G TC G A T T T C T A C A AGCT A C AGT AT C AA T A G GG T CAT A C T G T T CGAT G G A TT A T C CC A G C C A A TA C GT AT AA T A G GG T CAT A C T CGA G TC G A T T T C T A C A AGCT A C AA T A G GG T GT AT CAT A C G CC T CG GG A C G T G CC C A G G CC T G C A G G CC T CG GG A Ciclo 2 – Extensão ( 72ºC )
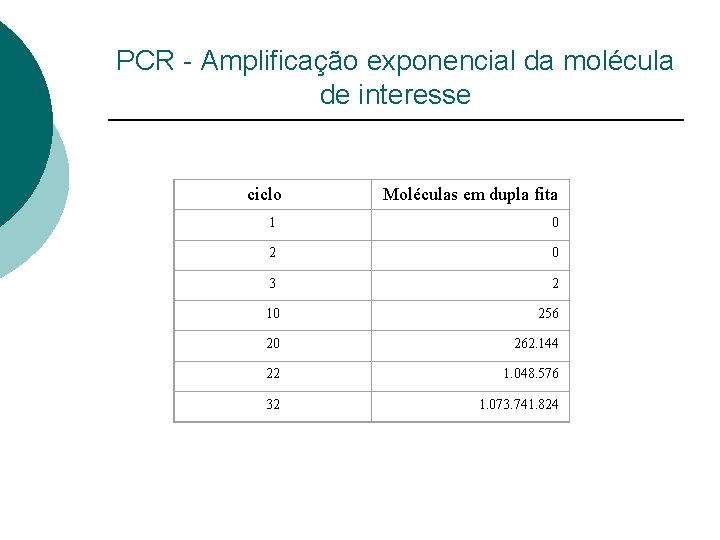
PCR - Amplificação exponencial da molécula de interesse ciclo Moléculas em dupla fita 1 0 2 0 3 2 10 256 20 262. 144 22 1. 048. 576 32 1. 073. 741. 824

Aplicações da PCR • Detecção de Mutações • Determinação do Sexo em Células pré-natais • Aconselhamento Genético • Medicina Forense • Identificação de Plantas Transgênicas • Acompanhamento no tratamento de Câncer • Evolução Molecular • Filogenia • Paternidade • Detecção de Infecções Virais e Bacterianas (Carga Viral)
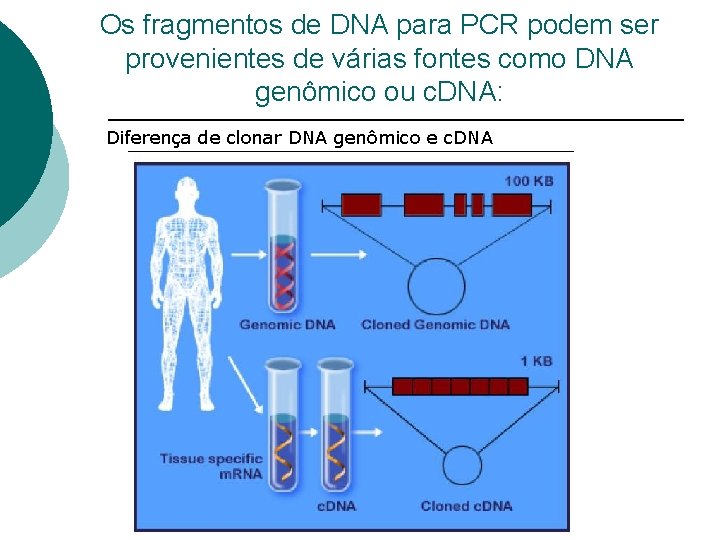
Os fragmentos de DNA para PCR podem ser provenientes de várias fontes como DNA genômico ou c. DNA: Diferença de clonar DNA genômico e c. DNA
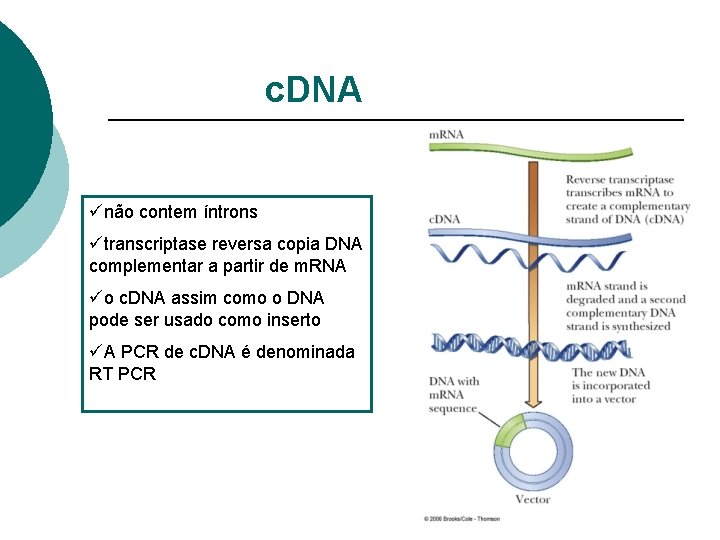
c. DNA ünão contem íntrons ütranscriptase reversa copia DNA complementar a partir de m. RNA üo c. DNA assim como o DNA pode ser usado como inserto üA PCR de c. DNA é denominada RT PCR

Ferramentas para análise de DNA
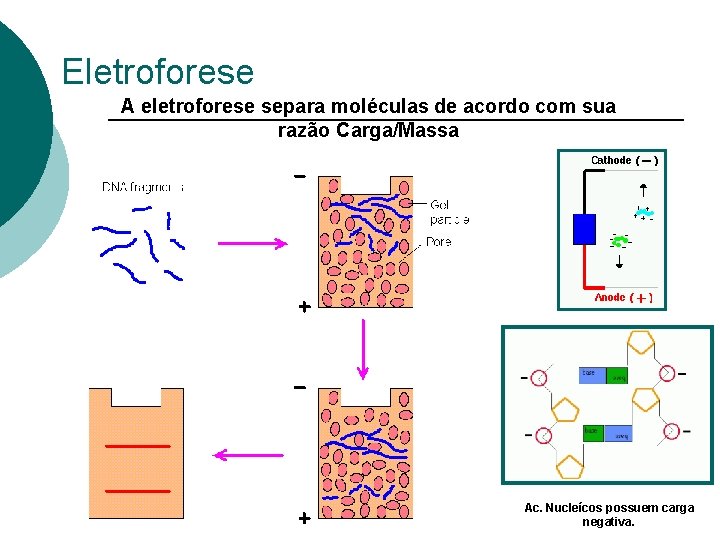
Eletroforese A eletroforese separa moléculas de acordo com sua razão Carga/Massa Ac. Nucleícos possuem carga negativa.
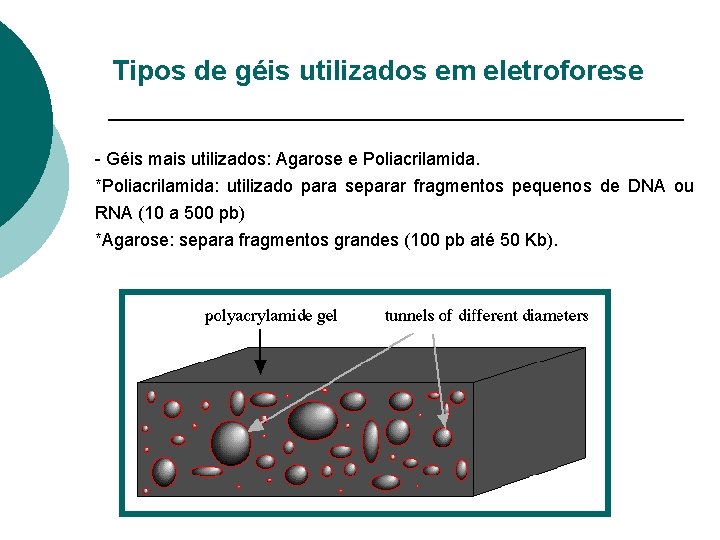
Tipos de géis utilizados em eletroforese - Géis mais utilizados: Agarose e Poliacrilamida. *Poliacrilamida: utilizado para separar fragmentos pequenos de DNA ou RNA (10 a 500 pb) *Agarose: separa fragmentos grandes (100 pb até 50 Kb).

Eletroforese em gel de agarose Concentração do gel de agarose Brometo de etídio
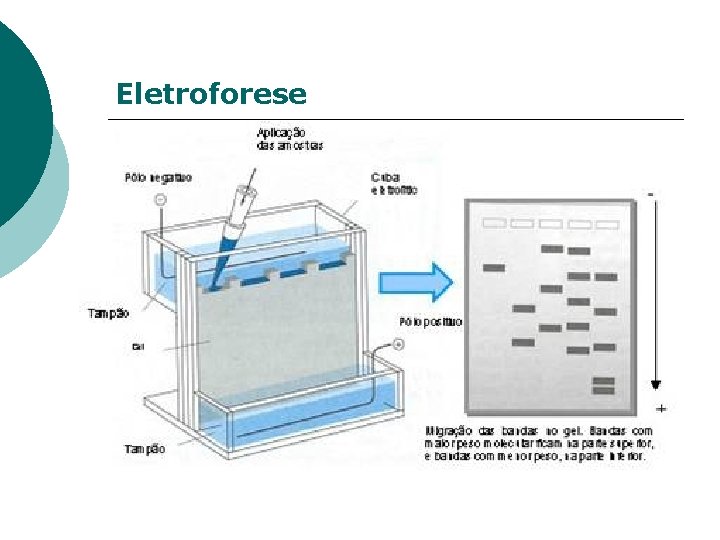
Eletroforese

Análise direta de DNA utilizando sondas de DNA SONDAS DE DNA: • Segmentos de ácidos nucléicos; • Clonados ou sintetizados; • Marcados (radioativamente ou não radioativamente) • Usados nas reações de hibridação DNA: DNA ou DNA: RNA • Finalidade: localizar uma seqüência de interesse por hibridação Hibridação de ácidos nucléicos: -Mistura de ácidos nucléicos de duas fontes -Desnaturação por calor ou ação química -Pareamento das bases complementares de sequências homólogas
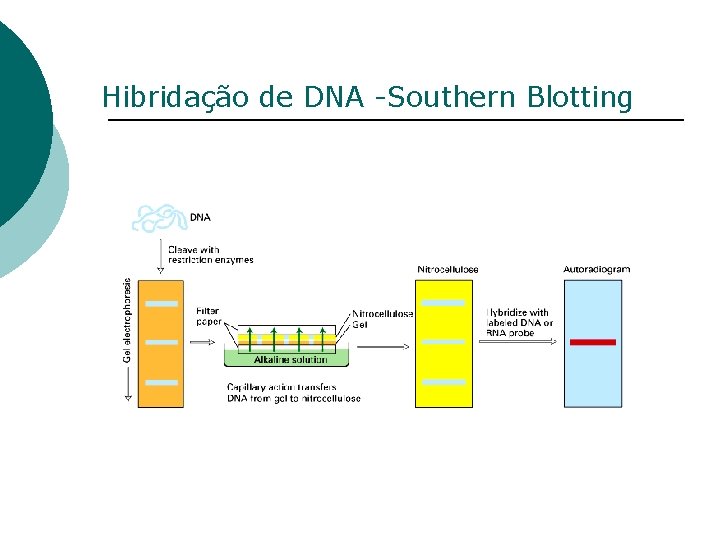
Hibridação de DNA -Southern Blotting
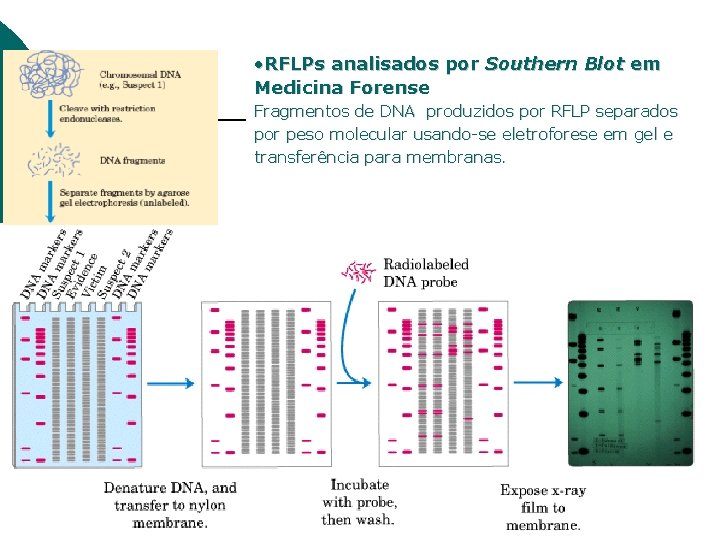
• RFLPs analisados por Southern Blot em Medicina Forense Fragmentos de DNA produzidos por RFLP separados por peso molecular usando-se eletroforese em gel e transferência para membranas.
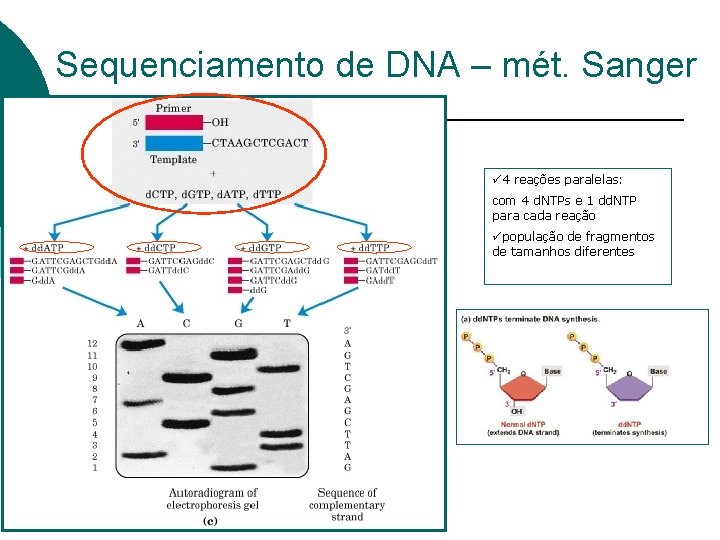
Sequenciamento de DNA – mét. Sanger ü 4 reações paralelas: com 4 d. NTPs e 1 dd. NTP para cada reação üpopulação de fragmentos de tamanhos diferentes
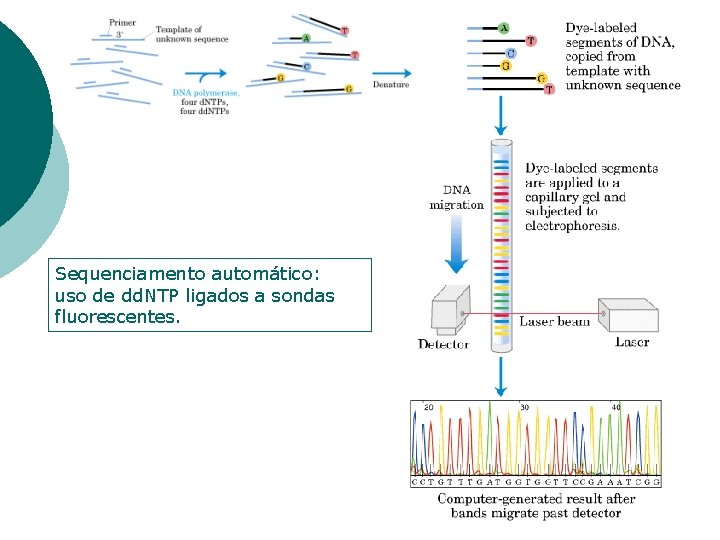
Sequenciamento automático: uso de dd. NTP ligados a sondas fluorescentes.
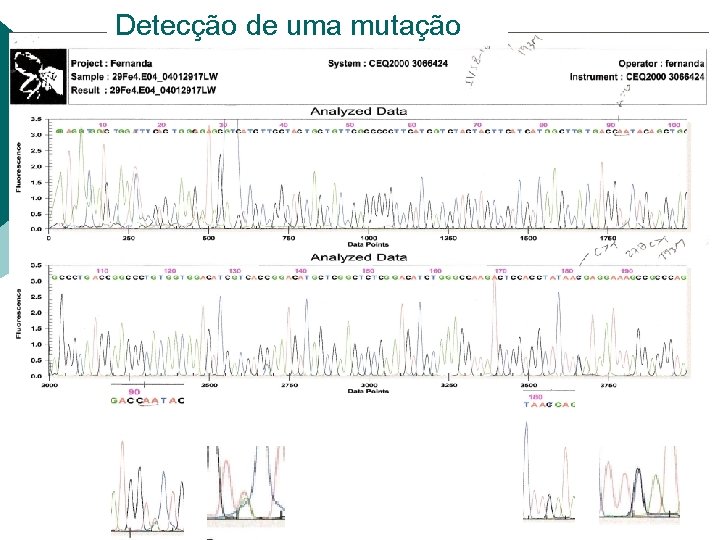
Detecção de uma mutação

Manipulação genética Clones ¡ Transgênicos ¡
Clone População de organismos, células ou moléculas, duplicadas de uma mesma origem e, portanto, idênticas.

O que é um clone ? ¡ O termo clone foi criado em 1903 pelo botânico Herbert J Weber , que pesquisava o cruzamento de plantas; ¡ Clone é um organismo gerado de modo assexuado, a partir de apenas 1 progenitor; ¡ Este termo foi utilizado por muito tempo para plantas e só se tornou polêmico frente a possibilidade da clonagem de mamíferos.

Como é realizada a clonagem? ¡ Deve haver uma célula doadora do núcleo e uma célula receptora; ¡ A célula doadora do núcleo pode ser uma célula embrionária ou uma célula adulta; ¡ A célula receptora pode ser um zigoto, ou seja, um ovo fertilizado por um espermatozóide ou um ovócito, ou seja, um ovo não fertilizado; ¡ O núcleo da célula receptora é retirado e descartado e então o núcleo da célula doadora é transferido; ¡ Nesta célula são dados choques elétricos de baixa voltagem para que o núcleo transplantado seja fundido ao ovócito.

Desde 1980 têm sido realizada a clonagem de mamíferos de modo experimental. Já foram clonados camundongos, carneiros, bezerros, porcos, gatos. . .

A ovelha Dolly ¡ ¡ Em 1997 foi clonada a ovelha Dolly pelo cientista escocês Ian Wilmut; Resultou da união de uma célula adulta, proveniente da glândula mamária da doadora com um ovócito proveniente de outra ovelha. Esse experimento levantou a polêmica sobre a clonagem de seres humanos. 14 de fevereiro de 2003 A ovelha Dolly, o primeiro mamífero clonado do mundo, foi sacrificado após a descoberta de sinais de uma doença pulmonar progressiva.

Clonar para quê ? ¡ No caso de bovinos, caprinos e suínos, as vantagens são manter as qualidades daquele animal, além da possibilidade de garantir a reprodução de animais transgênicos e sob risco de extinção; ¡ No caso de seres humanos alguns aspectos devem ser discutidos: - reprodutiva: tem como fim gerar um indivíduo - terapêutica: tem como objetivo a produção de tecidos para transplante.

Clonagem reprodutiva A clonagem reprodutiva auxiliaria casais com problemas reprodutivos e que não obtiveram sucesso na reprodução in vitro, porém: - a aparência dos clones pode ser distinta; - o comportamento e personalidade também podem ser diferentes (ex. gêmeos monozigóticos); - influência do ambiente no desenvolvimento de um indivíduo. Por que não clonar ? -Alto índice de erro: entre 100 embriões 1 daria certo (Dolly: 300 embriões e 1 acerto); -Morte prematura dos clones: a partir de célula adulta; -Há o desconhecimento dos processos genéticos envolvidos no sucesso destes embriões. -Problemas já conhecidos na clonagem de mamíferos: l peso do feto e da placenta muito aumentados; l alta freqüência de anomalias congênitas; l falecimento dos clones poucas horas após o nascimento por distúrbios respiratórios e circulatórios. -variabilidade da espécie; -questões éticas e morais: individualidade, alma, direitos;

Clonagem terapêutica ¡ ¡ As células-mãe (tronco) embrionárias podem se tornar qualquer tipo de célula existente no corpo, através de indução específica. A clonagem terapêutica de tecidos auxiliaria nos transplantes, regeneração de alguns tecidos. . .
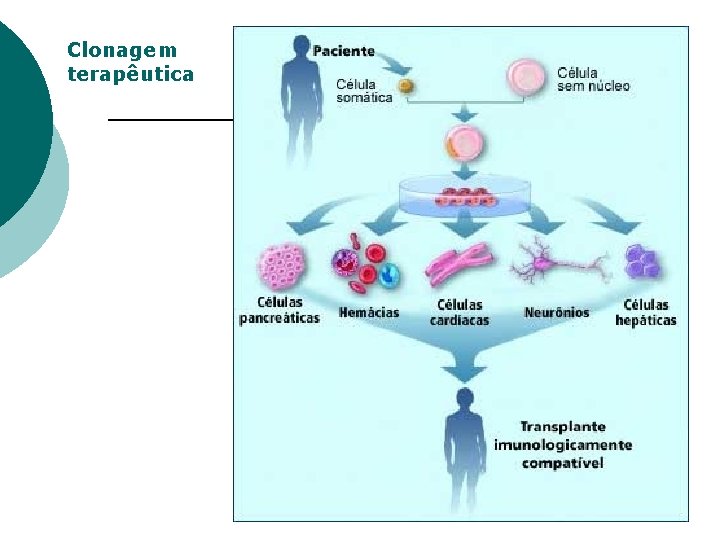
Clonagem terapêutica
Transgênicos Organismos transgênicos – Aqueles que possuem material genético de outro organismo. ex: bactérias transgênicas com gene da insulina, elas carregam o gene humano. 1983 - primeiro transgênico, fumo resistente a vírus. 1995 - já existiam mais de 700 transgênicos descritos Atualmente ainda se discutem prós e contras ao uso de transgênicos

Contras ¡ ¡ Riscos de contaminação da biodiversidade genética Resistência de insetos e pragas Impacto ecológico por remoção de plantas invasoras Reações alérgicas Prós ¡ ¡ Redução do uso de agrotóxicos Redução da compactação do solo Aumento da produtividade com baixo custo Redução da exploração de novas áreas agrícolas

Lista de alguns Transgênicos no “mercado” ¡ ¡ ¡ ¡ Tomate Algodão Milho Soja Feijão Couve Melancia Insulina Ex. Soja transgênica -uns 50 % da soja do Brasil é transgênica – tem enzima introduzida artificialmente, resistente ao herbicida gliofosfato- só precisa usar este herbicida no controle a plantas daninhas. -além das vantagens de custo, redução de agrotóxicos a soja em questão é de melhor produtividade. -por outro lado algumas plantas daninhas são resistentes, monopólio do herbicida, perda da parte benéfica da flora, gliofosfato com o tempo desequilibra os fatores bióticos e abióticos.

Ex. 1 Feijão Transgênico
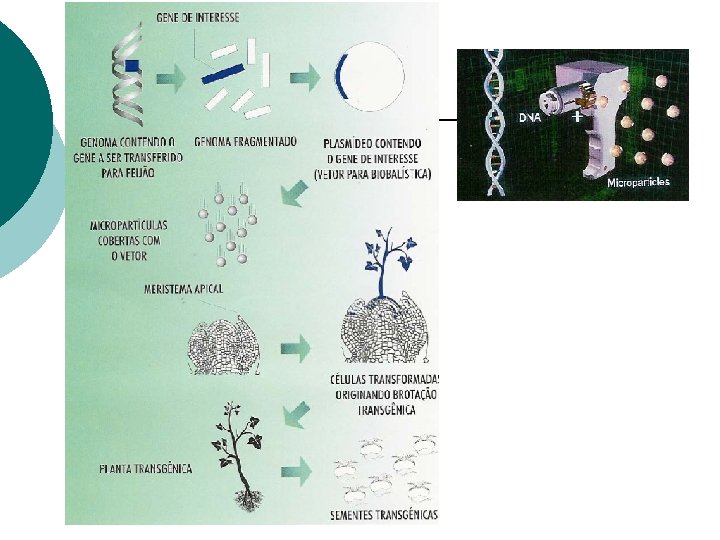
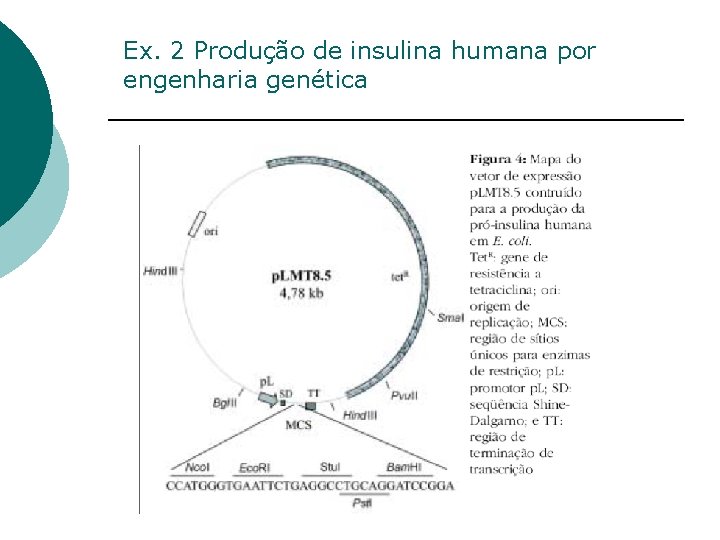
Ex. 2 Produção de insulina humana por engenharia genética

Salmão superexpressando hormônio do crescimento

Terapia Gênica ¡ ¡ Inserção de genes funcionais em células com genes defeituosos. Necessita vetor seguro e eficiente.

- Slides: 69