TECNICHE ELETTROANALITICHE I metodi elettrochimici si basano sulla
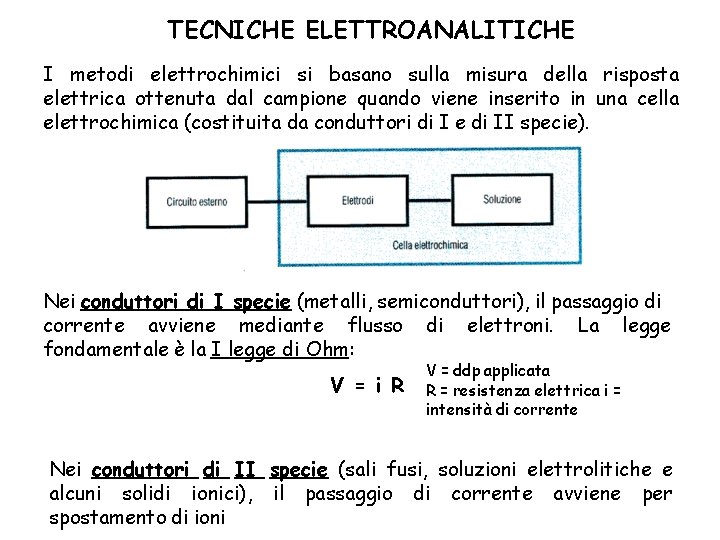
TECNICHE ELETTROANALITICHE I metodi elettrochimici si basano sulla misura della risposta elettrica ottenuta dal campione quando viene inserito in una cella elettrochimica (costituita da conduttori di I e di II specie). Nei conduttori di I specie (metalli, semiconduttori), il passaggio di corrente avviene mediante flusso di elettroni. La legge fondamentale è la I legge di Ohm: V = i R V = ddp applicata R = resistenza elettrica i = intensità di corrente Nei conduttori di II specie (sali fusi, soluzioni elettrolitiche e alcuni solidi ionici), il passaggio di corrente avviene per spostamento di ioni

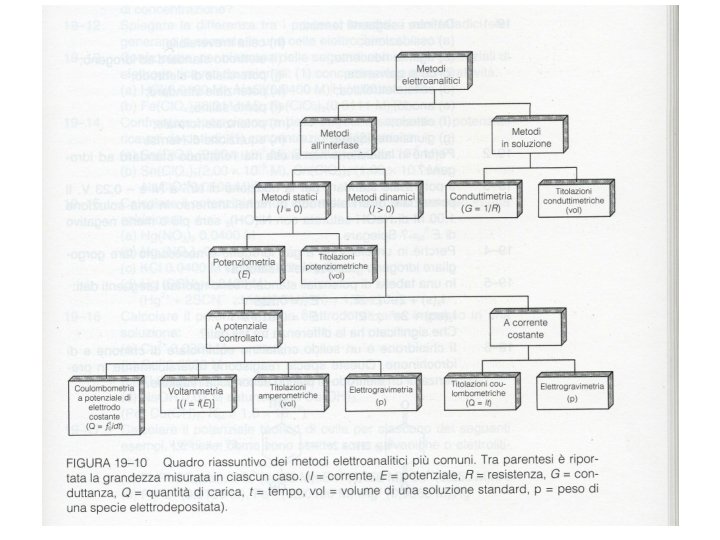
In elettrochimica, i parametri che possono essere sono: misurati E, cioè la differenza di potenziale (ddp) che di stabilisce tra due elettrodi immersi nella soluzione di misura, in potenziometria. Q, la quantità di carica elettrica che si ottiene applicando una ddp a due elettrodi, in coulombometria o in elettrogravimetria. i, l’intensità di corrente che passa tra gli elettrodi immersi nella soluzione al variare del potenziale applicato ad uno di essi, in voltammetria. R o , resistenza o conducibilità in conduttimetria

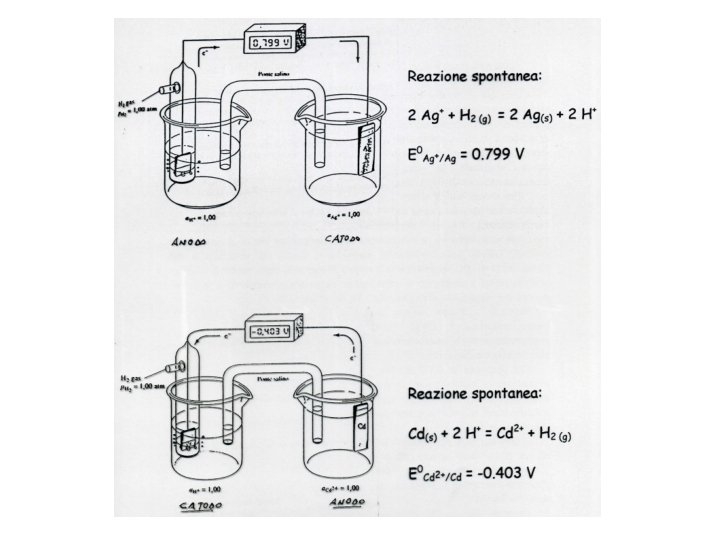
POTENZIOMETRIA I metodi potenziometrici sono metodi di analisi basati sulla misura della forza elettromotrice (f. e. m. ) di una cella galvanica. La cella galvanica è un dispositivo atto a convertire l’energia chimica di una reazione di ossido-riduzione in energia elettrica. Es. : 2 Ag+ + Cu (s) = 2 Ag (s) + Cu 2+ riduzione: Ag+ + 1 e- = Ag° ossidazione: Cu° = Cu 2+ + 2 e-
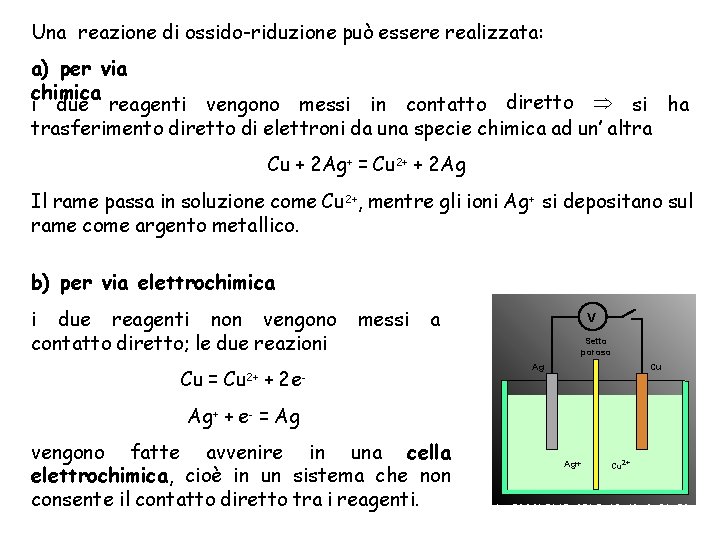
Una reazione di ossido-riduzione può essere realizzata: a) per via chimica i due reagenti vengono messi in contatto diretto si ha trasferimento diretto di elettroni da una specie chimica ad un’ altra Cu + 2 Ag+ = Cu 2+ + 2 Ag Il rame passa in soluzione come Cu 2+, mentre gli ioni Ag+ si depositano sul rame come argento metallico. b) per via elettrochimica i due reagenti non vengono contatto diretto; le due reazioni Cu = Cu + 2 e 2+ messi a - Ag + e = Ag + - vengono fatte avvenire in una cella elettrochimica, cioè in un sistema che non consente il contatto diretto tra i reagenti. V Setto poroso Ag Cu Zn 2+ Cu 2+ Ag+ Cu 2+
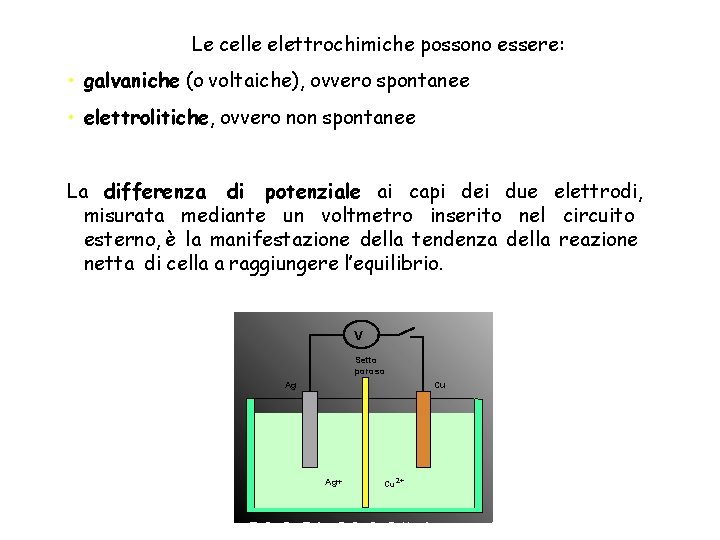
Le celle elettrochimiche possono essere: • galvaniche (o voltaiche), ovvero spontanee • elettrolitiche, ovvero non spontanee La differenza di potenziale ai capi dei due elettrodi, misurata mediante un voltmetro inserito nel circuito esterno, è la manifestazione della tendenza della reazione netta di cella a raggiungere l’equilibrio. V Setto poroso Ag Cu Zn 2+ Cu 2+ Ag+ Cu 2+
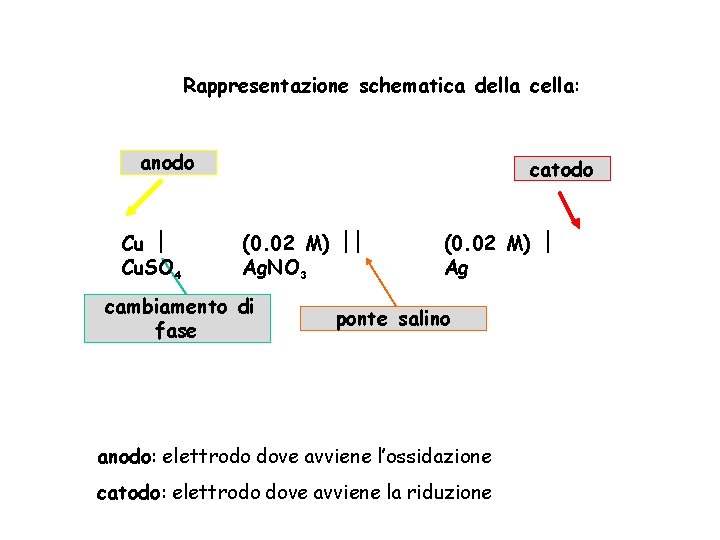
Rappresentazione schematica della cella: anodo Cu Cu. SO 4 catodo (0. 02 M) Ag. NO 3 cambiamento di fase (0. 02 M) Ag ponte salino anodo: elettrodo dove avviene l’ossidazione catodo: elettrodo dove avviene la riduzione
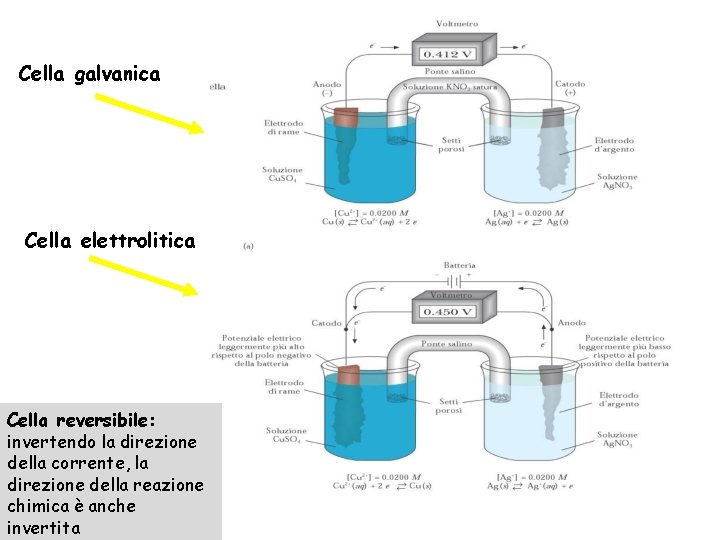
Cella galvanica Cella elettrolitica Cella reversibile: invertendo la direzione della corrente, la direzione della reazione chimica è anche invertita
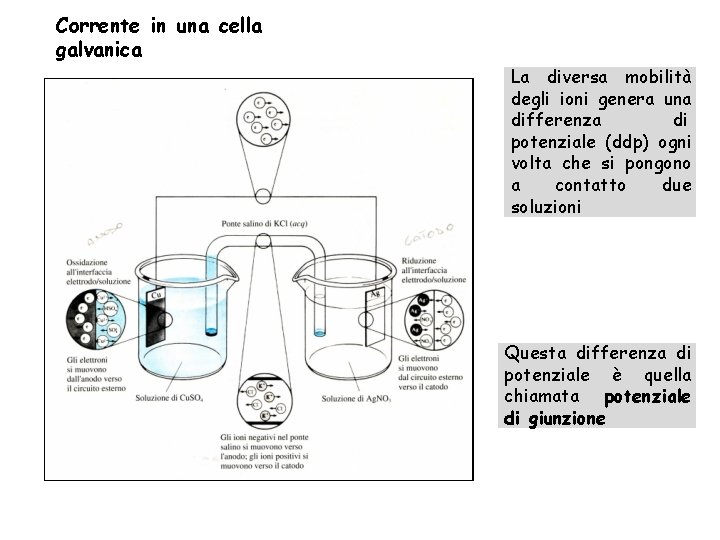
Corrente in una cella galvanica La diversa mobilità degli ioni genera una differenza di potenziale (ddp) ogni volta che si pongono a contatto due soluzioni Questa differenza di potenziale è quella chiamata potenziale di giunzione
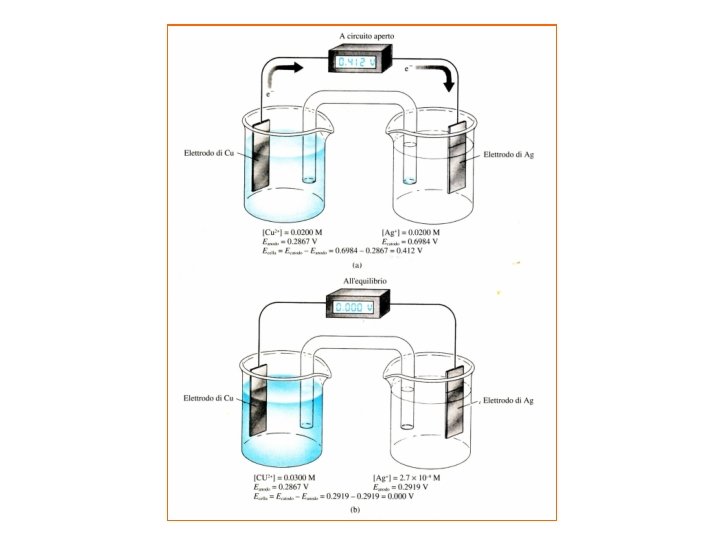

Pile di concentrazione • Processo di diluizione di una soluzione C 1 > C 2 E Cu 2+ (aq, C 1) Cu 2+ (aq, C 2) Cu 2++ 2 e- Cu E° Cu 2+/Cu RT - 2 F ln 1 E° [Cu 2+] Cu 2+/Cu + RT ln [Cu 2+] 2 F Maggiore è [Cu 2+] maggiore è E °. Il primo semielemento funziona da catodo e il secondo da anodo. (-) Cu| Cu 2+ (aq, C 1) | | Cu 2+ (aq, C 2) | Cu (+) E = EC -EA = 0, 0591 2 Log C 1 C 2 Gli E° essendo uguali si elidono La soluzione più concentrata si diluisce mentre quella più diluita si concentra. Quando C 1= C 2 , E ° = 0, la cella è scarica Elettrochimica

La serie elettrochimica dei potenziali standard Con l’assunzione del riferimento per l’ESI si può determinare il potenziale standard di un qualsiasi semielemento costituito da una coppia Oss/Rid, accoppiando l’ESI con il semielemento, in condizioni standard e misurando la f. e. m. della pila così ottenuta. Pt H 2(g, P =1 atm) H 3 O+(aq, 1 M) Zn. SO 4(aq, 1 M) Zn E°cella=0. 763 V Il polo negativo (anodo) è l’elettrodo di zinco E°Zn 2+/Zn = -0. 763 V potenziale standard del semielemento a zinco Pt H 2(g, P =1 atm) H 3 O+(aq, 1 M) Cu. SO 4(aq, 1 M) Cu E°cella=0. 337 V Il polo positivo (catodo) è l’elettrodo di rame E°Cu 2+/Cu = +0. 337 V potenziale standard del semielemento a rame
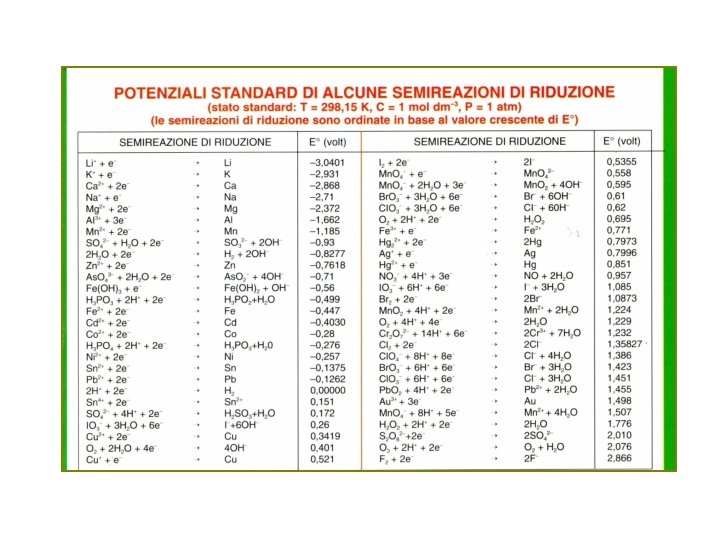

La serie elettrochimica dei potenziali standard • I valori sono tabulati come potenziali standard di riduzione; ogni semireazione elettrodica è riportata come riduzione • Il potenziale standard di riduzione di una certa coppia redox indica la capacità di questa coppia a comportarsi da ossidante o da riducente rispetto alla coppia H 3 O+/H 2 • Lo stesso criterio può essere facilmente esteso a qualsiasi altra coppia redox, confrontando i relativi potenziali standard • Calcolo immediato della f. e. m. standard (E°) di una cella formata da due semielementi qualsiasi (-) Zn Zn 2+(aq, 1 M) Cu 2+(aq, 1 M) Cu (+) E° = E°C-E°A = E°Cu 2+/Cu-E°Zn 2+/Zn = +0. 337 - (-0. 763) = +1. 100 V

Potenziale di una cella galvanica Ecella = E catodo - Eanodo + Egiunzione Il potenziale di ogni semicella può essere calcolato tramite l’equazione di Nernst E E RTln aox n. F arid R = costante generale dei gas (R = 8. 314 J/ mol K) T = temperatura espressa in °K n = numero di elettroni scambiati nelle reazione redox F = faraday (96500 Coulomb) a = attività della specie E° = potenziale nelle condizioni standard (nelle condizioni cioè in cui l’attività è unitaria) Riunendo i termini noti (a T = 25°C): E E 0. 05 n 91 log aox arid Per convenzione il potenziale elettrodico è un potenziale di riduzione: si riferisce cioè al processo scritto come riduzione
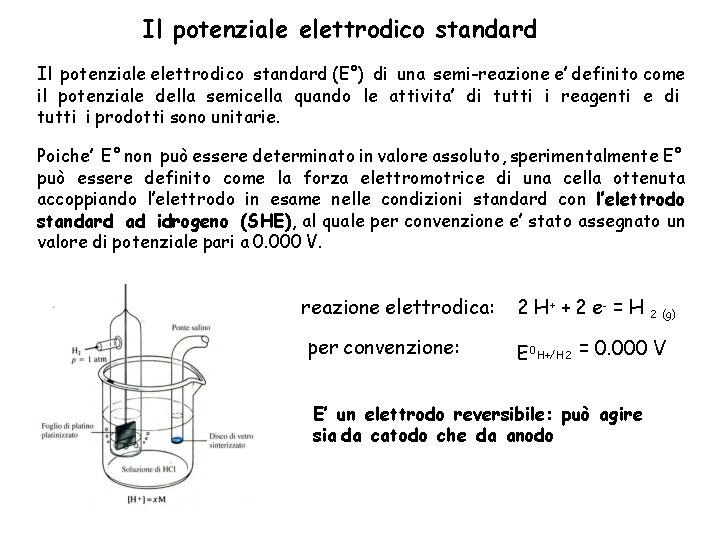
Il potenziale elettrodico standard (E°) di una semi-reazione e’ definito come il potenziale della semicella quando le attivita’ di tutti i reagenti e di tutti i prodotti sono unitarie. Poiche’ E° non può essere determinato in valore assoluto, sperimentalmente E° può essere definito come la forza elettromotrice di una cella ottenuta accoppiando l’elettrodo in esame nelle condizioni standard con l’elettrodo standard ad idrogeno (SHE), al quale per convenzione e’ stato assegnato un valore di potenziale pari a 0. 000 V. reazione elettrodica: per convenzione: 2 H+ + 2 e- = H 2 (g) E 0 H+/H 2 = 0. 000 V E’ un elettrodo reversibile: può agire sia da catodo che da anodo
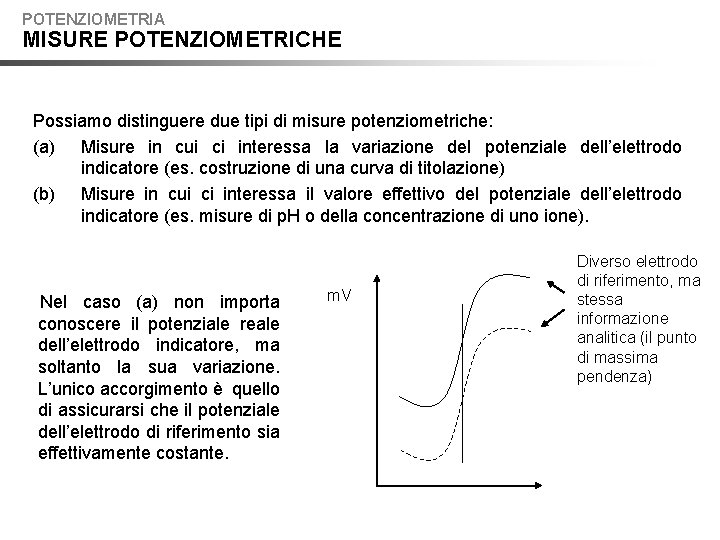
POTENZIOMETRIA MISURE POTENZIOMETRICHE Possiamo distinguere due tipi di misure potenziometriche: (a) Misure in cui ci interessa la variazione del potenziale dell’elettrodo indicatore (es. costruzione di una curva di titolazione) (b) Misure in cui ci interessa il valore effettivo del potenziale dell’elettrodo indicatore (es. misure di p. H o della concentrazione di uno ione). Nel caso (a) non importa conoscere il potenziale reale dell’elettrodo indicatore, ma soltanto la sua variazione. L’unico accorgimento è quello di assicurarsi che il potenziale dell’elettrodo di riferimento sia effettivamente costante. m. V Diverso elettrodo di riferimento, ma stessa informazione analitica (il punto di massima pendenza)
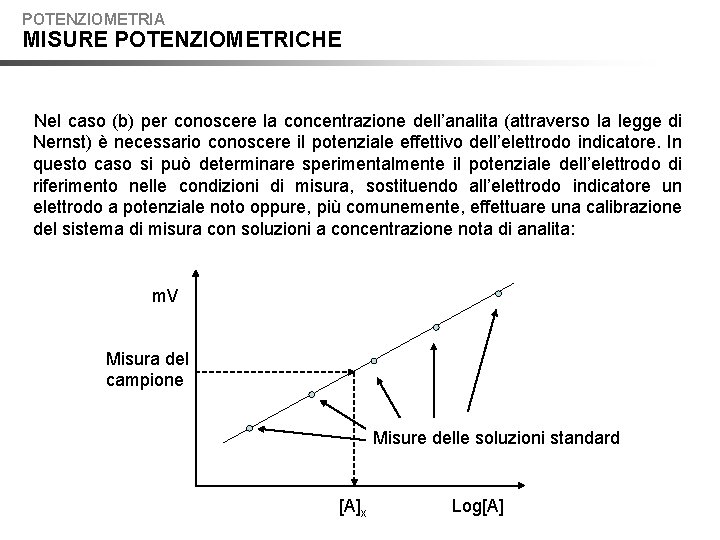
POTENZIOMETRIA MISURE POTENZIOMETRICHE Nel caso (b) per conoscere la concentrazione dell’analita (attraverso la legge di Nernst) è necessario conoscere il potenziale effettivo dell’elettrodo indicatore. In questo caso si può determinare sperimentalmente il potenziale dell’elettrodo di riferimento nelle condizioni di misura, sostituendo all’elettrodo indicatore un elettrodo a potenziale noto oppure, più comunemente, effettuare una calibrazione del sistema di misura con soluzioni a concentrazione nota di analita: m. V Misura del campione Misure delle soluzioni standard [A]x Log[A]
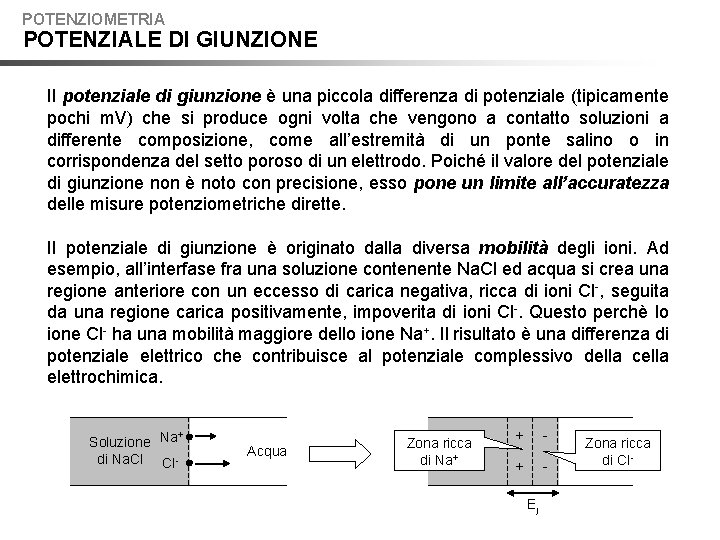
POTENZIOMETRIA POTENZIALE DI GIUNZIONE Il potenziale di giunzione è una piccola differenza di potenziale (tipicamente pochi m. V) che si produce ogni volta che vengono a contatto soluzioni a differente composizione, come all’estremità di un ponte salino o in corrispondenza del setto poroso di un elettrodo. Poiché il valore del potenziale di giunzione non è noto con precisione, esso pone un limite all’accuratezza delle misure potenziometriche dirette. Il potenziale di giunzione è originato dalla diversa mobilità degli ioni. Ad esempio, all’interfase fra una soluzione contenente Na. Cl ed acqua si crea una regione anteriore con un eccesso di carica negativa, ricca di ioni Cl-, seguita da una regione carica positivamente, impoverita di ioni Cl-. Questo perchè lo ione Cl- ha una mobilità maggiore dello ione Na+. Il risultato è una differenza di potenziale elettrico che contribuisce al potenziale complessivo della cella elettrochimica. + Soluzione Na di Na. Cl Cl- Acqua Zona ricca di Na+ + - + Ej Zona ricca di Cl-
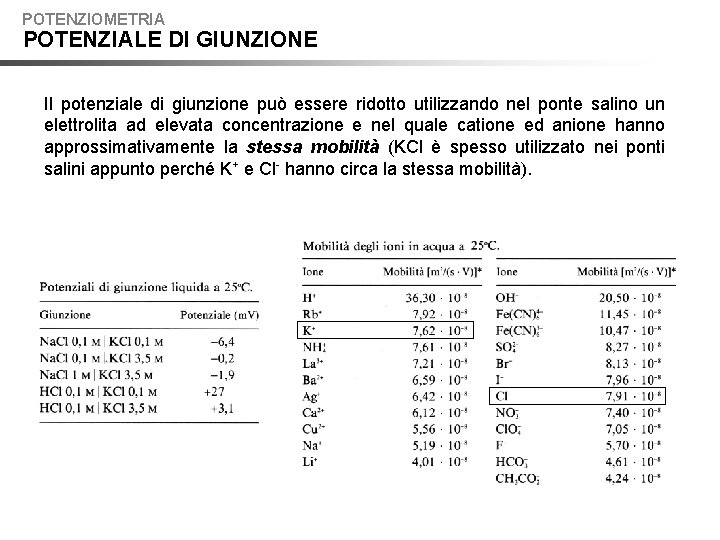
POTENZIOMETRIA POTENZIALE DI GIUNZIONE Il potenziale di giunzione può essere ridotto utilizzando nel ponte salino un elettrolita ad elevata concentrazione e nel quale catione ed anione hanno approssimativamente la stessa mobilità (KCl è spesso utilizzato nei ponti salini appunto perché K+ e Cl- hanno circa la stessa mobilità).

ELETTRODI: CLASSIFICAZIONE Gli elettrodi sono classificabili come: • elettrodi di riferimento • elettrodi di Ia e IIa specie, • elettrodi di ossidoriduzione, • elettrodi a membrana
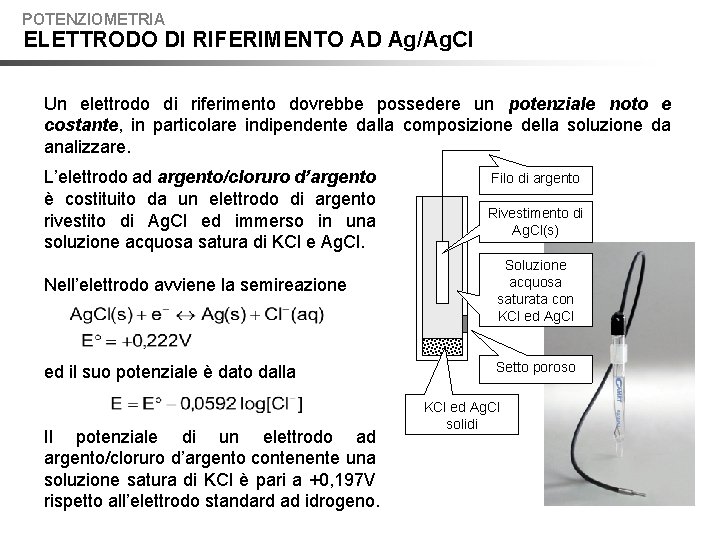
POTENZIOMETRIA ELETTRODO DI RIFERIMENTO AD Ag/Ag. Cl Un elettrodo di riferimento dovrebbe possedere un potenziale noto e costante, in particolare indipendente dalla composizione della soluzione da analizzare. L’elettrodo ad argento/cloruro d’argento è costituito da un elettrodo di argento rivestito di Ag. Cl ed immerso in una soluzione acquosa satura di KCl e Ag. Cl. Filo di argento Rivestimento di Ag. Cl(s) Nell’elettrodo avviene la semireazione Soluzione acquosa saturata con KCl ed Ag. Cl ed il suo potenziale è dato dalla Setto poroso Il potenziale di un elettrodo ad argento/cloruro d’argento contenente una soluzione satura di KCl è pari a +0, 197 V rispetto all’elettrodo standard ad idrogeno. KCl ed Ag. Cl solidi
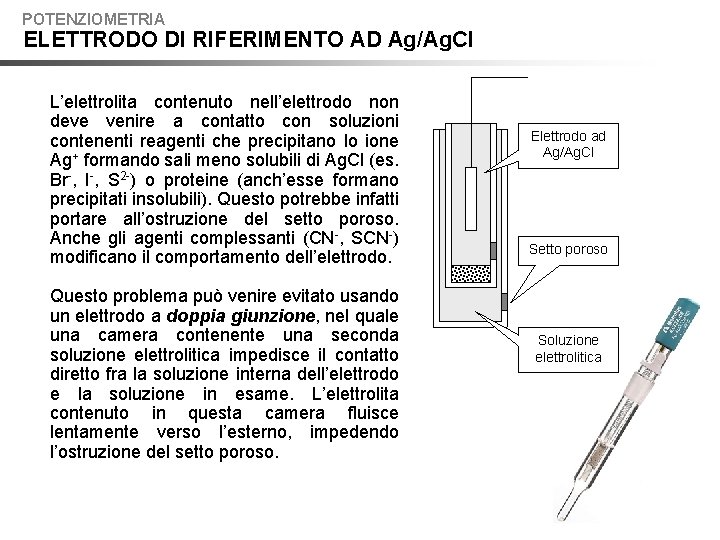
POTENZIOMETRIA ELETTRODO DI RIFERIMENTO AD Ag/Ag. Cl L’elettrolita contenuto nell’elettrodo non deve venire a contatto con soluzioni contenenti reagenti che precipitano lo ione Ag+ formando sali meno solubili di Ag. Cl (es. Br-, I-, S 2 -) o proteine (anch’esse formano precipitati insolubili). Questo potrebbe infatti portare all’ostruzione del setto poroso. Anche gli agenti complessanti (CN-, SCN-) modificano il comportamento dell’elettrodo. Questo problema può venire evitato usando un elettrodo a doppia giunzione, nel quale una camera contenente una seconda soluzione elettrolitica impedisce il contatto diretto fra la soluzione interna dell’elettrodo e la soluzione in esame. L’elettrolita contenuto in questa camera fluisce lentamente verso l’esterno, impedendo l’ostruzione del setto poroso. Elettrodo ad Ag/Ag. Cl Setto poroso Soluzione elettrolitica
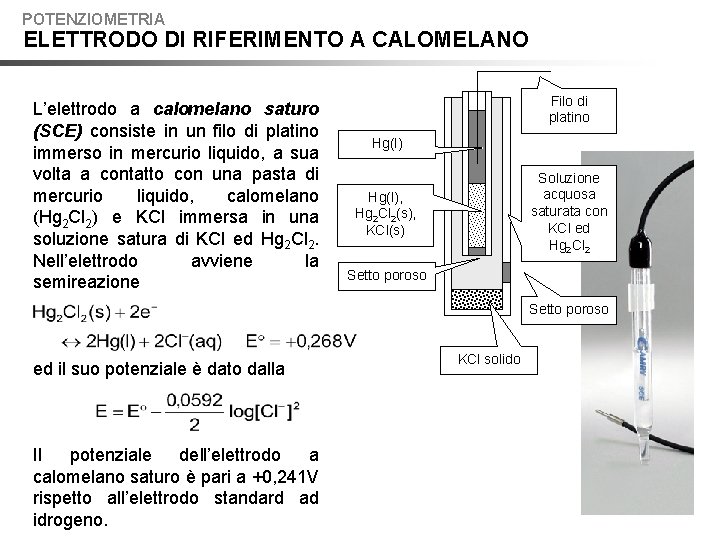
POTENZIOMETRIA ELETTRODO DI RIFERIMENTO A CALOMELANO L’elettrodo a calomelano saturo (SCE) consiste in un filo di platino immerso in mercurio liquido, a sua volta a contatto con una pasta di mercurio liquido, calomelano (Hg 2 Cl 2) e KCl immersa in una soluzione satura di KCl ed Hg 2 Cl 2. Nell’elettrodo avviene la semireazione Filo di platino Hg(l) Soluzione acquosa saturata con KCl ed Hg 2 Cl 2 Hg(l), Hg 2 Cl 2(s), KCl(s) Setto poroso ed il suo potenziale è dato dalla Il potenziale dell’elettrodo a calomelano saturo è pari a +0, 241 V rispetto all’elettrodo standard ad idrogeno. KCl solido
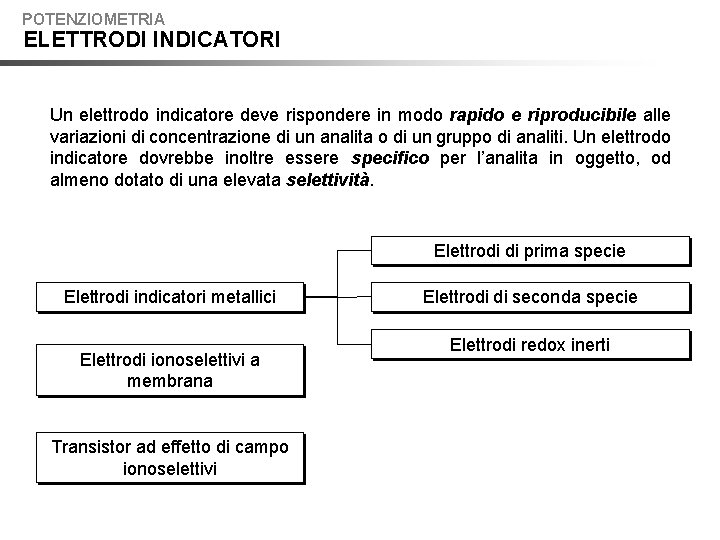
POTENZIOMETRIA ELETTRODI INDICATORI Un elettrodo indicatore deve rispondere in modo rapido e riproducibile alle variazioni di concentrazione di un analita o di un gruppo di analiti. Un elettrodo indicatore dovrebbe inoltre essere specifico per l’analita in oggetto, od almeno dotato di una elevata selettività. Elettrodi di prima specie Elettrodi indicatori metallici Elettrodi ionoselettivi a membrana Transistor ad effetto di campo ionoselettivi Elettrodi di seconda specie Elettrodi redox inerti

POTENZIOMETRIA ELETTRODI DI PRIMA SPECIE Un elettrodo indicatore di prima specie è costituito da un elettrodo di metallo puro immerso in una soluzione contenente un suo catione. Se l’equilibrio fra il metallo M ed il suo catione Mn+ può essere scritto come il potenziale dell’elettrodo indicatore Eind vale dove a. Mn+ è l’attività dello ione nella soluzione (o, in prima approssimazione, la sua concentrazione molare [Mn+]). Spesso il potenziale dell’elettrodo viene espresso in termini della funzione p dello ione (p. M = -log. M). In tal caso si ha:

POTENZIOMETRIA ELETTRODI DI SECONDA SPECIE I metalli non solo servono come elettrodi indicatori per il loro rispettivo catione, ma possono essere utilizzati anche per misurare l’attività di anioni che formano precipitati poco solubili o complessi stabili con questo catione (elettrodo indicatore di seconda specie). Se un metallo M forma un sale poco solubile MXn con un anione monovalente, in una soluzione saturata con MXn il potenziale di un elettrodo metallico dipenderà dall’attività dell’anione X-. Sulla base della seguente reazione elettrodica Il potenziale dell’elettrodo indicatore può essere scritto nella forma Se la concentrazione dello ione X- viene espressa sotto forma di p. X si ha

POTENZIOMETRIA ELETTRODI DI TERZA SPECIE Un conduttore inerte (costituito solitamente da un elettrodo di Pt, Pd, Au o carbone) immerso in una soluzione è in grado di rilevare il potenziale di un sistema redox contenuto nella soluzione stessa. Se nel sistema si verifica la seguente reazione di ossidoriduzione il potenziale di un elettrodo inerte immerso nella soluzione è dato dall’espressione
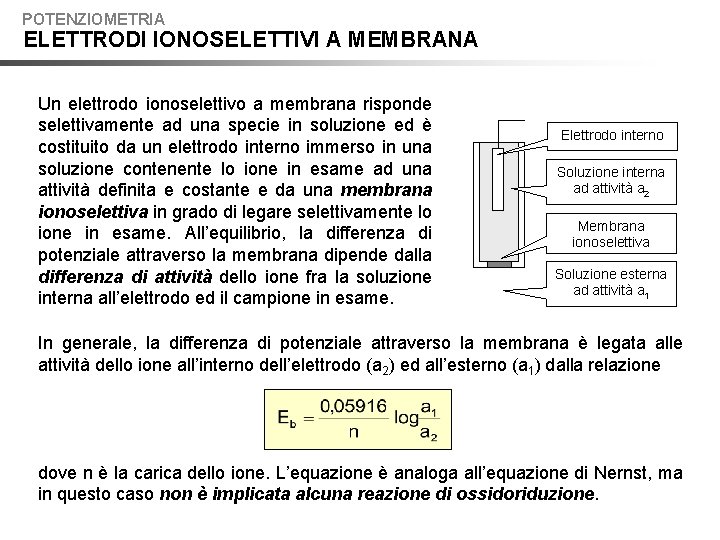
POTENZIOMETRIA ELETTRODI IONOSELETTIVI A MEMBRANA Un elettrodo ionoselettivo a membrana risponde selettivamente ad una specie in soluzione ed è costituito da un elettrodo interno immerso in una soluzione contenente lo ione in esame ad una attività definita e costante e da una membrana ionoselettiva in grado di legare selettivamente lo ione in esame. All’equilibrio, la differenza di potenziale attraverso la membrana dipende dalla differenza di attività dello ione fra la soluzione interna all’elettrodo ed il campione in esame. Elettrodo interno Soluzione interna ad attività a 2 Membrana ionoselettiva Soluzione esterna ad attività a 1 In generale, la differenza di potenziale attraverso la membrana è legata alle attività dello ione all’interno dell’elettrodo (a 2) ed all’esterno (a 1) dalla relazione dove n è la carica dello ione. L’equazione è analoga all’equazione di Nernst, ma in questo caso non è implicata alcuna reazione di ossidoriduzione.

Elettrodi a membrana o iono-selettivi (ISE) Tipi di elettrodi ISE: elettrodi a membrana di vetro elettrodi a membrana liquida elettrodi a membrana cristallina Requisiti fondamentali degli elettrodi ISE Un elettrodo ISE deve essere: Disponibile commercialmente e di facile costruzione Facilmente maneggiabile Robusto e con scarsa tendenza all’avvelenamento Avere buona riproducibilità e sufficiente range di validità Specifico Avere un tempo di risposta accettabile Risposta nernstiana
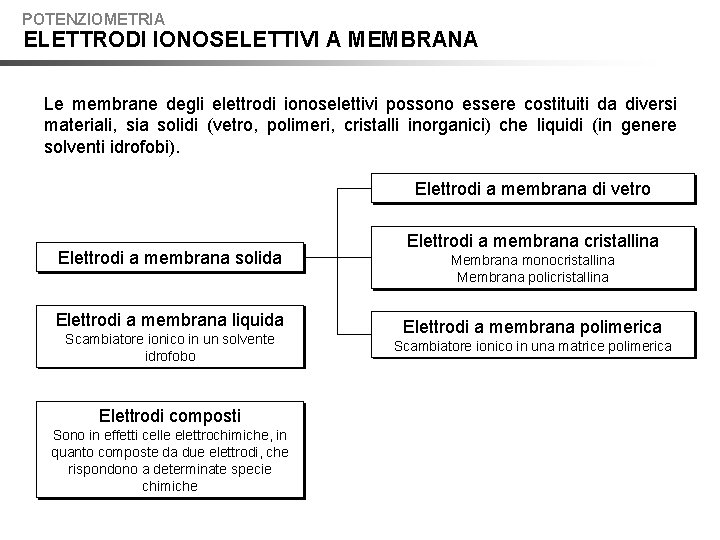
POTENZIOMETRIA ELETTRODI IONOSELETTIVI A MEMBRANA Le membrane degli elettrodi ionoselettivi possono essere costituiti da diversi materiali, sia solidi (vetro, polimeri, cristalli inorganici) che liquidi (in genere solventi idrofobi). Elettrodi a membrana di vetro Elettrodi a membrana solida Elettrodi a membrana liquida Scambiatore ionico in un solvente idrofobo Elettrodi composti Sono in effetti celle elettrochimiche, in quanto composte da due elettrodi, che rispondono a determinate specie chimiche Elettrodi a membrana cristallina Membrana monocristallina Membrana policristallina Elettrodi a membrana polimerica Scambiatore ionico in una matrice polimerica
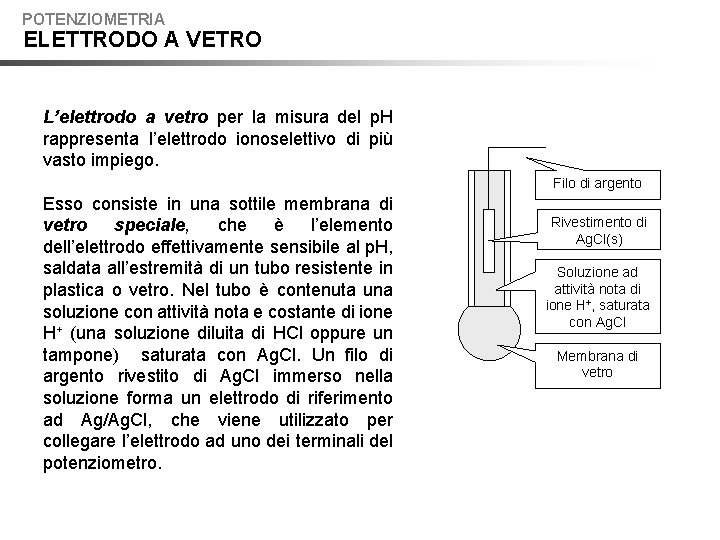
POTENZIOMETRIA ELETTRODO A VETRO L’elettrodo a vetro per la misura del p. H rappresenta l’elettrodo ionoselettivo di più vasto impiego. Filo di argento Esso consiste in una sottile membrana di vetro speciale, che è l’elemento dell’elettrodo effettivamente sensibile al p. H, saldata all’estremità di un tubo resistente in plastica o vetro. Nel tubo è contenuta una soluzione con attività nota e costante di ione H+ (una soluzione diluita di HCl oppure un tampone) saturata con Ag. Cl. Un filo di argento rivestito di Ag. Cl immerso nella soluzione forma un elettrodo di riferimento ad Ag/Ag. Cl, che viene utilizzato per collegare l’elettrodo ad uno dei terminali del potenziometro. Rivestimento di Ag. Cl(s) Soluzione ad attività nota di ione H+, saturata con Ag. Cl Membrana di vetro

POTENZIOMETRIA ELETTRODO A VETRO Il vetro silicato usato per le membrane è costituito da un insieme infinito tridimensionale di tetraedri Si. O 44 -, in cui ogni atomo di ossigeno è condiviso fra due atomi di silicio. Le cariche negative sono bilanciate da cationi (es. Na+ e Li+) che sono contenuti negli interstizi del reticolo. La membrana di vetro risponde al p. H in quanto è in grado di scambiare ioni H+ con le soluzioni con cui è a contatto. Per fare ciò il vetro deve essere idratato. In questo processo i cationi Na+ e Li+ vengono scambiati con gli ioni H+ della soluzione con la formazione di uno strato superficiale di “gel” contenente esclusivamente gruppi negativi Oliberi oppure legati a ioni H+ (in soluzioni fortemente alcaline si possono avere anche legami rilevanti con altri cationi come Na+).
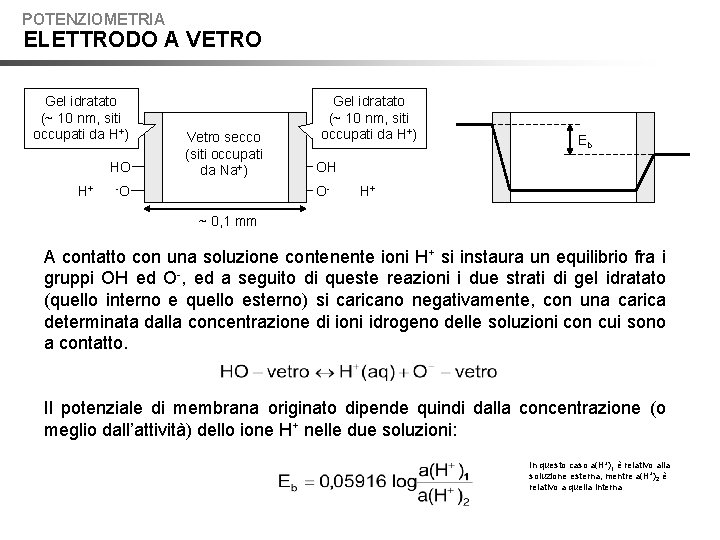
POTENZIOMETRIA ELETTRODO A VETRO Gel idratato (~ 10 nm, siti occupati da H+) HO H+ Vetro secco (siti occupati da Na+) -O Gel idratato (~ 10 nm, siti occupati da H+) Eb OH O- H+ ~ 0, 1 mm A contatto con una soluzione contenente ioni H+ si instaura un equilibrio fra i gruppi OH ed O-, ed a seguito di queste reazioni i due strati di gel idratato (quello interno e quello esterno) si caricano negativamente, con una carica determinata dalla concentrazione di ioni idrogeno delle soluzioni con cui sono a contatto. Il potenziale di membrana originato dipende quindi dalla concentrazione (o meglio dall’attività) dello ione H+ nelle due soluzioni: In questo caso a(H+)1 è relativo alla soluzione esterna, mentre a(H+)2 è relativo a quella interna

POTENZIOMETRIA ELETTRODO A VETRO Il potenziale di una elettrodo a vetro contiene vari contributi, ma soltanto il potenziale di membrana (Eb) è funzione del p. H della soluzione in esame. In particolare, esistono almeno tre contributi: il potenziale di membrana Eb, il potenziale dell’elettrodo di riferimento interno ad Ag/Ag. Cl e il potenziale di asimmetria Easimm: Raccogliendo i termini non dipendenti dall’attività dello ione idrogeno nella soluzione esterna si ottiene l’espressione • L’introduzione del potenziale di asimmetria (Easimm) deriva dalla osservazione sperimentale che in genere il potenziale di membrana non è nullo quando a 1 = a 2. Tale potenziale è in effetti determinato dalla non perfetta equivalenza delle due superfici della membrana. • Siccome per un elettrodo a vetro a 2 è mantenuta costante, 0, 05916 log a 2 può essere inglobato nella costante L.
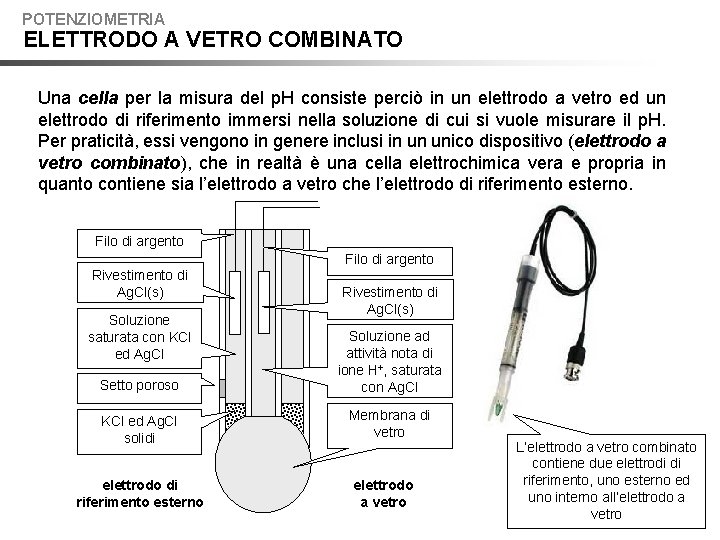
POTENZIOMETRIA ELETTRODO A VETRO COMBINATO Una cella per la misura del p. H consiste perciò in un elettrodo a vetro ed un elettrodo di riferimento immersi nella soluzione di cui si vuole misurare il p. H. Per praticità, essi vengono in genere inclusi in un unico dispositivo (elettrodo a vetro combinato), che in realtà è una cella elettrochimica vera e propria in quanto contiene sia l’elettrodo a vetro che l’elettrodo di riferimento esterno. Filo di argento Rivestimento di Ag. Cl(s) Soluzione saturata con KCl ed Ag. Cl Rivestimento di Ag. Cl(s) Setto poroso Soluzione ad attività nota di ione H+, saturata con Ag. Cl KCl ed Ag. Cl solidi Membrana di vetro elettrodo di riferimento esterno elettrodo a vetro L’elettrodo a vetro combinato contiene due elettrodi di riferimento, uno esterno ed uno interno all’elettrodo a vetro
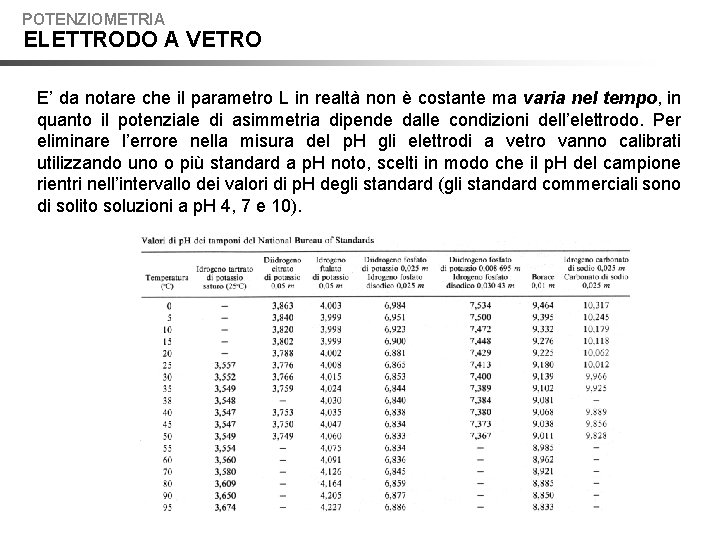
POTENZIOMETRIA ELETTRODO A VETRO E’ da notare che il parametro L in realtà non è costante ma varia nel tempo, in quanto il potenziale di asimmetria dipende dalle condizioni dell’elettrodo. Per eliminare l’errore nella misura del p. H gli elettrodi a vetro vanno calibrati utilizzando uno o più standard a p. H noto, scelti in modo che il p. H del campione rientri nell’intervallo dei valori di p. H degli standard (gli standard commerciali sono di solito soluzioni a p. H 4, 7 e 10).
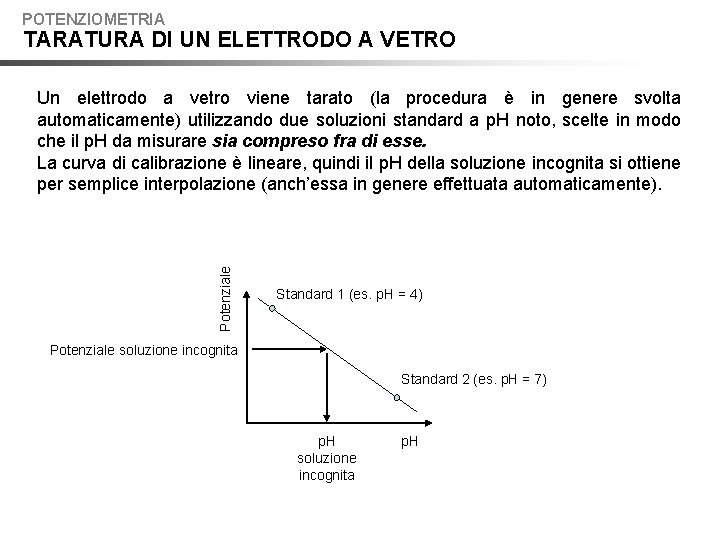
POTENZIOMETRIA TARATURA DI UN ELETTRODO A VETRO Potenziale Un elettrodo a vetro viene tarato (la procedura è in genere svolta automaticamente) utilizzando due soluzioni standard a p. H noto, scelte in modo che il p. H da misurare sia compreso fra di esse. La curva di calibrazione è lineare, quindi il p. H della soluzione incognita si ottiene per semplice interpolazione (anch’essa in genere effettuata automaticamente). Standard 1 (es. p. H = 4) Potenziale soluzione incognita Standard 2 (es. p. H = 7) p. H soluzione incognita p. H

Nonostante la misurazione del p. H sia forse la più comune in campo chimico, essa è soggetta a numerosi tipi di limitazioni. • L'errore alcalino. L'elettrodo a vetro ordinario diventa sensibile agli ioni di metalli alcalini e dà letture basse a valori di p. H maggiori di 9. • L'errore acido. I valori registrati dall'elettrodo a vetro tendono ad essere un po' alti quando il p. H è inferiore a circa 0. 5. • La disidratazione. Una membrana irregolare prestazione dell'elettrodo. disidratata può provocare una • La forza ionica insufficiente. Si è trovato che errori significativi (di 1 o 2 unità di p. H) possono verificarsi quando il p. H di campioni a bassa forza ionica, come l'acqua di lago o di torrente, viene misurato con un sistema di elettrodi vetro/calomelano. È stato dimostrato che la fonte primaria di tali errori è l’irriproducibilità dei potenziali di giunzione. • Il p. H dei tamponi standard. Qualsiasi imprecisione nella preparazione del tampone usato per la calibrazione o qualsiasi cambiamento nella sua composizione durante la conservazione provoca un errore nelle successive misure del p. H. L'azione dei batteri sui componenti di un tampone organico costituisce una comune causa di deterioramento.

POTENZIOMETRIA ELETTRODO A VETRO • La precisione e l’accuratezza della misura di p. H non possono comunque essere maggiori di quelle con le quali sono noti i p. H degli standard usati per la taratura (tipicamente 0, 01 unità di p. H) • L’accuratezza della misura è limitata dalla presenza dei potenziali di giunzione: se la composizione ionica dell’analita è diversa da quella degli standard il potenziale di giunzione varierà. Questo determina una incertezza aggiuntiva nella misura pari ad almeno 0, 01 unità di p. H • In soluzioni fortemente basiche ad elevata concentrazione di ioni Na+ l’elettrodo risponde anche allo ione sodio, dando un valore apparente di p. H inferiore a quello reale (errore alcalino) • Per ragioni non completamente chiarite, in soluzioni molto acide il p. H misurato è superiore a quello reale (errore acido) • Il raggiungimento dell’equilibrio fra la membrana di vetro e la soluzione non è istantaneo: il tempo richiesto può variare da pochi secondi per soluzioni ben tamponate ad alcuni muniti per soluzioni con bassa forza ionica • Gli elettrodi non conservati in acqua si disidratano e richiedono alcune ore di immersione prima di rispondere correttamente allo ione H+ • La taratura dell’elettrodo deve essere eseguita alla stessa temperatura alla quale si effettua la misura del p. H
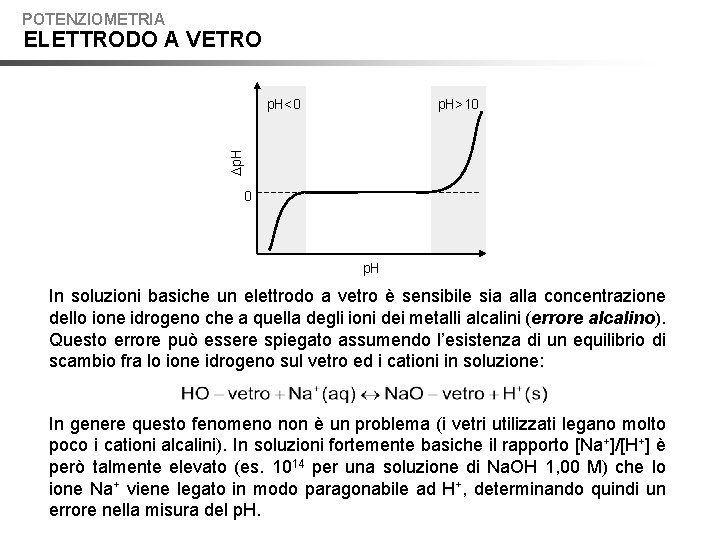
POTENZIOMETRIA ELETTRODO A VETRO p. H>10 Dp. H<0 0 p. H In soluzioni basiche un elettrodo a vetro è sensibile sia alla concentrazione dello ione idrogeno che a quella degli ioni dei metalli alcalini (errore alcalino). Questo errore può essere spiegato assumendo l’esistenza di un equilibrio di scambio fra lo ione idrogeno sul vetro ed i cationi in soluzione: In genere questo fenomeno non è un problema (i vetri utilizzati legano molto poco i cationi alcalini). In soluzioni fortemente basiche il rapporto [Na+]/[H+] è però talmente elevato (es. 1014 per una soluzione di Na. OH 1, 00 M) che lo ione Na+ viene legato in modo paragonabile ad H+, determinando quindi un errore nella misura del p. H.

TITOLAZIONI POTENZIOMETRICHE Le titolazioni potenziometriche sono eseguite misurando il potenziale di un elettrodo reversibile ad un certo analita durante la sua titolazione con un opportuno reagente. Si può quindi costruire direttamente la curva Potenziale/Volume di titolante. Le titolazioni potenziometriche forniscono dati più attendibili di quelli forniti dalle titolazioni che usano indicatori chimici, e sono inevitabili quando si devono eseguire in soluzioni colorate o torbide e per ricercare la presenza di specie insospettate. Queste titolazioni sono anche facilmente automatizzabili. Le titolazioni potenziometriche manuali, d'altro canto, hanno lo svantaggio di essere più lunghe di quelle che coinvolgono gli indicatori. 43
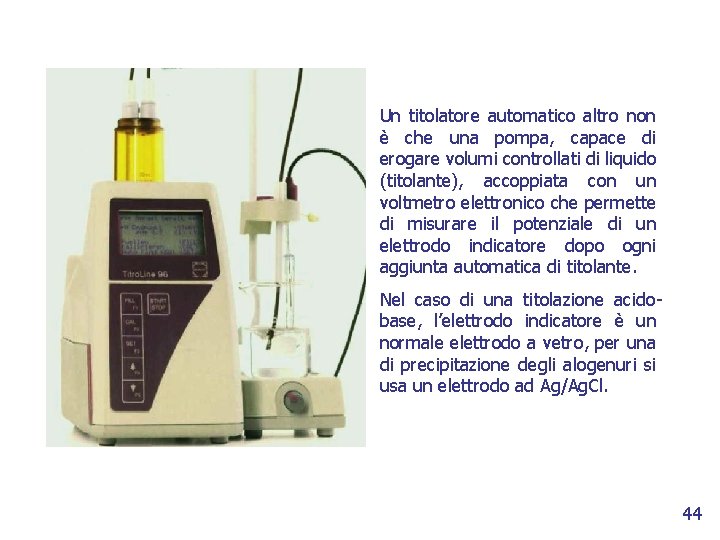
Un titolatore automatico altro non è che una pompa, capace di erogare volumi controllati di liquido (titolante), accoppiata con un voltmetro elettronico che permette di misurare il potenziale di un elettrodo indicatore dopo ogni aggiunta automatica di titolante. Nel caso di una titolazione acidobase, l’elettrodo indicatore è un normale elettrodo a vetro, per una di precipitazione degli alogenuri si usa un elettrodo ad Ag/Ag. Cl. 44
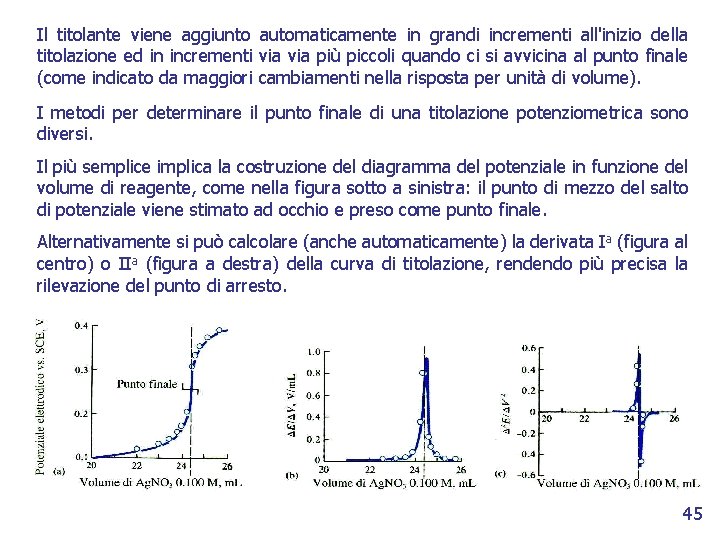
Il titolante viene aggiunto automaticamente in grandi incrementi all'inizio della titolazione ed in incrementi via più piccoli quando ci si avvicina al punto finale (come indicato da maggiori cambiamenti nella risposta per unità di volume). I metodi per determinare il punto finale di una titolazione potenziometrica sono diversi. Il più semplice implica la costruzione del diagramma del potenziale in funzione del volume di reagente, come nella figura sotto a sinistra: il punto di mezzo del salto di potenziale viene stimato ad occhio e preso come punto finale. Alternativamente si può calcolare (anche automaticamente) la derivata Ia (figura al centro) o IIa (figura a destra) della curva di titolazione, rendendo più precisa la rilevazione del punto di arresto. 45

TITOLAZIONE POTENZIOMETRICA Materiale occorrente 1 - piaccametro (millivoltmetro) 2 - elettrodo combinato 3 - termometro 4 - buretta 5 - ancoretta magnetica 6 - agitatore magnetico

Come eseguire una titolazione potenziometrica in pratica 1 - La soluzione da titolare se troppo concentrata (>1 M) va diluita e posta in un becher con ancoretta magnetica 2 - Titolare con una soluzione a titolo noto con l’ausilio di una buretta azzerata 3 - La parte sensibile dell’elettrodo indicatore deve essere completamente immerso nella soluzione senza toccare le pareti del recipiente 4 - La soluzione deve essere mantenuta in agitazione senza creare turbolenze 5 - Effettuare aggiunte cospicue (0. 5 -2 ml) di titolante fino a 1 -2 ml prima del previsto punto equivalente (viraggio) 6 - Dopo ogni aggiunta di titolante assicurarsi che il sistema abbia raggiunto l’equilibrio 7 - Dopo ogni aggiunta di titolante registrare il volume totale di titolante aggiunto e il valore di p. H o i m. V misurati 8 - Nell’intervallo di viraggio, l’aggiunta di titolante deve essere tanto più piccola quanto più ripida è la curva di titolazione 9 - Effettuare aggiunte cospicue (0. 5 -2 ml) di titolante dopo il viraggio. Non è necessario tarare il piaccametro con soluzioni tampone perché il punto equivalente è individuato dalla variazione relativa del p. H
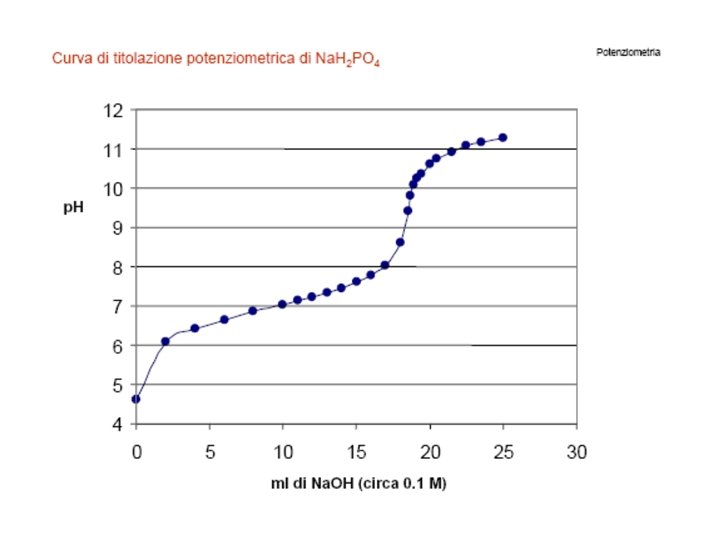
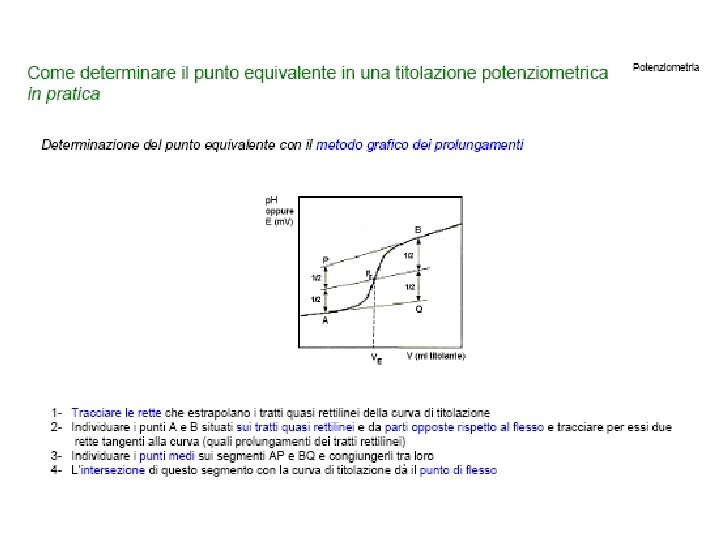
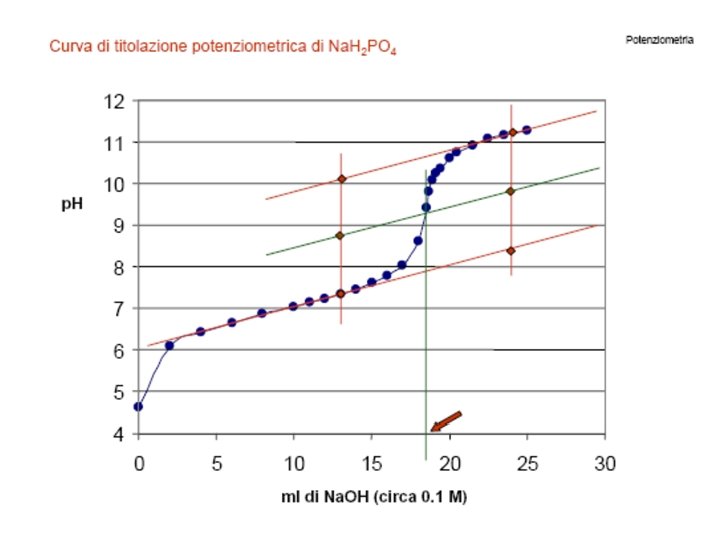


Applicazione analitica dei sensori potenziometrici MODO 1: applicazione diretta dell’equazione di Nernst: misura di Ecell e calcolo diretto della concentrazione non molto accurato: il comportamento dell’elettrodo dovrebbe essere ideale e note tutte le sue proprietà raramente si usa in questo modo diretto MODO 2: potenziometria di punto nullo usare due elettrodi indicatori per la stessa semireazione una semireazione nota e l’altra incognita variare la concentrazione nota fino a che Ecell = 0 questo metodo elimina problemi relativi all’attività degli analiti, ma richiede molto tempo di operazione.

MODO 3: metodo della retta di taratura misurare una serie di standard e produrre una retta di taratura. usare curve del segnale in funzione del log [C] interpolare il valore del segnale dell’analita MODO 4: metodo dell’aggiunta standard ISE presentano problemi a basse concentrazioni: tempi lunghi per raggiungere l’equilibrio grande errore relativo Il metodo dell’aggiunta standard minimizza questi problemi.
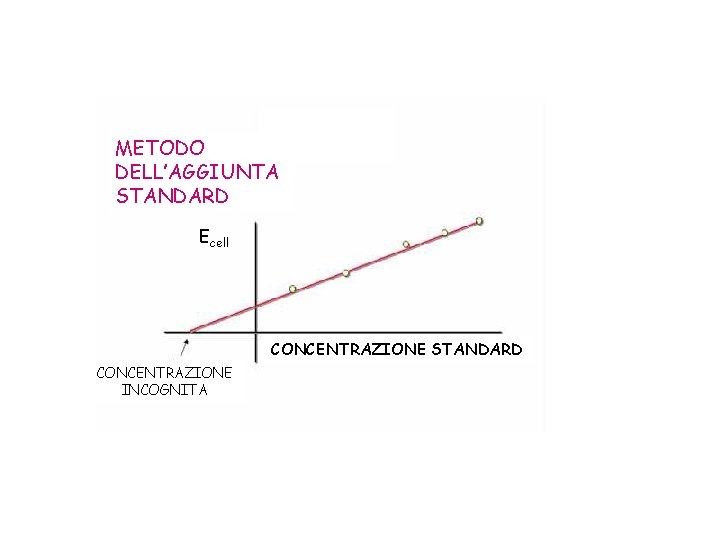
METODO DELL’AGGIUNTA STANDARD Ecell CONCENTRAZIONE STANDARD CONCENTRAZIONE INCOGNITA
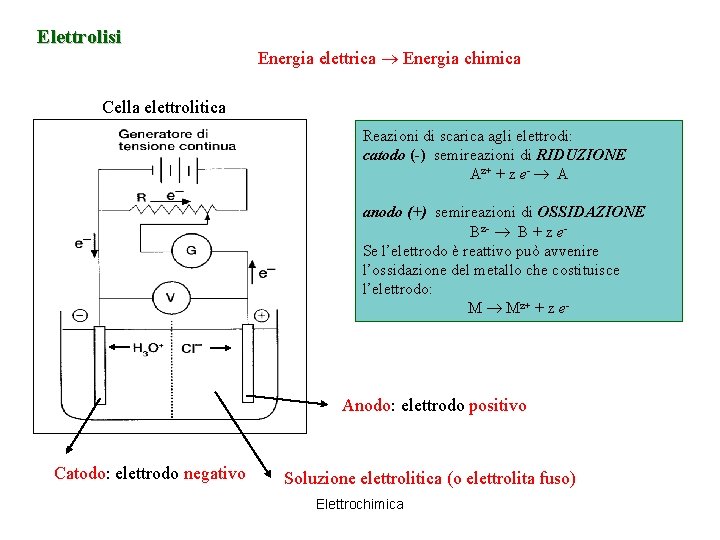
Elettrolisi Energia elettrica Energia chimica Cella elettrolitica Reazioni di scarica agli elettrodi: catodo (-) semireazioni di RIDUZIONE Az+ + z e- A anodo (+) semireazioni di OSSIDAZIONE Bz- B + z e. Se l’elettrodo è reattivo può avvenire l’ossidazione del metallo che costituisce l’elettrodo: M Mz+ + z e- Anodo: elettrodo positivo Catodo: elettrodo negativo Soluzione elettrolitica (o elettrolita fuso) Elettrochimica

Scarica delle specie agli elettrodi Difficilmente in una soluzione è presente una sola coppia redox. Allora, quale coppia si scarica per prima agli elettrodi? Al catodo si scarica per prima la coppia con in potenziale di riduzione più alto All’anodo si scarica per prima quella che ha il potenziale di riduzione più basso Spesso ci si basa sui valori di E° Fenomeni di SOVRATENSIONE possono invertire l’ordine di scarica Elettrochimica

Sovratensione La sovratensione ha origine cinetica Sovratensione di attivazione I processi elettrochimici sono notevolmente lenti e quindi spesso richiedono un’ aumento della tensione applicata Elettrodo sovratensione H 2 (V) Pt platinato 0. 05 Pt liscio 0. 67 Au 0. 80 Ag 1. 09 Cu 1. 25 Hg 1. 11 Grafite 1. 22 La sovratensione di H 2 è trascurabile solo su elettrodo di Pt platinato Elettrochimica

Elettrolisi dell’acqua corrente elettrica 2 H 2 O 2 H 2 (g) + O 2 (g) a) soluzione acida ([H 3 O+] >> 1, 00 10 -7 moli l-1) catodo (-) H 2 O anodo (+) 2 e- 2 H 3 O+ + 2 e- H 2 (g) + 2 3 H 2 O 1/2 O 2 (g) + 2 H 3 O+ + b) soluzione basica ([H 3 O+] << 1, 00 10 -7 moli l 1) catodo (-) anodo (+) 2 H 2 O + 2 e- H 2 (g) + 2 OH 4 OH- O 2 (g) + 2 H 2 O + 4 e- c) soluzione neutra ([H 3 O+] = 1, 00 10 -7 moli l-1) catodo (-) 2 H 2 O + 2 e- H 2 (g) + 2 OHanodo (+) 3 H 2 O 1/2 O 2 (g) + 2 H 3 O+ + 2 e. Elettrochimica

Elettrolisi di soluzioni Lo Zn può essere ottenuto per elettrolisi di soluzioni acquose di Zn. SO 4 (in presenza di H 2 SO 4 per acquose 2+ impedire l’idrolisi degli ioni Zn ). Come catodo si utilizza un elettrodo di Zn e come anodo un elettrodo di Pb: catodo (-) Zn : anodo (+) Pb : Zn 2+ + 2 e- Zn 3 H 2 O 1/2 O 2 (g) + 2 H 3 O+ + 2 e- Al catodo avviene la riduzione degli ioni Zn 2+ e non quella degli ioni H 3 O+ come dovrebbe essere in base ai valori di E° ( E°Zn 2+/Zn = - 0, 763 V), ciò è dovuto all’elevata sovratensione di H 2 sull’ elettrodo di Zn. All’anodo si ha l’ossidazione di H 2 O e non dello ione SO 42 - dato che: E°O 2/H 2 O = 1, 23 V; E°S 2 O 8/SO 42 -= 2, 01 V Elettrolisi di sali fusi Si utilizzano sali fusi per la produzione di metalli come Na, Mg, ecc. , (a causa dei loro potenziali di riduzione negativi non si possono usare soluzioni acquose perché si avrebbe la riduzione di acqua). Il Na si prepara per elettrolisi di un fuso costituito da Na. Cl (~40%) e Ca. Cl 2 (~60%) a 600 °C catodo (-) acciaio : anodo (+) grafite : Na+ + e- Na (l) 2 Cl- Cl 2 (g) + 2 e- Il Na (l) galleggia sul fuso e viene raccolto su kerosene per evitare il contatto con l’aria o l’umidità (il Na reagisce rapidamente con ossigeno e violentemente con acqua. Elettrochimica
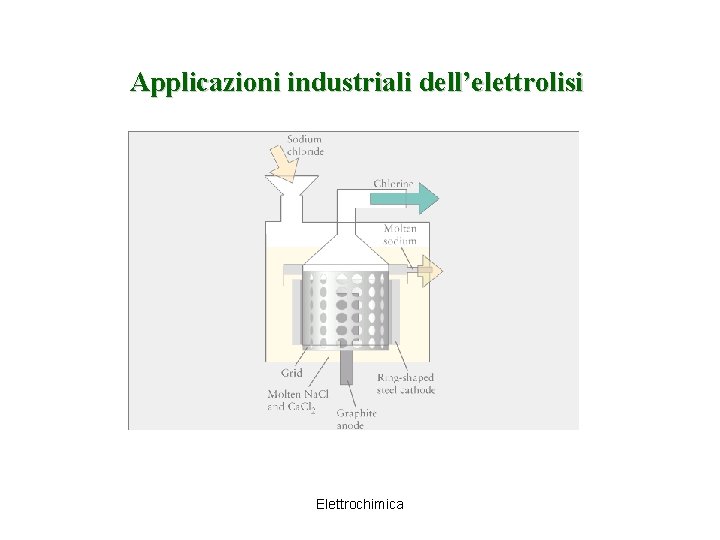
Applicazioni industriali dell’elettrolisi Elettrochimica

La corrosione dei metalli Insieme di fenomeni chimici che risultano nella degradazione di un metallo (peggioramento delle proprietà chimiche e fisiche). Alla base c’è sempre un processo di ossidazione del metallo che si corrode Corrosione di origine chimica: azione di sostanze come: CO, CO 2, SO 2, H 2 S, NH 3, H 2 SO 4, HNO 3, ecc. Corrosione dovuta alle correnti elettriche vaganti nel terreno; l’acqua e i sali funzionano come elettroliti, fenomeni di elettrolisi nei quali le strutture metalliche interrate fungono da elettrodi. Fenomeni di corrosione dovuti alla presenza contemporanea di ossigeno e acqua Elettrochimica

La corrosione dei metalli Elettrochimica

La corrosione dei metalli In generale, metalli con potenziale di riduzione molto alto resistono molto bene alla corrosione (Cu, E° = 0. 337 V; Au, E° = 1. 42 V) Alcuni metalli che hanno un potenziale di riduzione molto negativo (Al, E° = 1. 66 V; Ti, E° = - 0. 89 V; Cr, E° = - 0. 74 V) resistono meglio alla corrosione di altri metalli che hanno un E° molto meno negativo (Fe, E° = - 0. 45 V). Questo diverso comportamento è dovuto al fatto che questi metalli a contatto con l’atmosfera si ricoprono rapidamente, per inizio della corrosione, di un sottilissimo velo di ossido, molto aderente, insolubile che costituisce una barriera. Questo fenomeno è chiamato PASSIVAZIONE DEI METALLI Elettrochimica

La corrosione dei metalli Condizioni per la PASSIVAZIONE: • E° molto negativo, rapida corrosione iniziale del metallo; • formazione di uno strato molto sottile di ossido, insolubile e poco reattivo (barriera cinetica) • dimensioni reticolari dell’ossido poco diverse (10 -15%) da quelle del metallo: buona adesione tra strato di ossido e metallo. • Passivazione spontanea: migliore protezione contro la corrosione Elettrochimica

Corrosione galvanica Inclusioni di metalli più nobili (E° più alto) determinano la formazione di una pila chimica, e il metallo meno nobile passa in soluzione. Es. inclusioni di Cu (E° = 0, 337 V) nel Fe(E° = - 0. 45 V) (-) Anodo (Fe): Fe 2+ + 2 e- E° = - 0. 45 V (+) Catodo (Cu): O 2 + 4 e- + 2 H 2 O 4 OH- E° = 0. 401 V 2 Fe + 2 OH- Fe (OH)2 (s) Si sottraggono ioni Fe 2+ e di conseguenza se ne formano altri. L’inizio della precipitazione di Fe (OH)2 (s) segna l’inizio del processo di corrosione del Fe che così arruginisce 2 Fe (OH)2 (s) + 1/2 O 2 + H 2 O 2 Fe(OH)3 (s) Fe 2 O 3. H 2 O (s) + 2 H 2 O ossido di ferro (III) idrato: ruggine Elettrochimica
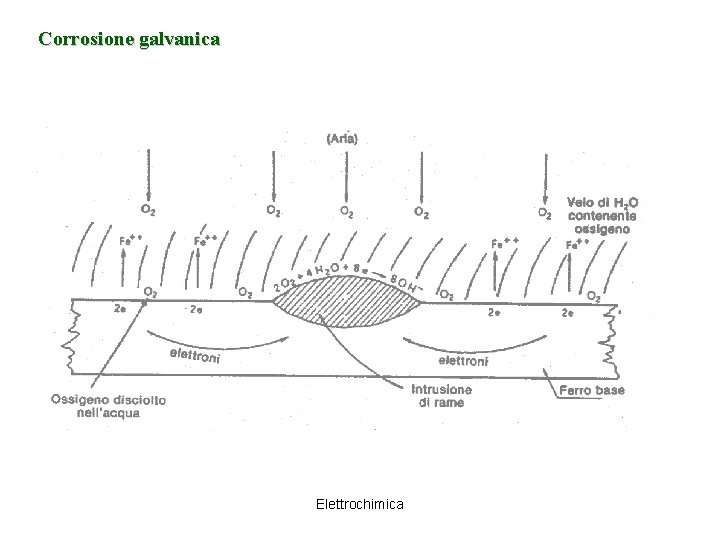
Corrosione galvanica Elettrochimica

Corrosione per aerazione differenziale E’ determinata da una diversa concentrazione di O 2 a contatto con una superficie metallica in presenza di un velo di umidità. Es: Superficie di Fe (purissimo) sulla quale in presenza di aria è stata deposta una goccia d’ acqua. Lo strato di acqua ai lati della goccia è più sottile di quello centrale e pertanto si ha una maggiore concentrazione di O 2 Si viene a creare una pila a concentrazione formata da due semielementi a O 2 + 2 H 2 O + 4 e- 4 OH- E= E° + 0, 0591 4 [O 2 ] Log [OH-]2 La zona dove [O 2] è maggiore funziona da catodo (estremità della goccia), mentre l’altra è l’anodo (zona centrale). Tuttavia, poiché E° O 2/OH--= 0. 401 V, all’anodo si ossida il Fe (E°Fe 2+/Fe = - 0, 44 V). Il prodotto è ancora l’ossido di Fe (III) idrato (ruggine) Elettrochimica
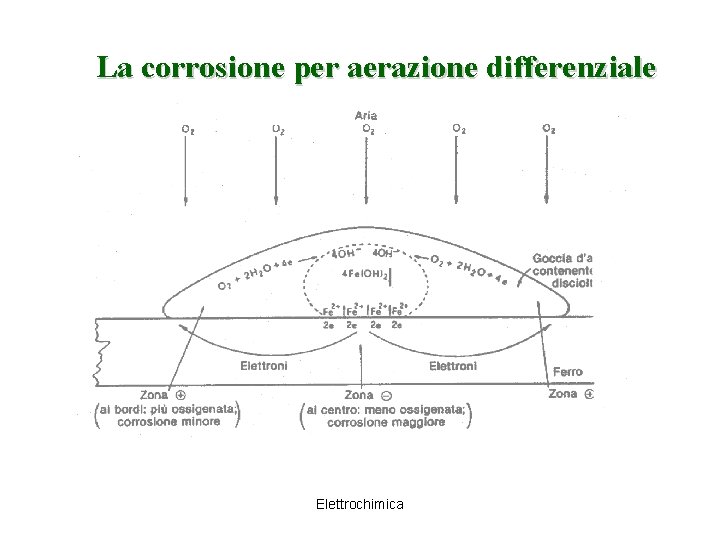
La corrosione per aerazione differenziale Elettrochimica

Riepilogo del meccanismo di corrosione Elettrochimica

Protezione dalla corrosione Esistono numerose tecniche per proteggere i metalli (Fe) dalla corrosione: �Rivestimenti con strati impermeabili (vernici, materie plastiche, vetro, ecc. ); lo strato non deve presentare difetti. �Elettrodeposizione: si forma un rivestimento con un metallo avente E° più negativo (Zn, Cr, Ni) che tende a passivarsi. Con metalli aventi E° maggiore del Fe, lo strato deve essere assolutamente continuo per evitare la corrosione galvanica. �Corrente impressa: L’oggetto di Fe da proteggere è collegato al polo (-) di una sorgente esterna di corrente continua mentre un altro blocco di lega ferrosa è collegato al polo (+). L’oggetto di Fe funziona da catodo di una cella elettrolitica e quindi non si ossida �Protezione catodica: L’oggetto di Fe viene collegato ad un altro metallo avente E° più negativo (es. Mg) che si comporta da anodo sacrificale ossidandosi al posto del Fe. Elettrochimica
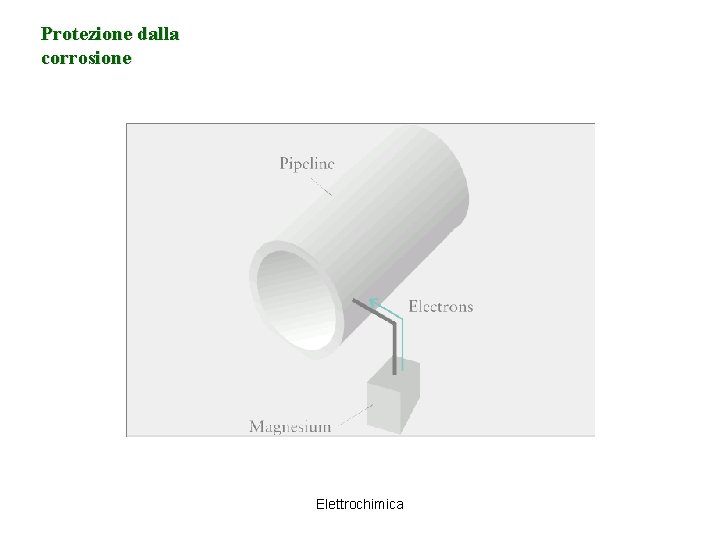
Protezione dalla corrosione Elettrochimica
- Slides: 71