TCNICAS DE CUANTIFICACIN DE MICROORGANISMOS TOTALES Microbiologa experimental

TÉCNICAS DE CUANTIFICACIÓN DE MICROORGANISMOS TOTALES § Microbiología experimental 2020 -1 § § Elaboró: Micro Exp. https: //www. facebook. com/profile. php? id=100010129183459 § Dudas y sugerencias en Inbox Micro Exp § Versión 3. 0.
z ¿Por qué cuantificar? § Expresar numéricamente una magnitud (RAE, 2015) § Uso de microorganismos como indicadores de calidad § Usos de microorganismos en procesos biotecnológicos= seguir un proceso

CLASIFICACIÓN DE MÉTODOS DE CUANTIFICACIÓN § z Métodos directos § § Métodos indirectos § § Determinan microorganismos vivos y muertos en una muestra Métodos para microorganismos viables § § Determinación de la actividad metabólica, biomasa y proteínas asociada al crecimiento microbiano Métodos para microorganismos totales § § Determinación del número de microorganismos en una muestra de manera directa (microscopía). Determina microorganismos vivos, capaces de replicarse Métodos para microorganismos viables pero no cultivables § Determina los microorganismos presentes en la muestra que son imposibles de cultivar en condiciones de laboratorio
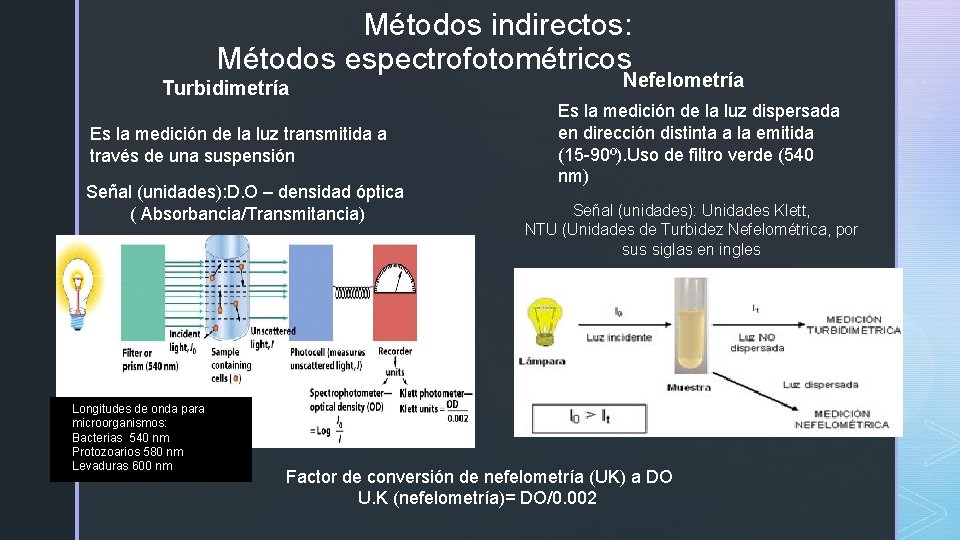
Métodos indirectos: Métodos espectrofotométricos Turbidimetría Es la medición de la luz transmitida a través de una suspensión Señal (unidades): D. O – densidad óptica ( Absorbancia/Transmitancia) Longitudes de onda para microorganismos: Bacterias 540 nm Protozoarios 580 nm Levaduras 600 nm Nefelometría Es la medición de la luz dispersada en dirección distinta a la emitida (15 -90º). Uso de filtro verde (540 nm) Señal (unidades): Unidades Klett, NTU (Unidades de Turbidez Nefelométrica, por sus siglas en ingles Factor de conversión de nefelometría (UK) a DO U. K (nefelometría)= DO/0. 002

CURVA ESTANDAR DE MC FARLAND § Tabla para la preparación de la curva de Mc Farland m. L 1% de Ba. Cl 2 m. L de Solución 1% H 2 SO 4 1 2 3 4 5 6 7 8 9 10 *Modificación de la tabla 2 NOM-181 -SSA 1 -1998

ACONDICIONAMIENTO DEL EQUIPO 1. En ambos equipos se recomienda encender la fuente de luz con anticipación 10 -15 min para asegurar una emisión constante de energía luminosa Nefelómetro: 2. Ajustar el blanco del método, coloca agua desionizada suficiente en la celda, 3. Introduce la celda y ajusta con el botón de autocero Espectrofotómetro: 2. Ajusta la longitud de onda a la que se realizará la medición, usualmente 600 nm para bacterias. 3. Ajustar el blanco del método, coloca agua desionizada suficiente en la celda, 3. Introduce la celda y ajusta con el botón de autocero
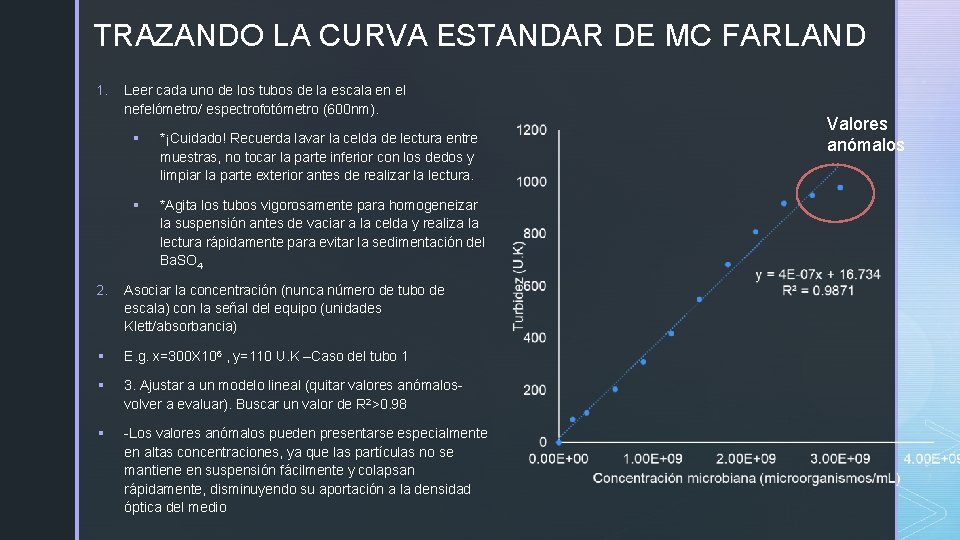
TRAZANDO LA CURVA ESTANDAR DE MC FARLAND 1. Leer cada uno de los tubos de la escala en el nefelómetro/ espectrofotómetro (600 nm). § *¡Cuidado! Recuerda lavar la celda de lectura entre muestras, no tocar la parte inferior con los dedos y limpiar la parte exterior antes de realizar la lectura. § *Agita los tubos vigorosamente para homogeneizar la suspensión antes de vaciar a la celda y realiza la lectura rápidamente para evitar la sedimentación del Ba. SO 4 2. Asociar la concentración (nunca número de tubo de escala) con la señal del equipo (unidades Klett/absorbancia) § E. g. x=300 X 106 , y=110 U. K –Caso del tubo 1 § 3. Ajustar a un modelo lineal (quitar valores anómalosvolver a evaluar). Buscar un valor de R 2>0. 98 § -Los valores anómalos pueden presentarse especialmente en altas concentraciones, ya que las partículas no se mantiene en suspensión fácilmente y colapsan rápidamente, disminuyendo su aportación a la densidad óptica del medio Valores anómalos
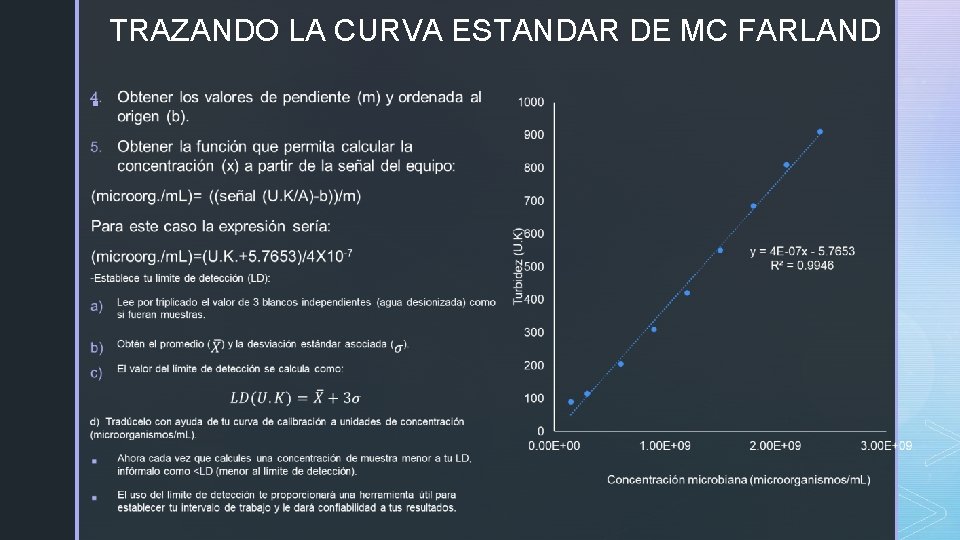
TRAZANDO LA CURVA ESTANDAR DE MC FARLAND §

EJEMPLO DE CÁLCULO PARA EL LÍMITE DE DETECCIÓN DETERMINACIÓN DE LÍMITE DE DETECCIÓN MEDIANTE EL USO DE BLANCOS § Blanco 1= 1 UK § Blanco 2= 0 UK § Blanco 3= 5 UK DETERMINACIÓN DE LÍMITE DE DETECCIÓN DE REGRESIÓN LINEAL Este método se basa en el análisis de la regresión lineal asociada a la curva, no requiere lectura de blancos, sin embargo, su valor puede estar sobreestimado Promedio=2 , D. E. =2. 65 LD (U. K)= 2+3(2. 65)= 9. 93 Traduciendo a concentración (microorganismo/m. L) LD (microorg. /m. L)=(9. 93. +5. 7653)/4 X 10 -7 )=40 X 107 § Por tanto, cualquier concentración calculada que de una concentración por debajo de este valor debe reportarse como <LD Toma en cuenta que el valor estimado con la regresión lineal es 4 veces mayor que el calculado con los blancos, sin embargo, puede ser una aproximación adecuada.

CALCULANDO LA CONCENTRACIÓN DE MICROORGANISMO EN UNA MUESTRA § Nefelómetría: z 2. Ajustar el blanco del método, introduce el tubo del matraz nefelométrico con medio estéril, sin inocular en la ranura del nefelómetro § 3. En equipos digitales, pulsa la tecla de “Lectura” /”Read. En equipos analógicos, girar la perilla hasta nivelar el señalamiento del lector. § § 4. Registra el resultado en bitácora en U. K. . § 5. Repite para cada tiempo de incubación/muestreo 6. Traduce con ayuda de la curva de Mc. Farland de U. K. a concentración UFC/m. L. § -eg. Si la muestra tuvo una señal de 450 UK, la concentración de microorganismos/m. L será : § (microorg. /m. L)= ((450+5. 7653)/4 X 10 -7))= 12 X 109 microorg. /m. L El informe debe realizarse con 2 cifras significativas, expresado en notación científica

VENTAJAS Y DESVENTAJAS § Método rápido de evaluación del crecimiento microbiano. § Permite realizar un seguimiento rápido de las cinéticas de crecimiento. DESVENTAJAS § No diferencia entre microorganismos vivos y muertos (método totales) § Microorganismos capsulados pueden presentar dificultades al ser evaluados (no homogéneo). § Metabolitos secundarios que aportan turbidez pueden interferir.
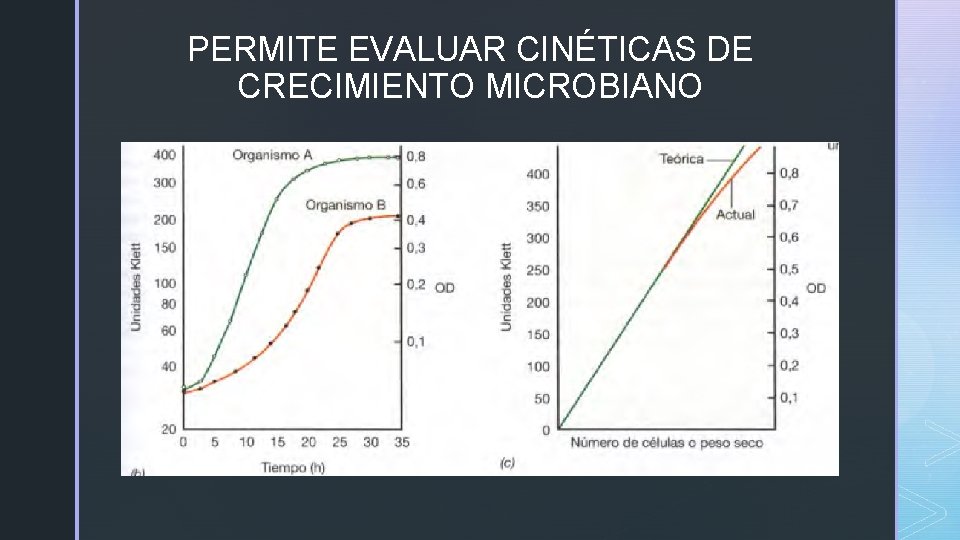
PERMITE EVALUAR CINÉTICAS DE CRECIMIENTO MICROBIANO
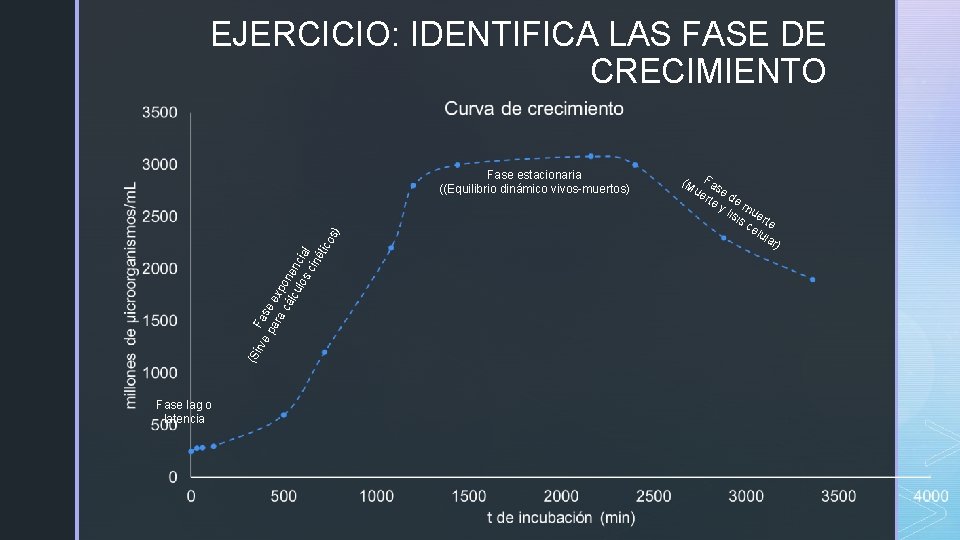
EJERCICIO: IDENTIFICA LAS FASE DE CRECIMIENTO (S irv Fa e p se ara ex cá pon lcu en los cia cin l éti co s) Fase estacionaria ((Equilibrio dinámico vivos-muertos) Fase lag o latencia (M Fas ue e rte de y l mu isi er s c te elu lar )
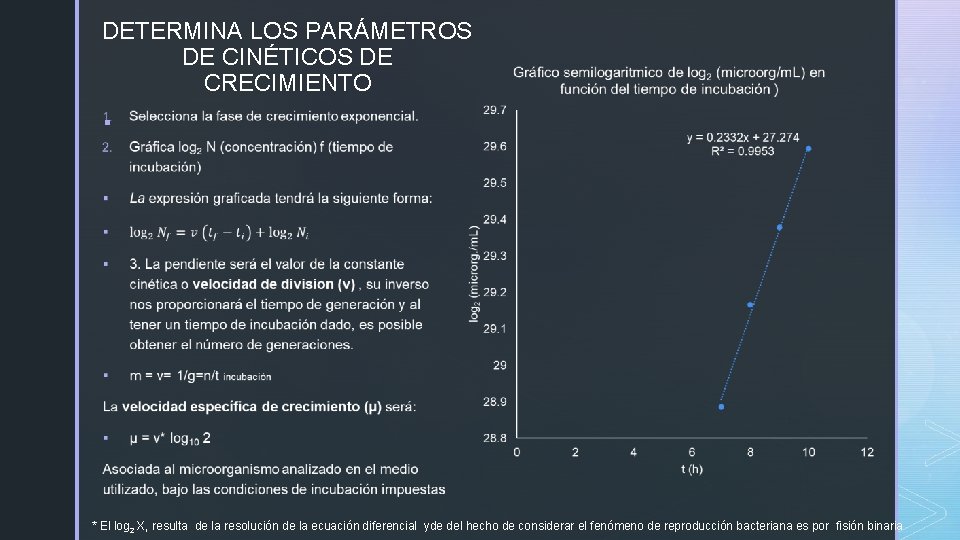
DETERMINA LOS PARÁMETROS DE CINÉTICOS DE CRECIMIENTO § * El log 2 X, resulta de la resolución de la ecuación diferencial yde del hecho de considerar el fenómeno de reproducción bacteriana es por fisión binaria
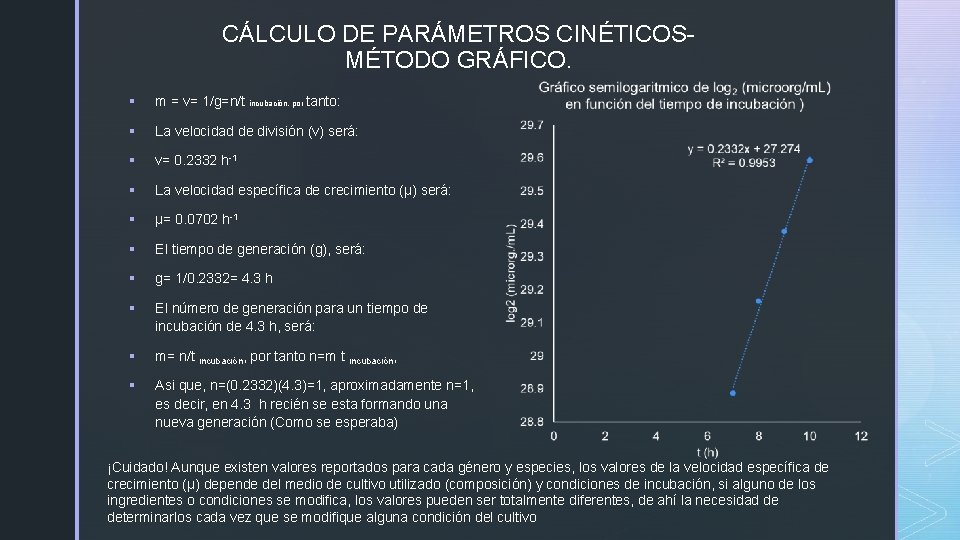
CÁLCULO DE PARÁMETROS CINÉTICOSMÉTODO GRÁFICO. § m = v= 1/g=n/t incubación, por tanto: § La velocidad de división (v) será: § v= 0. 2332 h-1 § La velocidad específica de crecimiento (µ) será: § µ= 0. 0702 h-1 § El tiempo de generación (g), será: § g= 1/0. 2332= 4. 3 h § El número de generación para un tiempo de incubación de 4. 3 h, será: § m= n/t incubación, por tanto n=m t incubación, § Asi que, n=(0. 2332)(4. 3)=1, aproximadamente n=1, es decir, en 4. 3 h recién se esta formando una nueva generación (Como se esperaba) ¡Cuidado! Aunque existen valores reportados para cada género y especies, los valores de la velocidad específica de crecimiento (µ) depende del medio de cultivo utilizado (composición) y condiciones de incubación, si alguno de los ingredientes o condiciones se modifica, los valores pueden ser totalmente diferentes, de ahí la necesidad de determinarlos cada vez que se modifique alguna condición del cultivo
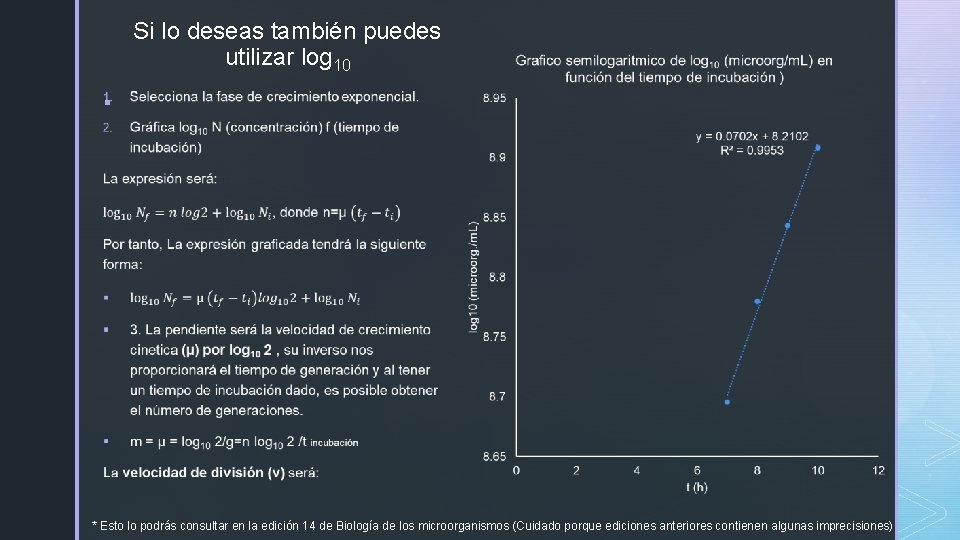
Si lo deseas también puedes utilizar log 10 § * Esto lo podrás consultar en la edición 14 de Biología de los microorganismos (Cuidado porque ediciones anteriores contienen algunas imprecisiones)
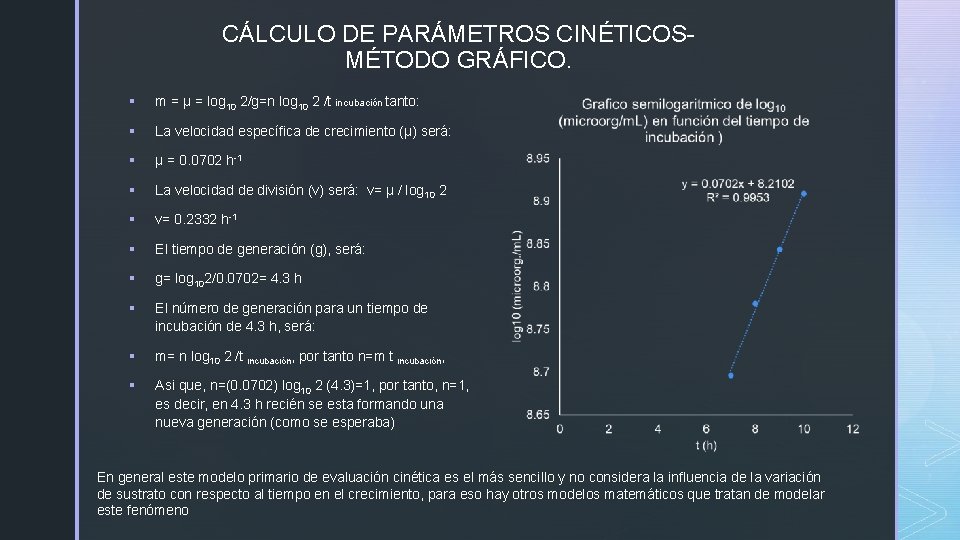
CÁLCULO DE PARÁMETROS CINÉTICOSMÉTODO GRÁFICO. § m = µ = log 10 2/g=n log 10 2 /t incubación tanto: § La velocidad específica de crecimiento (µ) será: § µ = 0. 0702 h-1 § La velocidad de división (v) será: v= µ / log 10 2 § v= 0. 2332 h-1 § El tiempo de generación (g), será: § g= log 102/0. 0702= 4. 3 h § El número de generación para un tiempo de incubación de 4. 3 h, será: § m= n log 10 2 /t incubación, por tanto n=m t incubación, § Asi que, n=(0. 0702) log 10 2 (4. 3)=1, por tanto, n=1, es decir, en 4. 3 h recién se esta formando una nueva generación (como se esperaba) En general este modelo primario de evaluación cinética es el más sencillo y no considera la influencia de la variación de sustrato con respecto al tiempo en el crecimiento, para eso hay otros modelos matemáticos que tratan de modelar este fenómeno
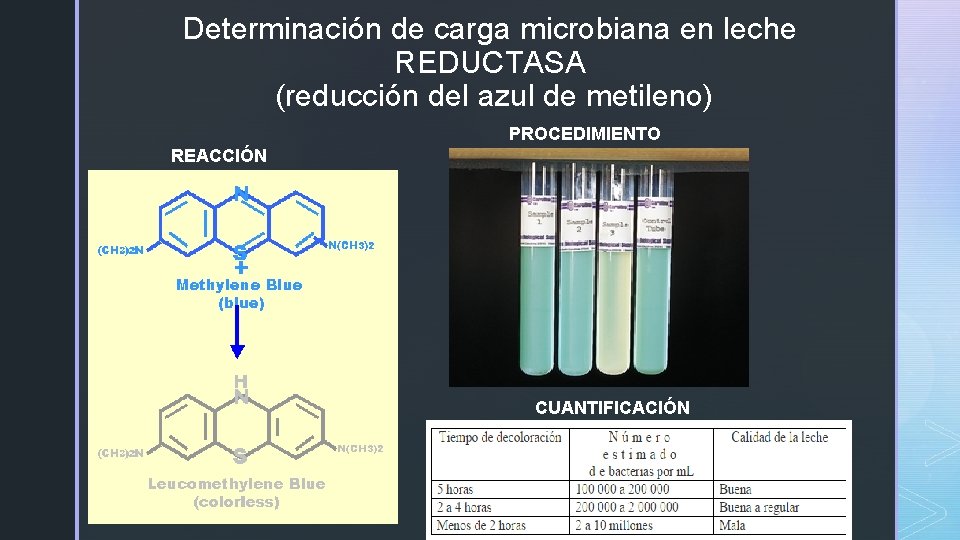
Determinación de carga microbiana en leche REDUCTASA (reducción del azul de metileno) PROCEDIMIENTO REACCIÓN CUANTIFICACIÓN
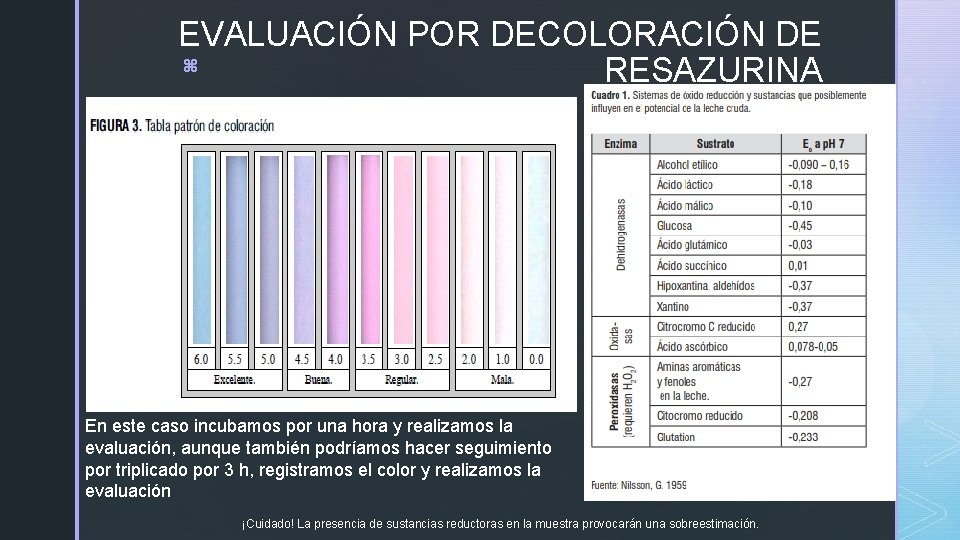
EVALUACIÓN POR DECOLORACIÓN DE z RESAZURINA En este caso incubamos por una hora y realizamos la evaluación, aunque también podríamos hacer seguimiento por triplicado por 3 h, registramos el color y realizamos la evaluación ¡Cuidado! La presencia de sustancias reductoras en la muestra provocarán una sobreestimación.

MÉTODOS DIRECTOS: RECUENTO MICROSCÓPICO Cuenta de Breed (Samuel C. Prescott y Robert S. Breed, 1910. Leche) Área de Extensión Am (µm 2) Área de campo Ac (µm 2) Tinción Observación a 100 x 10 campos (Promedio Ẋ) Cámara de Neubauer/ Cámara de Petroff- Hausser VENTAJAS Permite evaluar morfologías distintas. Permite evaluar movilidad Para ciertos microorganismos (moviles) puede ser un método de cuantificación de viables. DESVENTAJAS Presenta un sesgo por la presencia de asociaciones microbianas en muestras reales. En muestras con altas concentraciones el conteo no es confiable

PROBLEMA CUENTA DE BREED § Como parte de tu ejercicio profesional en 1. Conteo un laboratorio de análisis clínicos, se te de BAAR pide que de manera urgente determines la 3 concentración de BAAR y no BAAR en una 3 2 muestra de esputo procedente de un 2. Promedio de bacterias por campo=2. 6 BAAR/campo paciente con tuberculosis, para adecuar la 3. No de campos de observación sobre los que se realizó la dosis de antibiótico necesaria que debe extensión administrarse. Para lo cual, decides r campo=90 µm=0. 09 mm, por tanto, realizar su cuantificación por cuenta directa usando el método de Breed Acampo=3. 1416 X 0. 092 mm=0. 025 mm 2 § Para realizar la cuantificación, utilizas el objetivo de 100 x, que al calibrarlo da una longitud de 18 líneas de diámetro. La longitud de cada línea es de 10 µm. Tomas la muestra con un asa calibrada de 10 µL (0. 01 m. L), la esparces en un área de 10 mm X 15 mm, después de lo cual procedes a realizar una tinción BAAR y finalmente observas al microscopio, encontrando las siguientes observaciones por campo A inoculación=10 mm. X 15 mm=150 mm 2 No de campos=150/0. 025=6000 campos 3. Concentración bacteriana relacionando conteo de campos observados, campos sobre los que se realizó la extensión y volumen de extendido en m. L 4. Reportar con 2 cifras significativas y en notación científica.
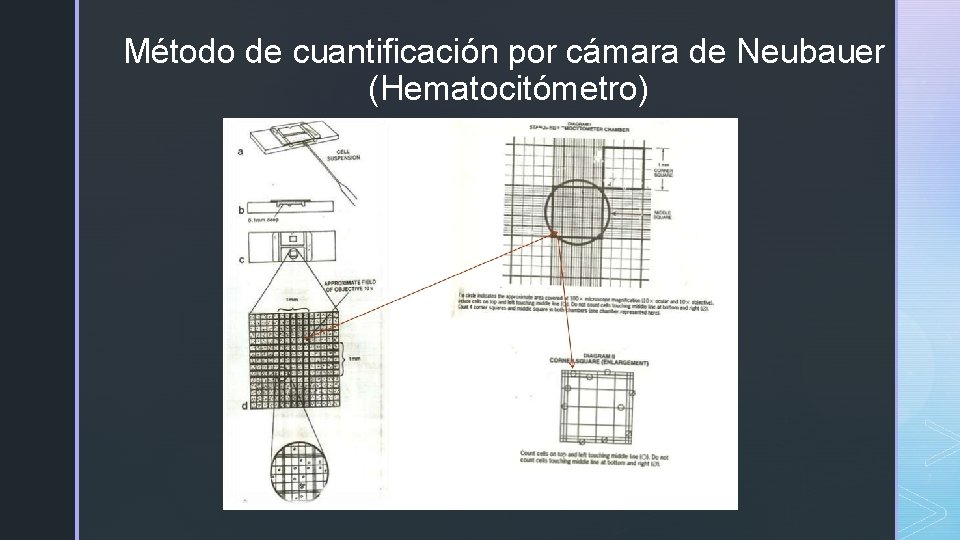
Método de cuantificación por cámara de Neubauer (Hematocitómetro)
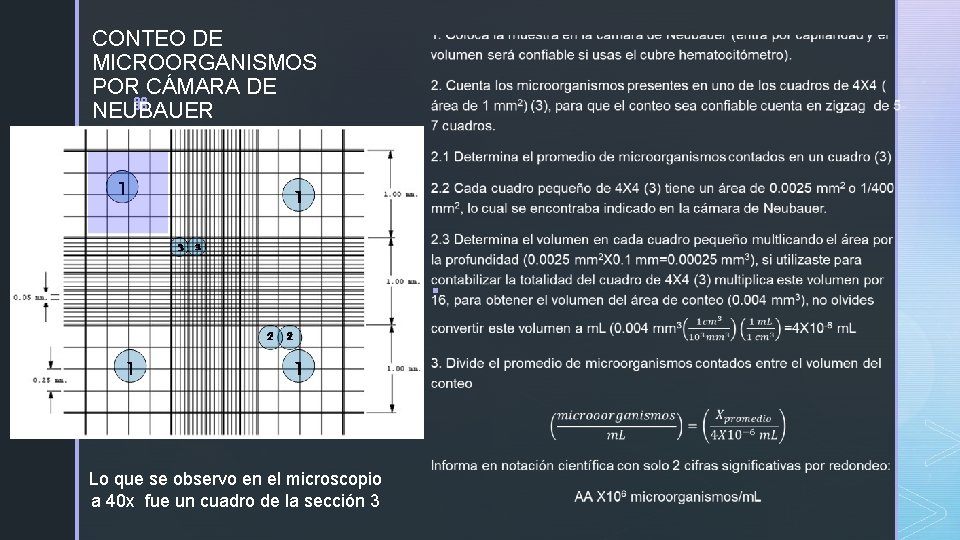
CONTEO DE MICROORGANISMOS POR CÁMARA DE z NEUBAUER § Lo que se observo en el microscopio a 40 x fue un cuadro de la sección 3
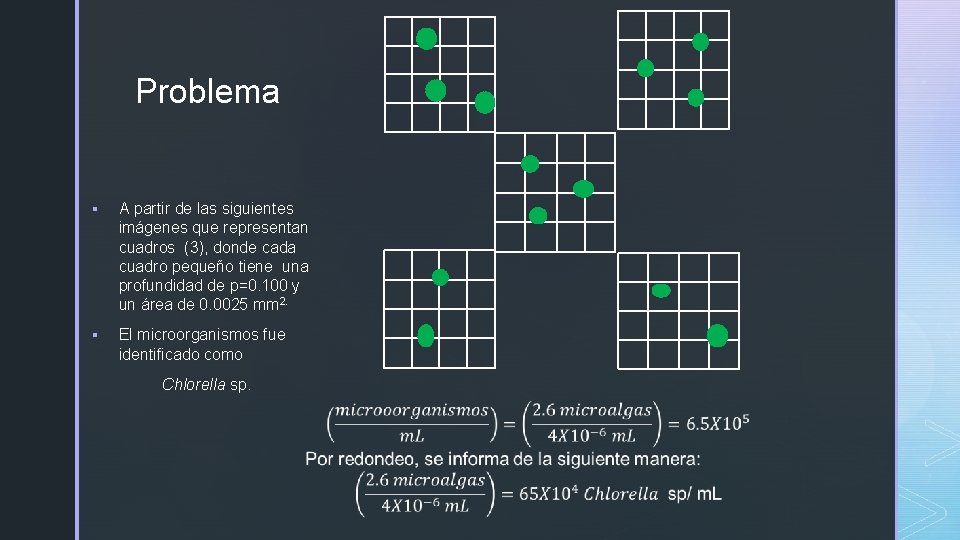
Problema § A partir de las siguientes imágenes que representan cuadros (3), donde cada cuadro pequeño tiene una profundidad de p=0. 100 y un área de 0. 0025 mm 2. § El microorganismos fue identificado como Chlorella sp.

z § MATERIAL DE APOYO La escala de Mc. Farland https: //www. youtube. com/watch? v=ch. Dt 1 f. CJm 3 k&fbclid=Iw. AR 2 CQCm_9 yvd 06 ow. V N 29 d-41 o. Jq. KJaai 2 m. OFae 9 fzq. LMHWZ 2 c. Dhcp. EAc. I 8 Y § Uso de la turbidimetría/densidad óptima para cuantificar https: //www. youtube. com/watch? v=bia_5 GFKV 3 E&fbclid=Iw. AR 1 UYUx_zgo 5 Dapbg ulxjjso 3 -SQTWWnt. M-yho 3_S 8 c_q. M 6 OS 1 Oq. YKODWEc § Recuento de microalgas por cámara de Neubauer https: //www. youtube. com/watch? v=29 W 913 Mn 2 ec&fbclid=Iw. AR 07 i 1 m. ICPsu 3610 l. H El 1 Qaf. OX 9 ia 5 N 5 KYv. Sxx. Ogb. Puux 0 Ykkl. OGnnj. B 528 § Método tiempo de decoloración azul de metileno-Reductasas https: //www. youtube. com/watch? v=E 9 w 1 IHRw 9 RY&fbclid=Iw. AR 01 Dv. N 5 hj_c. ZNp. L EZw. Q 7 Dnv. D 75 f. HXel. Q_8 Lm. Oo. R 4 U 8 GBS 84 i-z. Yf. VHG 8 m 8
- Slides: 25