Tcnicas de Biologia Molecular em Microbiologia Clnica TCNICAS

Técnicas de Biologia Molecular em Microbiologia Clínica TÉCNICAS DE AMPLIFICAÇÃO DE ÁCIDOS NUCLEICOS Prof. Doutor José Cabeda

Técnicas de amplificação de ácidos nucleicos PCR u Real Time PCR u NASBA/TMA u

PCR
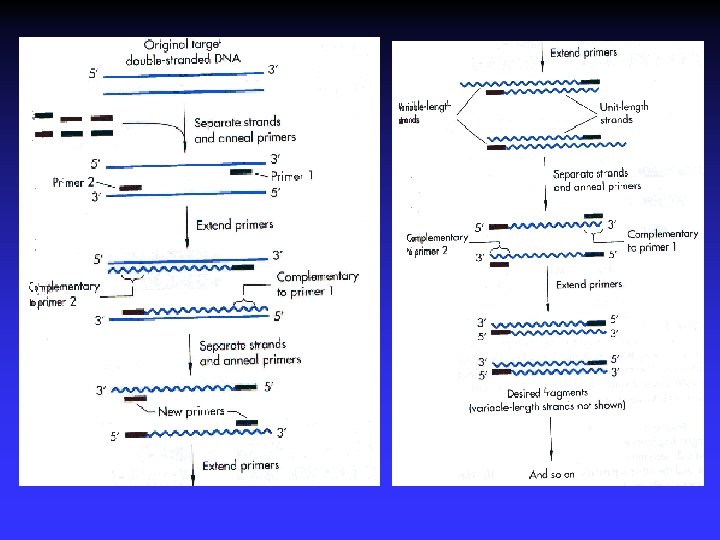
![OPTIMIZAÇÃO DO PCR [Mg. Cl 2] Th [d. NTP] [primers] [DNA] [inibidores] OPTIMIZAÇÃO DO PCR [Mg. Cl 2] Th [d. NTP] [primers] [DNA] [inibidores]](http://slidetodoc.com/presentation_image_h/2012b10c9c570451b7ec2d0d26dcb47d/image-5.jpg)
OPTIMIZAÇÃO DO PCR [Mg. Cl 2] Th [d. NTP] [primers] [DNA] [inibidores]

Variantes do PCR RT-PCR RT RNA Nested PCR 1º PCR 2º PCR c. DNA prod. ampl.
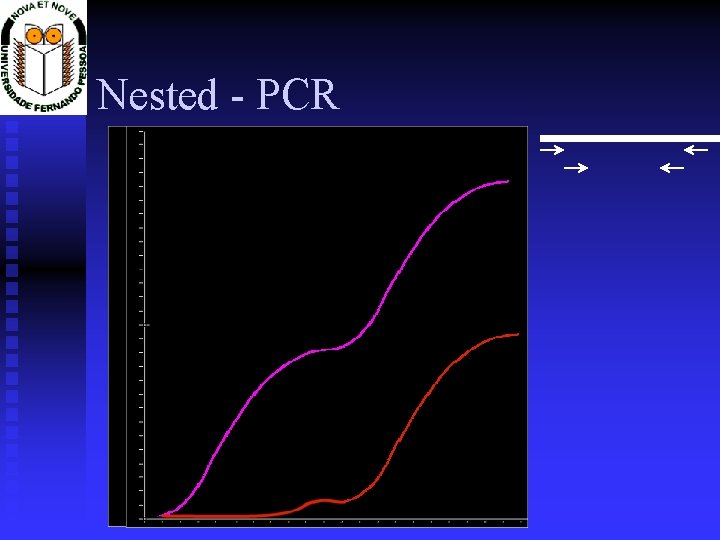
Nested - PCR
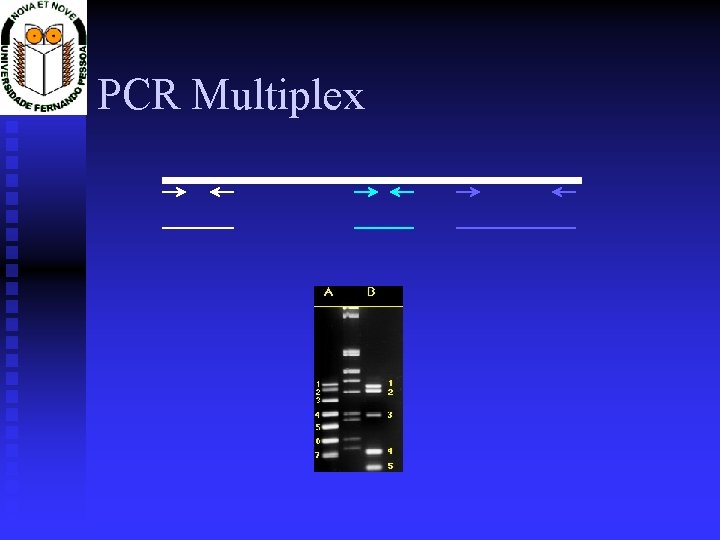
PCR Multiplex

Variantes do PCR RT-PCR Multiplex PCR Nested PCR Assymetric PCR Degenerate PCR Hot Start PCR In Situ PCR Long-PCR PCR-ELISA PCR-RFLP PCR-SSCP RAPD-PCR REP-PCR Touchdown PCR

Técnicas de amplificação de ácidos nucleicos PCR u Real Time PCR u NASBA/TMA u

Principio de funcionamento do Real-Time PCR Prof. Doutor José Cabeda
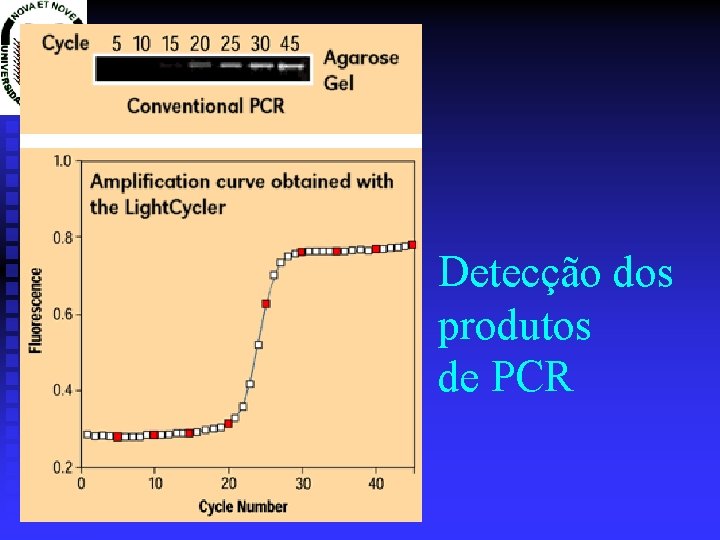
Detecção dos produtos de PCR

Montar uma reacção

Químicas Utilizáveis Prof. Doutor José Cabeda
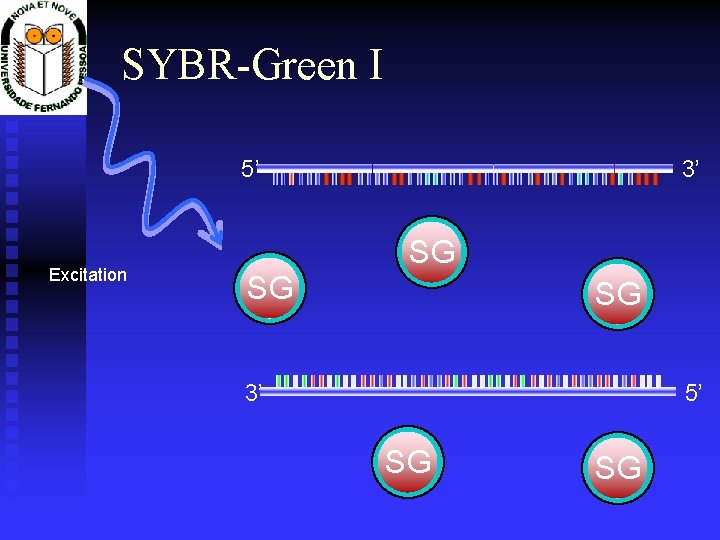
SYBR-Green I 3’ 5’ Excitation SG SG SG 3’ 5’ SG SG
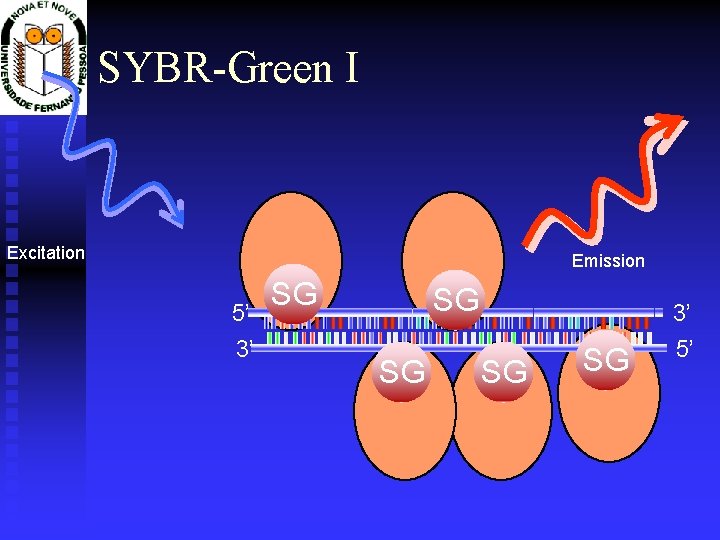
SYBR-Green I Excitation Emission 5’ 3’ SG SG SG 3’ 5’

Detcção com Syb. Green
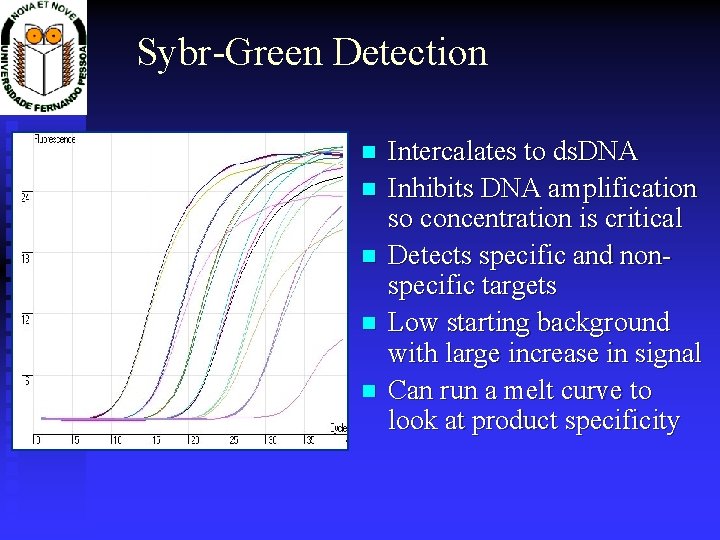
Sybr-Green Detection Intercalates to ds. DNA Inhibits DNA amplification so concentration is critical Detects specific and nonspecific targets Low starting background with large increase in signal Can run a melt curve to look at product specificity
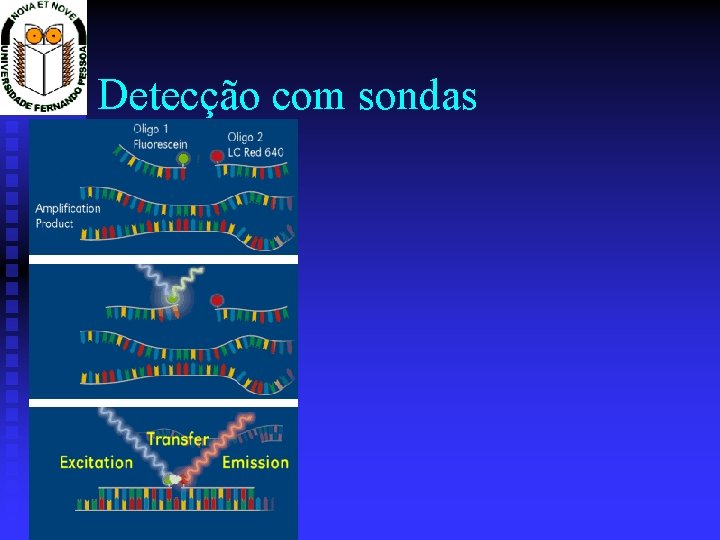
Detecção com sondas
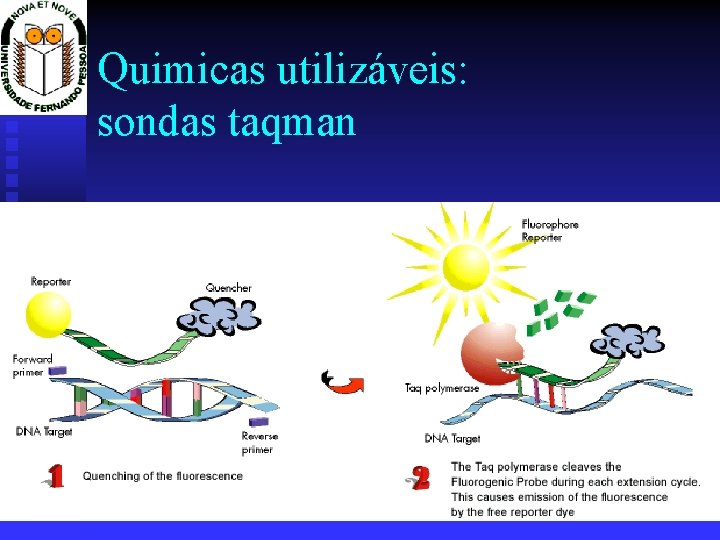
Quimicas utilizáveis: sondas taqman
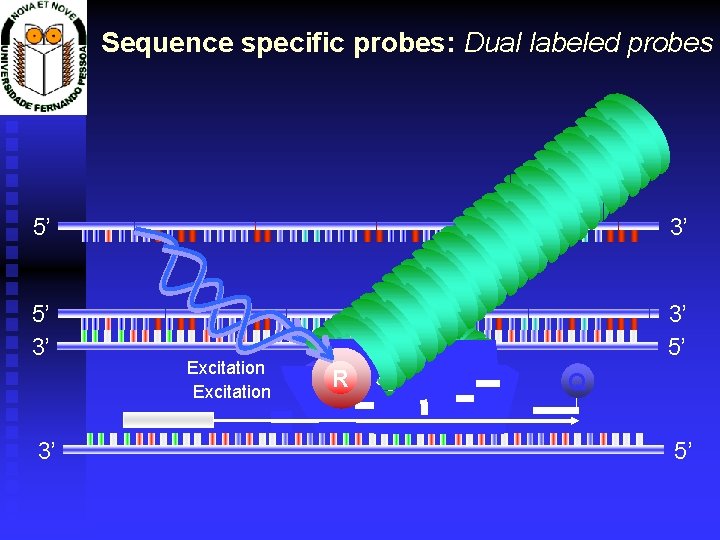
Sequence specific probes: Dual labeled probes 5’ 3’ 3’ 5’ RR R 3’ Excitation Q Q 5’
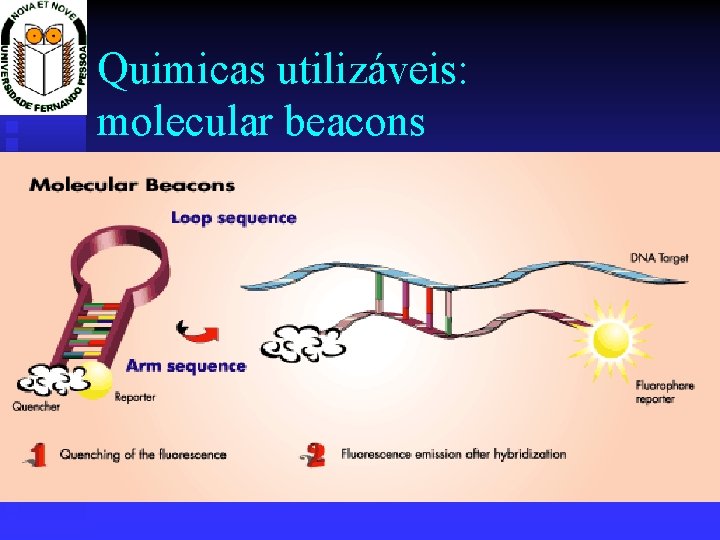
Quimicas utilizáveis: molecular beacons
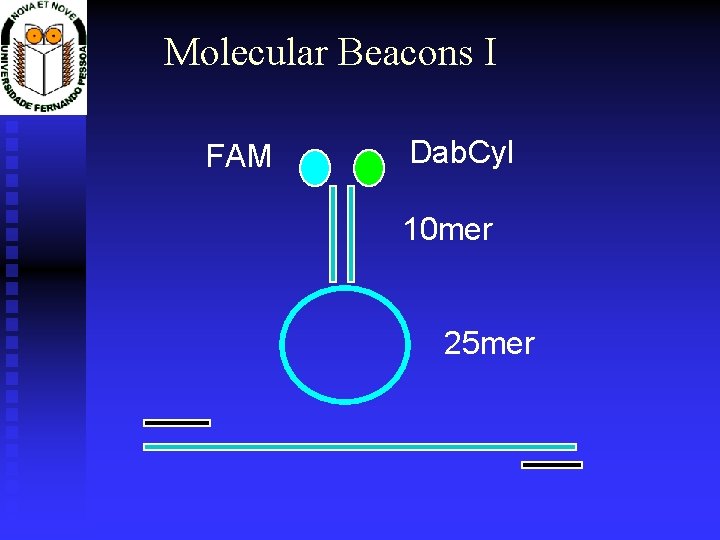
Molecular Beacons I FAM Dab. Cyl 10 mer 25 mer
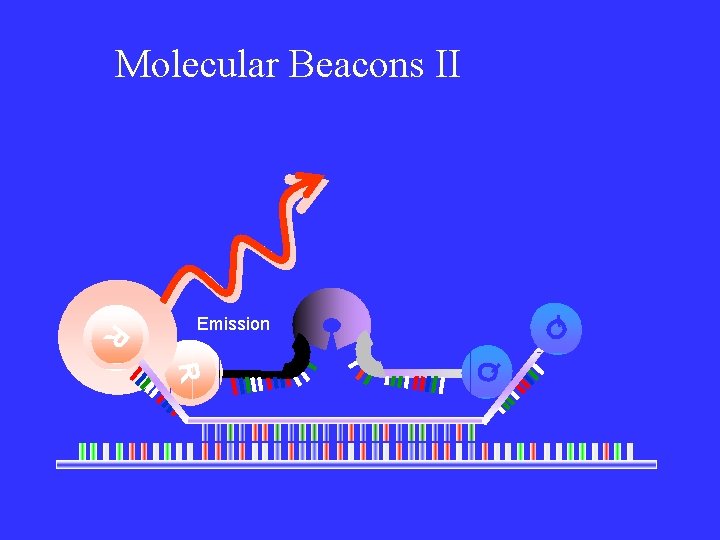
Molecular Beacons II Q Q R R Q R Excitation Emission

Molecular Beacons III Can be used to quantitation and mutation detection Need beacons for the normal and mutation sequence Design is difficult due to nature of folding structure Expensive when compared to FRET

Quimicas utilizáveis: sondas FRET
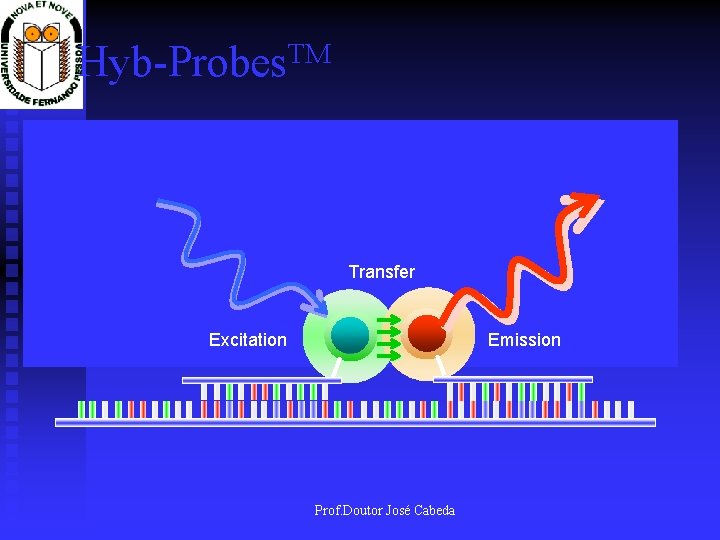
TM Hyb-Probes Oligo 1: Fluorescein Oligo 2: Quencher Transfer Excitation Emission Prof. Doutor José Cabeda

Quenched FRET analysis 5’ 3’ Two labeled probes, FAM at the 5’ and BH 1 on the 3’ When the probes hybridize the FAM energy is quenched by the BH 1 After the product is amplified run a melt curve to determine genotype Different melt points are seen for normal and mutation
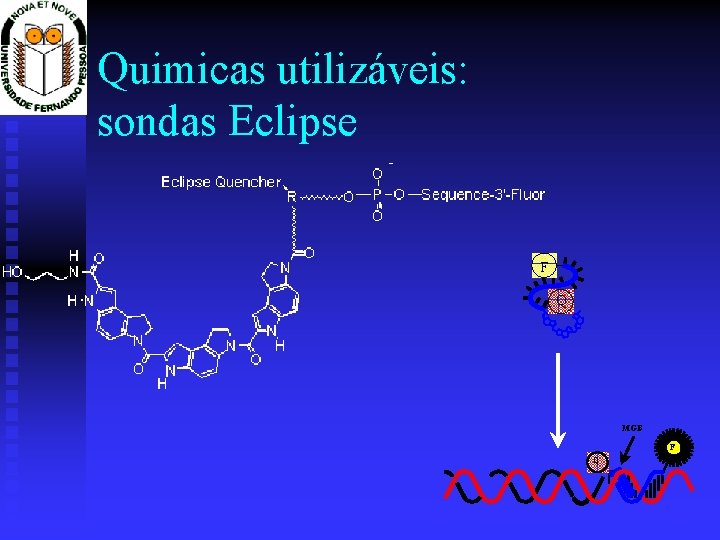
Quimicas utilizáveis: sondas Eclipse F Q MGB F Q

Aplicações Quantificação Prof. Doutor José Cabeda
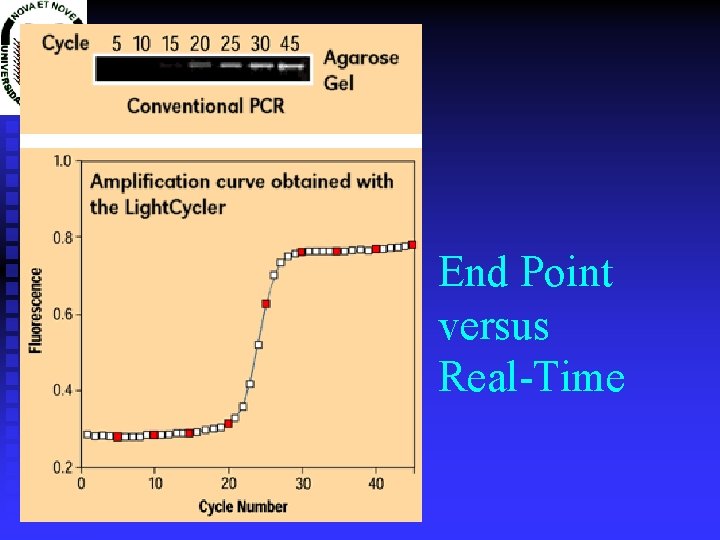
End Point versus Real-Time
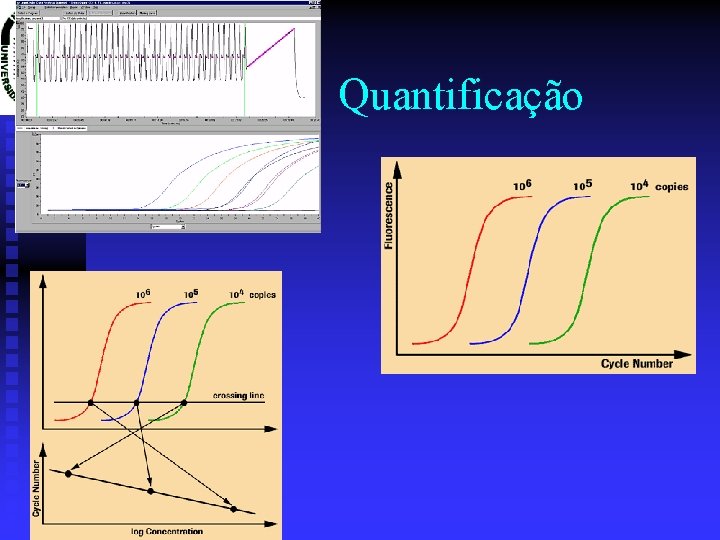
Quantificação

Aplicações Detecção de Mutações / SNP Prof. Doutor José Cabeda
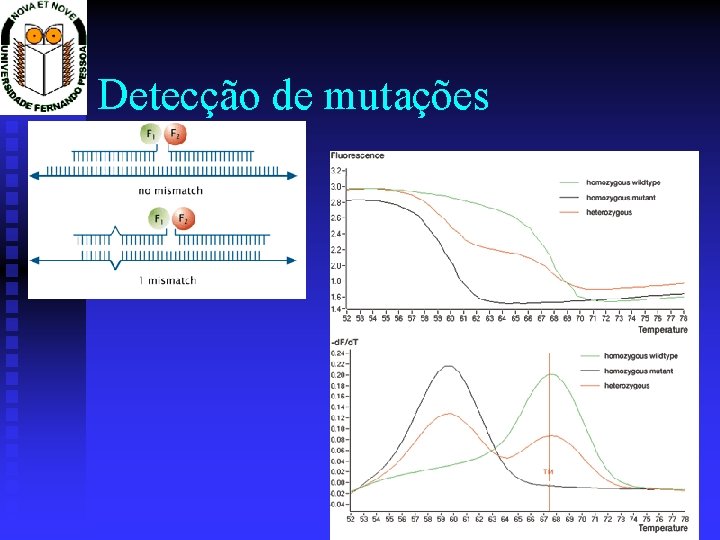
Detecção de mutações

Aplicações Multiplex Detection Prof. Doutor José Cabeda
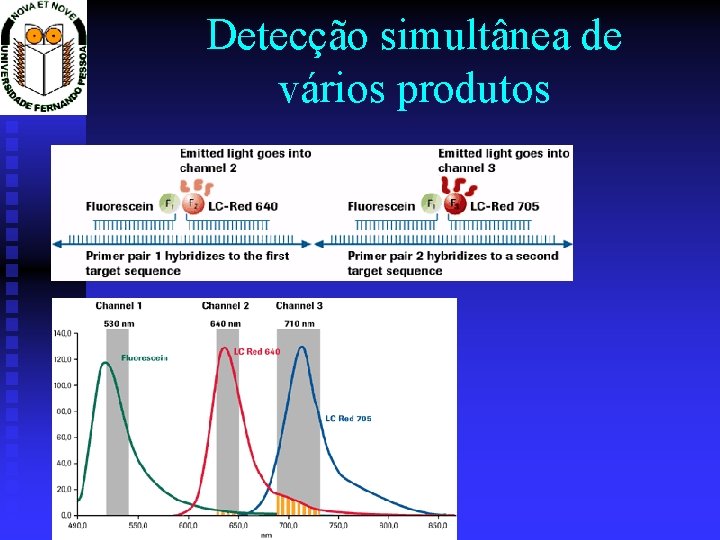
Detecção simultânea de vários produtos

Os equipamentos Prof. Doutor José Cabeda


Light. Cycler

Smart. Cycler

Rotorgene The samples spin continually during a run at 500 rpm The samples are heated and cooled in a low mass air oven Tubes are illuminated as they pass the detector On data acquisition energy is averaged over 20 revolutions to give the fluorescence of each sample Four Channels • • Ch 1: ex 470 nm, det 510 nm Ch 2: ex 530 nm, det 550 nm Ch 3: ex 585 nm, det 610 nm Ch 4: ex 625 nm, det 660 nm

Near Patient Testing Laboratório de Urgência

Técnicas de amplificação de ácidos nucleicos PCR u Real Time PCR u NASBA/TMA u
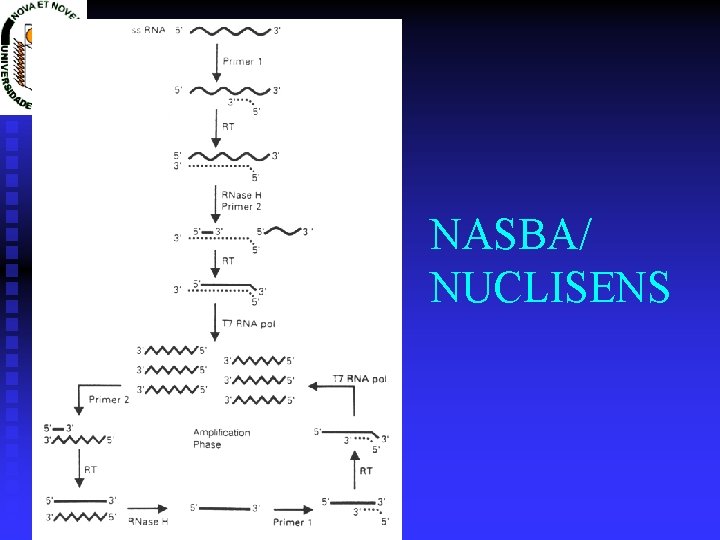
NASBA/ NUCLISENS
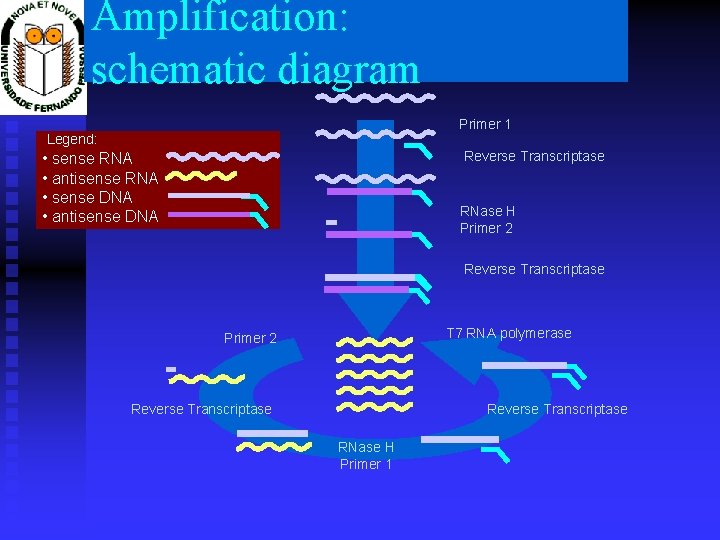
Amplification: schematic diagram Primer 1 Legend: Reverse Transcriptase • sense RNA • antisense RNA • sense DNA • antisense DNA RNase H Primer 2 Reverse Transcriptase T 7 RNA polymerase Primer 2 Reverse Transcriptase RNase H Primer 1

Técnicas de amplificação de Sinal b. DNA (Quantiplex)
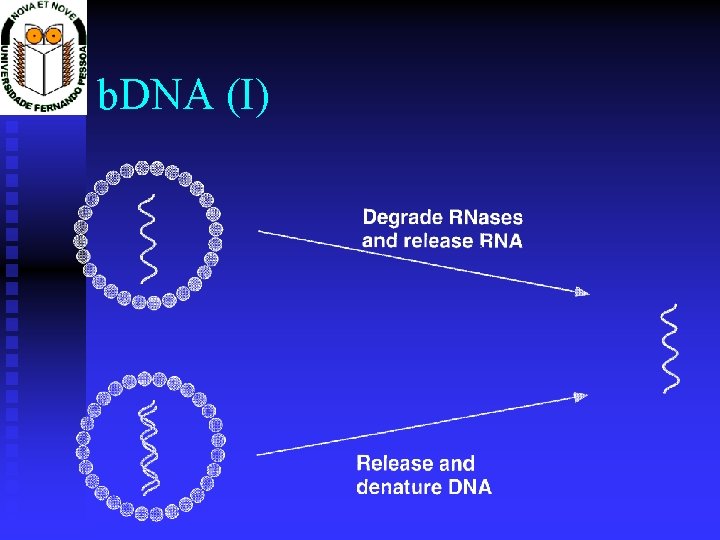
b. DNA (I)
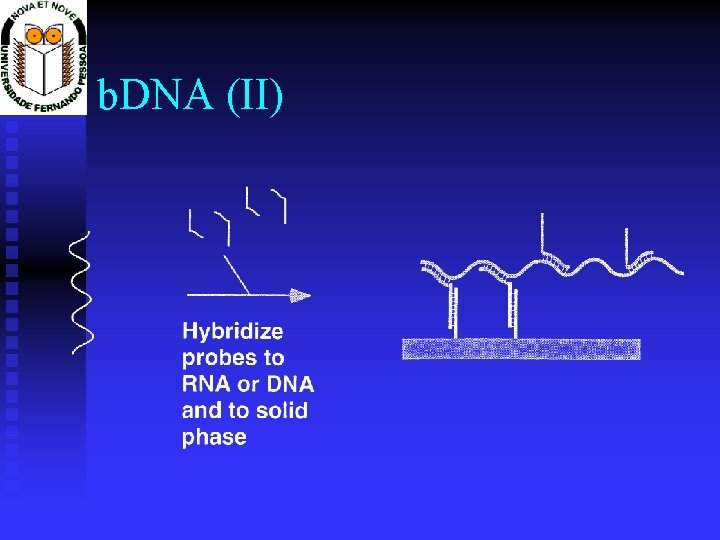
b. DNA (II)
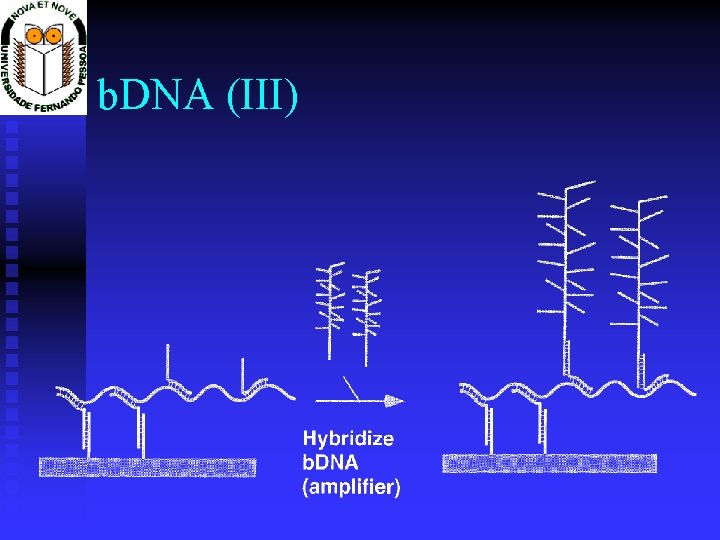
b. DNA (III)

b. DNA (IV)
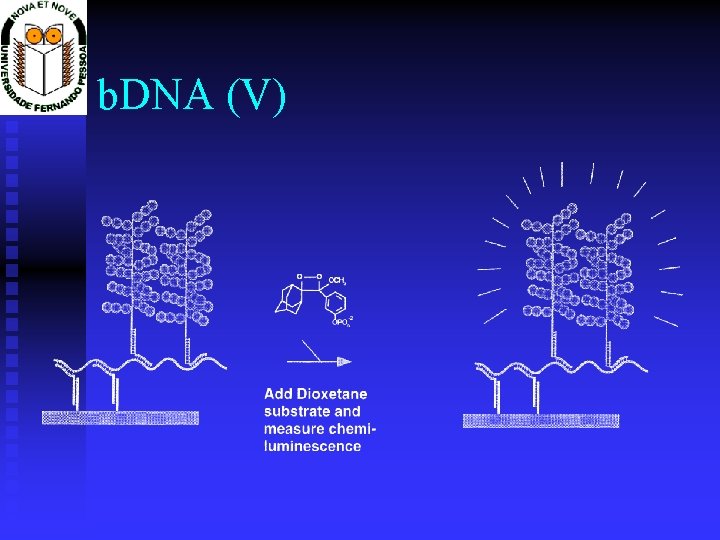
b. DNA (V)
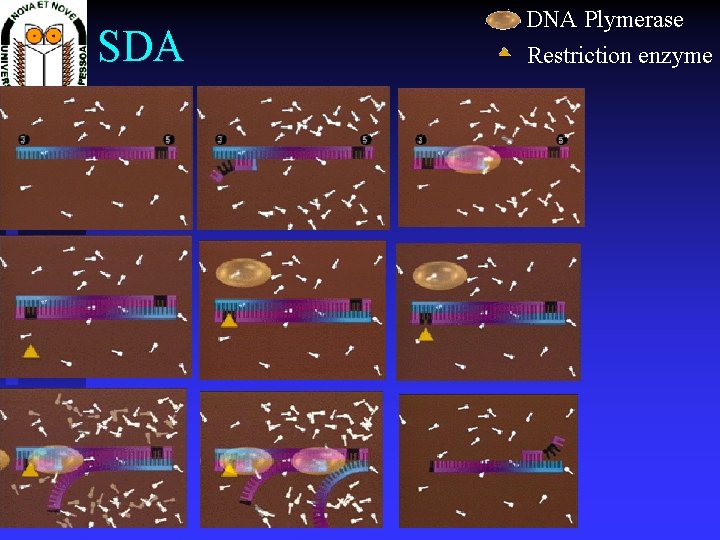
SDA DNA Plymerase Restriction enzyme

Aplicações de técnicas de amplificação de AN ao diagnóstico microbiológico Prof. Doutor José Cabeda

MÉTODOS CONVENCIONAIS NO DIAGNÓSTICO MICROBIOLÓGICO Caracterização microscópica Crescimento “in vitro” em meios sintéticos Caracterização bioquímica Demonstração imunológica da presença dos/ contacto com microorganismos

LIMITAÇÕES DOS MÉTODOS CONVENCIONAIS MÉTODO Cultural LIMITAÇÃO EXEMPLOS Meios e condições de cultura especiais Mycoplasma spp. , Legionella spp. . . Culturas celulares Vírus, bactérias intracelulares obrigatórias Incapacidade de crescer “in vitro” Microrganismos de crescimento lento M. leprae, T. pallidum, HPV, HCV. . Mycobacterium spp. , fungos

LIMITAÇÕES DOS MÉTODOS CONVENCIONAIS MÉTODO Serológico LIMITAÇÃO Sem utilidade na fase aguda diagnóstico retrospectivo Problemático no hospedeiro imunocomprometido Reactividade cruzada Interpretação complexa
DIAGNÓSTICO MOLECULAR • Diagnóstico etiológico em tempo Sensibilidade Especificidade Rapidez clinicamente útil • Evitar terapias empíricas • Administração precoce de terapia específica • Diminuição do tempo e custos da hospitalização PCR Tempo Real

ÁREAS DE APLICAÇÃO Ø Diagnóstico das Doenças Infecciosas Ø Detecção de Resistência aos Antimicrobianos UBM - HGSA

O que fazemos (Microbiologia) Microbiologia u Detecção/quantificação de agentes patogénicos t Vírus t Bactérias u Genotipagem viral u Detecção de resistências a drogas t Detecção de genótipos associados a resistência u Epidemiologia t Infecção nosocomial

Áreas de Intervenção (II) Urgentes Virologia u u u Detecção de agentes Identificação de agentes Resistências a drogas Microbiologia u u u Detecção de agentes Identificação de agentes Resistências a drogas Hematologia u Doenças oncológicas t Estudo de genes quimera t Estudo de Doença Res. Mín. t Estudo de monoclonalidade t Estudo de Quimerismo Não Urgentes Hematologia/Imunologia u Doenças Genéticas t Monogénicas • Estudo de Mutações • Estudo de haplótipos t Multifactoriais • Estudo de polimorfismos (factores genéticos de risco) Anatomia Patológica u Biópsias t Detecção de patogénios t Detecção de monoclonalidade u Thin. Prep t Detecção de HPV

Virologia Sistema Nervoso Central Transmissíveis p/ sangue HIV HSV 1/2 HBV EBV HCV CMV VZV Outros HHV-6 HTLV-1 Enterovirus HPV Poliomavirus (JCV e BKV)

Microbiologia u u u Detecção de bacterias Micobacterium tuberculosis Leptospira spp Pneumonias atípicas Legionella spp. t Legionella pneumophila t Legionella genus t Micoplasma pneumoniae t Chlamydia pneumoniae t u u u u Staphylococcus spp. Enterococcus spp. Helicobacter pylori Clostridium difficile (tcd. A, tcd. B) Bordetella pertussis Borrelia burgdorferi 16 S r. DNA Identificação de bactérias Micobacterium tuberculosis complex Micobacterium avium complex Micobacterium kanzasii Micobacterium intracelulare Micobacterium Gordonae Resistencias a drogas Meticilina Glicopeptídeos Rifampicina Isoniazida Antiretrovirais

Escolha da tecnologia (I) Real-Time-PCR Mais rápido (até 1 hora) Mais sensível Menor risco de contaminação Uma só tecnologia faz u Amplificação u Detecção u Caracterização PCR convencional Mais barato Muitos protocolos disponíveis Mais fácil de montar para: u Multiplex u Nested

Escolha da tecnologia (II) R. A. P. I. D (Yahoo) Light. Cycler Smart. Cycler-TD (cepheid) 7000 / 7300 / 7500 / 7900 HT (Applied Biosystems) MX 3000 P MX 4000 (Stratagene) Rotorgene Myi. Q (pyrosequencing) (Bio. Rad) Opticon Chromo 4 (MJ Research) http: //www. biocompare. com/matrix/2838/Real-Time-Thermal-Cyclers-(Thermocyclers). html

Escolha da tecnologia (III) Light. Cycler O mais rápido (cerca de 20’) Muitos protocolos disponíveis 32 amostras/corrida Fluorocromos limitados na versão original Smart. Cycler Bastante rápido (cerca de 30’) Disponível em 25 ml e 100 ml: u PCR preparatívos u Aumento do input amostra u Conversão de PCR convencional facilitada 16 estações independentes u 16 programas simultânos u Apenas 16 amostras
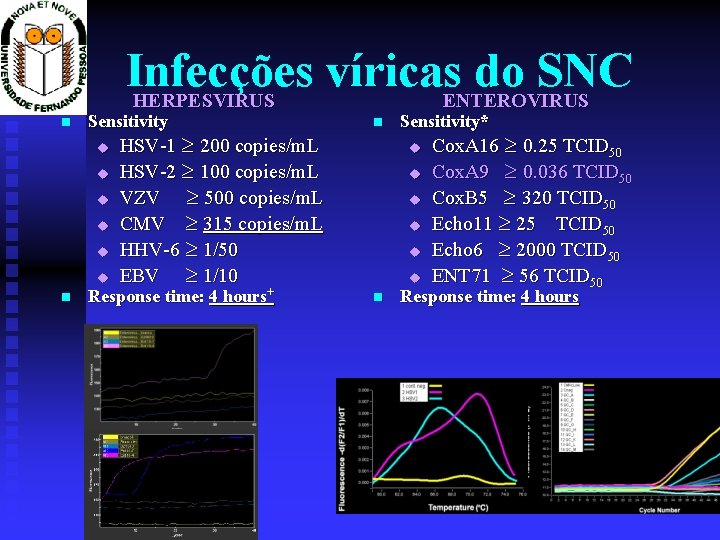
Infecções víricas do SNC HERPESVIRUS ENTEROVIRUS Sensitivity u u u HSV-1 200 copies/m. L HSV-2 100 copies/m. L VZV 500 copies/m. L CMV 315 copies/m. L HHV-6 1/50 EBV 1/10 Response time: 4 hours+ Sensitivity* u u u Cox. A 16 0. 25 TCID 50 Cox. A 9 0. 036 TCID 50 Cox. B 5 320 TCID 50 Echo 11 25 TCID 50 Echo 6 2000 TCID 50 ENT 71 56 TCID 50 Response time: 4 hours
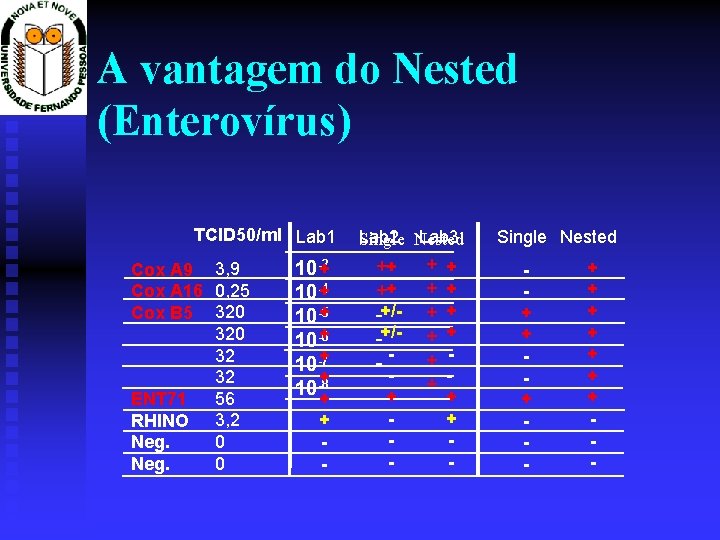
A vantagem do Nested (Enterovírus) TCID 50/ml Lab 1 Cox A 9 3, 9 Cox A 16 0, 25 Cox B 5 320 32 32 56 ENT 71 RHINO 3, 2 0 Neg. + 10 -2 + 10 -4 + 10 -5 + 10 -6 + 10 -7 + 10 -8 + + - Lab 2 Lab 3 Single Nested ++ ++ -+/-+/--+ - + + + - Single Nested + + + - + + + + -
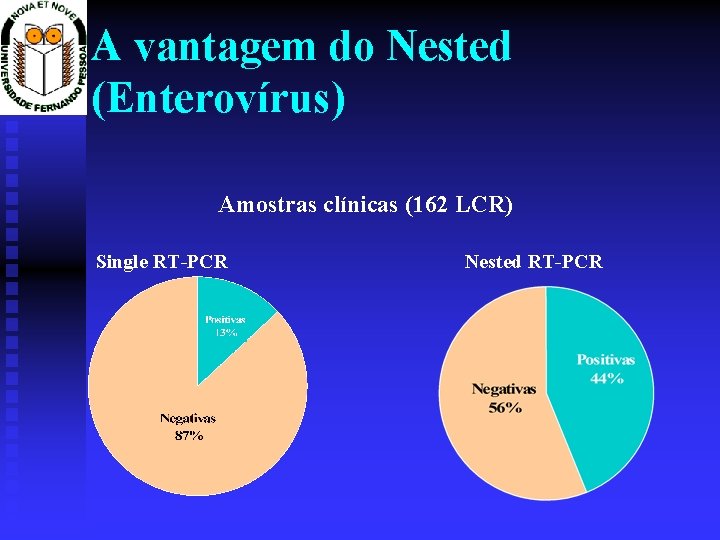
A vantagem do Nested (Enterovírus) Amostras clínicas (162 LCR) Single RT-PCR Nested RT-PCR
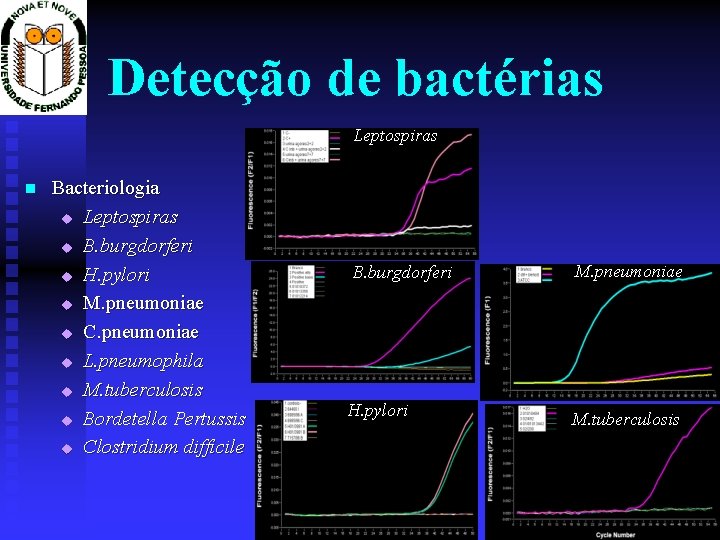
Detecção de bactérias Leptospiras Bacteriologia u Leptospiras u B. burgdorferi u H. pylori u M. pneumoniae u C. pneumoniae u L. pneumophila u M. tuberculosis u Bordetella Pertussis u Clostridium difficile B. burgdorferi M. pneumoniae H. pylori M. tuberculosis

Helicobacter pylori Biópsias Gástricas Frescas Biópsias Gástricas Fixadas Extracção de DNA: § Homogeneização dos Tecidos § Lise Celular § Desnaturação Proteica § Tampão de Lise de Tecidos § Fast Prep § Temperatura de 95 ºC § Proteinase K § Magna Pure LC DNA Isolation Kit - Tissue 60 m
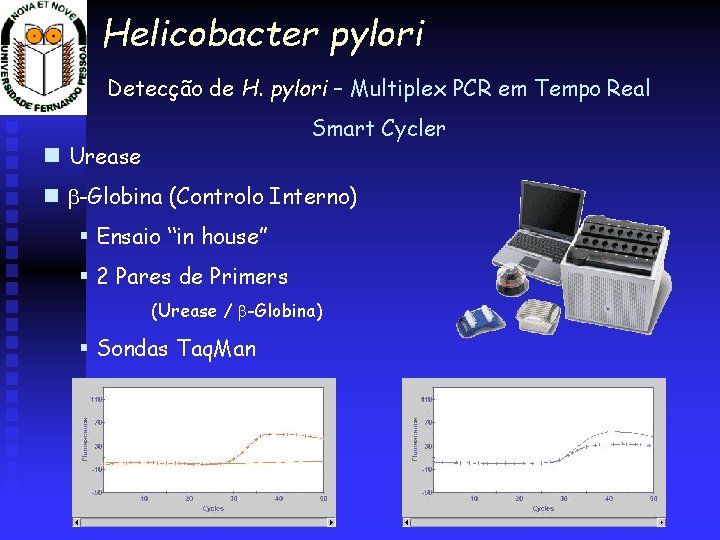
Helicobacter pylori Detecção de H. pylori – Multiplex PCR em Tempo Real Smart Cycler Urease -Globina (Controlo Interno) § Ensaio “in house” § 2 Pares de Primers (Urease / -Globina) § Sondas Taq. Man
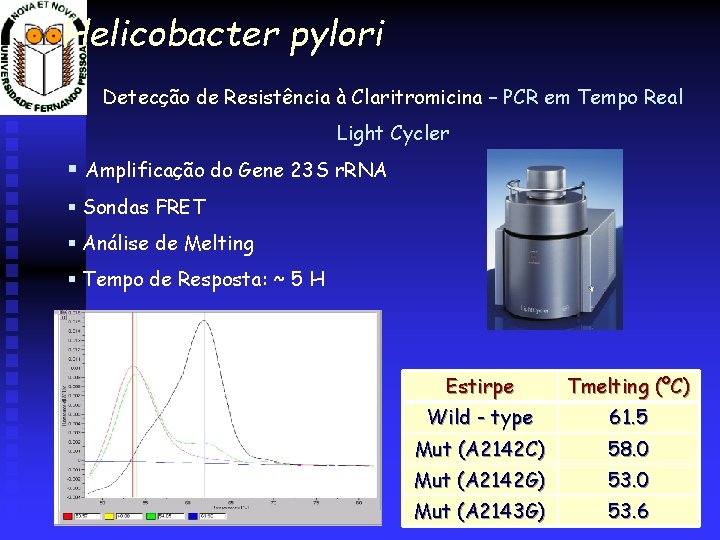
Helicobacter pylori Detecção de Resistência à Claritromicina – PCR em Tempo Real Light Cycler § Amplificação do Gene 23 S r. RNA § Sondas FRET § Análise de Melting § Tempo de Resposta: ~ 5 H Estirpe Tmelting (ºC) Wild - type 61. 5 Mut (A 2142 C) 58. 0 Mut (A 2142 G) 53. 0 Mut (A 2143 G) 53. 6

PNEUMONIAS ATÍPICAS M. pneumoniae, C. pneumoniae e L. pneumophila TÉCNICA: PCR em Tempo Real – SMART CYCLER 3 ENSAIOS DE PCR Efectuados individualmente para a detecção de cada um dos microrganismos
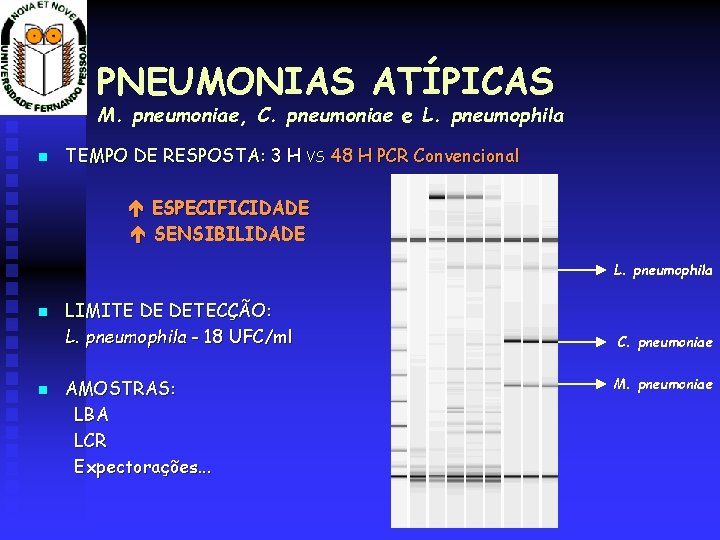
PNEUMONIAS ATÍPICAS M. pneumoniae, C. pneumoniae e L. pneumophila TEMPO DE RESPOSTA: 3 H VS 48 H PCR Convencional ESPECIFICIDADE SENSIBILIDADE L. pneumophila LIMITE DE DETECÇÃO: L. pneumophila - 18 UFC/ml AMOSTRAS: LBA LCR Expectorações. . . C. pneumoniae M. pneumoniae
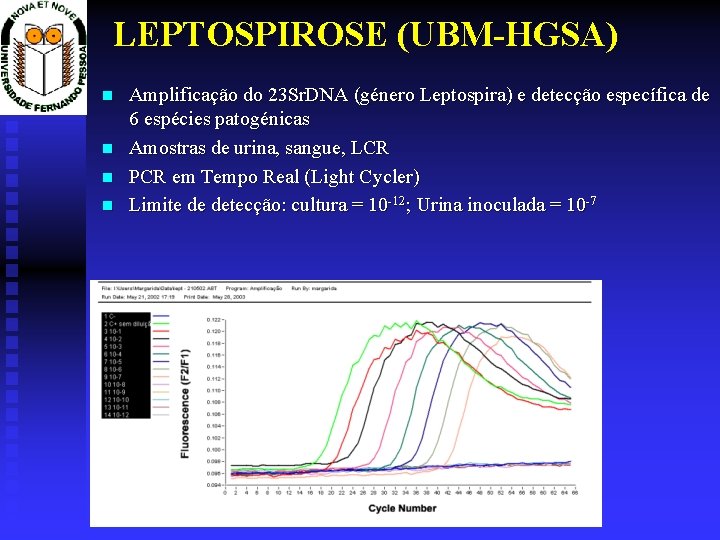
LEPTOSPIROSE (UBM-HGSA) Amplificação do 23 Sr. DNA (género Leptospira) e detecção específica de 6 espécies patogénicas Amostras de urina, sangue, LCR PCR em Tempo Real (Light Cycler) Limite de detecção: cultura = 10 -12; Urina inoculada = 10 -7
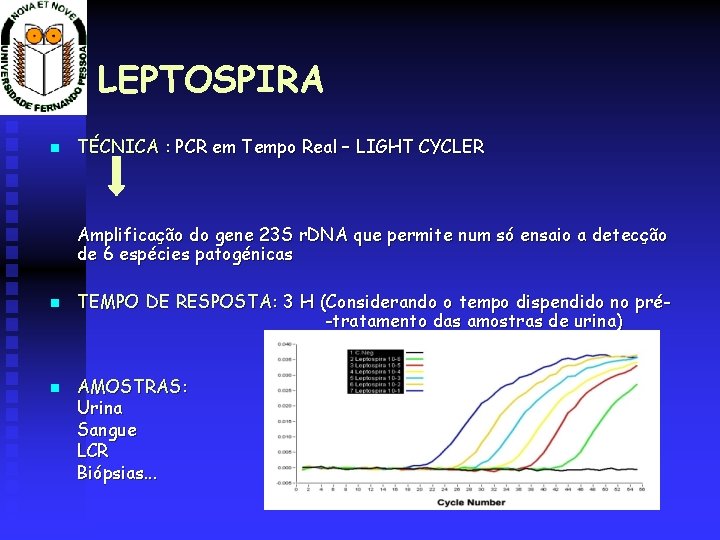
LEPTOSPIRA TÉCNICA : PCR em Tempo Real – LIGHT CYCLER Amplificação do gene 23 S r. DNA que permite num só ensaio a detecção de 6 espécies patogénicas TEMPO DE RESPOSTA: 3 H (Considerando o tempo dispendido no pré-tratamento das amostras de urina) AMOSTRAS: Urina Sangue LCR Biópsias. . .

Bordetella pertussis Detecção molecular de IS 481 § Amostras: t Secreções nasofarínge t Zaragatoa nasofarínge § Armazenar a 4ºC § Volume mínimo amostra 400 ml § Extracção de ácidos nucleicos t EZ 1 Bio. Robot – Qiagen
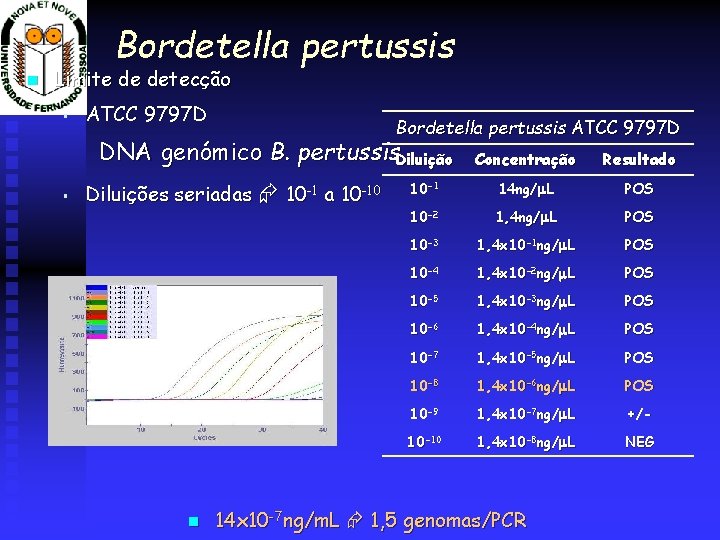
Bordetella pertussis Limite de detecção § ATCC 9797 D Bordetella pertussis ATCC 9797 D DNA genómico B. pertussis. Diluição § Diluições seriadas 10 -1 a 10 -10 Concentração Resultado 10 -1 14 ng/m. L POS 10 -2 1, 4 ng/m. L POS 10 -3 1, 4 x 10 -1 ng/m. L POS 10 -4 1, 4 x 10 -2 ng/m. L POS 10 -5 1, 4 x 10 -3 ng/m. L POS 10 -6 1, 4 x 10 -4 ng/m. L POS 10 -7 1, 4 x 10 -5 ng/m. L POS 10 -8 1, 4 x 10 -6 ng/m. L POS 10 -9 1, 4 x 10 -7 ng/m. L +/- 10 -10 1, 4 x 10 -8 ng/m. L NEG 14 x 10 -7 ng/m. L 1, 5 genomas/PCR
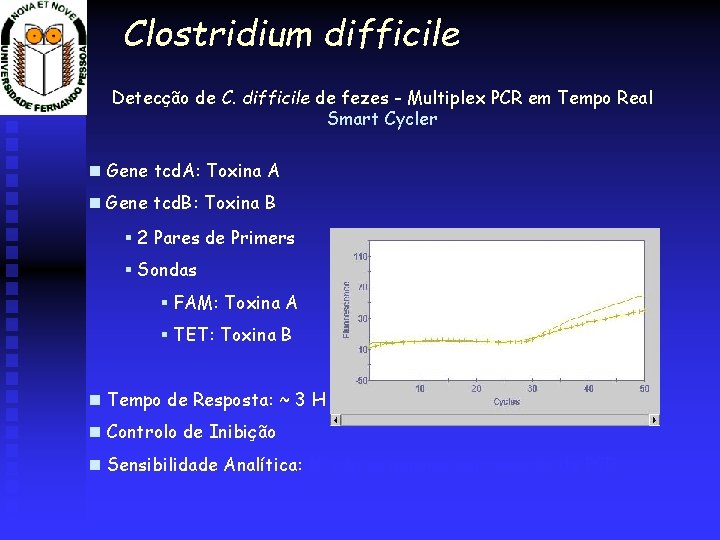
Clostridium difficile Detecção de C. difficile de fezes - Multiplex PCR em Tempo Real Smart Cycler Gene tcd. A: Toxina A Gene tcd. B: Toxina B § 2 Pares de Primers § Sondas § FAM: Toxina A § TET: Toxina B Tempo de Resposta: ~ 3 H Controlo de Inibição Sensibilidade Analítica: 10 cópias genoma por reacção de PCR
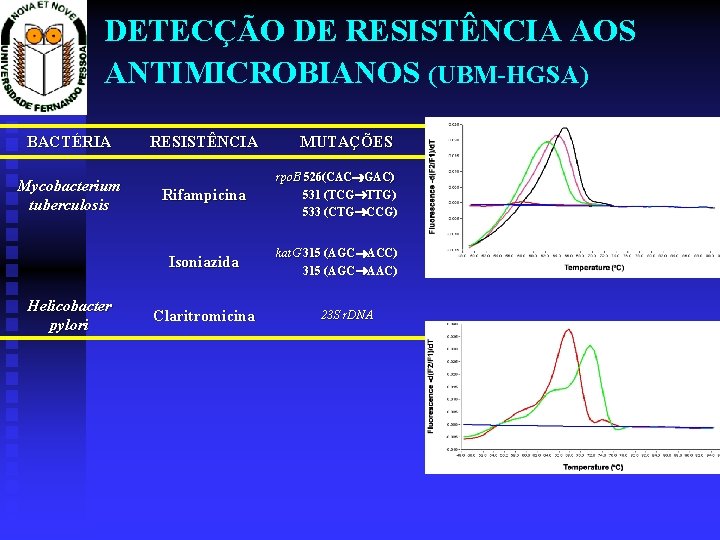
DETECÇÃO DE RESISTÊNCIA AOS ANTIMICROBIANOS (UBM-HGSA) BACTÉRIA Mycobacterium tuberculosis Helicobacter pylori RESISTÊNCIA MUTAÇÕES Rifampicina rpo. B 526(CAC GAC) 531 (TCG TTG) 533 (CTG CCG) Isoniazida kat. G 315 (AGC ACC) 315 (AGC AAC) Claritromicina 23 S r. DNA
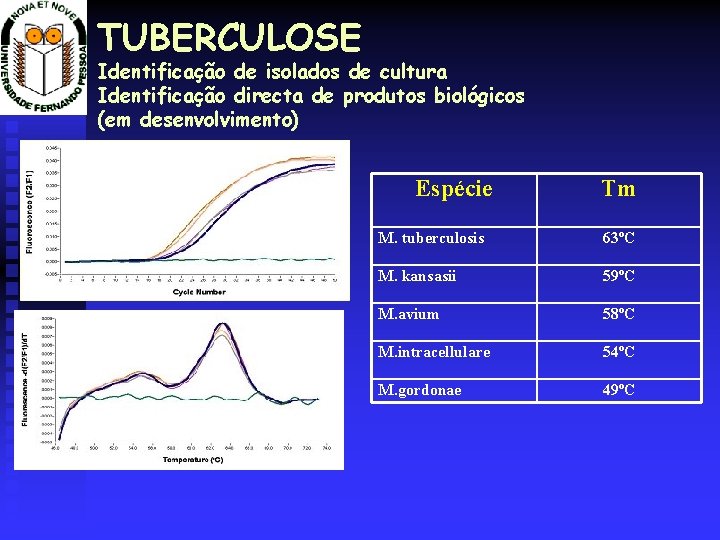
TUBERCULOSE Identificação de isolados de cultura Identificação directa de produtos biológicos (em desenvolvimento) Espécie Tm M. tuberculosis 63ºC M. kansasii 59ºC M. avium 58ºC M. intracellulare 54ºC M. gordonae 49ºC
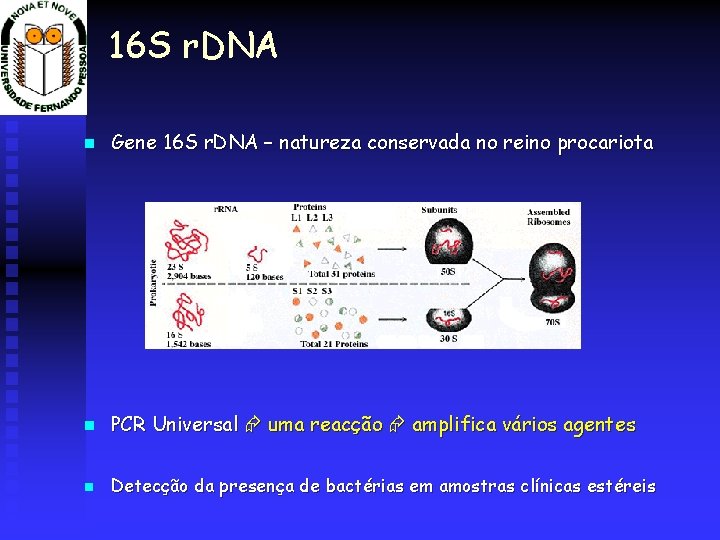
16 S r. DNA Gene 16 S r. DNA – natureza conservada no reino procariota PCR Universal uma reacção amplifica vários agentes Detecção da presença de bactérias em amostras clínicas estéreis

16 S r. DNA Aplicações: § LCR, Sangue, produtos biológicos “estéreis” Problemas: § Detecção de bactérias inviáveis § Risco de contaminação laboratorial § Risco de contaminação na colheita Correlacionar resultados positivos com a clínica

16 S r. DNA Inactivação do DNA exógeno (irradiação UV reagentes/material) Extracção de ácidos nucleicos § Bactérias Gram - § Bactérias Gram + § Micobactérias § Lise enzimática / mecânica § Magna Pure LC, Roche t Amplificação § Total Nucleic Acid Isolation Kit Smart Cycler, Cepheid - PCR em Tempo Real Múltiplos controlos negativos (extracção, amplificação)

16 S r. DNA Sensibilidade analítica do método § S. aureus 160 UFC/m. L § E. coli 200 UFC/m. L Aplicação a 76 amostras de LCR (Meningite Bacteriana Aguda) § Sensibilidade: 80%; Especificidade: 94. 5% § VPP: 84%; VPN: 92. 7% Resultado – POSITIVO/NEGATIVO

16 S r. DNA Espécie Origem PCR em tempo real E. coli ATCC 25922 Pos S. aureus ATCC 25923 Pos E. faecalis ATCC 25212 Pos S. pneumoniae ATCC 6305 Pos P. mirabilis ATCC 12453 Pos E. cloacae ATCC 13047 Pos K. pneumoniae ATCC 13883 Pos P. aeruginosa ATCC 27853 Pos H. influenzae ATCC 49766 Pos N. meningitidis Isolado clínico Pos L. monocytogenes Isolado clínico Pos S. epidermidis Isolado clínico Pos S. agalactiae Isolado clínico Pos M. tuberculosis Isolado clínico Pos Leptospira sp Isolado clínico Pos

16 S r. DNA Estirpes detectadas por outros autores com os mesmos primers Acinetobacter calcoaceticus Clostridium perfringens Aeromonas hydrophila Corynebacterium genitalium Alcaligenes faecalis Erysipelothrix rhusiophathiae Bacteroides fragilis Gardnerella vaginalis Campylobacter fetus Lactobacillus acidophilus Campylobacter jejuni Leuconostoc paramesenteroides Eikenella corrodens Micrococcus luteus Flavobacterium meningosepticum Mycoplasma genitalium Legionella pneumophila Mycoplasma hominis Moraxella catarrhalis Mycoplasma pneumoniae Neisseria gonorrhoeae Peptostreptococcus anaerobius Providencia stuartii Peptostreptococcus magnus Salmonella typhimurium Propionibacterium acnes Serratia marcescens Streptococcus mitis Yersinia enterocolitica Streptococcus sanguis

16 S r. DNA Desafio: sensibilidade sem comprometer a especificidade t Kits de Extracção MGrade t Enzimas Low. DNA Essencial: Resultados positivos Identificação do produto amplificado § Distinguir contaminações de verdadeiros positivos § Correlação com clínica Valor Preditivo Positivo Sensibilidade
- Slides: 88