Tavola periodica e propriet periodiche https www youtube

Tavola periodica e proprietà periodiche https: //www. youtube. com/watch? v=Vg. VQKCcfwn. U

1789 Lavoisier pubblica una lista di 33 elementi chimici raggruppati in 4 classi (gas, metalli, nonmetalli e elementi terrosi).
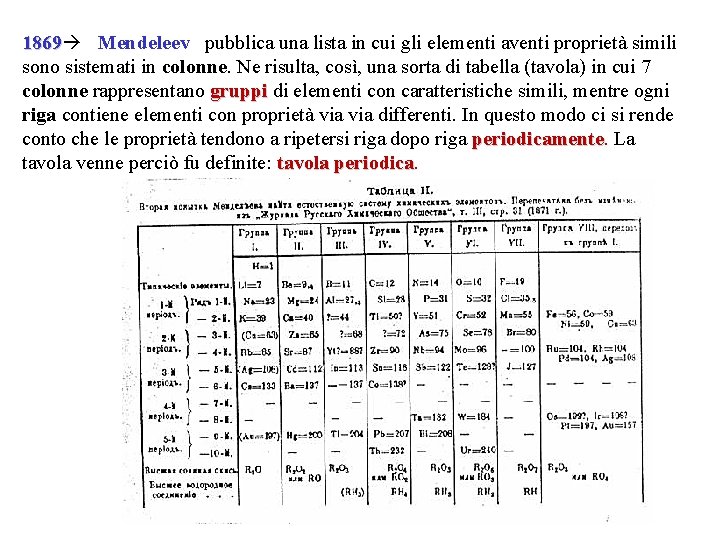
1869 Mendeleev, pubblica una lista in cui gli elementi aventi proprietà simili 1869 sono sistemati in colonne. Ne risulta, così, una sorta di tabella (tavola) in cui 7 colonne rappresentano gruppi di elementi con caratteristiche simili, mentre ogni riga contiene elementi con proprietà via differenti. In questo modo ci si rende conto che le proprietà tendono a ripetersi riga dopo riga periodicamente La tavola venne perciò fu definite: tavola periodica

Lo stesso Mendeleev si accorge che, per raggruppare gli elementi secondo caratteristiche simili, non sempre può essere rispettato l’ordine di massa atomica. Così, ad esempio, pone l’arsenico As nel gruppo di azoto N e fosforo P, lasciando vuoti due posti, prevedendo l’esistenza di due elementi, all’epoca sconosciuti) Tali elementi furono scoperti alla fine dell’ 800: il gallio e il germanio Altro esempio è l’ordine del tellurio Te e dello Iodio I invertito rispetto alla massa, sempre per rispettare le caratteristiche.
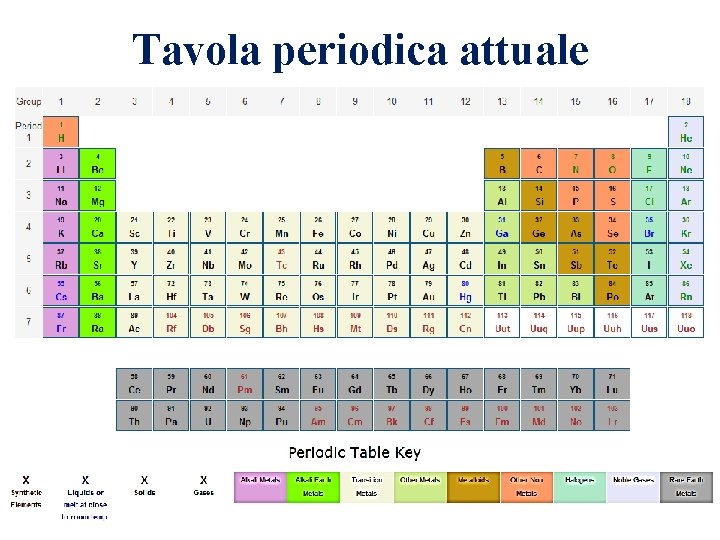
Tavola periodica attuale
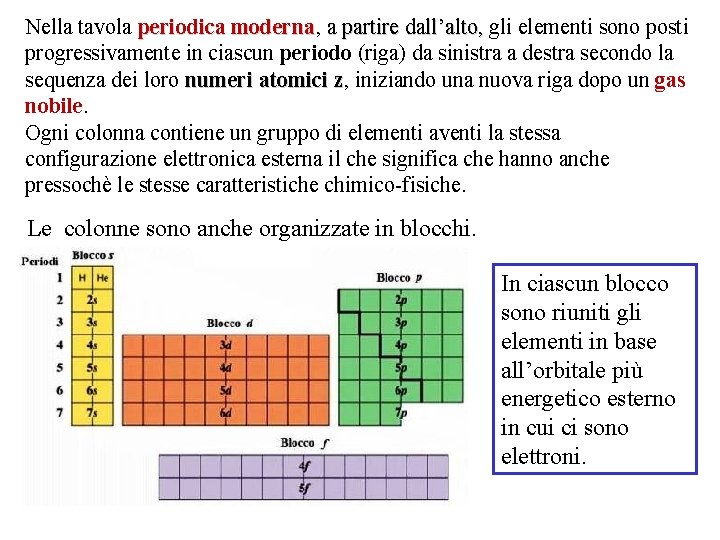
Nella tavola periodica moderna, moderna a partire dall’alto, gli elementi sono posti progressivamente in ciascun periodo (riga) da sinistra a destra secondo la sequenza dei loro numeri atomici z, z iniziando una nuova riga dopo un gas nobile. Ogni colonna contiene un gruppo di elementi aventi la stessa configurazione elettronica esterna il che significa che hanno anche pressochè le stesse caratteristiche chimico-fisiche. Le colonne sono anche organizzate in blocchi. In ciascun blocco sono riuniti gli elementi in base all’orbitale più energetico esterno in cui ci sono elettroni.
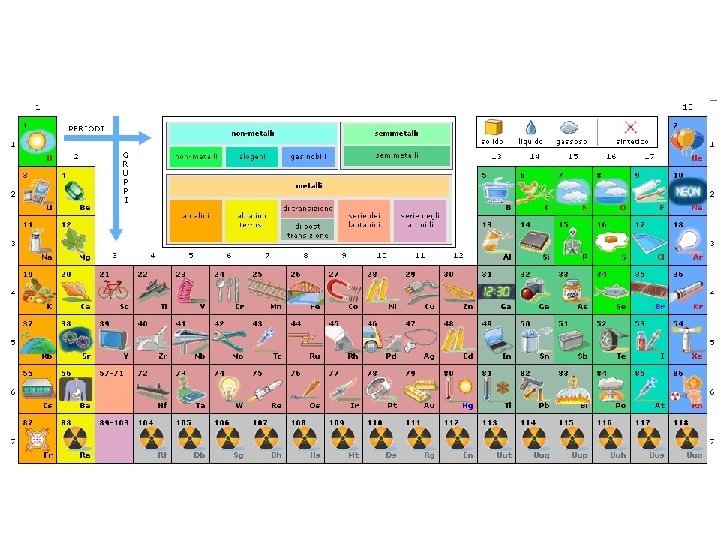

Elementi del primo gruppo üSE ESPOSTI ALL’ARIA, REAGISCONO IMMEDIATAMENTE CON L’OSSIGENO E L’UMIDITÀ DELL’ARIA VELOCEMENTE DI UNA PATINA DI OSSIDI ü TUTTI I METALLI ALCALINI SONO MORBIDI E SI TAGLIANO FACILMENTE CON UN COLTELLO. üREAGISCONO CON H 20 LIBERANDO ENERGIA SOTTOFORMA DI CALORE E IDROGENO https: //www. youtube. com/watch? v=d. VJUXJ 6 a. K 3 w

Secondo gruppo metalli alcalino terrosi: Be, Mg, Ca, Sr, Ba, Ra üreagiscono con l’H 20 ma, in modo meno violento rispetto ai metalli primo gruppo Idrossido di Calcio o CALCE Materiale da costruzione Ca(s)+ 2 H 2 O(l)→ Ca(OH)2(s) + H 2(g) Ca. CO 3(s) →Ca. O + CO 2 CALCE VIVA disinfettante ambienti

Metalli di transizione ü molto stabili üalcuni molto resistenti Es. Titanio: bassa densità la stessa del tessuto osseo protesi elevata robustezza industria aerospaziale; Mercurio (Hg): unico metallo liquido a T ambiente (Tfusione =-38°C)

Tra i metalli di transizione…. . …. quelli “preziosi” ü i più stabili della tavola ü Lucenti ü Duttili ü Manleabili ü buoni conduttori di calore ed elettricità

Un metallo un po’ …scherzoso: il Gallio ü https: //www. youtube. com/watch? v=j 5 c. V 1 zsl. Ejg ü È un metallo con punto di fusione molto basso: 29. 8°C ü Il galinstano è una miscela costituita da gallio, indio e stagno, liquida , di colore argenteo a temperatura ambiente e viene utilizzata per creare termometri chimici senza mercurio

I semimetalli si comportano sia come metalli , sia come non metalli ü il silicio üTra i più abbondanti elementi crosta terrestre üOssido di silicio, costituisce il vetro ü principale componente di microchip (semiconduttore) ü nella fabbricazione di celle fotovoltaiche

I non metalli Il carbonio: costituisce tutte le molecole organiche, biomolecole. Grafite / diamantel Fosforo, Zolfo, Azoto, Ossigeno

Alogeni • Elementi del settimo gruppo • Sono presenti a T ambiente nei tre stati di aggregazione della materia: • Cloro: gas • Bromo: liquido • Iodio: solido

Ultimo gruppo della tavola Hanno bassissima reattività

http: //ebook. scuola. zanichelli. it/at kinschimica/la-tavola-periodicadegli-elementi www. ptable. com/? lang=it
- Slides: 17