Tartalom Az atom fogalma felptse Az atom elektronszerkezete




















- Slides: 30

Tartalom • • • Az atom fogalma, felépítése Az atom elektronszerkezete Rendszám, tömegszám, izotópok fogalma Radioaktivitás fogalma A molekula, ion, mól, moláris tömeg fogalma • anyagi rendszerek felosztása

Az atom

John Dalton (1803)

Az atom • Az atomok a kémiailag legegyszerűbb részecskék • A szokásos kémiai folyamatokban nem alakulnak át egymássá. • A kémiai reakció során az anyag atomjai átrendeződnek és így egy másik fajta anyag jön létre.


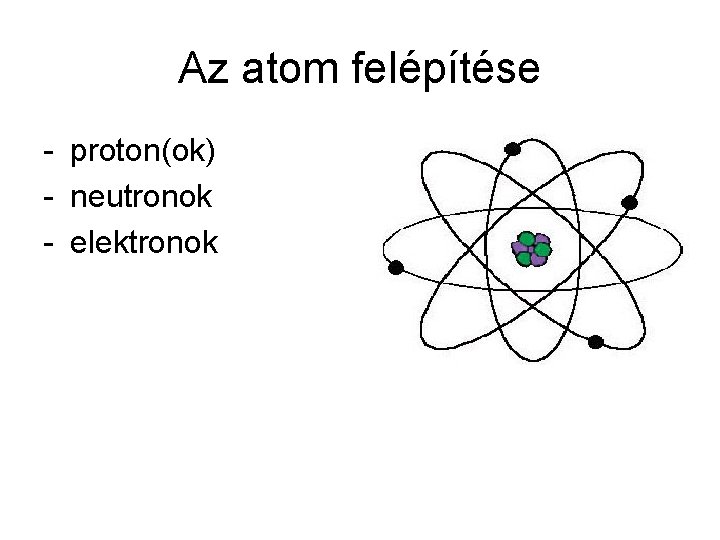
Az atom felépítése - proton(ok) - neutronok - elektronok

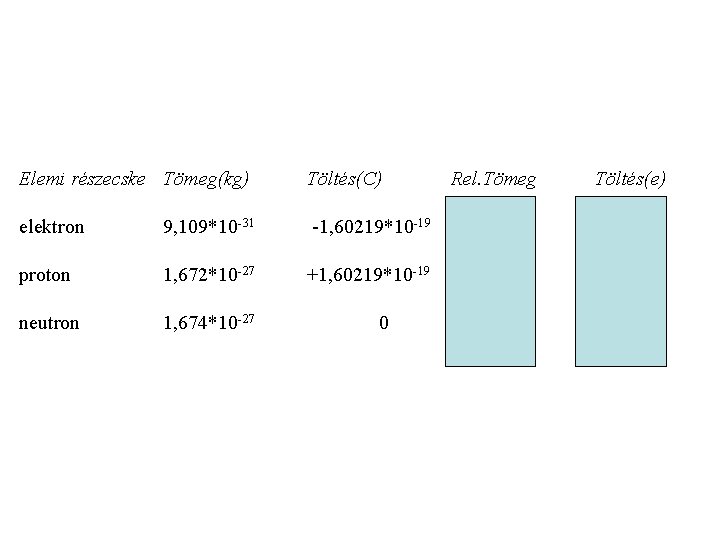
Elemi részecske Tömeg(kg) Töltés(C) elektron 9, 109*10 -31 -1, 60219*10 -19 0, 00055 -1 proton 1, 672*10 -27 +1, 60219*10 -19 1, 00728 +1 neutron 1, 674*10 -27 1, 00866 0 0 Rel. Tömeg Töltés(e)


Miből áll az atommag? Protonok+neutronok Mi a rendszám? (Z): Protonok száma Neutronok száma (N) Mi a tömegszám? (A)= Z+ N

Lehet-e törtszám a tömegszám?

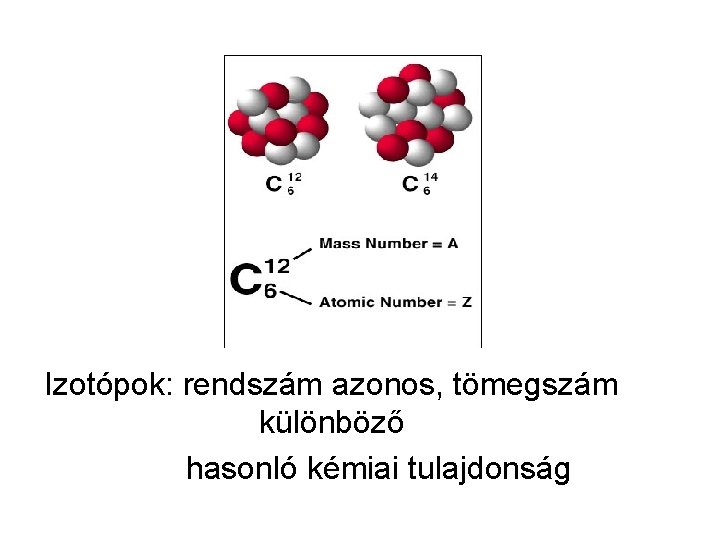
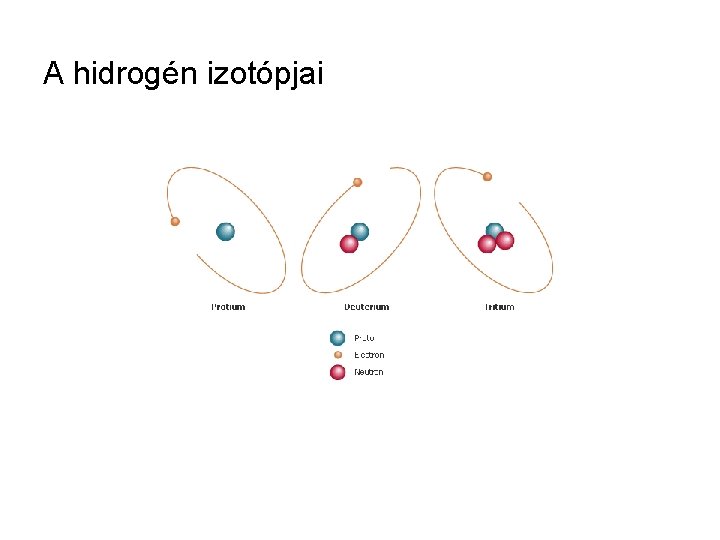
Izotópok: rendszám azonos, tömegszám különböző hasonló kémiai tulajdonság

A hidrogén izotópjai


• Radioaktív anyagok - Az atommag nem stabilis. Nagy energiájú radioaktív sugárzás közben felbomlik. (Ez már nem kémiai reakció)

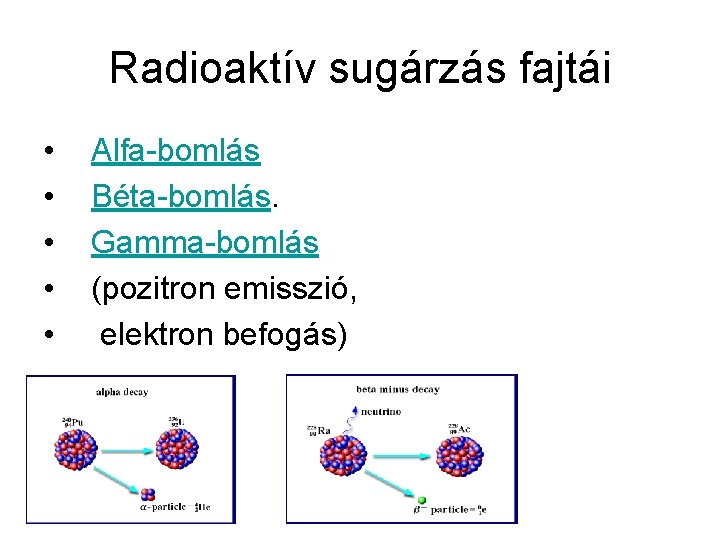
Radioaktív sugárzás fajtái • • • Alfa-bomlás Béta-bomlás. Gamma-bomlás (pozitron emisszió, elektron befogás)

Rádioaktivitás mértékének kifejezése • Minden esetben veszélyesek-e a radioaktív anyagok? • Fajlagos aktivitás > 70 k. Bq/kg. (Bequerel) • Egységnyi tömegű mintában 1 másodperc alatt végbemenő bomlások száma. • Mit jelent az, hogy K-40 fajlagos aktivitása 30, 4 Bq/g? • A természetes urán fajlagos aktivitása: 2, 54*104 Bq/g. Veszélyes anyagnak számít-e?

További mérőszámok és kérdések • • • Gray RBE Fertőz-e a sugárfertőzés? Különösen veszélyesek-e a nagyon hosszú felezési idejű izotópok? Ugyanaz a dózis kis adagokban vagy egyszerre a veszélyesebb?

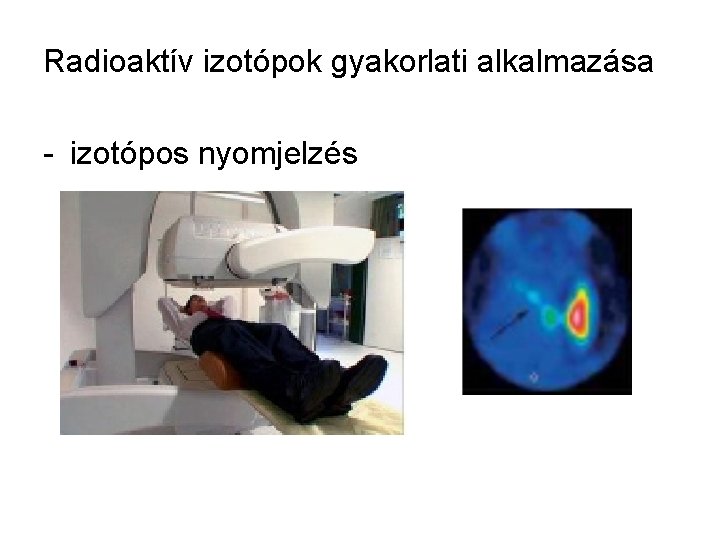
Radioaktív izotópok gyakorlati alkalmazása - izotópos nyomjelzés

Hevesy György (1885 -1966) a radioaktív izotóp nyomjelzés módszerének megalkotója. Munkáját 1913 -ban kémiai Nobel-díjjal ismerték el.

- Rákos betegségek gyógyítása 60 Co izotóppal - Kormeghatározás 14 C izotóppal

Az atom elektronszerkezete • Elektronhéj: • Az atommagtól adott távolságban lévő elektronok összessége • Vegyérték elektronok: A külső le nem zárt elektronhéjon (ritkábban a belső, telítetlen alhéjokon) lévő elektronok.

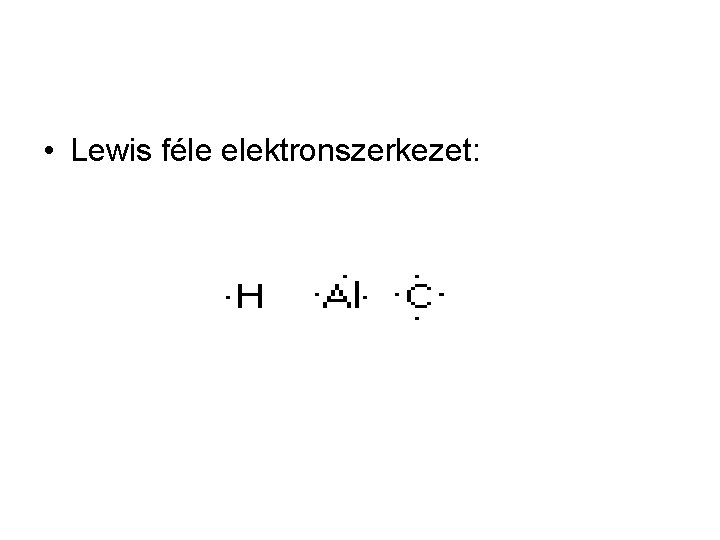
• Lewis féle elektronszerkezet:

Oktett szabály • Az atomok arra törekszenek, hogy a vegyértékhéjukon nyolc elektron legyen. A kötéseket ennek megfelelően alakítják ki. Korlátai: Az átmeneti fémekre és egyes nemfémes vegyületekre nem alkalmazható. Pl. : SF 6

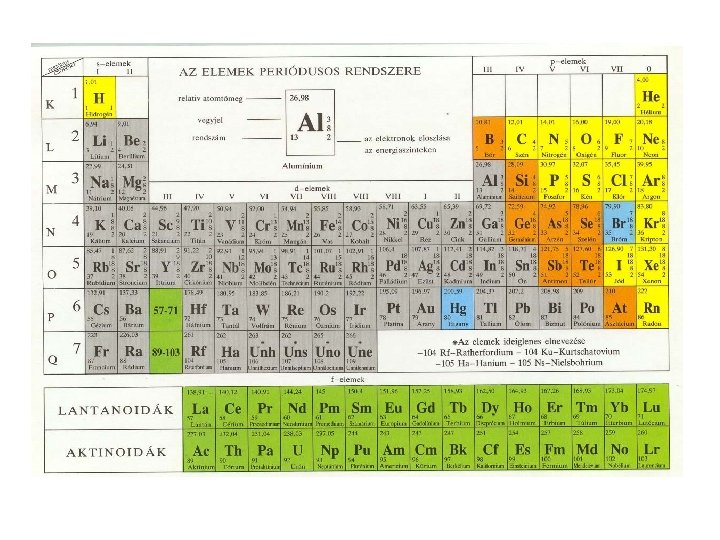
• Hány vegyérték elektronja van a következő elemeknek? Rajzoljuk fel a Lewis elektronszerkezetüket! O, N, C, Mg, K, Cl, F, Ne Ezek az elemek, hogyan érhetik el a stabilis szerkezetet?

molekula • Pl. : H 2 O • Molekula: Két vagy több azonos vagy különböző atomból álló részecske melyben az atomok elsőrendű kémiai kötéssel (kovalens kötéssel)kapcsolódnak egymáshoz.

ion: • Pl. Na+, NH 4+ • Ion: Elektromos töltéssel rendelkező atom vagy molekula

Mól, moláris tömeg Mól: Az anyagmennyiség mértékegysége - molnyi mennyiségű anyag 6*1023 db részecskét tartalmaz Moláris tömeg: Molnyi mennyiségű anyag tömege


• Elem vegyület vagy keverék? : csapvíz, desztillált víz levegő bronz etil-alkohol, sütőpor réz-szulfát oldat, szacharóz, oxigén, cink. • A keverékek ezek közül homogének vagy heterogének?
