Tamponlar AsitBazlar ve Konsantrasyon trleri Prof Dr Yeim

Tamponlar, Asit-Bazlar, ve Konsantrasyon türleri Prof. Dr. Yeşim Özarda 1

Asitler ve bazlar Günlük hayatımızda yer alan bazı asit ve bazlar 2
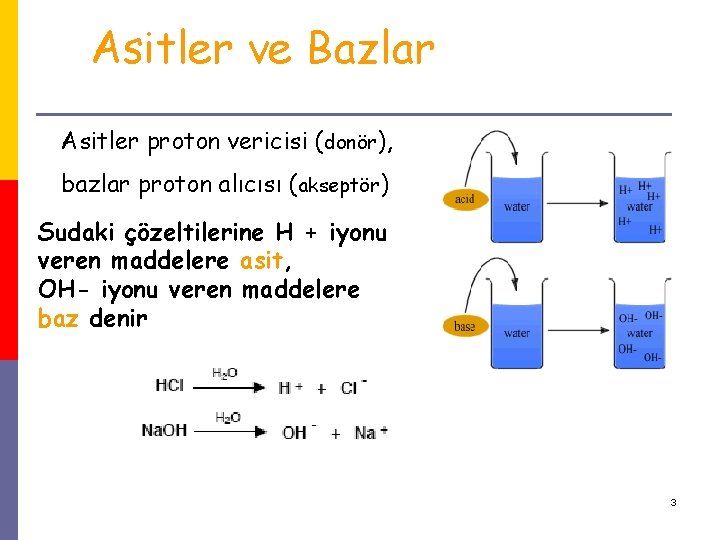
Asitler ve Bazlar Asitler proton vericisi (donör), bazlar proton alıcısı (akseptör) Sudaki çözeltilerine H + iyonu veren maddelere asit, OH- iyonu veren maddelere baz denir 3
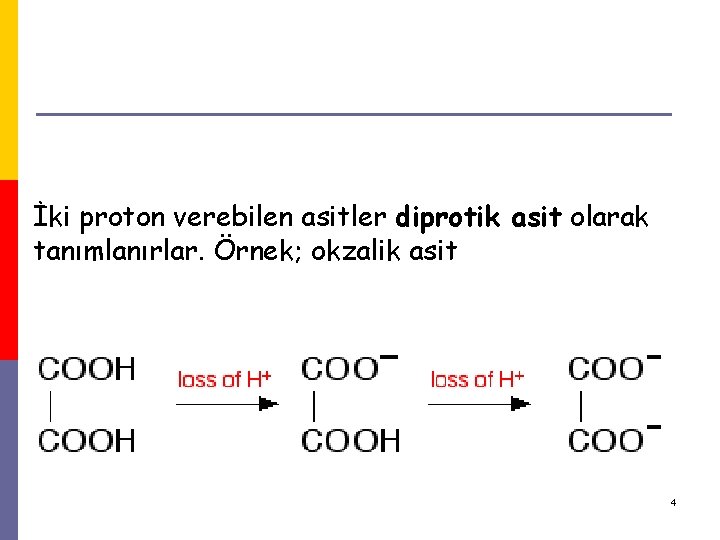
İki proton verebilen asitler diprotik asit olarak tanımlanırlar. Örnek; okzalik asit 4
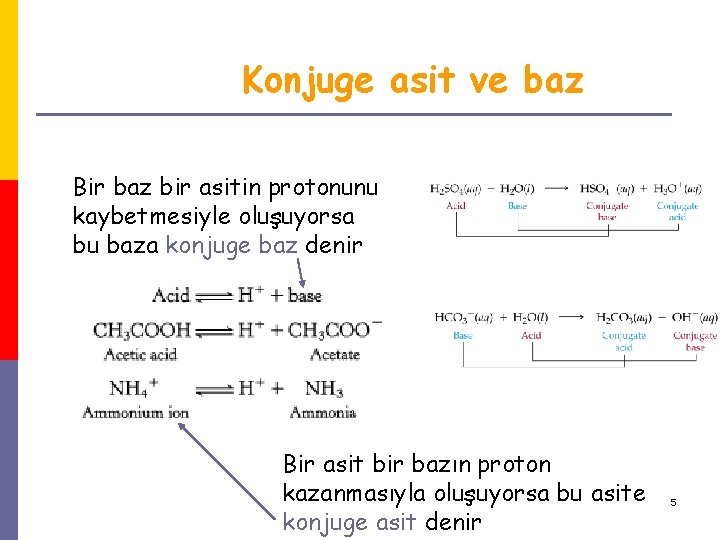
Konjuge asit ve baz Bir baz bir asitin protonunu kaybetmesiyle oluşuyorsa bu baza konjuge baz denir Bir asit bir bazın proton kazanmasıyla oluşuyorsa bu asite konjuge asit denir 5
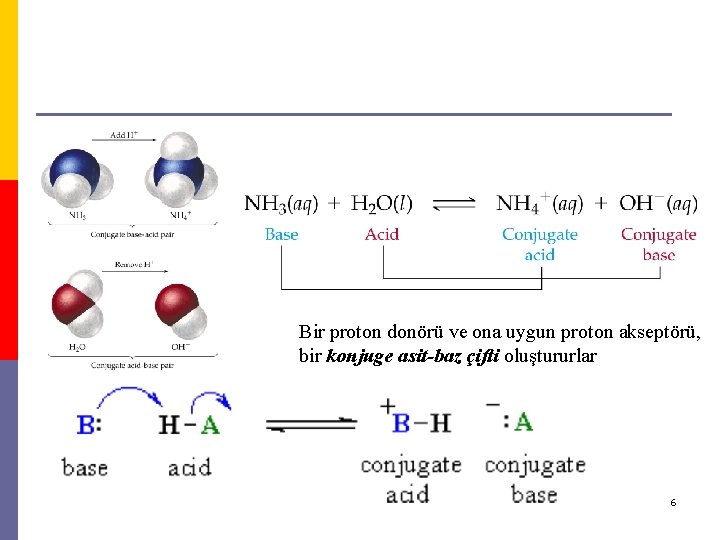
Bir proton donörü ve ona uygun proton akseptörü, bir konjuge asit-baz çifti oluştururlar 6
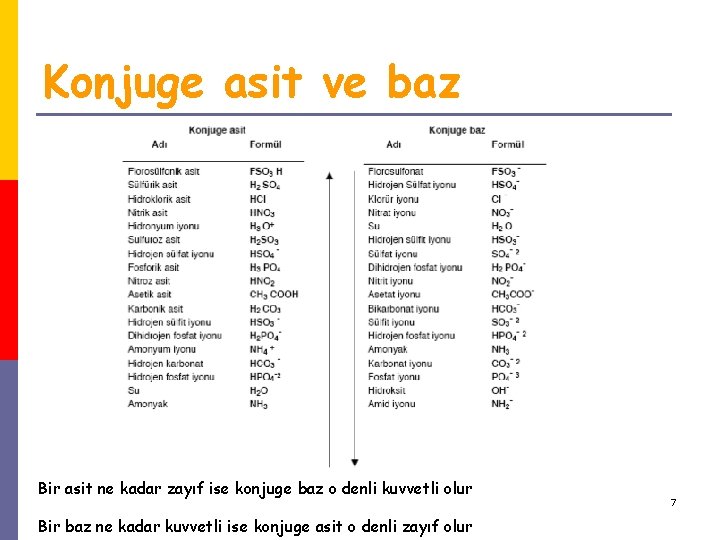
Konjuge asit ve baz Bir asit ne kadar zayıf ise konjuge baz o denli kuvvetli olur Bir baz ne kadar kuvvetli ise konjuge asit o denli zayıf olur 7

Asit ve Bazların kuvveti • Çözeltilerde tamamen iyonlaşarak tüm protonlarını veren asitler ‘kuvvetli asit’ • Çözeltilerde kısmen iyonlaşarak protonlarının bir kısmını veren asitler ‘zayıf asit’ 8
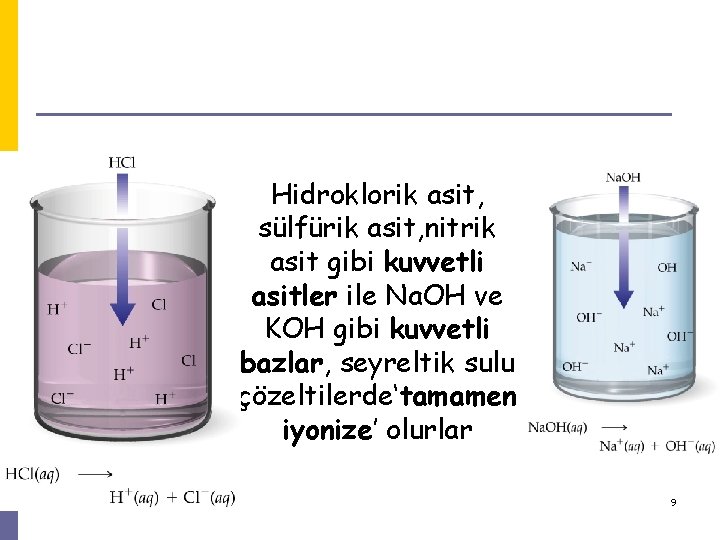
Hidroklorik asit, sülfürik asit, nitrik asit gibi kuvvetli asitler ile Na. OH ve KOH gibi kuvvetli bazlar, seyreltik sulu çözeltilerde‘tamamen iyonize’ olurlar 9
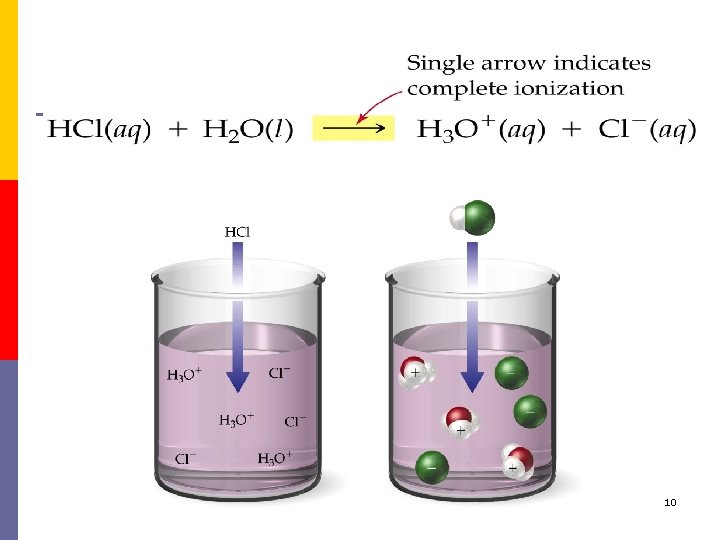
10

p. H Bir çözeltinin p. H’ı, çözeltideki H+ iyonları konsantrasyonunun eksi (-) logaritmasıdır. p. H, bir çözelti için bir karakteristiktir 11
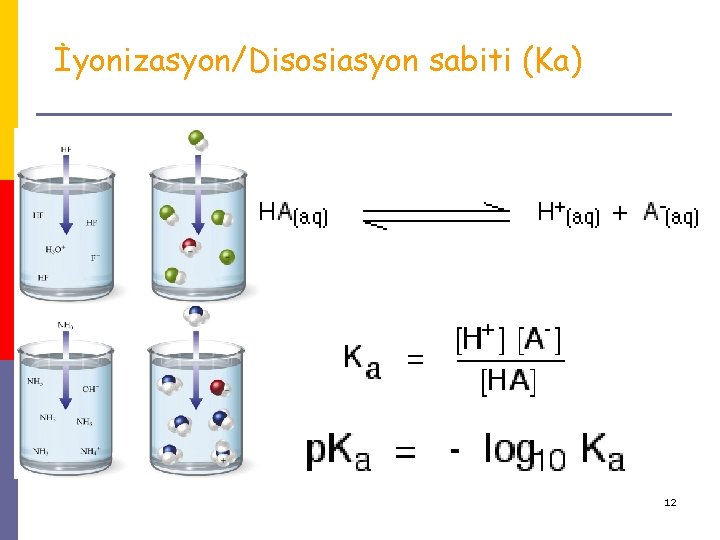
İyonizasyon/Disosiasyon sabiti (Ka) 12
![Henderson – Hesselbach Denklemi -log [Ka] = - log [H+] - log [A-] [HA] Henderson – Hesselbach Denklemi -log [Ka] = - log [H+] - log [A-] [HA]](http://slidetodoc.com/presentation_image_h/d9a33a3ee30a4faa2a4a8923677f9451/image-13.jpg)
Henderson – Hesselbach Denklemi -log [Ka] = - log [H+] - log [A-] [HA] -log [H+] = - log Ka - log [A-] p. H = p Ka + log [HA] 13

p. Ka değeri küçük olan asit, kuvvetli olarak disosiye olur; kuvvetli asittir 14

25 o. C’de nötral bir çözeltinin p. H’ı 7’dir (nötr) • Bir çözeltinin p. H’ı 7’den küçükse asidiktir • Bir çözeltinin p. H’ı 7’den büyükse alkali veya baziktir 15

Zayıf asit ve bazlar, biyolojik sistemlerde bulunurlar; metabolizmada ve metabolizmanın düzenlenmesinde önemli rol oynarlar Zayıf asidin p. Ka değerine eşit p. H’da, zayıf asit ve bunun konjuge bazı eşit konsantrasyonlarda bulunur • Daha düşük p. H’larda asit konsantrasyonu fazla • Daha yüksek p. H’larda ise asidin konjuge bazının konsantrasyonu fazla 16

Nötralizasyon reaksiyonu p p Asitler bazlar ile reaksiyona girdiği zaman suyu ve su içinde çözünmüş iyonik bir bileşik (tuz) meydana getirirler HCl + Na. OH Asit Baz H 2 O + Na. Cl Su Tuz 17

Zayıf asitlerin p. Ka değerleri titrasyon grafiği çizilerek bulunabilir; -Belirli volümdeki asit örneği, konsantrasyonu bilinen kuvvetli bir baz (genellikle Na. OH) çözeltisi ile titre edilir -Na. OH, bir indikatör boya veya bir p. H metre ile nötralizasyon sağlandığı anlaşılıncaya kadar, aside yavaş ilave edilir 18

Asidin belirli bir volümüne belirli miktarlarda Na. OH eklendikçe p. H ölçümü yapılır, eklenen Na. OH miktarlarına karşılık p. H değerlerinin grafiği çizilir 19

Tampon çözeltiler Zayıf bir asit (proton donörü) ve onun konjuge bazını (proton akseptörü) eşit miktarlarda içeren karışımlar tampon sistemi [A-] = [HA] p. H = p Ka 20
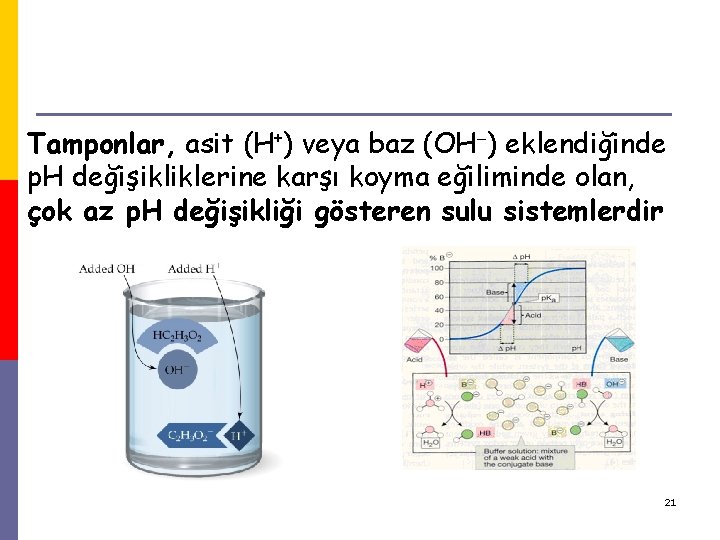
Tamponlar, asit (H+) veya baz (OH ) eklendiğinde p. H değişikliklerine karşı koyma eğiliminde olan, çok az p. H değişikliği gösteren sulu sistemlerdir 21
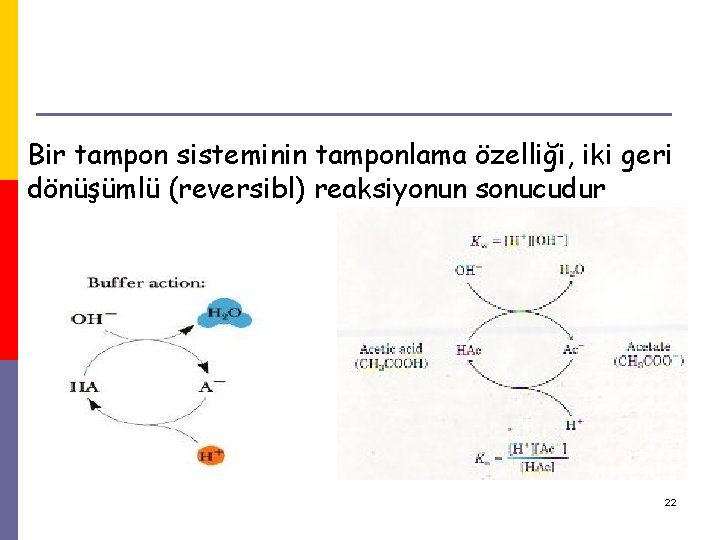
Bir tampon sisteminin tamponlama özelliği, iki geri dönüşümlü (reversibl) reaksiyonun sonucudur 22

İnsan vücudundaki kan plazmasının p. H değeri 7. 4 (7. 35 -7. 45) civarındadır. Bu değer 7. 0 den aşağıya veya 7. 8 den yukarı çıkarsa insan sağlığı için tehlikeli sonuçlar ortaya çıkabilir Kan plazmasının temel tampon sistemi bikarbonat/karbonik asit sistemidir 23

24
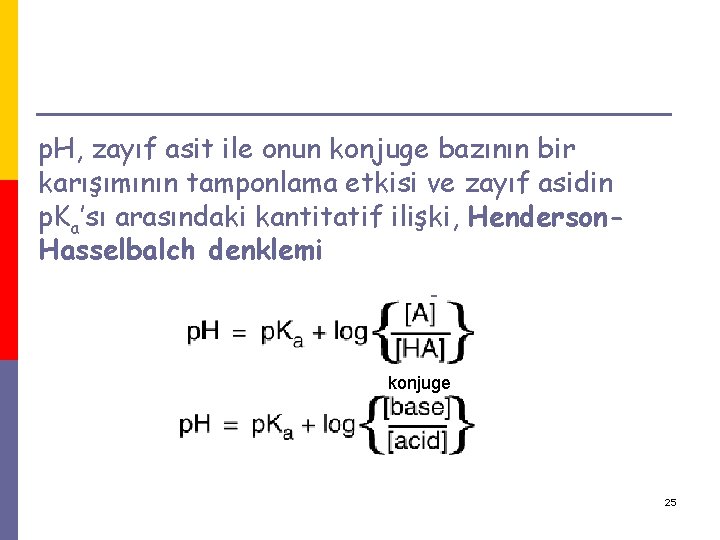
p. H, zayıf asit ile onun konjuge bazının bir karışımının tamponlama etkisi ve zayıf asidin p. Ka’sı arasındaki kantitatif ilişki, Henderson. Hasselbalch denklemi - konjuge 25

• Henderson-Hasselbalch denklemi, verilen bir p. H aralığında proton donör ve proton akseptörünün molar oranlarından, herhangi bir asidin p. Ka değerini hesaplamak için; Örnek; laktik asit konsantrasyonunun 0, 010 M ve konjuge bazı (laktat) konsantrasyonunun 0, 087 M olduğu laktat tamponunun p. H’ı 4, 80 ise laktik asidin p. Ka değeri? 26

27

• Henderson-Hasselbalch denklemi, herhangi bir p. H’da proton donör ve proton akseptörün molar oranını hesaplamak için; Örnek; asetik asidin p. Ka değeri 4, 76 olduğuna göre asetik asit ve konjuge bazından (asetat) ve p. H’ı 5, 30 olan asetat tamponu hazırlamak için gerekli asetat ve asetik asidin molar konsantrasyon oranı? 28

29

AMFOTER MADDELER Hem proton vericisi (donör), hem proton alıcısı (akseptör) olan maddelere amfoter maddeler denir 30

Amfolitler Hem asitlerle, hem de bazlarla tuz oluşturabilen maddelere amfolitler veya amfoter elektrolitler denir 31

Amfolitler, amfolitin izoelektrik noktası denen bir p. H ortamında, eşit sayıda negatif ( ) ve pozitif (+) yük içerirler (H+A ); -İzoelektrik noktadan düşük p. H ortamında (asit ortam), katyon (pozitif yüklü iyon; H+2 A) halinde bulunurlar -İzoelektrik noktadan yüksek p. H ortamında (bazik ortam) ise anyon (negatif yüklü iyon; A ) halinde bulunurlar 32
İndikatörler Sulu çözeltide ortamın H+ iyonu konsantrasyonuna (p. H’ına) göre renk değiştiren maddelerdir İndikatörler, genellikle amfoter maddelerdir 33
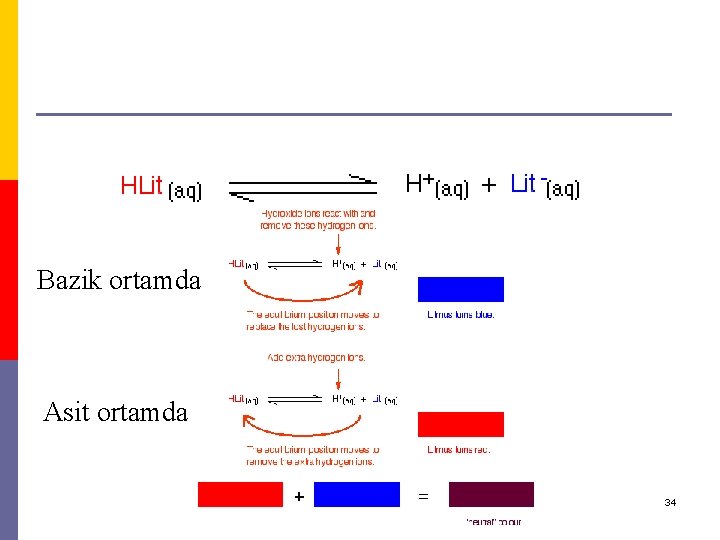
Bazik ortamda Asit ortamda 34
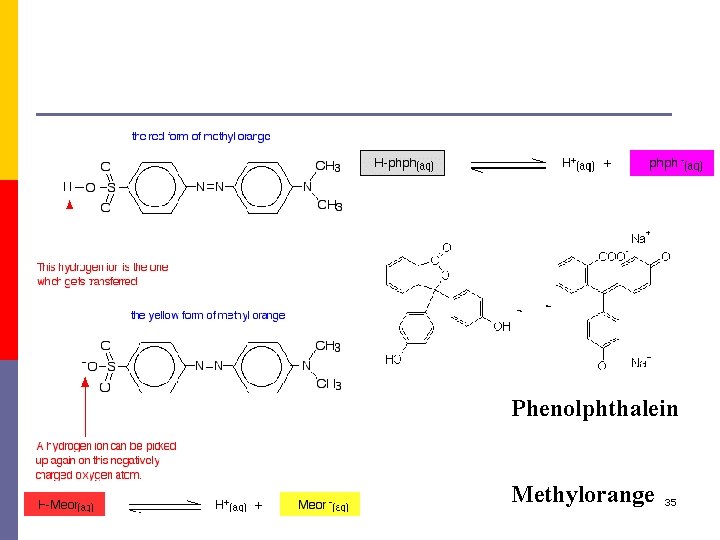
Phenolphthalein Methylorange 35
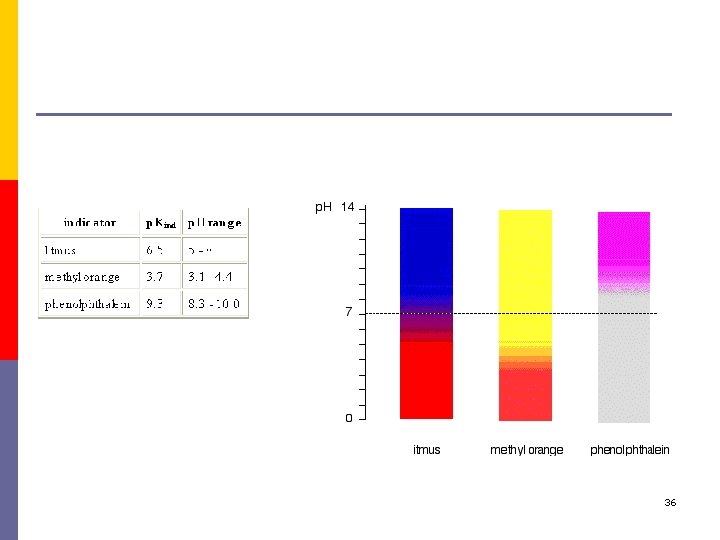
36

İndikatörün renk değiştirdiği noktaya dönüm noktası denir 37

Sulu çözeltilerin p. H’ı, genellikle bir amfolit olan ve ortamın H+ iyonu konsantrasyonuna (p. H) göre renk değiştiren indikatör boyalar yardımıyla ölçülebilir. Bu yöntemlere kolorimetrik yöntemler denir 38
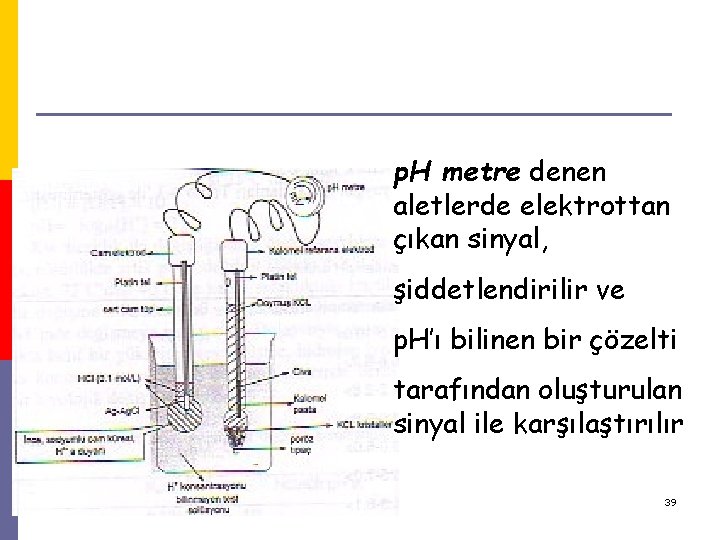
p. H metre denen aletlerde elektrottan çıkan sinyal, şiddetlendirilir ve p. H’ı bilinen bir çözelti tarafından oluşturulan sinyal ile karşılaştırılır 39

Sulu çözeltilerin p. H’ı, elektrometrik yöntemler olarak adlandırılan, iki elektrot arasındaki potansiyel farkının bir galvanometre ile ölçülmesi esasına dayanan yöntemlerle daha hassas olarak ölçülebilir 40

41

ÇÖZELTİ Çözücü (solvent) denen dağıtıcı faz ile bir veya birçok dağıtmış fazdan; çözünen (solut) kurulan sıvı örnek durum çözelti (solusyon) olarak tanımlanır 42

Konsantrasyon Bir çözeltinin konsantrasyonu, çözeltinin belirli bir volümü içinde çözünmüş olan madde (substrat) miktarıdır 43

Çözünen Madde Miktarına göre Çözeltiler; 1) Seyreltik (Dilüe) çözeltiler: çözünmüş madde miktarının az olduğu çözeltilerdir (konsantrasyonu düşük çözeltiler) 2) Derişik (Konsantre) çözeltiler: çözünmüş madde miktarının fazla olduğu çözeltilerdir (konsantrasyonu yüksek çözeltiler) 3) Doymuş (satüre) çözeltiler: çözünmüş madde miktarının maksimum olduğu çözeltilerdir 44

Çözeltilerin Seyreltilmesi Konsantre bir çözeltiden dilüe bir çözelti hazırlanmasına seyreltme denir 1: 10’luk seyreltme yapılırken konsantre çözeltiden 1 birim alınarak toplam hacim olan 10 birime tamamlanır Seri seyreltmeler, içerisinde çözünen madde miktarının gittikçe azaldığı bir seri seyreltmelerdir 45

Çözelti konsantrasyonları Kullanılan bazı ifadeler; -Yüzde (%) -Molarite (M) -Molalite (m) -Normalite (N) 46

Yüzdeler %w/v (ağırlık/hacim) %w/w (ağırlık/ağırlık) %v/v (hacim/hacim) 47

% w/v konsantrasyon %w/v , genellikle g/d. L (g/100 m. L)’ye karşılık gelir Çözelti konsantrasyonu % 5 w/v; 5 gr çözünen 100 m. L çözeltide 48

% w/w konsantrasyon %w/w, genellikle g/g’a karşılık gelir. Çözelti konsantrasyonu % 5 w/w; 5 gr çözünen 100 gr çözeltide 49

% v/v konsantrasyon %v/v, genellikle m. L/m. L’ye karşılık gelir. Hem çözücünün, hem de çözünenin sıvı olduğu çözeltileri ifade etmek için kullanılır. Çözelti konsantrasyonu % 70 v/v; 70 m. L çözünen 100 m. L çözeltide 50

Molarite (M) 1 L çözeltideki mol sayısıdır. Ölçüm birimi mol/L 5 M çözelti; çözeltinin 1 litresinde 5 mol çözünen bulunur 51

Molalite (m) 1000 g çözeltideki mol sayısıdır. 1 molal çözelti; 1000 gr çözücüde 1 mol çözünen bulunur Klinik laboratuvarlarda kullanılan çözeltiler sulu çözeltiler olduğu için molalite ile molarite arasında bir fark yoktur 52

Normalite (N) 1 L çözeltideki ekivalan ağırlık sayısıdır. Ölçüm birimi Eq/L’dir. 2 N çözelti; çözeltinin 1 litresinde 2 Eq çözünen bulunur 53

SU Hem katı hem de sıvı halde iken, birbirine hidrojen köprüsü bağlarıyla bağlanma yeteneğindedir; Su molekülleri, dipol karakterdedir 54

SU Polar biyomoleküller su içerisinde rahatça çözünürler Polar olmayan biyomoleküller su içerisinde zayıf çözünürler. Yağlar ve bunlara bağlı yapılar suda hem çözünmezler, hem de suyla etkileşimden kaçınırlar 55

Suyun iyonizasyonu Hidronyum ve hidroksil iyonlarına ayrışır; Sulu çözeltilerde, saf suda olduğu gibi H+ ile OH konsantrasyonları eşit olduğunda, çözeltinin nötral p. H’ da olduğu ifade edilir Nötral p. H’da H+ ile OH ’nin konsantrasyonu birbirine eşit ve 10 -7 M’dır 56
- Slides: 56