TABLA PERIODICA tablaperver 1 0 La primera persona

TABLA PERIODICA tablaperver 1. 0

La primera persona que intentó imponer algún orden en el caos de los elementos químicos fue Berzelius, clasificándolos en metales y no metales Dobeneiner (Johan W. Dobereiner 1790 -1849) elaboró otra clasificación basada en los pesos atómicos y en algunas propiedades físicas y químicas de los elementos. A estos grupos los denominó triadas y la ley se llamó ley de las triadas. Newlands (John Newlands 1838 -1898) propuso la ley de las octavas. En donde consideró que si se colocan los elementos en orden creciente de sus pesos atómicos, después de cada siete elementos aparece un octavo, cuyas propiedades son semejantes al primero. Chancoutois elaboró otra clasificación en forma de espiral en orden creciente de los pesos atómicos de los elementos al cual llamó caracol telúrico. Mendeleev y Meyer (científico ruso Dimitri Ivanovich Mendeleev 1830 -1990 y el químico alemán de San Petesburgo julio Lothar Meyer 1830 -1900) trabajando de manera independiente, llegaron simultáneamente a clasificar los elementos, basándose en sus propiedades físicas y químicas. Mendeleev, con gran visión dejó los huecos pertenecientes a los elementos desconocidos, anticipando sus propiedades con genial aproximación La clasificación actual se basa en la propuesta de Werner (Alfred Werner) llamada tabla periódica.

IA VIIIA La tabla se divide en dos grupos IIIA Grupo “A” son los elementos representativos IVA VA VIIA

Grupo “B” son los elementos Transición IIIB IVB VB VIIB VIII B IB IIB

IA VIIIA 8 columnas para el grupo “A” … y 10 para IIA IIIA el grupo “B” IIIB IVB VB VIIB VIII B IB IVA VA VIIA
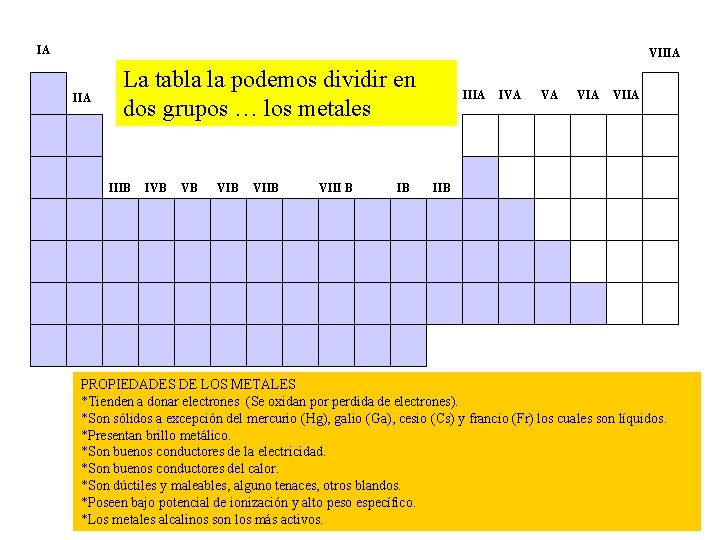
IA VIIIA La tabla la podemos dividir en dos grupos … los metales IIIB IVB VB VIIB VIII B IB IIIA IVA VA VIIA IIB PROPIEDADES DE LOS METALES *Tienden a donar electrones (Se oxidan por perdida de electrones). *Son sólidos a excepción del mercurio (Hg), galio (Ga), cesio (Cs) y francio (Fr) los cuales son líquidos. *Presentan brillo metálico. *Son buenos conductores de la electricidad. *Son buenos conductores del calor. *Son dúctiles y maleables, alguno tenaces, otros blandos. *Poseen bajo potencial de ionización y alto peso específico. *Los metales alcalinos son los más activos.

IA VIIIA Y los no metales IIIA IVA VA VIIA B C N O F IIIB IVB VB VIIB VIII B IB IIB Si P S Cl As Se Br Te I PROPIEDADES DE LOS NO METALES *Tienden a ganar electrones (se reducen por ganancia de electrones) *No poseen aspecto ni brillo metálico. *Son malos conductores de calor y electricidad. *No son dúctiles, maleables, ni tenaces. *Tienen tendencia a ganar electrones *Al unirse son el oxígeno forman anhídridos y estos al reaccionar con el agua forman oxiácidos. *Los halógenos y el oxígeno son los más activos. *Varios no metales presentan alotropía. At

IA IIA En la línea entre los metales y los no metales hay una serie de elementos con características no muy definidas llamados semimetales. IIIB IVB VB VIIB VIII B IB IIB VIIIA IVA VA VIIA B Si Ge As Sb Te Po At

GRUPOS Ó FAMILIAS IA H Li Na K Rb Cs Fr IIA VIIIA La familia de los metales alcalinos IIIB IVB VB VIIB VIII B IB IVA VA VIIA

GRUPOS Ó FAMILIAS IA VIIIA IIA La familia de los metales Be alcalinotérreos Mg Ca Sr Ba Ra IIIB IVB VB VIIB VIII B IB IVA VA VIIA

GRUPOS Ó FAMILIAS IA IIA VIIIA La familia del boro B IIIB IVB VB VIIB VIII B IB IIB Al Ga In Tl IVA VA VIIA

GRUPOS Ó FAMILIAS IA IIA VIIIA La familia del carbono IVA C IIIB IVB VB VIIB VIII B IB IIB Si Ge Sn Pb VA VIIA

GRUPOS Ó FAMILIAS IA IIA VIIIA La familia del nitrógeno IVA VA N IIIB IVB VB VIIB VIII B IB IIB P As Sb Bi VIA VIIA

GRUPOS Ó FAMILIAS IA IIA VIIIA La familia del oxigeno o también llamada calcógenos IIIB IVB VB VIIB VIII B IB IIIA IVA VA VIA O S Se Te Po VIIA

GRUPOS Ó FAMILIAS IA IIA VIIIA La familia de los halógenos IVA VA VIIA F IIIB IVB VB VIIB VIII B IB IIB Cl Br I At

GRUPOS Ó FAMILIAS IA IIA VIIIA La familia de los gases nobles o gases inertes. IIIB IVB VB VIIB VIII B IB IVA VA VIIA He Ne IIB Ar Kr Xe Rn

GRUPOS Ó FAMILIAS IA IIA VIIIA Los metales de transición IIIB IVB VB VIIB VIII B IB IIB Sc Ti V Cr Mn Fe Co Ni Cu Zn Y Zr Nb Mo Tc Ru Rh Pd Ag Cd La Hf Ta w Re Os Ir Pt Au Hg Ac Rf Ha Sg Ns Hs Mt. Uun. Uuu IVA VA VIIA
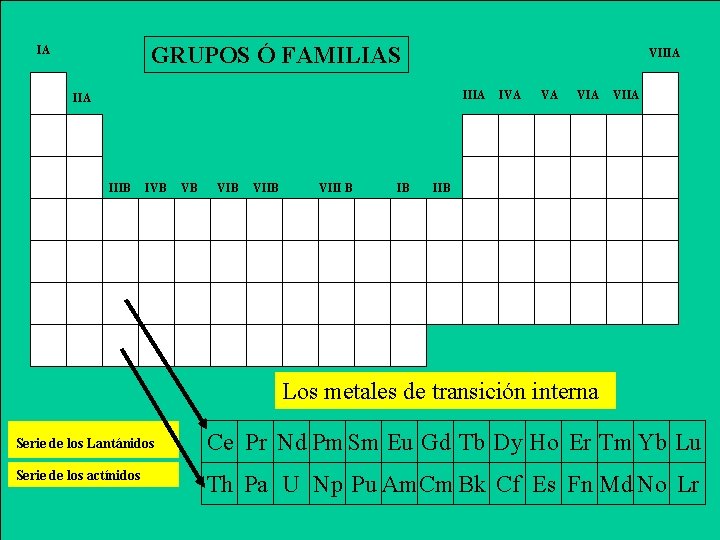
GRUPOS Ó FAMILIAS IA VIIIA IIA IIIB IVB VB VIIB VIII B IB IVA VA VIIA IIB Los metales de transición interna Serie de los Lantánidos Serie de los actínidos Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Th Pa U Np Pu Am. Cm Bk Cf Es Fn Md No Lr

PERIODOS IA 1 2 3 4 5 6 7 IIA VIIIA La tabla tiene 7 periodos horizontales IIIB IVB VB VIIB VIII B IB IVA VA VIIA

PERIODOS IA 1 2 3 4 5 6 7 IIA VIIIA La tabla tiene 7 periodos horizontales IIIB IVB VB VIIB VIII B IB IVA VA VIIA

PERIODOS IA 1 2 3 4 5 6 7 IIA VIIIA La tabla tiene 7 periodos horizontales IIIB IVB VB VIIB VIII B IB IVA VA VIIA

PERIODOS IA 1 2 3 4 5 6 7 IIA VIIIA La tabla tiene 7 periodos horizontales IIIB IVB VB VIIB VIII B IB IVA VA VIIA

PERIODOS IA 1 2 3 4 5 6 7 IIA VIIIA La tabla tiene 7 periodos horizontales IIIB IVB VB VIIB VIII B IB IVA VA VIIA

PERIODOS IA 1 2 3 4 5 6 7 IIA VIIIA La tabla tiene 7 periodos horizontales IIIB IVB VB VIIB VIII B IB IVA VA VIIA

PERIODOS IA 1 2 3 4 5 6 7 IIA VIIIA La tabla tiene 7 periodos horizontales IIIB IVB VB VIIB VIII B IB IVA VA VIIA

¿Sabes qué se necesita para elaborar Tiempo de Éxito? AYUDANOS A MANTENER ESTA PÁGINA Nuestra página es de carácter didáctico y actualmente estamos trabajando en las materias de Química inorgánica, Química orgánica, Introducción a la Bioquímica, Álgebra y Biología I. Si te ha servido en algo y deseas apoyar para que se pueda conservar esta pagina web, de antemano mil gracias, tu aportación por pequeña que sea es muy importante. www. tiempodeexito. com
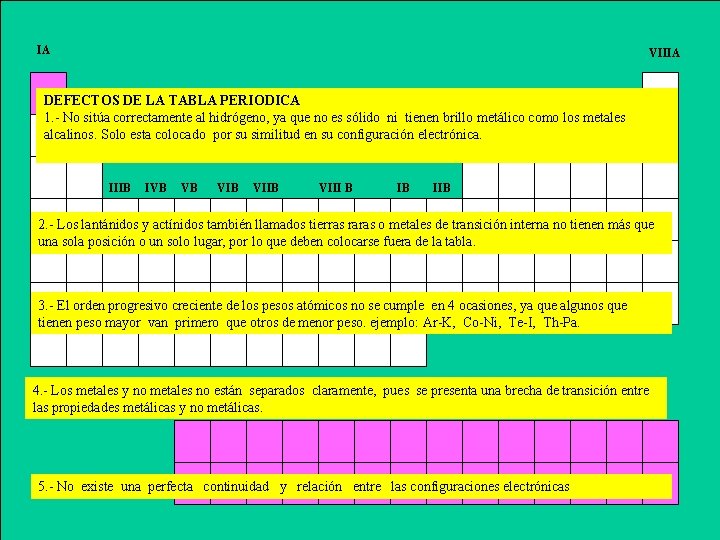
IA VIIIA IVA VA VIIA IIA DEFECTOS DE LA TABLA PERIODICA 1. - No sitúa correctamente al hidrógeno, ya que no es sólido ni tienen brillo metálico como los metales alcalinos. Solo esta colocado por su similitud en su configuración electrónica. IIIB IVB VB VIIB VIII B IB IIB 2. - Los lantánidos y actínidos también llamados tierras raras o metales de transición interna no tienen más que una sola posición o un solo lugar, por lo que deben colocarse fuera de la tabla. 3. - El orden progresivo creciente de los pesos atómicos no se cumple en 4 ocasiones, ya que algunos que tienen peso mayor van primero que otros de menor peso. ejemplo: Ar-K, Co-Ni, Te-I, Th-Pa. 4. - Los metales y no metales no están separados claramente, pues se presenta una brecha de transición entre las propiedades metálicas y no metálicas. 5. - No existe una perfecta continuidad y relación entre las configuraciones electrónicas
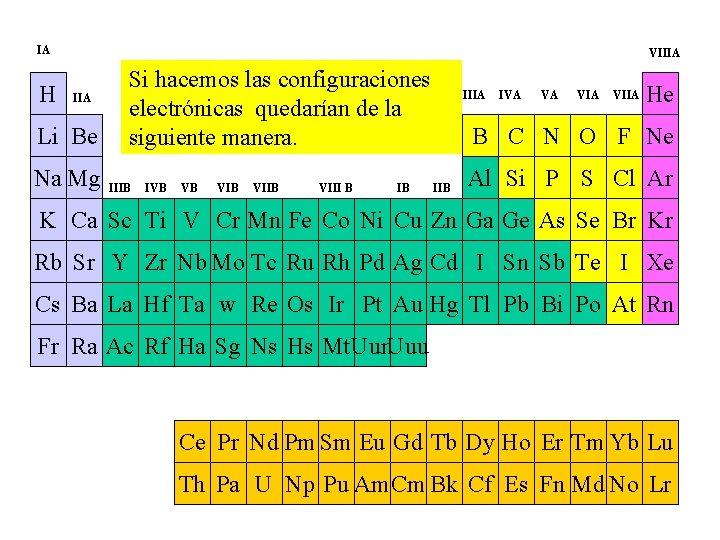
IA H VIIIA Li Be Na Mg Si hacemos las configuraciones electrónicas quedarían de la siguiente manera. IIIB IVB VB VIIB VIII B IB IIIA IVA VA VIIA He B C N O F Ne IIB Al Si P S Cl Ar K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd I Sn Sb Te I Xe Cs Ba La Hf Ta w Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn Fr Ra Ac Rf Ha Sg Ns Hs Mt. Uun. Uuu Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Th Pa U Np Pu Am. Cm Bk Cf Es Fn Md No Lr
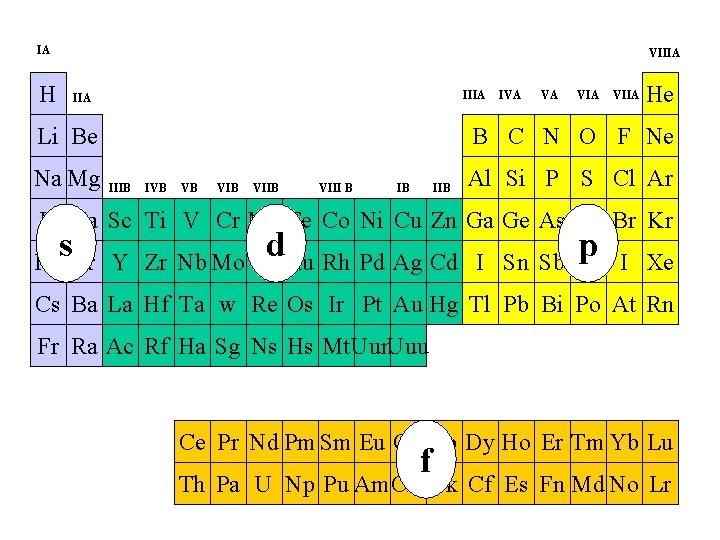
IA VIIIA H IIIA Li Be Na Mg IVA VA VIIA He B C N O F Ne IIIB IVB VB VIIB VIII B IB IIB Al Si P S Cl Ar K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr s d p Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd I Sn Sb Te I Xe Cs Ba La Hf Ta w Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn Fr Ra Ac Rf Ha Sg Ns Hs Mt. Uun. Uuu Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu f Th Pa U Np Pu Am. Cm Bk Cf Es Fn Md No Lr
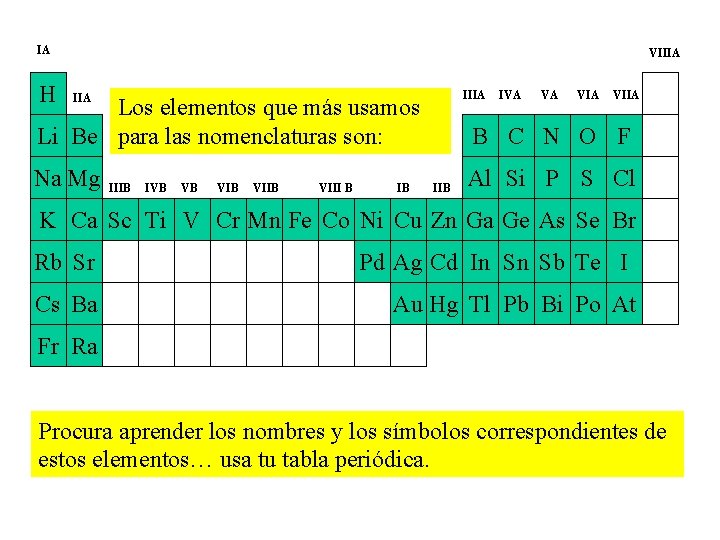
IA H VIIIA IIA Los elementos que más usamos Li Be para las nomenclaturas son: Na Mg IIIB IVB VB VIIB VIII B IB IVA VA VIIA B C N O F IIB Al Si P S Cl K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Rb Sr Cs Ba Pd Ag Cd In Sn Sb Te I Au Hg Tl Pb Bi Po At Fr Ra Procura aprender los nombres y los símbolos correspondientes de estos elementos… usa tu tabla periódica.
IA H VIIIA Usos de algunos elementos son: haz clic IIIB IVB VB VIIB VIII B IB IVA VA VIIA

HIDRÓGENO
IA VIIIA IIA Mg IIIB IVB VB VIIB VIII B IB IVA VA VIIA

MAGNESIO
IA VIIIA IIA IIIB IVB VB VIIB VIII B IB IIB Al IVA VA VIIA

ALUMINIO
IA VIIIA IIA IVA C IIIB IVB VB VIIB VIII B IB IIB VA VIIA

CARBONO

- Slides: 39