TABLA PERIDICA Su construccin desde la Distribucin Electrnica

TABLA PERIÓDICA Su construcción desde la Distribución Electrónica Autor: IQ Luís Fernando Montoya Valencia. luismontoy@une. net. co Profesor titular Centro de Ciencia Básica Escuela de ingenierías A un “Clic” del conocimiento http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es

El objetivo de este trabajo es presentar Una fundamentación teórica, relacionada desde lo cotidiano, resumida en un algoritmo Varios ejemplos orientados desde el algoritmo El reto es “IMAGINAR” (respaldado en el permitan: algoritmo), que va a Para desarrollar competencias que aparecer con ella siguiente “clic”, si estamos de acuerdo § Construir tabla periódica continuar, y si no regresar para al final poder afirmar -!lo § Analizar propiedades periódicas hicimos¡§ Dominar los no metales A un “Clic” del conocimiento http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es
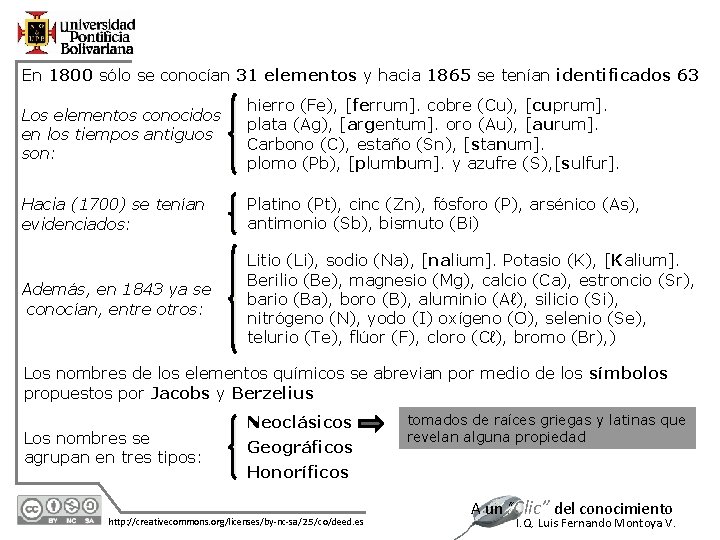
En 1800 sólo se conocían 31 elementos y hacia 1865 se tenían identificados 63 Los elementos conocidos en los tiempos antiguos son: hierro (Fe), [ferrum]. cobre (Cu), [cuprum]. plata (Ag), [argentum]. oro (Au), [aurum]. Carbono (C), estaño (Sn), [stanum]. plomo (Pb), [plumbum]. y azufre (S), [sulfur]. Hacia (1700) se tenían evidenciados: Platino (Pt), cinc (Zn), fósforo (P), arsénico (As), antimonio (Sb), bismuto (Bi) Además, en 1843 ya se conocían, entre otros: Litio (Li), sodio (Na), [nalium]. Potasio (K), [Kalium]. Berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba), boro (B), aluminio (Aℓ), silicio (Si), nitrógeno (N), yodo (I) oxígeno (O), selenio (Se), telurio (Te), flúor (F), cloro (Cℓ), bromo (Br), ) Los nombres de los elementos químicos se abrevian por medio de los símbolos propuestos por Jacobs y Berzelius Los nombres se agrupan en tres tipos: 12/1/2020 Neoclásicos Geográficos tomados de raíces griegas y latinas que revelan alguna propiedad Honoríficos http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

En 1869 Lothar Meyer publicó un esquema de clasificación basado en orden creciente de peso atómico En marzo de 1869 Dimitri Mendeléiev entregaba a los químicos rusos y alemanes su primera tabla periódica, basado también, en orden creciente de peso atómico En ésta, los elementos con propiedades semejantes se distribuían en líneas horizontales. Los espacios vacíos habrían de ser, algunos años mas tarde, rellenados por elementos cuyas propiedades Mendeléiev ya había previsto con gran precisión. Con la introducción del concepto del número atómico (Z) formulado por el químico inglés Moseley, en 1913, se comprobó que las propiedades químicas de los elementos son una función periódica de ese número atómico y no de la masa atómica. Este nuevo concepto no invalidó la tabla ordenada por Mendeléiev, sino que por el contrario aclaró algunas discrepancias que aún quedaban en ella. 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

PRESENTACIÓN: La tabla periódica (TP) es una cuadrícula en la cual se ubican los diferentes elementos según su DISTRIBUCIÓN ELECTRÓNICA (DE) En muchos textos nos dicen que es según su número atómico (Z), esta afirmación puede inducir que la ubicación de los elementos en la tabla periódica no depende de la distribución electrónica Para determinar la celda de cada elemento, en la cual se asigna su símbolo, hay que definir la columna (vertical) y la fila (horizontal), conocida como período, basados en su distribución electrónica (DE) abreviada La columna está dada por La fila (período), está dada por el la “terminación” de la DE máximo coeficiente del subnivel s Celda (coincide con el retén) En algunos textos, la fila la particularizan según la terminación de la DE, así: Si termina en el subnivel s su coeficiente es el período Si termina en el subnivel p su coeficiente es el período Si termina en el subnivel d su coeficiente mas uno es el período Si termina en el subnivel f su coeficiente mas dos es el período ¿Que ocurrirá cuando termine en g? 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Como las columnas están dadas por la terminación de la DE, en la tabla periódica actual existen 4 zonas: Zona s con dos columnas: s 1 y s 2 Zona p con seis columnas: desde p 1 hasta p 6 Zona d Zona f con diez columnas: desde d 1 hasta d 10 con catorce columnas: desde f 1 hasta f 14 El orden de dichas zonas (por DE) es s, f, d, p n retenes 1 2 3 1 s 2 4 12 4 5 6 7 20 38 2 s 2 p 3 s 3 p 3 d 4 f 5 d 6 p Primero ubicamos los retenes, ya que son los números atómicos conocidos por todos Z DE abreviada columna fila 2 1 s 2 1 s 2 2 4 s 4 p 4 d 4 f 4 1 s… 2 s 2 5 s 5 p 5 d 5 f 12 1 s… 3 s 2 3 6 s 6 p 6 d 6 f 20 1 s… 4 s 2 4 7 s 7 p 7 d 7 f 38 1 s… 5 s 2 5 0 1 2 3 56 1 s… 6 s 2 6 88 1 s… 7 s 2 7 56 88 ℓ Herramienta para DE 6 s 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es La ubicación de los retenes es tan elemental Como “copiar pegar” o “Ctrlc Ctrlv” A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Zona f Períodos o filas Zona s S 1 S 2 f 1 1 1 2 2 3 4 3 11 12 f 3 f 5 f 6 f 8 Zona d f 10 f 12 f 14 d 1 de 14 x 7 = 98 celdas sólo se ocupan 14 x 2 d 3 d 5 Zona p d 7 d 9 p 1 p 2 p 3 p 4 p 5 p 6 5 6 7 8 9 10 13 14 15 16 17 18 4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 5 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 6 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 7 87 88 89 90 91 92 93 94 95 96 97 98 99 100 101 102 103 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 retenes Post retenes Anti retenes Por lógica, a la izquierda de cada retén ubicamos el anterior de cada retén, (anti - retén) Por DE, a la derecha de cada retén ubicamos el posterior de cada retén, (post - retén) Z 5 DE abreviada columna fila 1 s… 2 s 2 2 p 1 2 13 1 s… 3 s 2 3 p 1 3 21 1 s… 4 s 2 3 d 1 4 39 57 1 s… 5 s 2 4 d 1 1 s… 6 s 2 4 f 1 d 1 f 1 5 6 89 1 s… 7 s 2 5 f f 7 12/1/2020 1 1 Por DE podemos completar con “el que sigue”, (norma de Aufbau) Vemos que en la zona f hay un gran desperdicio de papel, para imprimir “ecológicamente” los tipógrafos recortan las dos filas (tierras raras) y queda una tabla de 18 columnas, conocida como la tabla capicúa en la cual están los elementos capitales (importantes) http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Zona s Zona d 2 3 4 3 11 12 4 19 20 5 37 38 Zona f 2 7 87 88 Tabla capicúa 5 6 7 8 9 10 13 14 15 16 17 18 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 6 55 56 Períodos o 1 1 p 2 p 3 p 4 p 5 p 6 filas s 1 s 2 Zona p 103 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 Uno de los pocos textos que tiene bien el corte de la zona f es el la American Chemical Society: “Química un Proyecto de la ACS”. Editorial REVERTÉ. España 2005 fila f 1 f 2 f 3 f 4 f 5 f 6 f 7 f 8 f 9 f 10 f 11 f 12 f 13 f 14 6 57 58 59 60 61 62 63 64 65 66 67 68 69 70 Lantánidos el elemento Z = 57 es el lantano (La) 7 89 90 91 92 93 94 95 96 97 98 99 100 101 102 Actínidos el elemento Z = 89 es el actinio (Ac) Tierras raras Los tipógrafos no saben química o no saben contar, al recortar la Zona f: algunos cortan del 58 al 71 y del 90 al 103, otros cortan del 57 al 71 y del 89 al 103 Observe que tipo de error posee su tabla periódica 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
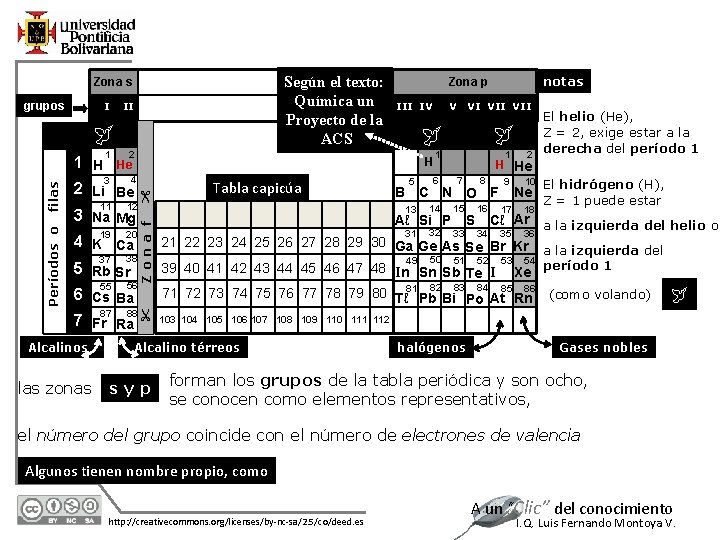
Según el texto: Química un Proyecto de la ACS Zona s grupos I II Zona f 20 55 56 6 Cs Ba 88 87 7 Fr Ra las zonas V Tabla capicúa 1 1 2 El helio (He), Z = 2, exige estar a la derecha del período 1 H He 5 6 7 13 14 15 31 32 33 82 83 8 B C N O F Aℓ Si P S 16 34 9 10 Ne 17 18 35 36 El hidrógeno (H), Z = 1 puede estar Cℓ Ar a la izquierda del helio o 21 22 23 24 25 26 27 28 29 30 Ga Ge As Se Br Kr a la izquierda del 49 50 51 52 53 54 39 40 41 42 43 44 45 46 47 48 In Sn Sb Te I Xe período 1 84 86 71 72 73 74 75 76 77 78 79 80 Tℓ 81 Pb Bi Po At 85 Rn (como volando) 103 104 105 106 107 108 109 110 111 112 Alcalino térreos syp VI VII H Períodos o 19 4 K Ca 38 37 5 Rb Sr Alcalinos III IV 2 filas 1 1 H He 4 3 2 Li Be 12 11 3 Na Mg notas Zona p halógenos Gases nobles forman los grupos de la tabla periódica y son ocho, se conocen como elementos representativos, el número del grupo coincide con el número de electrones de valencia Algunos tienen nombre propio, como 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Nota: en 1966 Georgii Flerov y otros científicos prepararon el elemento 104 y lo llamaron Kurchatovio, (en honor a un físico nuclear ruso), pero Ghiorso lo había identificado como Rutherforio. Una disputa similar ocurrió entre 1967 y 1970 con el elemento 105 denominado Nielsborio por los soviéticos y Hahnio por los estadounidenses. Para evitar disputas políticas y nacionalistas la IUPAC (Unión Internacional de Química Pura y Aplicada) decidió que los elementos posteriores al 103 no podrían llevar nombres relacionados con personas (honoríficos), lugares o cuerpos celestes (geográficos) La IUPAC estableció un código numérico para identificarlos (nil=0, un=1, bi=2, etc. ) y la adición del sufijo “ium”. Obedeciendo la IUPAC: El 104 se llama: El 105 es: un-nil-quart-ium ( unilquartium), y su símbolo en Unq un-nil-pent-ium (unilpentium), y su símbolo en Unp El nombre del elemento 111, usando el código numérico sería: un-un-un-ium 12/1/2020 (unununium), y su símbolo en Uuu http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
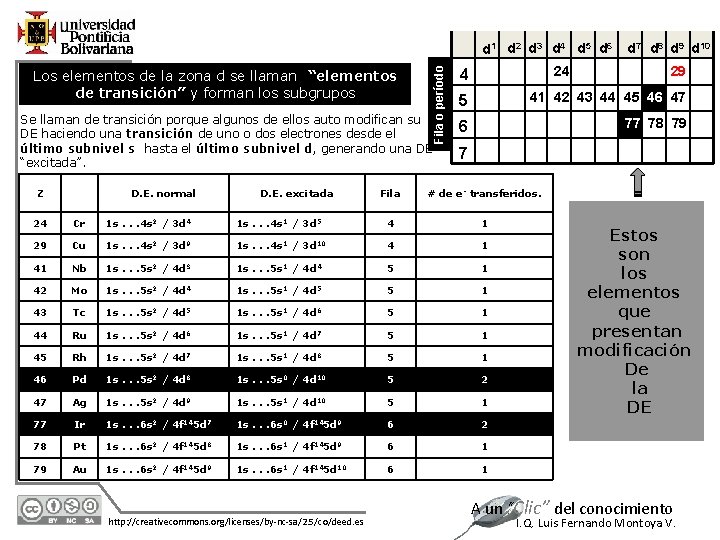
Los elementos de la zona d se llaman “elementos de transición” y forman los subgrupos Fila o período d 1 d 2 d 3 d 4 d 5 d 6 Se llaman de transición porque algunos de ellos auto modifican su DE haciendo una transición de uno o dos electrones desde el último subnivel s hasta el último subnivel d, generando una DE “excitada”. Z D. E. normal D. E. excitada 4 21 22 23 24 25 26 27 28 29 30 5 39 40 41 42 43 44 45 46 47 48 6 71 72 73 74 75 76 77 78 79 80 7 103 104 105 106 107 108 109 110 111 112 Fila # de e- transferidos. 24 Cr 1 s. . . 4 s 2 / 3 d 4 1 s. . . 4 s 1 / 3 d 5 4 1 29 Cu 1 s. . . 4 s 2 / 3 d 9 1 s. . . 4 s 1 / 3 d 10 4 1 41 Nb 1 s. . . 5 s 2 / 4 d 3 1 s. . . 5 s 1 / 4 d 4 5 1 42 Mo 1 s. . . 5 s 2 / 4 d 4 1 s. . . 5 s 1 / 4 d 5 5 1 43 Tc 1 s. . . 5 s 2 / 4 d 5 1 s. . . 5 s 1 / 4 d 6 5 1 44 Ru 1 s. . . 5 s 2 / 4 d 6 1 s. . . 5 s 1 / 4 d 7 5 1 45 Rh 1 s. . . 5 s 2 / 4 d 7 1 s. . . 5 s 1 / 4 d 8 5 1 46 Pd 1 s. . . 5 s 2 / 4 d 8 1 s. . . 5 s 0 / 4 d 10 5 2 47 Ag 1 s. . . 5 s 2 / 4 d 9 1 s. . . 5 s 1 / 4 d 10 5 1 77 Ir 1 s. . . 6 s 2 / 4 f 145 d 7 1 s. . . 6 s 0 / 4 f 145 d 9 6 2 78 Pt 1 s. . . 6 s 2 / 4 f 145 d 8 1 s. . . 6 s 1 / 4 f 145 d 9 6 1 79 Au 1 s. . . 6 s 2 / 4 f 145 d 9 1 s. . . 6 s 1 / 4 f 145 d 10 6 1 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es d 7 d 8 d 9 d 10 Estos son los elementos que presentan modificación De la DE A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
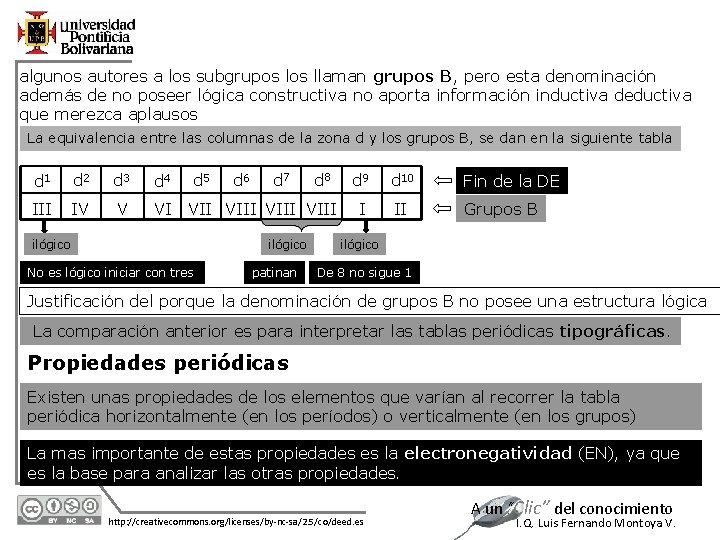
algunos autores a los subgrupos llaman grupos B, pero esta denominación además de no poseer lógica constructiva no aporta información inductiva deductiva que merezca aplausos La equivalencia entre las columnas de la zona d y los grupos B, se dan en la siguiente tabla d 1 d 2 d 3 d 4 III IV V VI d 5 d 6 d 7 d 8 VIII ilógico No es lógico iniciar con tres patinan d 9 d 10 Fin de la DE I II Grupos B ilógico De 8 no sigue 1 Justificación del porque la denominación de grupos B no posee una estructura lógica La comparación anterior es para interpretar las tablas periódicas tipográficas. Propiedades periódicas Existen unas propiedades de los elementos que varían al recorrer la tabla periódica horizontalmente (en los períodos) o verticalmente (en los grupos) La mas importante de estas propiedades es la electronegatividad (EN), ya que es la base para analizar las otras propiedades. 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Electronegatividad (EN) Indica la fuerza con la cual el núcleo atrae los electrones de valencia, existen varias escalas de valores de EN arbitrariamente establecidas, la mas divulgada es la escala de Linus Pauling que posee para el flúor un valor máximo de 4. 0 y para el Francio un valor mínimo de 0. 7 Mayor EN F Fr En los períodos aumenta de izquierda a derecha En los grupos aumenta de abajo a arriba grupos Los elementos de baja EN tienden a perder electrones y adquieren carga positiva y se clasifican como + metales M Los elementos de alta EN tienden a ganar electrones y adquieren carga negativa y se clasifican como no metales n. M Los no metales se encuentran en la parte superior derecha de la tabla, y son 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es Fila o período Menor EN Periódicamente la EN aumenta del Fr al F III IV V VI VII 2 B C N O F 3 Si P S Cℓ 4 As Se Br 5 6 Te I At A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
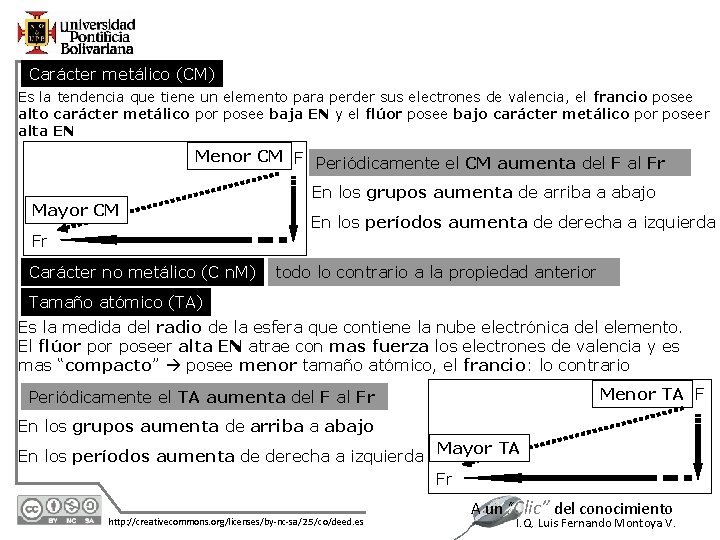
Carácter metálico (CM) Es la tendencia que tiene un elemento para perder sus electrones de valencia, el francio posee alto carácter metálico por posee baja EN y el flúor posee bajo carácter metálico por poseer alta EN Menor CM F Periódicamente el CM aumenta del F al Fr Mayor CM Fr Carácter no metálico (C n. M) En los grupos aumenta de arriba a abajo En los períodos aumenta de derecha a izquierda todo lo contrario a la propiedad anterior Tamaño atómico (TA) Es la medida del radio de la esfera que contiene la nube electrónica del elemento. El flúor poseer alta EN atrae con mas fuerza los electrones de valencia y es mas “compacto” posee menor tamaño atómico, el francio: lo contrario Menor TA F Periódicamente el TA aumenta del F al Fr En los grupos aumenta de arriba a abajo En los períodos aumenta de derecha a izquierda Mayor TA Fr 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
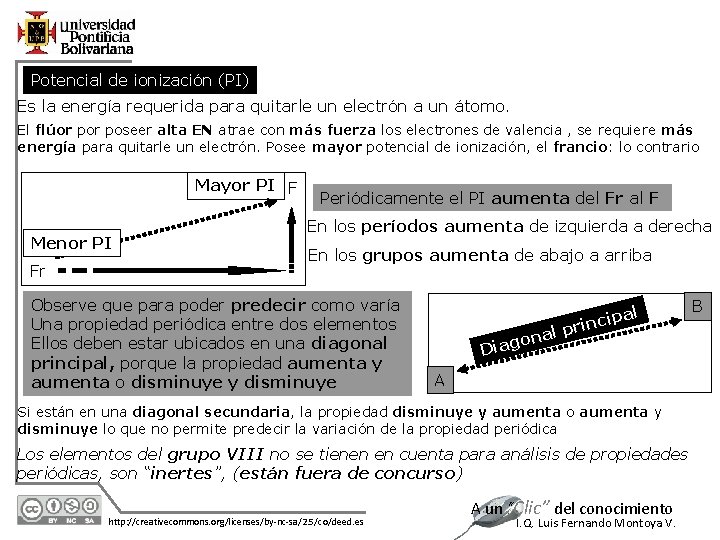
Potencial de ionización (PI) Es la energía requerida para quitarle un electrón a un átomo. El flúor poseer alta EN atrae con más fuerza los electrones de valencia , se requiere más energía para quitarle un electrón. Posee mayor potencial de ionización, el francio: lo contrario Mayor PI F Menor PI Fr Periódicamente el PI aumenta del Fr al F En los períodos aumenta de izquierda a derecha En los grupos aumenta de abajo a arriba Observe que para poder predecir como varía Una propiedad periódica entre dos elementos Ellos deben estar ubicados en una diagonal principal, porque la propiedad aumenta y aumenta o disminuye y disminuye D nal o g a i l p ipa rinc A Si están en una diagonal secundaria, la propiedad disminuye y aumenta o aumenta y disminuye lo que no permite predecir la variación de la propiedad periódica Los elementos del grupo VIII no se tienen en cuenta para análisis de propiedades periódicas, son “inertes”, (están fuera de concurso) 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V. B

Los elementos del grupo VIII cumplen la norma del octeto y poseen distribución electrónica estable, no tienden a ganar ni a perder electrones, por esto se conocen como elementos inertes o nobles Los elementos representativos tratan de ganar o perder electrones para adquirir la configuración electrónica del gas noble mas próximo a ellos formando iones isoelectrónicos (igual número de electrones) con dicho gas noble Estos iones poseen una carga característica (típica), dependiendo del grupo al cual pertenece el elemento, así: Los metales alcalinos tienden a perder un electrón originando iones de carga +1 Los metales alcalino térreos tienden a perder dos electrones originando iones de carga Los halógenos tienden a ganar un electrón originando iones de carga +2 -1 Los anfígenos (grupo VI) térreos tienden a ganar dos electrones originando iones de carga - 2 En estado libre, son diatómicos (X 2): O, N, H y los halógenos El enlace formado entre no metales se conoce como enlace covalente y las cargas son aparentes, los electrones se comparten El enlace formado entre no metal y metal se conoce como enlace iónico y las cargas son reales, los electrones se transfieren 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Ilustraciones: Para los siguientes elementos hipotéticos, determinar su número atómico si de ellos conocemos: A está en el período 4, columna d 7. o sus coordenadas son (d 7, 4) Procedimiento: como pertenece al período 4, (el período está dado por el máximo coeficiente del subnivel s), su DE va desde 1 s hasta el retén 4 s van 20 ey continuamos la DE hasta el siguiente d 7, ( la terminación de la DE nos 7 confirma la columna), así: 1 s … 4 s /3 d Van 20 e- R/ el número atómico de A es 20 + 7 = 27 Este ejercicio puede llevar a equivocaciones a quienes crean que la DE va desde: 1 s … hasta 4 d 7 1 s … 5 s/ 4 d 7 van 38 e- Quien cometa este error está cambiando la definición de período. el número atómico sería 45, pero este elemento está en el período 5 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

B está en el período 6, columna f 10. sus coordenadas son (f 10, 6) Procedimiento: como pertenece al período 6, (el período está dado por el máximo coeficiente del subnivel s), su DE va desde 1 s hasta el retén 6 s van 56 ey continuamos la DE hasta el siguiente f 10, ( la terminación de la DE nos confirma la columna), así: 1 s … 6 s /4 f 10 Van 56 e- R/ el número atómico de B es 56 + 10 = 66 Si cambia la definición de período, cree que la DE termina en 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es 6 f 10 A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

C si gana tres electrones queda “isoelectrónico” con el gas noble del período 5 Procedimiento: isoelectrónico significa: - iso (igual), electrónico (electrones) - que cuando el elemento gana tres electrones queda con el mismo número de electrones del gas noble del período 5 Vamos a determinar cuántos electrones tiene el gas noble del período 5. Su DE va desde 1 s hasta el retén 5 s van 38 ey continuamos la DE hasta el siguiente p 6, (los gases nobles son los del grupo VIII, columna p 6) 1 s … 5 s /4 d 10 5 p 6 van 38 e- El número atómico del gas noble es: 38 + 10 + 6 = 54 C después de ganar 3 e- queda con 54 e-, (isoelectrónicos) por lo tanto él tenía 51 e. R/ el número atómico de C es 51 Su DE es: 1 s … 5 s /4 d 10 5 p 3 (p 3, 5) van 38 e 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

D está en el período 6, columna p 4. sus coordenadas son (p 4, 6) Procedimiento: como pertenece al período 6, (el período está dado por el máximo coeficiente del subnivel s), su DE va desde 1 s hasta el retén 6 s van 56 ey continuamos la DE hasta el siguiente p 4, ( la terminación de la DE nos confirma la columna), así: 1 s … 6 s /4 f 14 5 d 106 p 4 Van 56 e- R/ el número atómico de D es 56 + 14 + 10 + 4 = 84 E es el halógeno del período 3 Vamos a determinar cuántos electrones tiene el halógeno del período 3. Su DE va desde 1 s hasta el retén 3 s van 12 ey continuamos la DE hasta el siguiente p 5, (los halógenos son los del grupo VII, columna p 5) (p 5, 3) 1 s … 3 s /3 p 5 van 12 e- R/ El número atómico de E es: 12 + 5 = 17 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

F es el metal alcalino del período 7 Vamos a determinar cuántos electrones tiene el metal alcalino térreo del período 7. Su DE va desde 1 s hasta el retén 7 s 2 van 88 ela DE termina en s 1, (los alcalino son los del grupo I, columna s 1) R/ el número atómico de F es 88 - 1 1 s … 7 s 1 (s 1, 7) G está en el período 3, y posee cinco electrones de valencia Procedimiento: como pertenece al período 3, (el período está dado por el máximo coeficiente del subnivel s), su DE va desde 1 s hasta el retén 3 s van 12 ey continuamos la DE hasta el siguiente p 3. Por poseer cinco electrones de valencia está en el grupo V, columna p 3 (el número de electrones de valencia y el grupo coinciden), así: 1 s … 3 s /3 p 3 (p 3, 3) Van 12 e- R/ el número atómico de G es 12 + 3 = 15 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.

Los iones H 2 -, I 1+ son isoelectrónicos con J 1 - y el número atómico de J es 53 Iniciamos el análisis con el elemento J, ya que de él conocemos su número atómico J posee 53 electrones Su DE es: 1 s … 5 s /4 d 10 5 p 5 (p 5, 5) van 38 e- Para J ser ión de carga -1 gana un electrón Los iones H 2 -, I 1+ y J 1 - poseen 54 electrones J 1 - posee 54 electrones por ser isoelectrónicos H gana dos electrones para ser el ión H 2 - y queda con 54 electrones H tenía 52 electrones Su DE es: R/ 1 s … 5 s /4 d 10 5 p 4 el número atómico de H es 52 (p 4, 5) van 38 e- I pierde un electrón para ser el ión I 1+ y queda con 54 electrones I tenía 55 electrones Su DE es: R/ 1 s … 5 s /4 d 10 5 p 66 s 1 el número atómico de I es 55 (s 1, 6) van 38 e 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
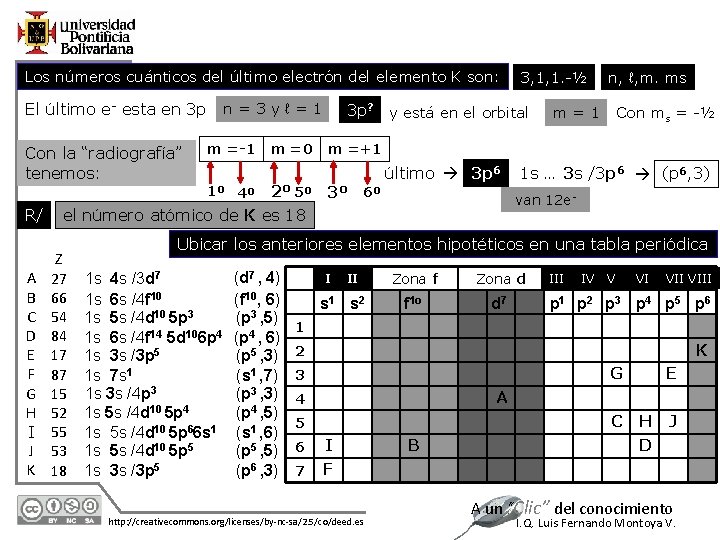
Los números cuánticos del último electrón del elemento K son: El último e- esta en 3 p Con la “radiografía” tenemos: R/ A B C D E F G H I J K n=3 yℓ=1 m =-1 m =0 3 p? y está en el orbital n, ℓ, m. ms m=1 Con ms = -½ m =+1 2º 5º 3º 6º el número atómico de K es 18 Z 27 66 54 84 17 87 15 52 55 53 18 3, 1, 1. -½ 1º 4º último 3 p 6 1 s … 3 s /3 p 6 (p 6, 3) van 12 e- Ubicar los anteriores elementos hipotéticos en una tabla periódica 1 s 4 s /3 d 7 1 s 6 s /4 f 10 1 s 5 s /4 d 10 5 p 3 1 s 6 s /4 f 14 5 d 106 p 4 1 s 3 s /3 p 5 1 s 7 s 1 1 s 3 s /4 p 3 1 s 5 s /4 d 10 5 p 4 1 s 5 s /4 d 10 5 p 66 s 1 1 s 5 s /4 d 10 5 p 5 1 s 3 s /3 p 5 12/1/2020 (d 7 , 4) (f 10, 6) (p 3 , 5) (p 4 , 6) (p 5 , 3) (s 1 , 7) (p 3 , 3) (p 4 , 5) (s 1 , 6) (p 5 , 5) (p 6 , 3) I II s 1 s 2 Zona f Zona d f 1 o d 7 III IV V VI VIII p 1 p 2 p 3 p 4 p 5 p 6 1 K 2 3 G E C H J D A 4 5 6 I 7 F http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es B A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
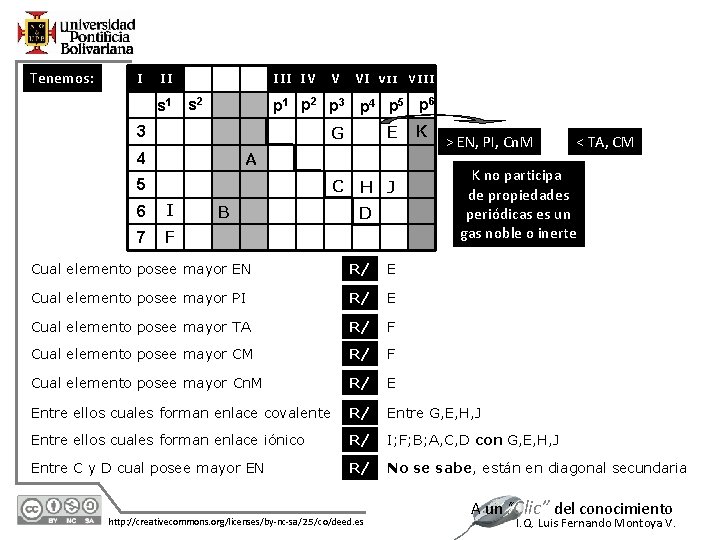
Tenemos: I II IV V s 1 s 2 p 1 p 2 p 3 p 4 p 5 p 6 3 VI VIII G E C H J A 4 5 6 I 7 F B D K > EN, PI, Cn. M < TA, CM K no participa de propiedades periódicas es un gas noble o inerte Cual elemento posee mayor EN R/ E Cual elemento posee mayor PI R/ E Cual elemento posee mayor TA R/ F Cual elemento posee mayor CM R/ F Cual elemento posee mayor Cn. M R/ E Entre ellos cuales forman enlace covalente R/ Entre G, E, H, J Entre ellos cuales forman enlace iónico R/ I; F; B; A, C, D con G, E, H, J Entre C y D cual posee mayor EN R/ No se sabe, están en diagonal secundaria 12/1/2020 http: //creativecommons. org/licenses/by-nc-sa/2. 5/co/deed. es A un “Clic” del conocimiento I. Q. Luis Fernando Montoya V.
- Slides: 24