Tabla Peridica Propiedades Peridicas Colegio Agustiniano El Bosque

Tabla Periódica Propiedades Periódicas Colegio Agustiniano El Bosque Un proyecto educativo único y propio Ciencias Naturales Química / 8° Básico

Objetivos y contenidos a tratar ü v v Contenidos Objetivos Propiedades Atómicas: Radio atómico (R. A. ) Energía de ionización (E. I. ) Afinidad electrónica (A. E. ) Electronegatividad (E. N. ) Conocer y comprender en que consisten las Propiedades atómicas, como se clasifican, caracterizan y utilizan para el estudio de los átomos en la tabla periódica y la importancia del orden electrónica para comprender su interacción con otros átomos, principalmente en la formación de nuevos compuestos.

Orientaciones para el estudio de este tema… Pon atención a los siguientes puntos para poder ayudar a poder desarrollar de mejor manera esta presentación: Ø Ø Ø Ø Ø Te recomiendo contar con un lugar para poder estudiar, no debe ser una sala de estudio, puede ser el comedor de tu casa, lo importante es que lo ordenes y acomodes para ti y tus artículos de estudio. Por unos minutos desconéctate del celular, has de cuenta que estas en la sala de clases y deja el móvil en silencio. Organiza tu tiempo y mantén una continuidad de principio a fin de esta presentación, lo que te permitirá no perder el hilo de el o los temas a estudiar. Lee con atención y calma la información que recibirás así como las instrucciones para los desafíos o ejercitación que se encuentra al final de esta presentación. Visita cada link sugerido ya sea durante la presentación o al final de ella, dado que tienen como objetivo poder explicar o reforzar de una manera distinta el contenido abordado. Cuando apliques lo aprendido, trata en primera instancia de resolverlo por ti mismo, cuando ya no logres hacerlo pasa a apoyarte de las diapositivas anteriores o del texto escolar, luego al finalizar, podrás siempre encontrar el solucionario de la actividad en esta presentación. No es necesario imprimir estas diapositivas, para realizar la actividad será suficiente con que la registres en tu cuaderno de asignatura, sino lo posees podrás realizarlo en una hoja anexa que luego podrás pegar en tu cuaderno. Para todos los temas que se traten, en esta y en todas las presentaciones que trabajemos, podrás apoyarte del texto escolar. De no poseerlo, se adjuntará en cada ppt el link para verlo en línea. Lo más importante es que confíes en tus capacidades, eres capaz de lograr lo que te propongas.

Para comenzar… ¿Qué son las PROPIEDADES PERIÓDICAS? En caso de dudas, puedes consultar el texto escolar, entre las páginas 178 a la 181. https: //curriculumnacional. mineduc. cl/ 614/articles-145405_recurso_pdf. pdf
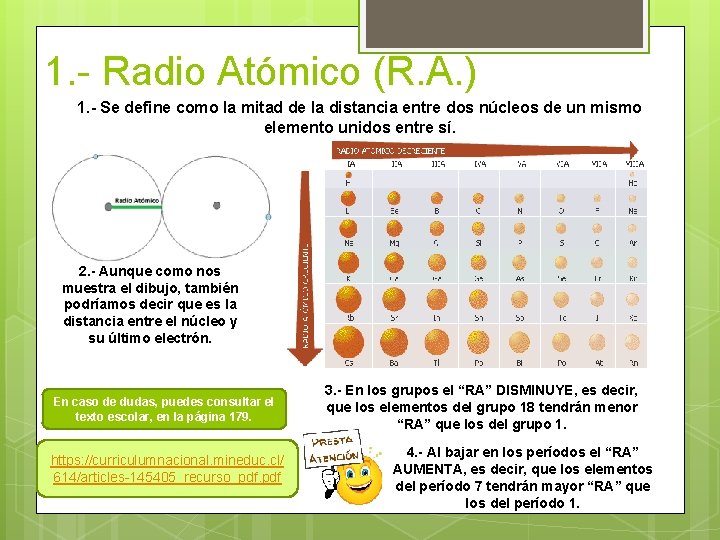
1. - Radio Atómico (R. A. ) 1. - Se define como la mitad de la distancia entre dos núcleos de un mismo elemento unidos entre sí. 2. - Aunque como nos muestra el dibujo, también podríamos decir que es la distancia entre el núcleo y su último electrón. En caso de dudas, puedes consultar el texto escolar, en la página 179. https: //curriculumnacional. mineduc. cl/ 614/articles-145405_recurso_pdf. pdf 3. - En los grupos el “RA” DISMINUYE, es decir, que los elementos del grupo 18 tendrán menor “RA” que los del grupo 1. 4. - Al bajar en los períodos el “RA” AUMENTA, es decir, que los elementos del período 7 tendrán mayor “RA” que los del período 1.
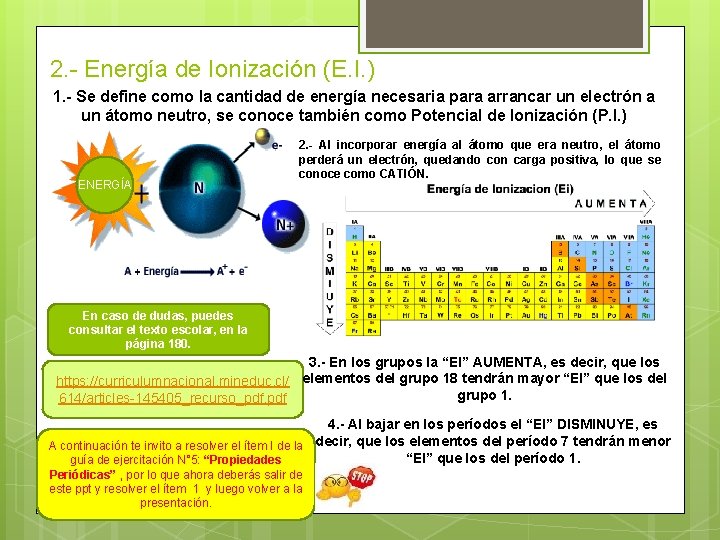
2. - Energía de Ionización (E. I. ) 1. - Se define como la cantidad de energía necesaria para arrancar un electrón a un átomo neutro, se conoce también como Potencial de Ionización (P. I. ) ENERGÍA 2. - Al incorporar energía al átomo que era neutro, el átomo perderá un electrón, quedando con carga positiva, lo que se conoce como CATIÓN. En caso de dudas, puedes consultar el texto escolar, en la página 180. 3. - En los grupos la “EI” AUMENTA, es decir, que los https: //curriculumnacional. mineduc. cl/ elementos del grupo 18 tendrán mayor “EI” que los del grupo 1. 614/articles-145405_recurso_pdf. pdf 4. - Al bajar en los períodos el “EI” DISMINUYE, es A continuación te invito a resolver el ítem I de la decir, que los elementos del período 7 tendrán menor “EI” que los del período 1. guía de ejercitación N° 5: “Propiedades Periódicas” , por lo que ahora deberás salir de este ppt y resolver el ítem 1 y luego volver a la presentación.
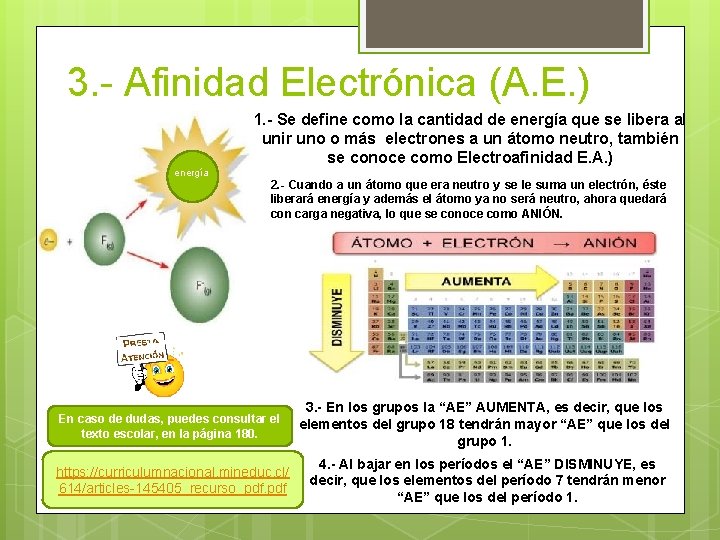
3. - Afinidad Electrónica (A. E. ) energía 1. - Se define como la cantidad de energía que se libera al unir uno o más electrones a un átomo neutro, también se conoce como Electroafinidad E. A. ) 2. - Cuando a un átomo que era neutro y se le suma un electrón, éste liberará energía y además el átomo ya no será neutro, ahora quedará con carga negativa, lo que se conoce como ANIÓN. En caso de dudas, puedes consultar el texto escolar, en la página 180. 3. - En los grupos la “AE” AUMENTA, es decir, que los elementos del grupo 18 tendrán mayor “AE” que los del grupo 1. https: //curriculumnacional. mineduc. cl/ 614/articles-145405_recurso_pdf. pdf 4. - Al bajar en los períodos el “AE” DISMINUYE, es decir, que los elementos del período 7 tendrán menor “AE” que los del período 1.

4. - Electronegatividad (E. N. ) 1. - Se define como la capacidad que posee un átomo para atraer hacía si mismo los electrones de otro átomo para formar enlaces químicos. 2. - En este caso no existe pérdida ni ganancia de electrones. Aquí se comparten los electrones para formar enlaces. 3. - En los grupos la “EN” AUMENTA, es decir, que los elementos del grupo 18 tendrán mayor “EN” que los del grupo 1. En caso de dudas, puedes consultar el texto escolar, en la página 181. https: //curriculumnacional. mineduc. cl/ 614/articles-145405_recurso_pdf. pdf 4. - Al bajar en los períodos el “EN” DISMINUYE, es decir, que los elementos del período 7 tendrán menor “EN” que los del período 1.
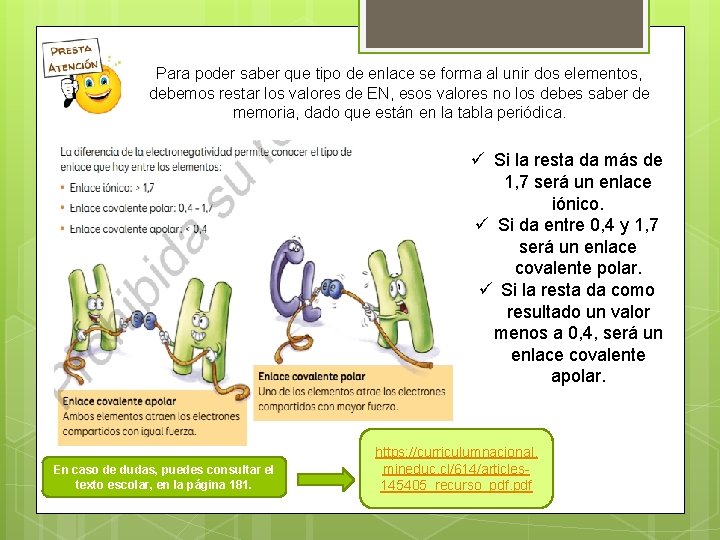
Para poder saber que tipo de enlace se forma al unir dos elementos, debemos restar los valores de EN, esos valores no los debes saber de memoria, dado que están en la tabla periódica. ü Si la resta da más de 1, 7 será un enlace iónico. ü Si da entre 0, 4 y 1, 7 será un enlace covalente polar. ü Si la resta da como resultado un valor menos a 0, 4, será un enlace covalente apolar. En caso de dudas, puedes consultar el texto escolar, en la página 181. https: //curriculumnacional. mineduc. cl/614/articles 145405_recurso_pdf. pdf

Pongamos a pruebo lo aprendido. A continuación te invito a resolver el ítem II de la guía de ejercitación N° 5: “Propiedades Periódicas” , por lo que ahora deberás salir de este ppt y resolver el ítem 2 y luego volver a la presentación.

Antes de seguir con el ppt realiza tu propio trabajo, luego continúa para comparar los resultados. Para conocer la respuesta a la pregunta de la diapositiva anterior y la justificación de la misma, observa el siguiente video. https: //www. youtube. com/watch? v= 4 Uexqpl. Plao

Gracias por tu atención… Recuerda que cualquier duda o consulta la puedes realizar a través del correo electrónico: quimica 8 bas@agustiniano. cl A continuación te invito a acceder con el siguiente link a una AUTOEVALUACIÓN , donde se evaluará lo estudiado durante esta presentación. https: //forms. gle/De 7 n 6 nrwo 3 MSw. ZZE 9
- Slides: 12