Tabela Peridica e Propriedades DISCIPLINA QUMICA GERAL PROFESSORA

Tabela Periódica e Propriedades DISCIPLINA: QUÍMICA GERAL PROFESSORA: CLEIA SALLES CURSO: TECNÓLOGO (1 U/1 T)

Mendeleev os elementos se agrupavam junto com propriedades químicas similares numa seqüência lógica através do aumento dos pesos atômicos. n Moseley Mostrou que o critério mais adequado da seqüência era o dos números atômicos. n
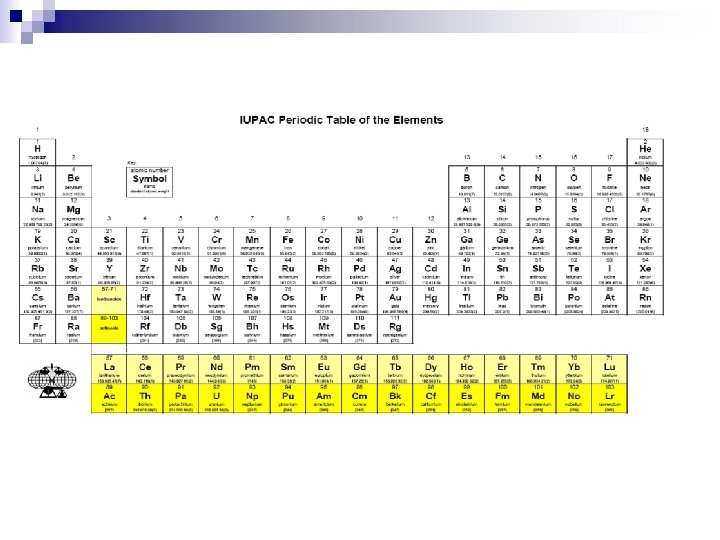
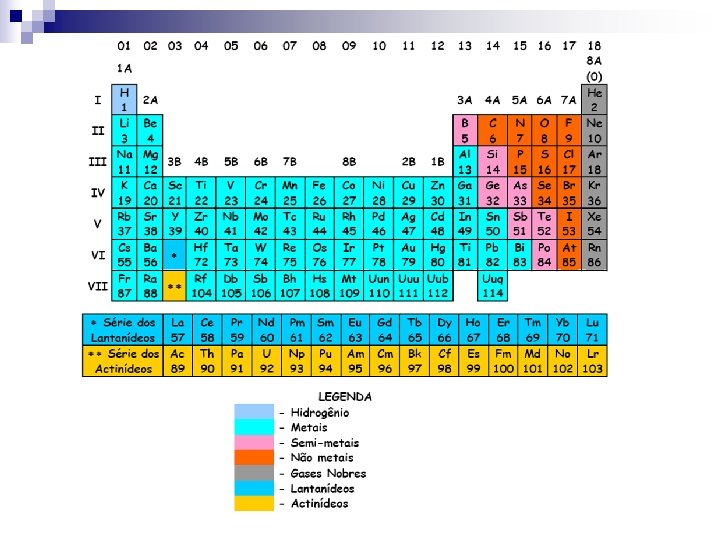
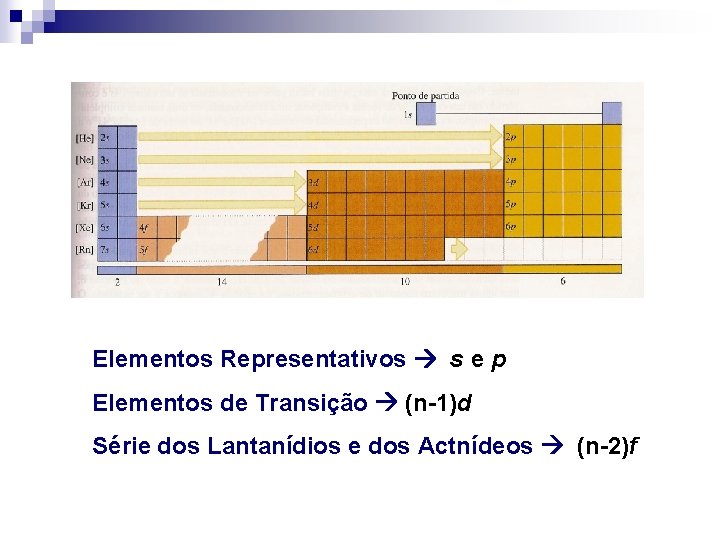
Elementos Representativos s e p Elementos de Transição (n-1)d Série dos Lantanídios e dos Actnídeos (n-2)f

Configuração Eletrônica da Última Camada dos Elementos da Tabela Periódica
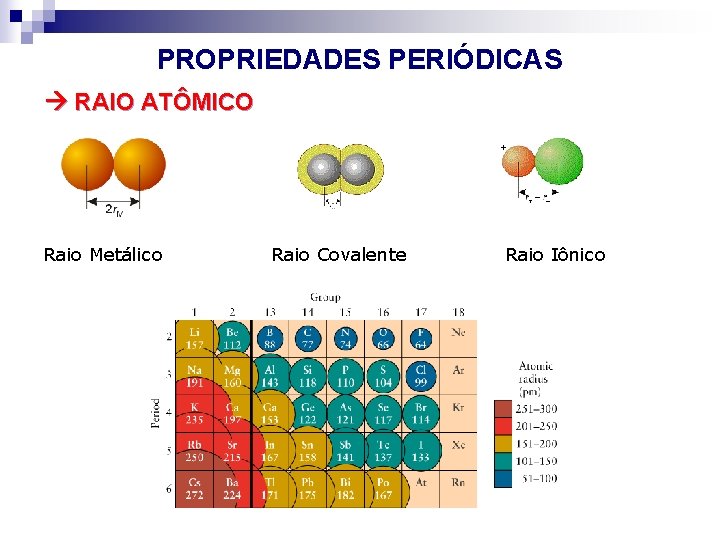
PROPRIEDADES PERIÓDICAS RAIO ATÔMICO Raio Metálico Raio Covalente Raio Iônico

O raio atômico aumenta para baixo em um grupo, e dentro dos blocos s e p, e decresce da esquerda para a direita ao longo de um período.

Raios de Cátions e nions são maiores que seus átomos neutros Cátions são menores do que seus átomos neutros Cátions e ânions isoeletrônicos, pode-se afirmar que quanto maior a carga do cátion, menor o seu raio e quanto maior a carga do ânion, maior o raio.
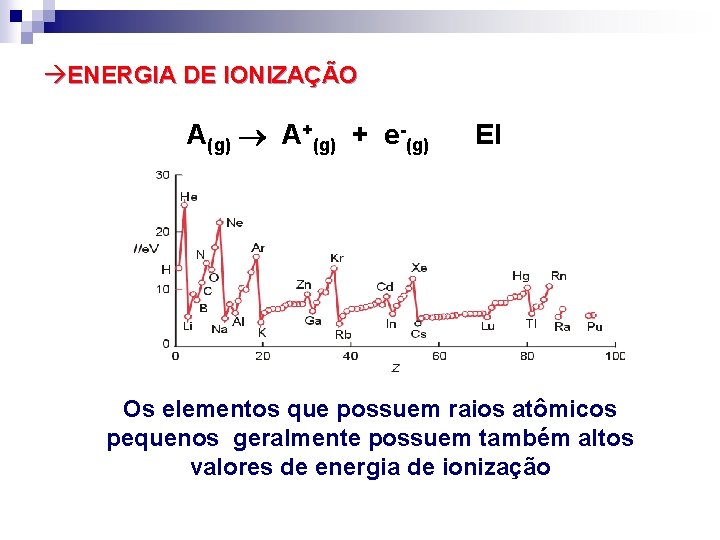
àENERGIA DE IONIZAÇÃO A(g) A+(g) + e-(g) EI Os elementos que possuem raios atômicos pequenos geralmente possuem também altos valores de energia de ionização

A Energia de Ionização decresce de cima para baixo em um grupo, nos períodos cresce da esquerda para a direita.

AFINIDADE ELETRÔNICA A(g) + e-(g) A-(g) HAE AE maiores para elementos próximos do flúor As segundas, terceiras afinidades eletrônicas são sempre processos forçados.
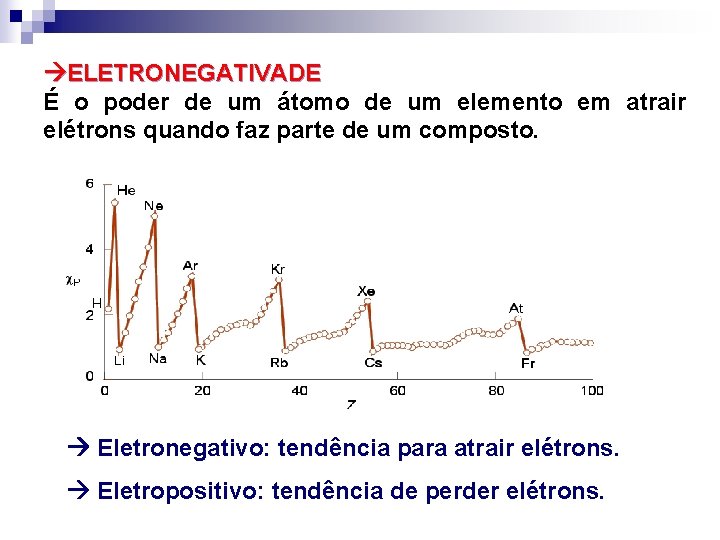
ELETRONEGATIVADE É o poder de um átomo de um elemento em atrair elétrons quando faz parte de um composto. Eletronegativo: tendência para atrair elétrons. Eletropositivo: tendência de perder elétrons.
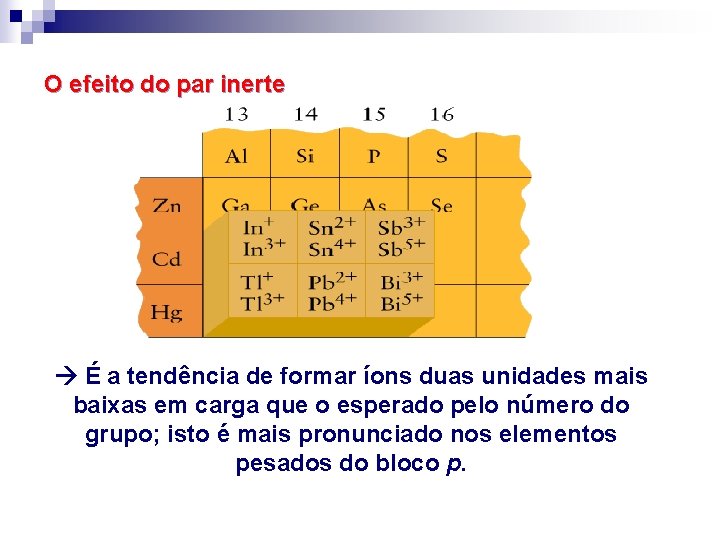
O efeito do par inerte É a tendência de formar íons duas unidades mais baixas em carga que o esperado pelo número do grupo; isto é mais pronunciado nos elementos pesados do bloco p.
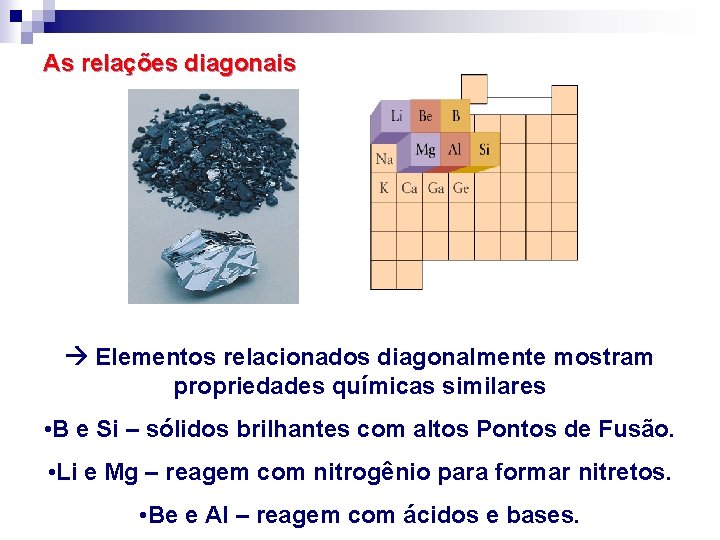
As relações diagonais Elementos relacionados diagonalmente mostram propriedades químicas similares • B e Si – sólidos brilhantes com altos Pontos de Fusão. • Li e Mg – reagem com nitrogênio para formar nitretos. • Be e Al – reagem com ácidos e bases.
- Slides: 15