Tabela peridica dos elementos Tabela Peridica e Propriedades
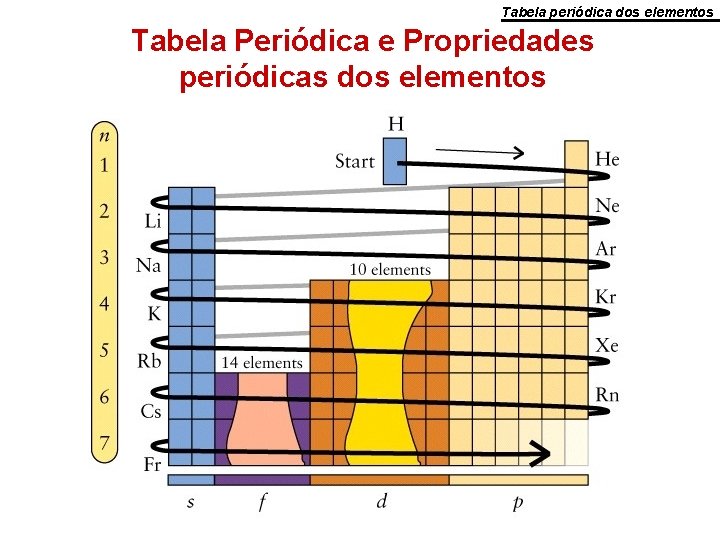
Tabela periódica dos elementos Tabela Periódica e Propriedades periódicas dos elementos

A Tabela Periódica Moderna 1. Elementos arranjados em ordem crescentes de seus números atômicos; 2. Baseado na Periodicidade (propriedades dos elementos são funções periódicas de seus números atômicos). 3. Consiste de grupos e períodos. 4. Fornece informações úteis propriedades dos elementos. sobre as
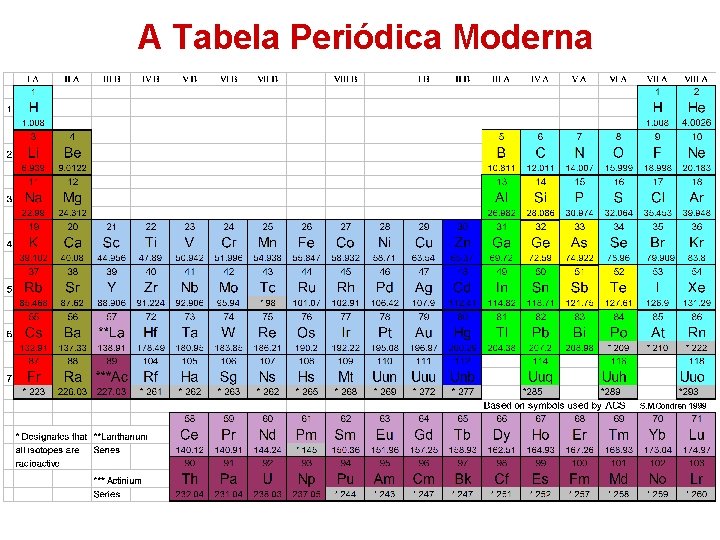
A Tabela Periódica Moderna
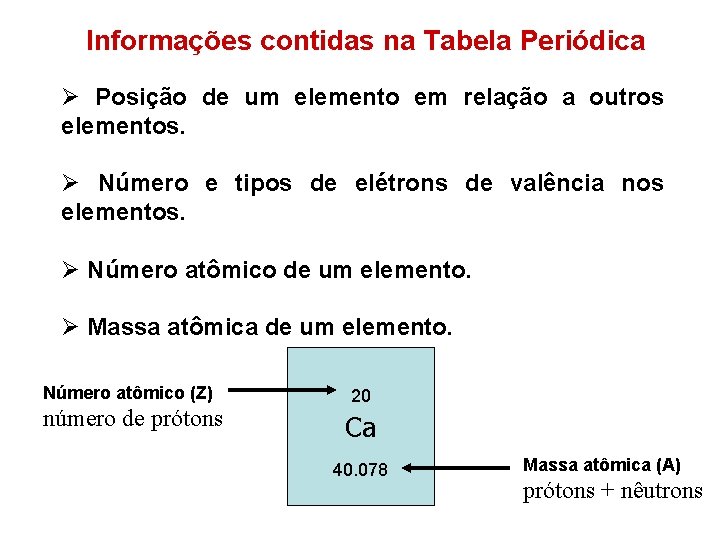
Informações contidas na Tabela Periódica Ø Posição de um elemento em relação a outros elementos. Ø Número e tipos de elétrons de valência nos elementos. Ø Número atômico de um elemento. Ø Massa atômica de um elemento. Número atômico (Z) número de prótons 20 Ca 40. 078 Massa atômica (A) prótons + nêutrons

Organização da Tabela Periódica Períodos: estão arranjados horizontalmente na tabela periódica Esses elementos têm o mesmo número de camadas de valência. 2º Período 6º Período
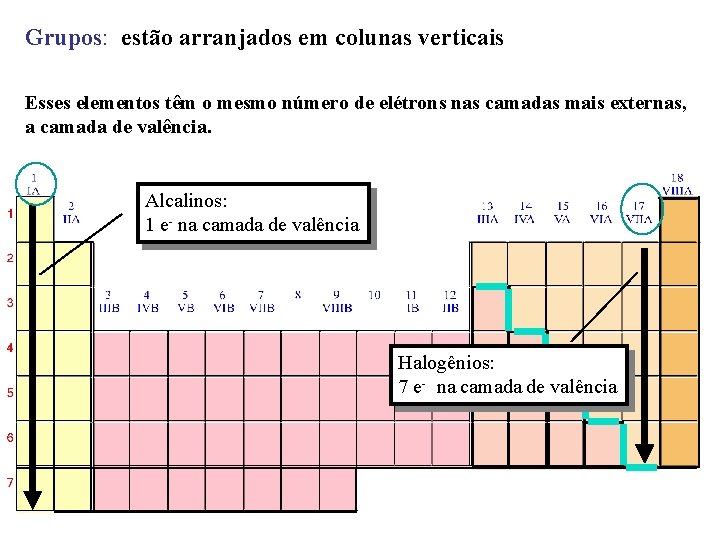
Grupos: estão arranjados em colunas verticais Esses elementos têm o mesmo número de elétrons nas camadas mais externas, a camada de valência. Alcalinos: 1 e- na camada de valência Halogênios: 7 e- na camada de valência

Classificação dos elementos Os elementos na Tabela Periódica podem ser classificados de diferentes formas. Ø grupo principal; Ø metais de transição; Ø Lantanídeos* e Actinídeos. *Terras Raras: Lantanídeos mais o Y e Sc
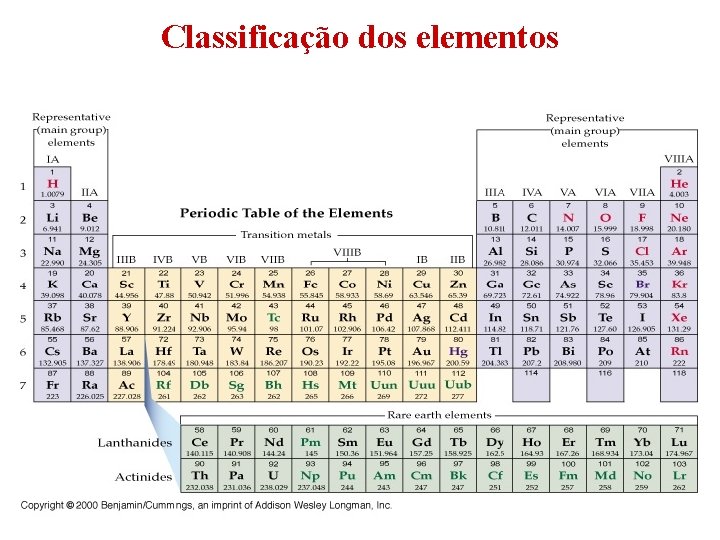
Classificação dos elementos
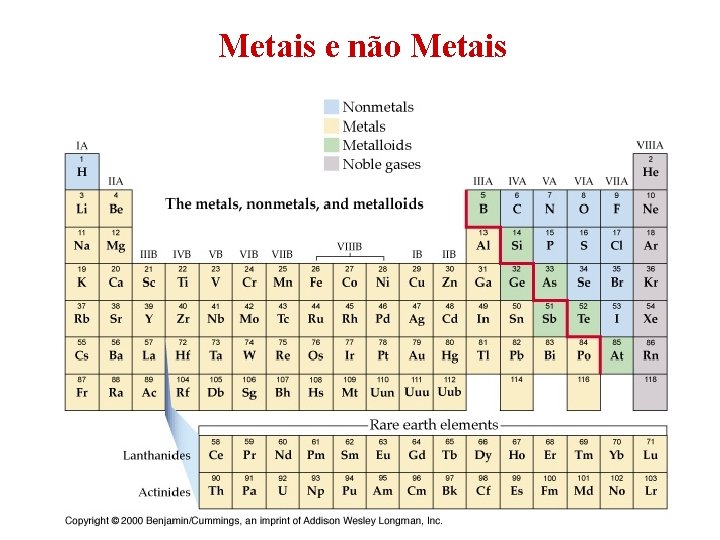
Metais e não Metais
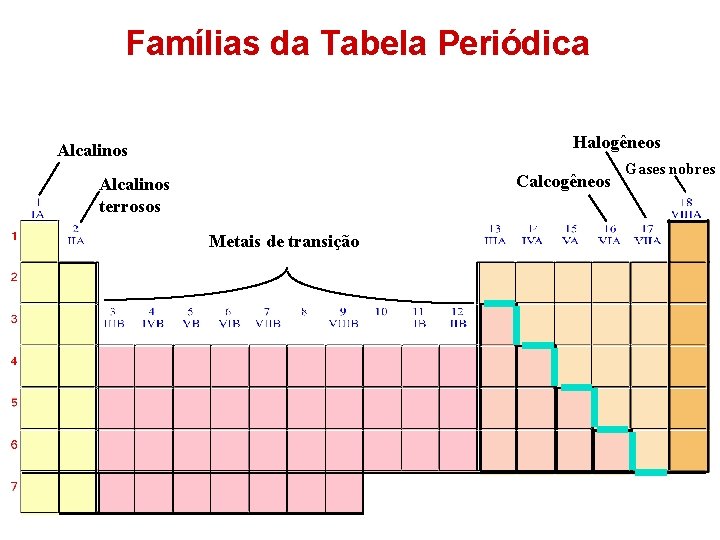
Famílias da Tabela Periódica Halogêneos Alcalinos Calcogêneos Alcalinos terrosos Metais de transição Gases nobres

Configuração eletrônica a partir da Tabela Periódica H 1 s 1 He 1 s 2 Li Be 2 s 1 2 s 2 Na Mg 3 s 1 3 s 2 K 4 s 1 Sc 3 d 1 Rb 5 s 1 Ca 4 s 2 Sr 5 s 2 Y 4 d 1 V Ti Cr Mn Fe Co 3 d 2 3 d 3 4 s 13 d 5 3 d 6 3 d 7 Zr Nb Mo Tc Ru Rh 4 d 2 4 d 3 5 s 14 d 5 4 d 6 4 d 7 Cs 6 s 1 Ba 6 s 2 La 5 d 1 Hf Ta W Re Os 5 d 2 5 d 3 6 s 15 d 5 5 d 6 Fr 7 s 1 Ra 7 s 2 Ac Rf 6 d 1 6 d 2 Db Sg Bh 6 d 3 7 s 16 d 5 Ni 3 d 8 Ni 4 d 8 Ir Ni 7 5 d 5 d 8 Hs Mt 6 d 6 6 d 7 Cu 4 s 13 d 10 Ag 5 s 14 d 10 Au 6 s 15 d 10 B 2 p 1 C N O 2 3 2 p 2 p 2 p 4 F 2 p 5 Ne 2 p 6 Al 3 p 1 Si 3 p 2 S P 3 3 p 3 p 4 Cl 3 p 5 Ar 3 p 6 Zn Ga Ge 3 d 10 4 p 1 4 p 2 Cd In Sn 10 4 d 5 p 1 5 p 2 As Se 4 p 3 4 p 4 Be 4 p 5 Sb Te 5 p 3 5 p 4 I 5 p 5 Kr 4 p 6 Xe 5 p 6 Hg Tl Pb 5 d 10 6 p 1 6 p 2 Bi Po At 6 p 3 6 p 4 6 p 5 Rn 6 p 6

Propriedades gerais dos elementos Ø Tamanho dos átomos • Os átomos não possuem tamanhos rígidos, fixos. • Seus tamanhos ou raios são definidos pelo mapa de densidade eletrônica em compostos que formam. • Em uma molécula A 2 em que a distância entre um núcleo e outro é d, então o raio de um átomo A é ½d.
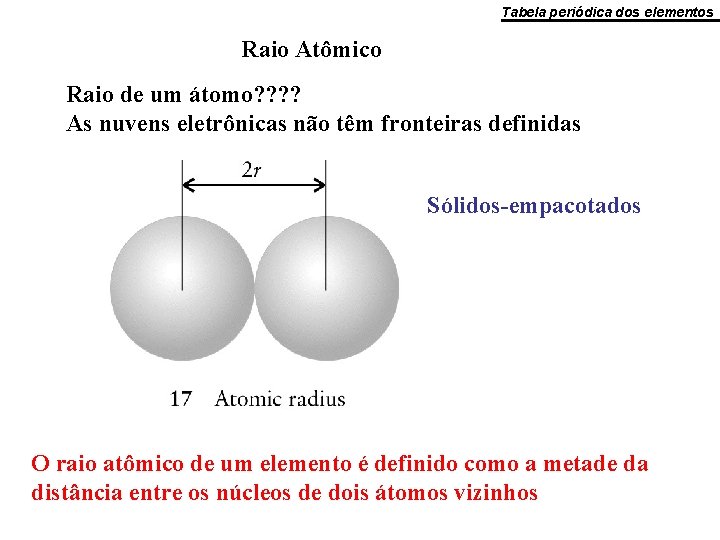
Tabela periódica dos elementos Raio Atômico Raio de um átomo? ? As nuvens eletrônicas não têm fronteiras definidas Sólidos-empacotados O raio atômico de um elemento é definido como a metade da distância entre os núcleos de dois átomos vizinhos
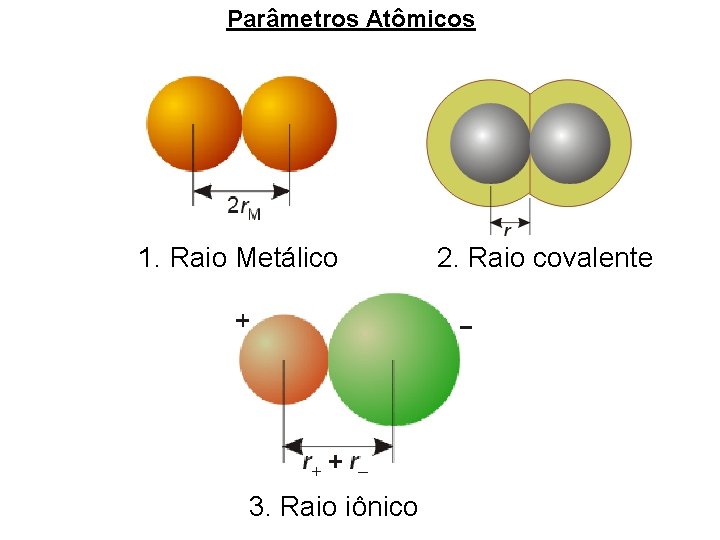
Parâmetros Atômicos 1. Raio Metálico 3. Raio iônico 2. Raio covalente
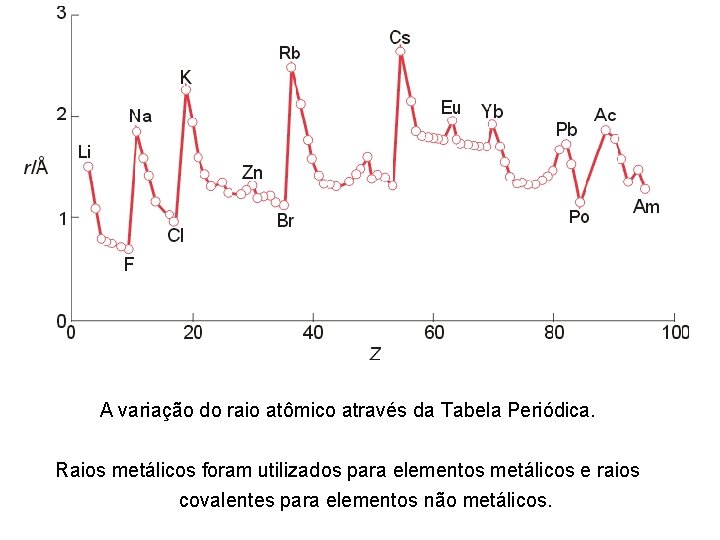
A variação do raio atômico através da Tabela Periódica. Raios metálicos foram utilizados para elementos metálicos e raios covalentes para elementos não metálicos.
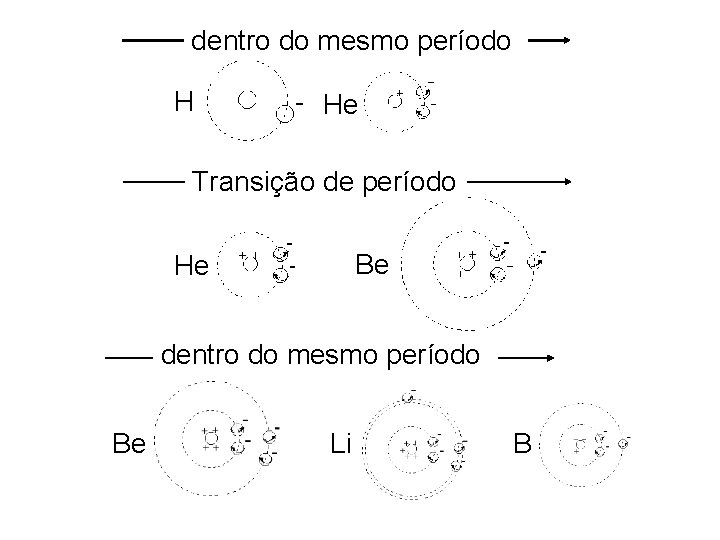
dentro do mesmo período H He Transição de período Be He dentro do mesmo período Be Li B

Ø Tamanho dos átomos Dados • O tamanho dos átomos diminui periodicamente da esquerda para a direita ao longo de um período – o aumento da carga nuclear resulta em aumento gradativo da força de atração nuclear por todos os elétrons de uma mesma camada eletrônica. • Descendo ao longo de um grupo, o tamanho do átomo aumenta – efeito dos níveis eletrônicos que vão sendo acrescentados.

Ø Carga Nuclear Efetiva • Em um átomo polieletrônico, temos que considerar a existência de forças - Cada elétron é atraído pelo núcleo (carga nuclear); - Cada elétron repele outros elétrons. • Quaisquer de ca entre o núcleo e elétron de interesse reduzirão a atração para o núcleo (carga nuclear). • A carga nuclear “liquida” atraindo elétrons extenos é chamado de carga nuclear efetiva (Zef). • Esta pode ser estimada numericamente subtraindo um fator de blindagem Zef = Z -
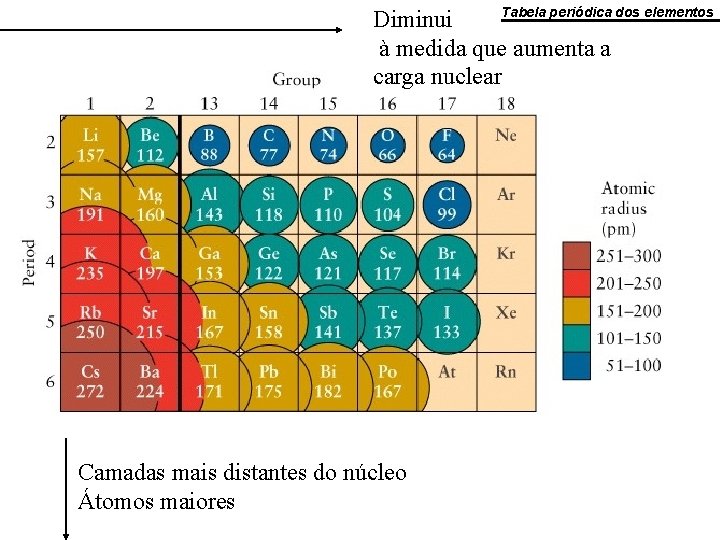
Tabela periódica dos elementos Diminui à medida que aumenta a carga nuclear Camadas mais distantes do núcleo Átomos maiores

Ø Tamanho dos íons • Os metais geralmente formam íons positivos. • Os íons metálicos são menores que os átomos a partir dos quais foram gerados: Quando se forma um íon positivo a carga nuclear efetiva é aumentada. • Um íon positivo é sempre menor que o átomo correspondente. • Os íons negativos são maiores que os átomos correspondentes.
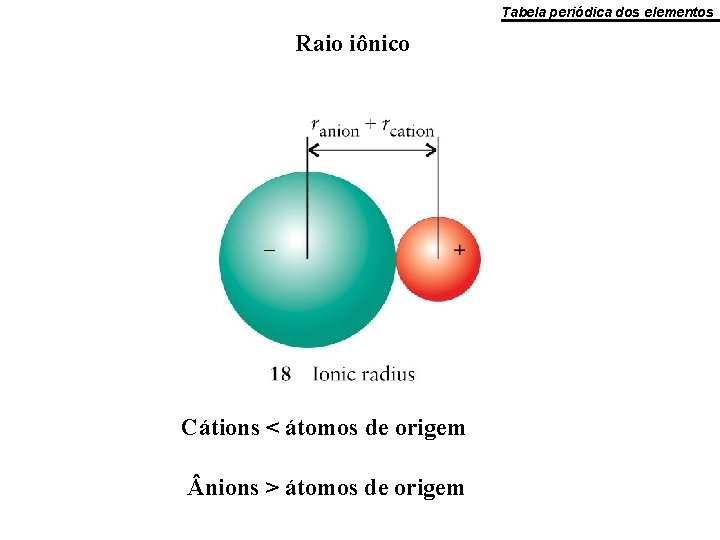
Tabela periódica dos elementos Raio iônico Cátions < átomos de origem nions > átomos de origem
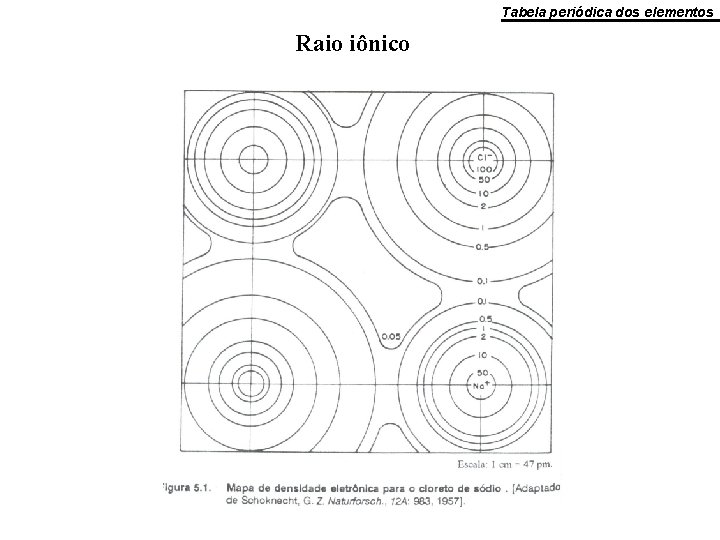
Tabela periódica dos elementos Raio iônico
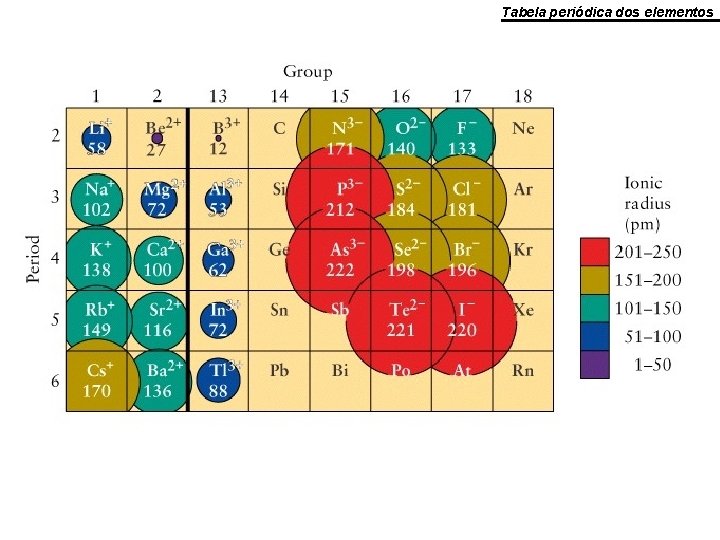
Tabela periódica dos elementos
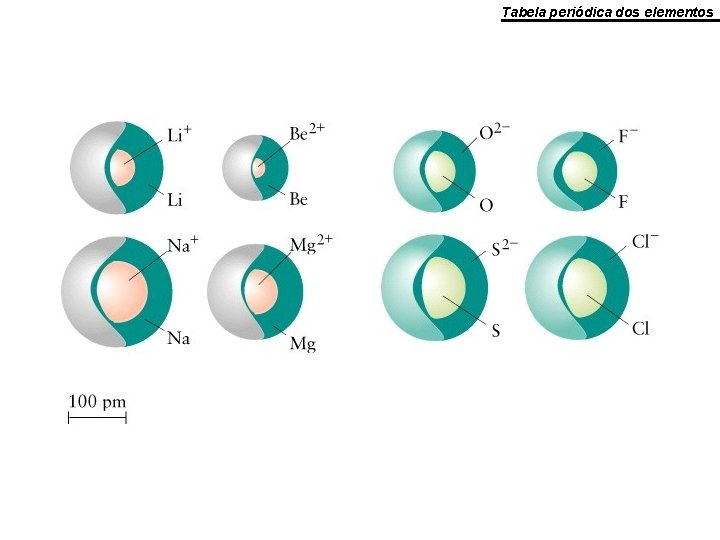
Tabela periódica dos elementos
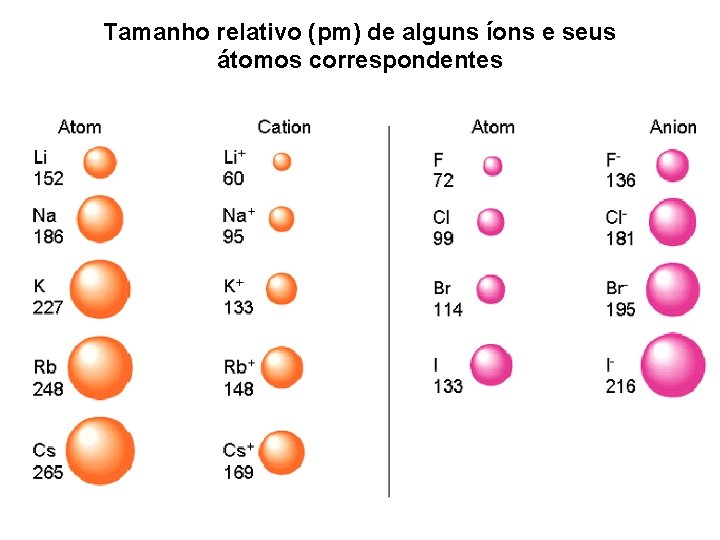
Tamanho relativo (pm) de alguns íons e seus átomos correspondentes

Ø Tendências observadas nos raios iônicos 1. Nos grupos representativos, os raios aumentam nos grupos de cima para baixo. Ex. : Li+ = 0, 76 Å, Na+ = 1, 02 Å, K+ = 1, 38 Å 2. Qualquer que seja o período da tabela periódica, os raios iônicos decrescem da esquerda para a direita. Ex. : Na+ = 1, 02 Å, Mg 2+ = 0, 720 Å, Al 3+ = 0, 535 Å 3. Os raios iônicos decrescem à medida que a valência aumenta. Ex. : Cr 2+ = 0, 80 Å (spin alto), Cr 3+ = 0, 615 Å, Cr 4+ = 0, 55 Å, Cr 5+ = 0, 49 Å e Cr 6+ = 0, 44 Å 4. Os orbitais d e f não blindam eficientemente a carga nuclear. Contração lantanídica – tamanho dos elementos da segunda e da terceira séries de elementos de transição são praticamente iguais.

Ø Energias de ionização • A quantidade de energia necessária para remover o elétron mais fracamente ligado de um átomo gasoso isolado é designado energia de ionização. Na(g) -----> Na+(g) + e - • As energias de ionização são determinadas a partir de dados espectroscópicos e são medidos em k. J mol-1. • A primeira energia de ionização, I 1, é a energia necessária para remover o primeiro elétron, transformando M em M+. Ex. : Na Na+ + e- • A segunda energia de ionização, I 2, é a energia necessária para remover o segundo elétron. Ex. : Na+ Na 2+ + e-

• Os fatores que influenciam as energias de ionização são: 1. O tamanho do átomo. 2. A carga no núcleo. 3. A eficiência com que os níveis eletrônicos internos blindam a carga nuclear. 4. O tipo de elétron envolvido (s, p, d ou f).
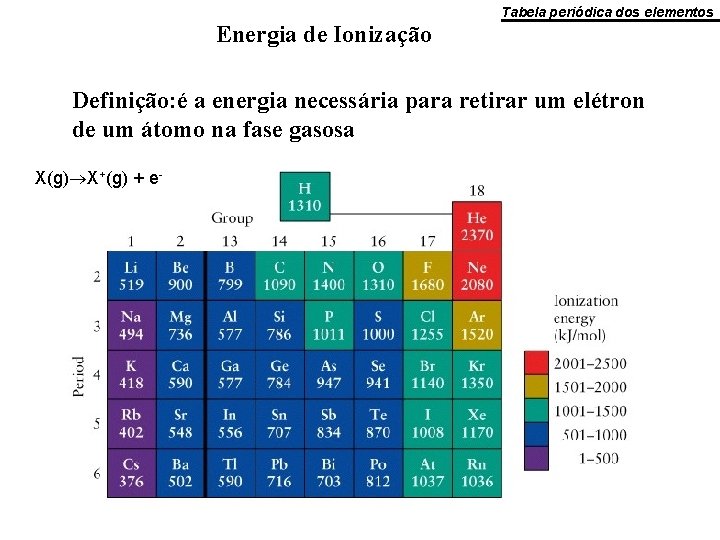
Tabela periódica dos elementos Energia de Ionização Definição: é a energia necessária para retirar um elétron de um átomo na fase gasosa X(g) X+(g) + e-
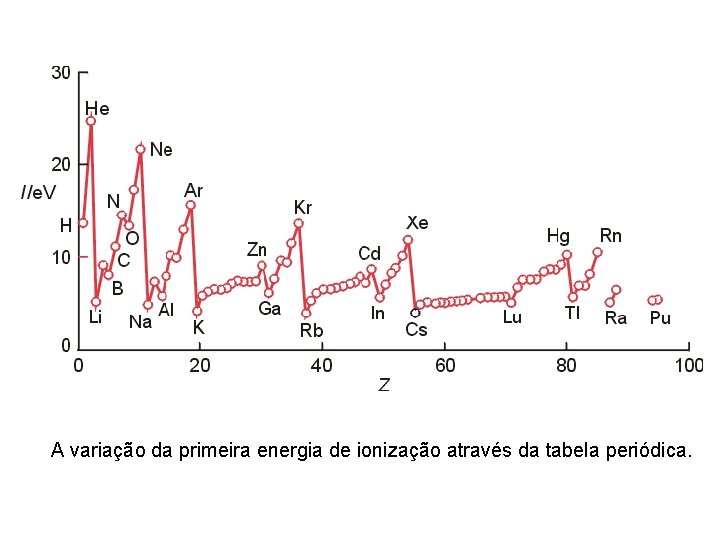
A variação da primeira energia de ionização através da tabela periódica.

Ø Primeira e segunda energias de ionização para os elementos do Grupo 1 • I 2>>I 1 1ª 2ª Li 520 7. 296 Na 496 4. 563 K 419 3. 069 Rb 403 2. 650 Cs 376 2. 420 Fr • Os elementos do Grupo 1 apresentam apenas 1 e- no nível mais externo. A remoção do segundo e- requer uma energia muito maior, pois envolve os e- de um nível eletrônico interno completamente preenchido.
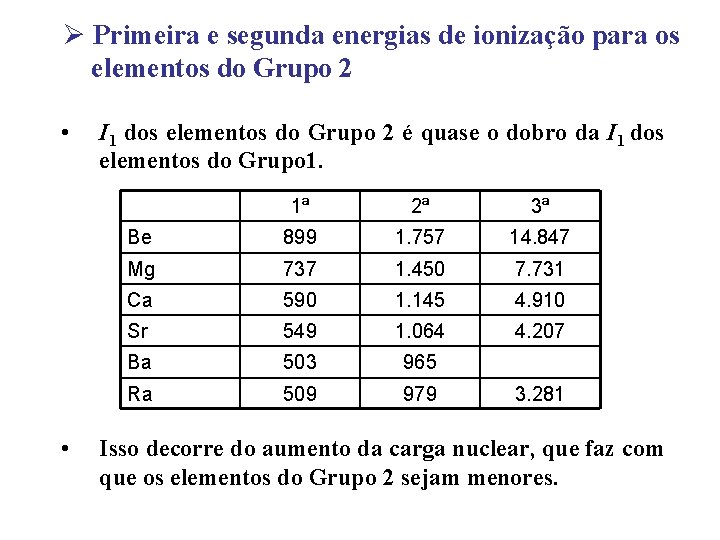
Ø Primeira e segunda energias de ionização para os elementos do Grupo 2 • • I 1 dos elementos do Grupo 2 é quase o dobro da I 1 dos elementos do Grupo 1. 1ª 2ª 3ª Be 899 1. 757 14. 847 Mg 737 1. 450 7. 731 Ca 590 1. 145 4. 910 Sr 549 1. 064 4. 207 Ba 503 965 Ra 509 979 3. 281 Isso decorre do aumento da carga nuclear, que faz com que os elementos do Grupo 2 sejam menores.

Energia de Ionização -A energia de ionização aumenta em um período e diminui no grupo; -O comportamento é inverso ao comportamento observado para o tamanho dos átomos; -Depois da saída de um elétron a saída de um segundo elétron é mais difícil;

Ø Afinidade eletrônica (Ea) • A energia liberada quando um elétron é adicionado a um átomo gasoso é designado afinidade eletrônica. Geralmente apenas um elétron é acrescentado, formando um íon mononegativo. Ex. 1: • • • Cl (g) + e- Cl-(g) E = -349 k. J/mol O íon Cl- é mais estável que o átomo Cl Cl configuração [Ne]3 s 23 p 5 Cl- configuração [Ne]3 s 23 p 6 O íon tem a mesma configuração eletrônica do Ar O íon Cl- é facilmente formado.
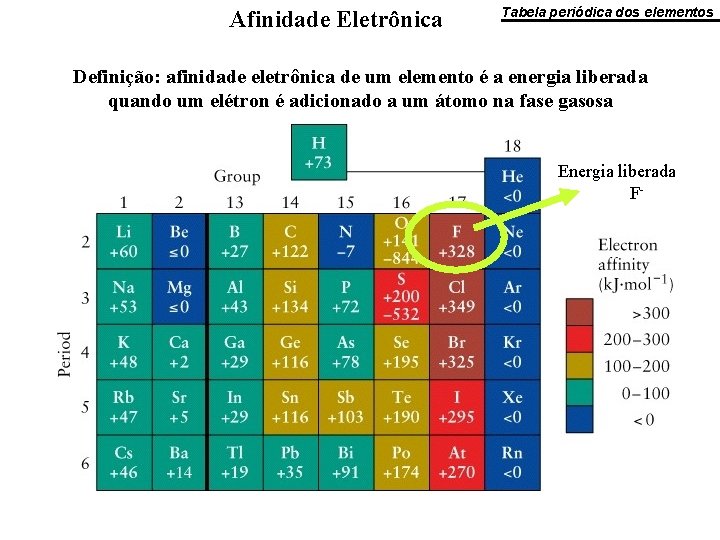
Afinidade Eletrônica Tabela periódica dos elementos Definição: afinidade eletrônica de um elemento é a energia liberada quando um elétron é adicionado a um átomo na fase gasosa Energia liberada F-
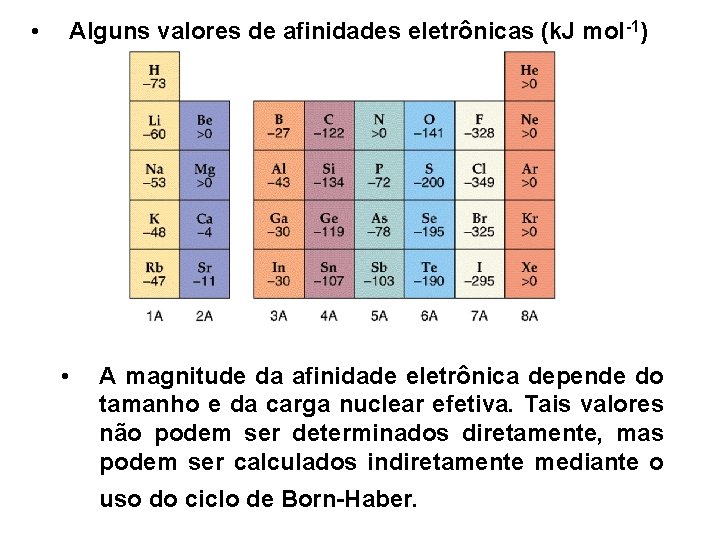
• Alguns valores de afinidades eletrônicas (k. J mol-1) • A magnitude da afinidade eletrônica depende do tamanho e da carga nuclear efetiva. Tais valores não podem ser determinados diretamente, mas podem ser calculados indiretamente mediante o uso do ciclo de Born-Haber.
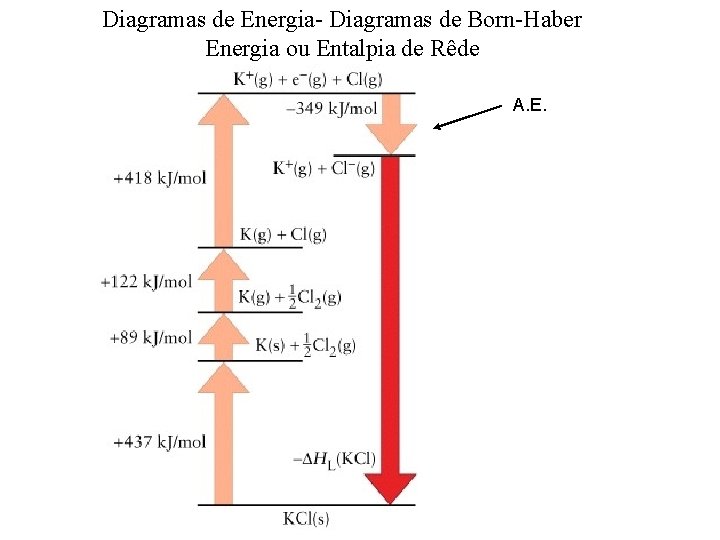
Diagramas de Energia- Diagramas de Born-Haber Energia ou Entalpia de Rêde A. E.
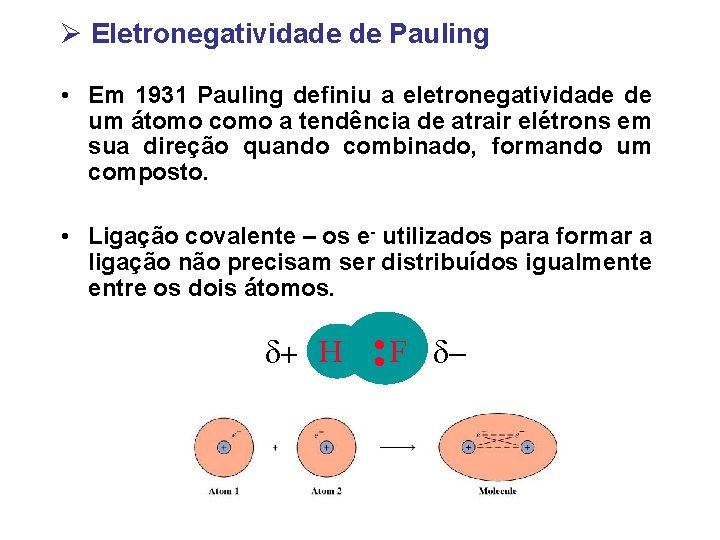
Ø Eletronegatividade de Pauling • Em 1931 Pauling definiu a eletronegatividade de um átomo como a tendência de atrair elétrons em sua direção quando combinado, formando um composto. • Ligação covalente – os e- utilizados para formar a ligação não precisam ser distribuídos igualmente entre os dois átomos. H • • F

Polaridade nas ligações químicas Eletronegatividade Ligações covalentes entre átomos com diferentes tendências para atrair elétrons cargas parciais H-Cl + - A nuvem eletrônica é deformada no sentido do átomo com maior tendência para atrai-la
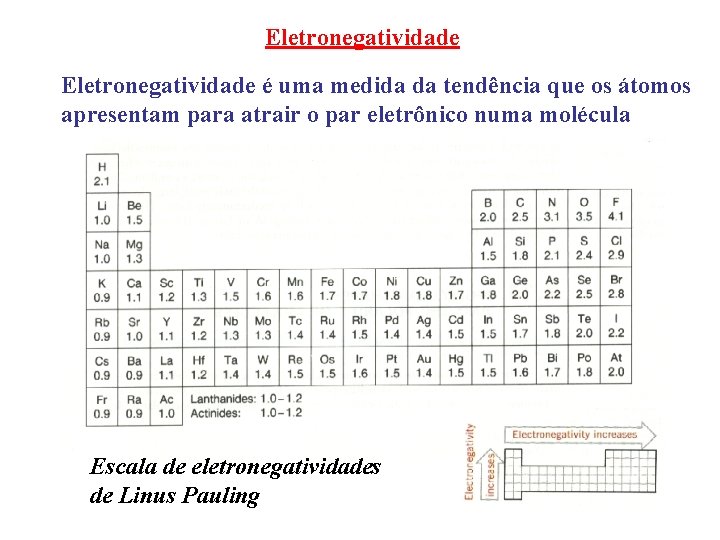
Eletronegatividade é uma medida da tendência que os átomos apresentam para atrair o par eletrônico numa molécula Escala de eletronegatividades de Linus Pauling

- Eletronegatividade de Mulliken (Roberto Mulliken) Se átomos tem maior Energia de Ionização (I) e maior Afinidade Eletrônica (Ea), deverá ter a tendência de receber e não de perder elétrons, ao formar compostos. Portanto: é muito mais eletronegativo!! - Se tem menor I e menor Ea, perderá elétrons. Portanto: É eletropositivo!! Eletronegatividade Mulliken ( M): Valor médio entre I e Ea do elemento: M = ½ (I + Ea) Elementos perto do Fluor: I e Ea são grandes, portanto possuem M maior
- Slides: 41