Syror baser och salter Syror En syra bildas

Syror, baser och salter

Syror �En syra bildas när ett surt ämne löses i vatten och bildar vätejoner (H+). Syror leder därför alltid ström. �Surt ämne + vatten → vätejoner + negativa joner �En stark syra uppdelas fullständigt i joner i vatten. �Exempel: Svavelsyra H 2 SO 4, Saltsyra HCl, Salpetersyra HNO 3 �En svag syra uppdelas bara delvis i joner i vatten. �T. ex. kolsyra H 2 CO 3 citronsyra, ättiksyra
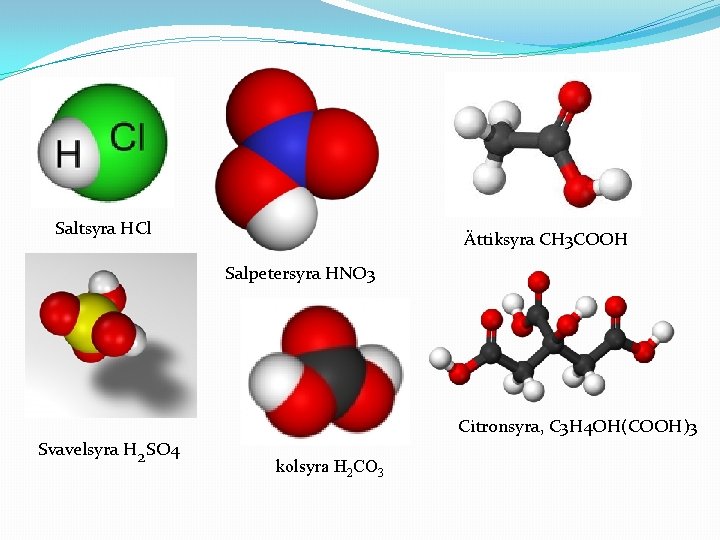
Saltsyra HCl Ättiksyra CH 3 COOH Salpetersyra HNO 3 Citronsyra, C 3 H 4 OH(COOH)3 Svavelsyra H 2 SO 4 kolsyra H 2 CO 3

Syror och deras vattenlösningar �Saltsyra är en gas (väteklorid)löst i vatten. När gasen löses i vatten bildas joner av alla molekylerna. �HCl(g) + H 2 O→ H+ + Cl- (aq) �Väteklorid + vatten → saltsyra �Svavelsyra är svaveltrioxid SO 3 löst i vatten �SO 3 (g) + H 2 O → 2 H+ + SO 42 -

Baser Basiska ämnen är motsatsen till sura Några vanliga basiska ämnen: Natriumhydroxid Na. OH Kaliumhydroxid KOH Ammoniak NH 3

Basers egenskaper �Frätande �Känns ”hala” �Alla baser ger hydroxidjoner OH- i vattenlösningar Na. OH KOH

Bas i vattenlösning Ett basiskt ämne i vattenlösning: Na. OH Na+ + OHNH 3 + H 2 O NH 4+ + OHJu högre koncentration hydroxidjoner desto högre p. H-värde

Neutralisation Syra + bas neutralisation H+ + OH- H 2 O (vatten) Exempel: Saltsyra blandas med natriumhydroxid HCl + Na. OH H 2 O + Na. Cl Vätejon och hydroxidjon bildar vattenmolekyl. Kloridjon och natriumjon bildar saltet natriumklorid OHH+

Salter �Salter är en grupp av ämnen. �De består av joner. �Positiva och negativa joner bildar ett salt. �I fast form: kristaller �I vattenlösning: fria joner Annika Adolfsson
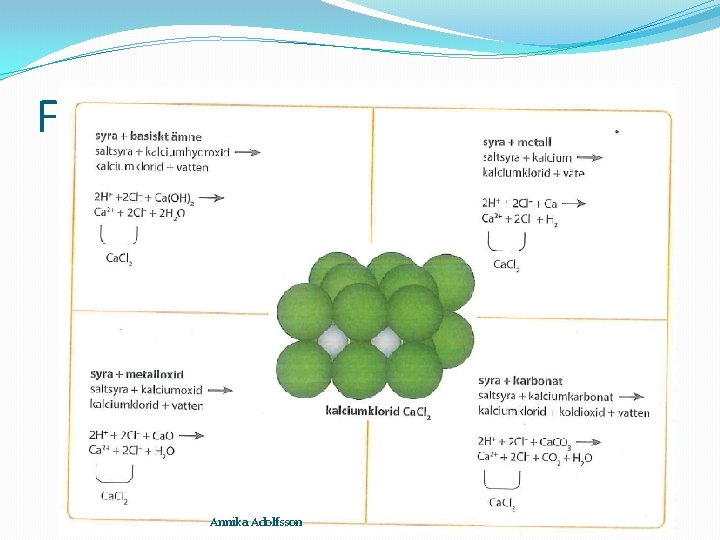
Fyra sätt att framställa salt: Annika Adolfsson
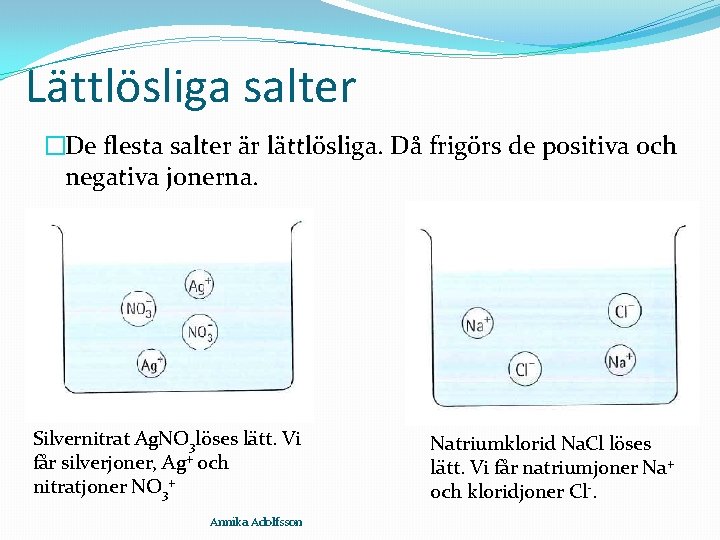
Lättlösliga salter �De flesta salter är lättlösliga. Då frigörs de positiva och negativa jonerna. Silvernitrat Ag. NO 3 löses lätt. Vi får silverjoner, Ag+ och nitratjoner NO 3+ Annika Adolfsson Natriumklorid Na. Cl löses lätt. Vi får natriumjoner Na+ och kloridjoner Cl-.

Svårlösliga salter 1) Vi löser upp två lättlösliga salter. Får fria joner: Na. Cl→ Na+ + Cl. Ag. NO 3 → Ag+ +NO 3+ 2) Silverjonerna och kloridjonerna bildar ett svårlösligt salt: Ag+ +Cl- → Ag. Cl Annika Adolfsson �Svårlösliga salter syns som vita fällningar. �Vi kan använda detta för att undersöka om en lösning innehåller kloridjoner: droppa i silverjoner och se om du får en fällning!

Bariumsulfat är också svårlösligt Två lättlösliga salter: Annika Adolfsson Blandas dessa lösningar så bildas en fällning av bariumsulfat. Används för att testa om något innehåller sulfat

Metallsalter �Metallsalter ger olika färger när de värms. Detta används i fyrverkerier. Annika Adolfsson

Natriumklorid Na. Cl �Kallas koksalt �Används som krydda och konserveringsmedel �Nödvändigt i kroppen �Finns i havet och i gruvor �Viktig råvara vid tillverkning av klorgas och natriumhydroxid, Annika Adolfsson

Ammoniumklorid, NH 4 Cl �Kallas salmiak �Bildas av ammoniak och saltsyra �Fanns förr i batterier (salmiakbatterier) �Finns i lakrits Annika Adolfsson

Kalciumklorid, Ca. Cl 2 �Drar till sig vatten. �Används för att hindra grusvägar från att damma. �Finns i s. k. torrbollar för att hålla utrymmen torra. Annika Adolfsson

Nitrater �Finns många nitrater: kaliumnitrat, natriumnitrat, kalciumnitrat, ammoniumnitrat. �Alla innehåller nitratjon, NO 3�Nitrater innehåller kväve. Kväve används som gödningsmedel. Annika Adolfsson

�Kalciumkarbonat finns i naturen som: Kalciumkarbonat, Ca. CO 3 kalksten, marmor och krita. Marmor Kalksten Annika Adolfsson Klippor av krita

Kalciumkarbonat, Ca. CO 3 �Kalksten krossas och används för att höja p. H-värdet i sjöar och på åkrar. �Kalksten används vid glastillverkning �Marmor och kalksten används som golvmaterial och bänkskivor m. m. Annika Adolfsson

Murbruk Annika Adolfsson Kalciumkarbonat värms. Koldioxid avgår. Vi får bränd kalk. 2. Bränd kalk + vatten ger släckt kalk som används i murbruk. 3. När murbruket stelnar tar det upp koldioxid från luften. Vi får kalciumkarbonat igen. 1.
- Slides: 21