Syrer og baser Eksempler p hverdagskemikalier Hvad er
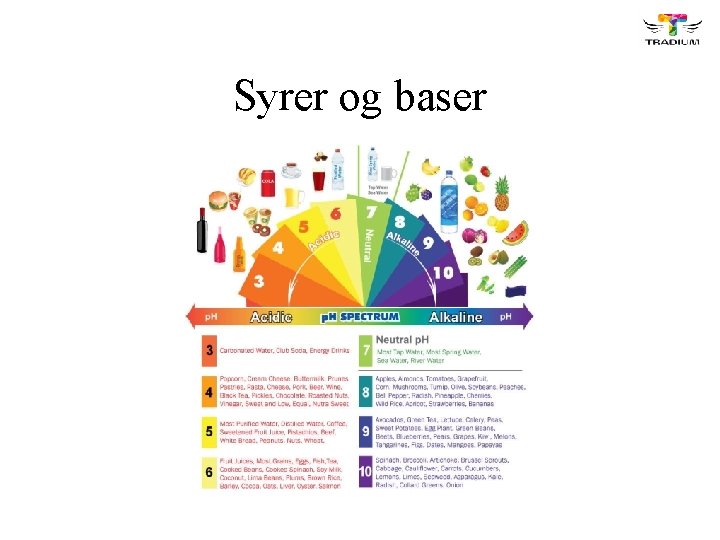
Syrer og baser

Eksempler på hverdagskemikalier

Hvad er en syre? • En syre er et molekyle eller en ion der kan + afgive en hydron (H )

Hvilke krav stiller det til syremolekylet/ionen? • Molekylet/ionen skal indeholde et H-atom, og et eller flere meget elektronegative atomer. • Fx: O, N, C, S, P • Det betyder at molekylet skal være polært

Hvad er en base? • En base er et molekyle eller en ion der kan optage en hydron (H+)

Hvilke krav stiller det til basemolekylet/ionen? Enten: • Skal ionen være negativt ladet Eller • Molekylet skal være polært, med et ikkebindende elektronpar
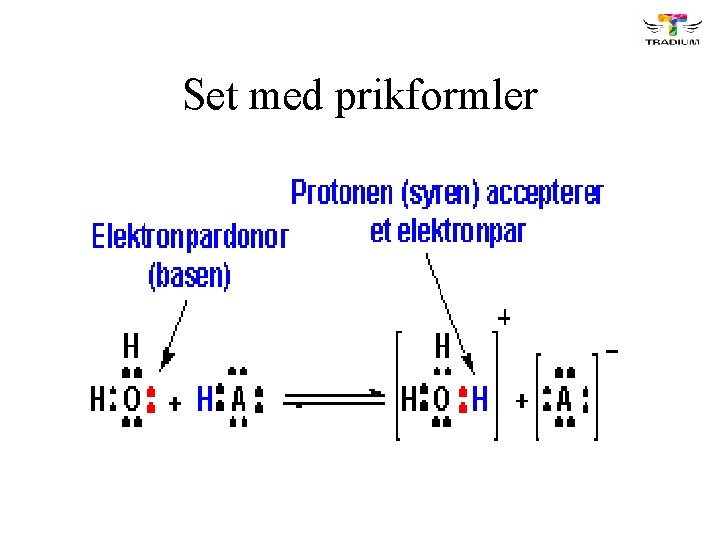
Set med prikformler

Stærke uorganiske syrer: • Stærke syrer vil afgive alle hydroner til vand • H 2 SO 4: er en syre fordi molekylet indeholder 1 S-atom og 4 O-atomer, indeholder H og er meget polært • HCl: er en syre fordi molekylet er meget polært og indeholder 1 H-atom • HNO 3: (som ovenfor) Svovlsyre Saltsyre Salpetersyre

Svage uorganiske syrer Svage syrer afgiver kun delvis deres hydroner til vand • H 2 CO 3 er en syre fordi molekylet indeholder 1 C-atom, 3 O-atomer og H, og molekylet er polært • H 2 PO 4 - er en syre, selvom molekylet er negativt ladet

Organiske syrer • Indeholder alle en –COOH gruppe Fx. : methansyre HCOOH ethansyre propansyre etc. CH 3 COOH CH 3 CH 2 COOH

Stærke baser • OH- er en base fordi molekylet er negativt ladet, og derfor kan tiltrække en hydron (H+)

Middelstærke baser • HCO 3 - er en base, fordi ionen er negativt ladet, og derfor kan tiltrække en hydron (H+) • NH 3 er en base, fordi molekylet er polært og indeholder et ikke bindende elektronpar

H 2 O • Er en syre: fordi molekylet indeholder H og O, og fordi molekylet er polært • Er en base: fordi molekylet er polært og indeholder et ikke-bindende elektronpar

H 2 O Vand kaldes for en amfolyt, fordi vand har både syre og base egenskaber. Egenskaberne afgøres af hvad vand ellers reagerer med. Der findes andre amfolytter ud over vand

Korresponderende syrer og baser • Når en syre afgiver en hydron (H+) omdannes den til sin korresponderende base (syrerest) • Fx: HCl bliver til Cl. HCOOH bliver til HCOOH 2 CO 3 bliver til HCO 3 -

En sur opløsning • Man gør en opløsning sur ved at komme syre i vand. • Derved bliver opløsningens p. H-værdi < 7

En basisk opløsning • Man gør en opløsning basisk ved at komme en base i vand. • Derved bliver opløsningens p. H-værdi > 7

p. H • Er et mål for en opløsnings surhedsgrad • p. H = -log[H+]

neutralisation • - en sur opløsning og en basisk opløsning reagerer sammen og danner en saltvandsopløsning
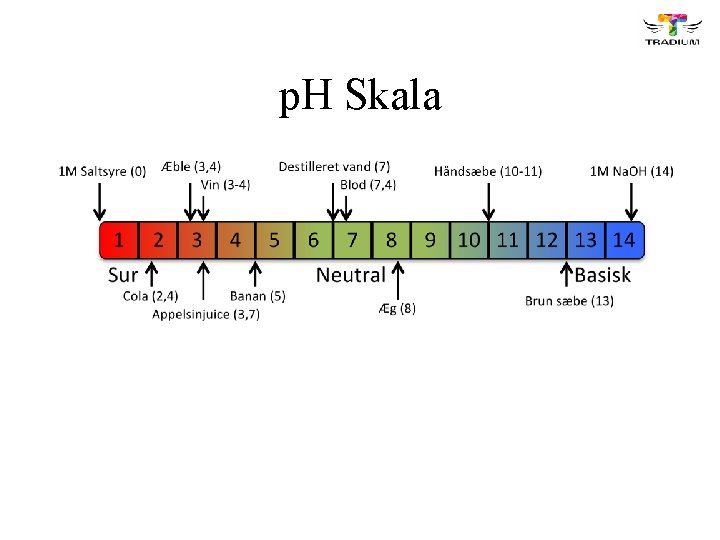
p. H Skala
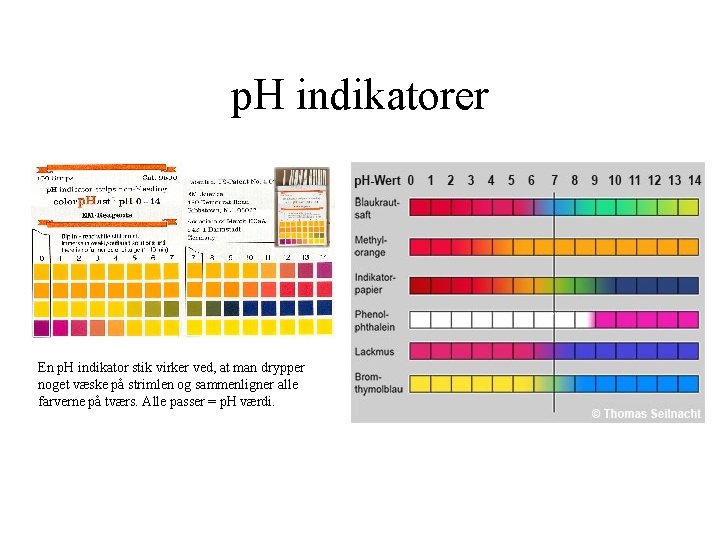
p. H indikatorer En p. H indikator stik virker ved, at man drypper noget væske på strimlen og sammenligner alle farverne på tværs. Alle passer = p. H værdi.
- Slides: 21