Syrer baser og salter Syrer og baser er

Syrer, baser og salter

Syrer og baser er vanlige stoffer • Syrer finner vi i mange matvarer. • Baser finner vi ofte blant vaskemidler.
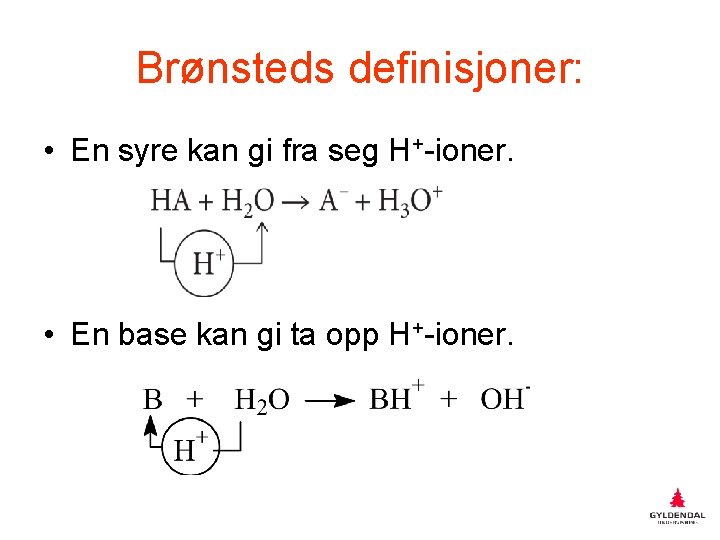
Brønsteds definisjoner: • En syre kan gi fra seg H+-ioner. • En base kan gi ta opp H+-ioner.

Protolyser • I en protolyse går det et H+-ion fra et stoff til et annet. • I vannløsning er det alltid et vannmolekyl som gir fra seg eller tar opp H+. • Når en syre gir fra seg H+, blir resten av syra til den korresponderende basen. • Her er A- den korresponderende basen til HA.

Vannets egenprotolyse • Vann er en amfolytt, og kan virke både som en syre og som en base.

Sterke syrer og baser • En sterk syre eller base er spaltet fullstendig i ioner. HCl + H 2 O → H 3 O+ + Cl-
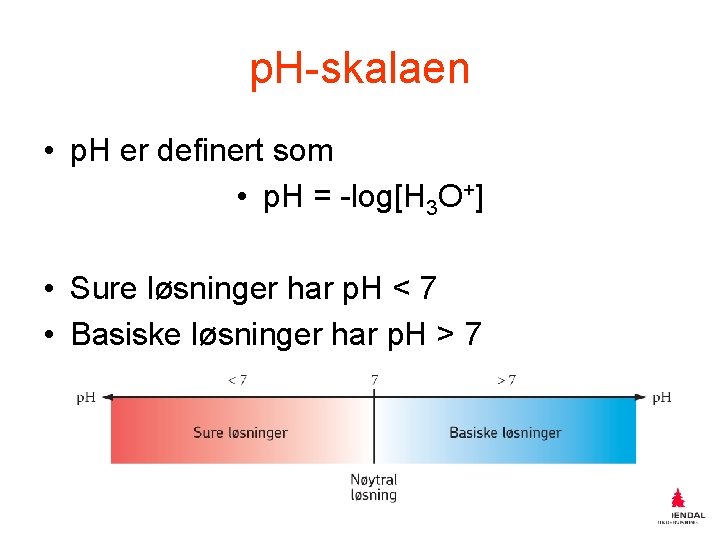
p. H-skalaen • p. H er definert som • p. H = -log[H 3 O+] • Sure løsninger har p. H < 7 • Basiske løsninger har p. H > 7

p. H-beregninger i sterke syrer • Vi regner at alle syremolekylene er spaltet i ioner. • For en enprotisk syre HA gjelder da at [H 3 O+] = [HA]
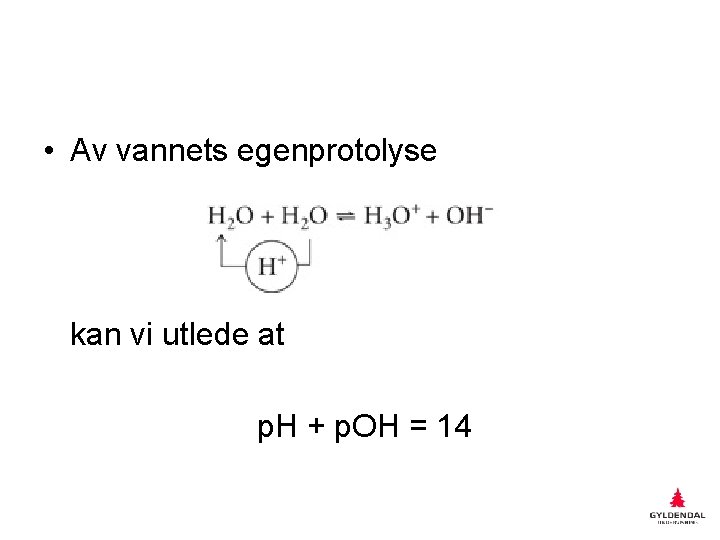
• Av vannets egenprotolyse kan vi utlede at p. H + p. OH = 14
![p. H-beregninger i sterke baser • I sterke baser finner vi først [OH-], og p. H-beregninger i sterke baser • I sterke baser finner vi først [OH-], og](http://slidetodoc.com/presentation_image_h/866eee05318fa4a5ff8535c843e4d7ac/image-10.jpg)
p. H-beregninger i sterke baser • I sterke baser finner vi først [OH-], og deretter p. OH og p. H. • Husk på at mange sterke baser er toprotiske! • Ca(OH)2 g. Ca 2+ + 2 OH-

p. H-beregninger i svake syrer • I en svak syre er bare en liten del av syremolekylene spaltet i ioner. CH 3 COOH + H 2 O H 3 O+ + CH 3 COO- • For å regne ut p. H, må vi bruke syrekonstanten Ka. Den er definert ved

p. H-beregninger i svake baser • I en svak base er bare en liten del av basemolekylene spaltet i ioner. NH 3 + H 2 O NH 4+ + OH- • For å regne ut p. H, må vi bruke basekonstanten Kb. Den er definert ved

Sammenhengen mellom Ka og Kb • Mellom syrekonstanten Ka for en svak syre og basekonstanten Kb for den korresponderende basen har vi følgende sammenheng: Ka ∙ Kb = 1, 0 ∙ 10− 14 (mol/L)2

Sure og basiske salter • For salter har vi følgende regler for sure og nøytrale kationer: Enverdige metallioner og de toverdige ionene i gruppe II er p. H-nøytrale. De andre toverdige metallionene og metallioner med høyere ladning er sure.

• Dette ser vi på bildet:

• For salter har vi følgende regler for sure, nøytrale og basiske anioner: • Sure anioner finner vi hos mellomproduktene ved protolyse av flerprotiske syrer. Eksempel: HSO 4 • p. H-nøytrale anioner har sterke korresponderende syrer. Eksempel: Cl • Basiske anioner har svake korresponderende syrer. Eksempel: CN-

Sure og basiske oksider • Oksider kan være både sure og basiske. • Sure oksider er oksider som løses i vann og danner en sur løsning eller som løses i sterke baser. Eks: SO 2 • Basiske oksider er oksider som løses i vann og danner en basisk løsning eller som løses i sterke syrer. Eks: Ca. O

Nøytraliseringer • En nøytralisering er en reaksjon mellom en syre og en base. • Det dannes da vann og et salt: HCl + Na. OH → H 2 O + Na. Cl • Når vi skal bestemme styrken på en syre, kan vi gjøre dette ved å titrere den mot en base med kjent konsentrasjon.

Indikatorer • En syre-baseindikator er et stoff som har ulik farge i sur og basisk løsning. • Mange plantefarger er avhengige av surheten i jorda og i cellesaftene.

• Kjemisk er indikatoren en svak, organisk syre der syra og den korresponderende basen har ulik farge. HIn + H 2 O g H 3 O+ + In- • En indikator har blandingsfargen mellom HIn og In- (”slår om”) når p. H i løsningen = p. KIn.
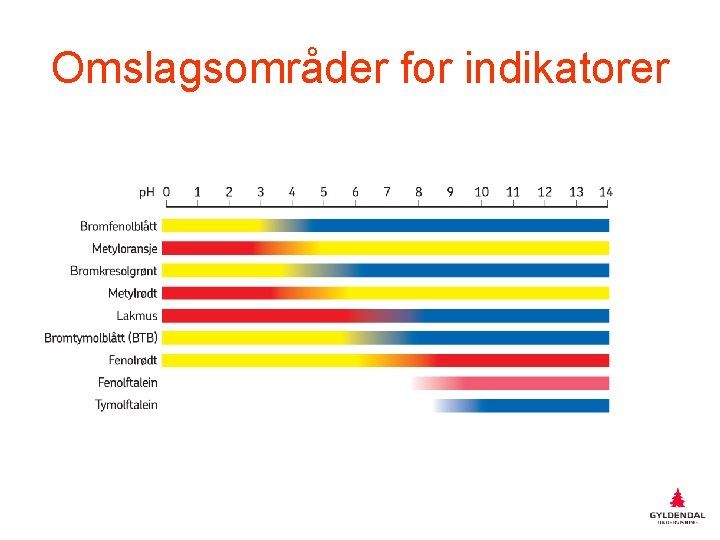
Omslagsområder for indikatorer
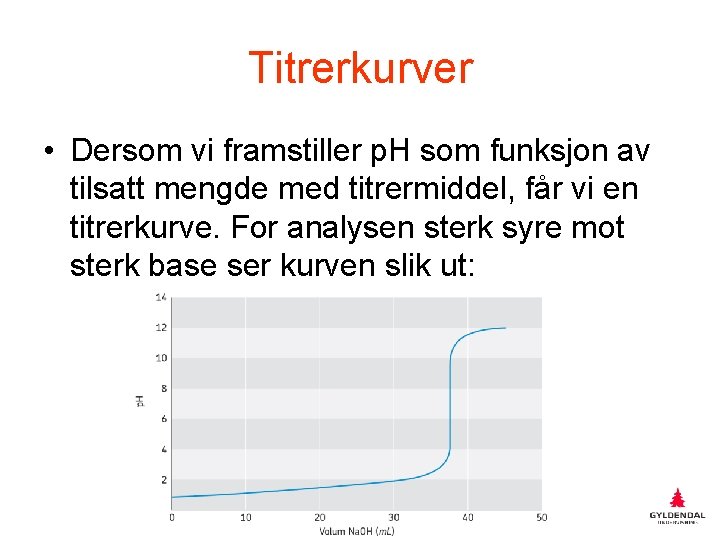
Titrerkurver • Dersom vi framstiller p. H som funksjon av tilsatt mengde med titrermiddel, får vi en titrerkurve. For analysen sterk syre mot sterk base ser kurven slik ut:
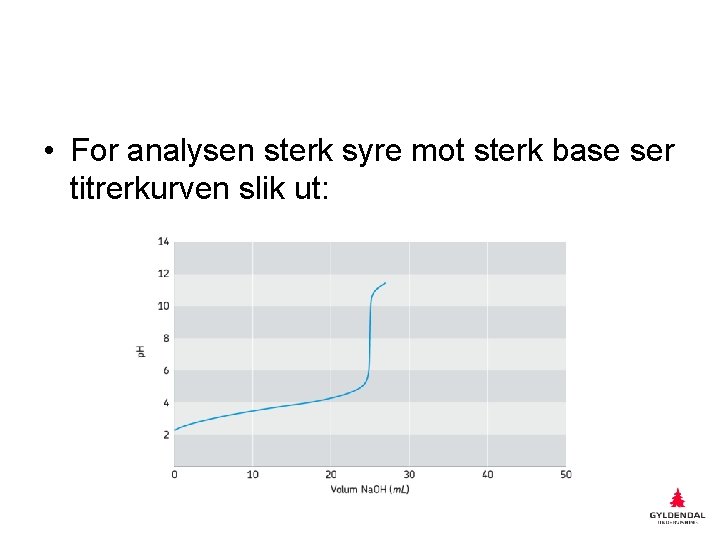
• For analysen sterk syre mot sterk base ser titrerkurven slik ut:

Indikatorvalg i titreringer • Prinsippet er at vi skal velge en indikator som har omslagsområde så nær p. Hverdien ved ekvivalenspunktet som mulig. • Titrerer vi en sterk syre mot en sterk base, får vi dannet et nøytralt salt. Vi bruker for eksempel BTB som indikator, da den slår om ved p. H = 7.

• Titrerer vi en svak syre mot en sterk base, får vi laget et basisk salt. Vi bruker da for eksempel fenolftalein som indikator, da den slår om ved p. H > 7.
- Slides: 25