SYNDROME DE GUILLAIN BARRE Introduction Maladie rare 0

SYNDROME DE GUILLAIN BARRE

Introduction Maladie rare : 0, 4 à 4/100 000 h Ubiquitaire Tous les âges Pronostic Court terme: atteinte respiratoire (20 à 30%) Long terme: séquelles motrices (10 à 20 %) Décès 5 à 10 % Hughes Lancet 2005 Orlikowski Neurocritical Care 2004
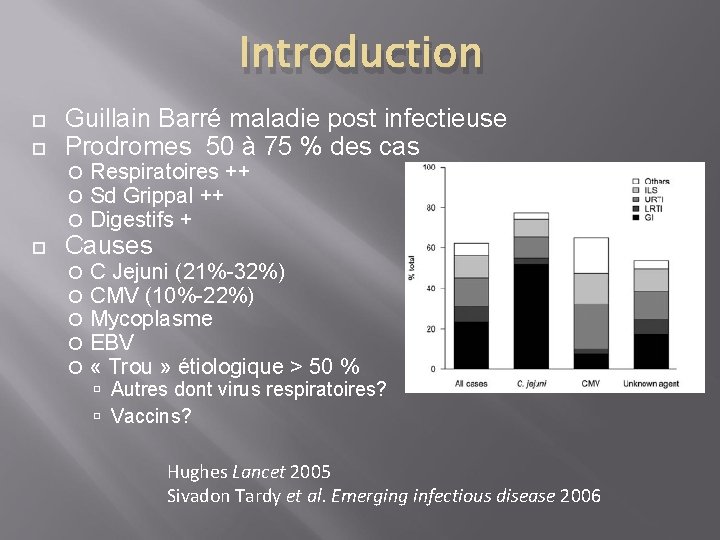
Introduction Guillain Barré maladie post infectieuse Prodromes 50 à 75 % des cas Respiratoires ++ Sd Grippal ++ Digestifs + Causes C Jejuni (21%-32%) CMV (10%-22%) Mycoplasme EBV « Trou » étiologique > 50 % Autres dont virus respiratoires? Vaccins? Hughes Lancet 2005 Sivadon Tardy et al. Emerging infectious disease 2006

Comparaison GBS associé à C Jejuni et CMV Yuki Lancet infectious disease 2001
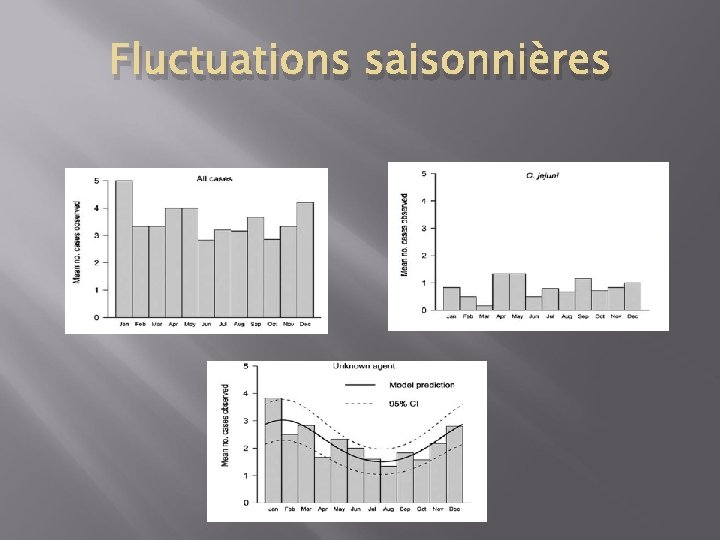
Fluctuations saisonnières
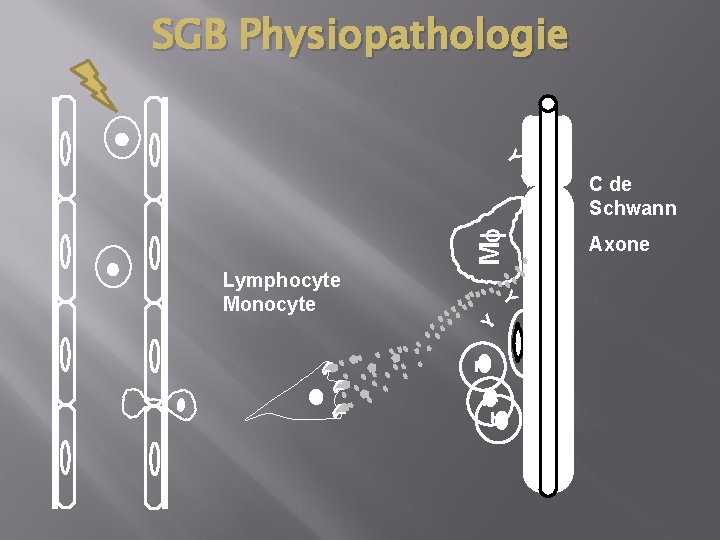
SGB Physiopathologie Y Mf Y TT T Y Y Lymphocyte Monocyte C de Schwann Axone
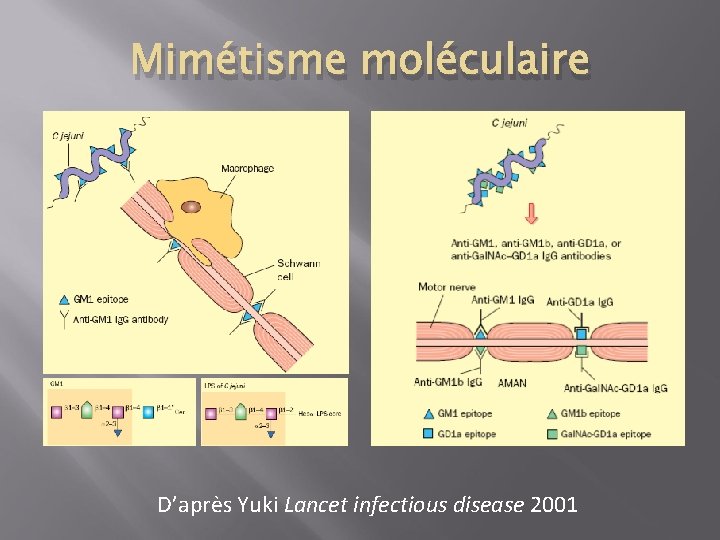
Mimétisme moléculaire D’après Yuki Lancet infectious disease 2001
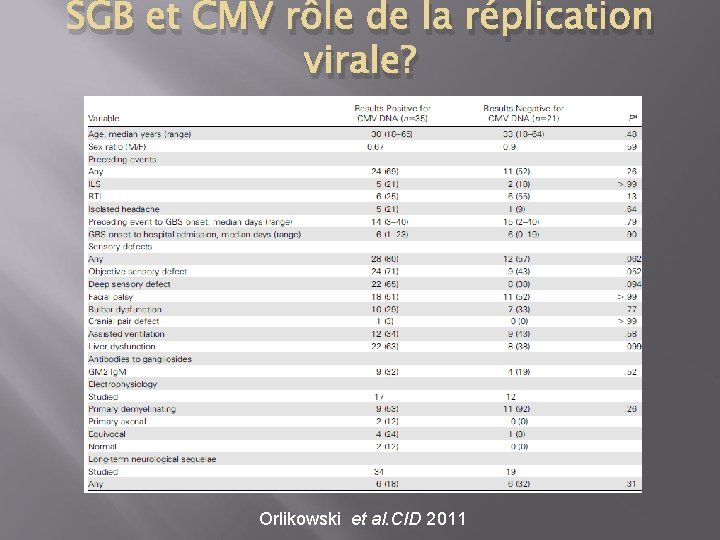
SGB et CMV rôle de la réplication virale? Orlikowski et al. CID 2011

SGB diagnostic § § § Forme classique Déficit moteur ascendant à prédominance proximale globalement symétrique < de 4 semaines Signes sensitifs discrets subjectifs ++, douleurs Atteinte des paires crâniennes, PF ++ Abolition des ROT
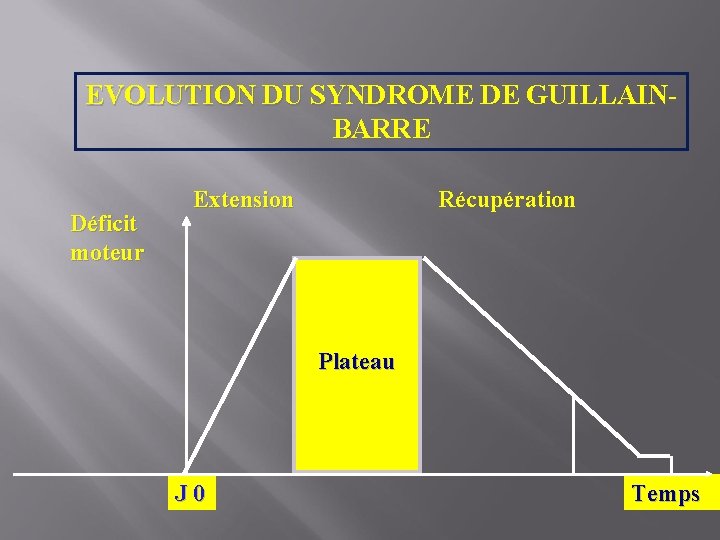
EVOLUTION DU SYNDROME DE GUILLAINBARRE Déficit moteur Extension Récupération Plateau J 0 Temps

SGB diagnostic § § § Evolution en 4 phases Prodromiques sd infectieux dans le mois précédent Ascendante: extension des paralysies (12 j en moyenne mais peut être <24 h) Plateau : stabilisation Récupération Durée des différentes phases extrêmement variables d’un sujet a l’autre
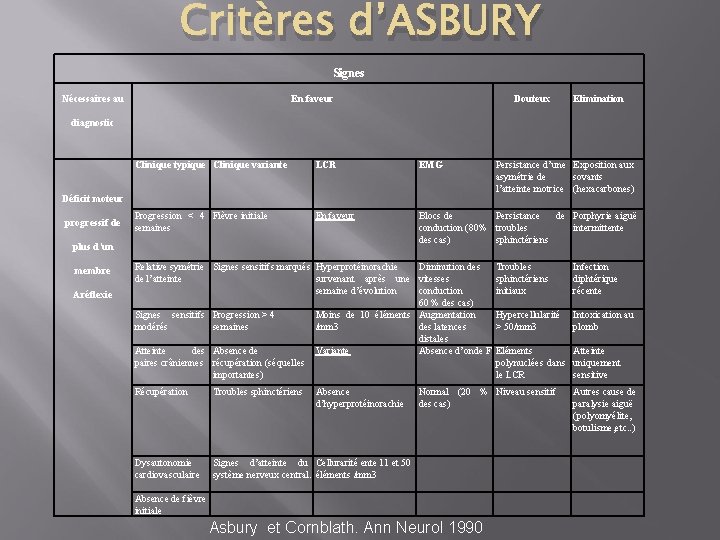
Critères d’ASBURY Signes Nécessaires au En faveur Douteux Elimination diagnostic Clinique typique Clinique variante LCR EMG Progression < 4 Fièvre initiale semaines En faveur Blocs de Persistance de Porphyrie aiguë conduction (80% troubles intermittente des cas) sphinctériens Déficit moteur progressif de plus d’un membre Aréflexie Relative symétrie Signes sensitifs marqués Hyperprotéinorachie Diminution des de l’atteinte survenant après une vitesses semaine d’évolution conduction 60 % des cas) Signes sensitifs Progression > 4 Moins de 10 éléments Augmentation modérés semaines /mm 3 des latences distales Atteinte des Absence de Variante Absence d’onde F paires crâniennes récupération (séquelles importantes) Récupération Troubles sphinctériens Absence d’hyperprotéinorachie Dysautonomie cardiovasculaire Signes d’atteinte du Cellurarité ente 11 et 50 système nerveux central. éléments /mm 3 Persistance d’une Exposition aux asymétrie de sovants l’atteinte motrice (hexacarbones) Troubles sphinctériens initiaux Infection diphtérique récente Hypercellularité > 50/mm 3 Intoxication au plomb Eléments Atteinte polynuclées dans uniquement le LCR sensitive Normal (20 % Niveau sensitif des cas) Absence de fièvre initiale Asbury et Cornblath. Ann Neurol 1990 Autres cause de paralysie aiguë (polyomyélite, botulisme, etc. . )

Pièges § § § Manifestation dysautonomique (ascension): bradycardie, tachycardie, HTA, hypo. TA voire arrêt cardiaque, SIADH Troubles sphinctériens possibles (secondaires) Pseudo niveau sensitifs ROT conservés initialement Evolution descendante des paralysie avec atteinte inaugurale des paires crâniennes (passage avec Miller Fisher)

Examens complémentaires diagnostic § § § Ponction lombaire: dissociation albuminocytologique Electromyographie: atteinte démyélinisante, atteinte axonale, sensitivomotrice, sensitive Peuvent être normaux les 15 premiers jours, non nécessaires au diagnostic

Formes électro-cliniques § § § AIDP 80 - 90% AMAN 10 - 20% AMSAN MILLER FISHER <5% Forme de passage avec MF Pan-dysautonomie aiguë : exceptionnelle

Diagnostic différentiel • • Atteintes médullaires: • Compression • Pathologie vasculaire médullaire • Infectieuse, inflammatoire, etc… Syndrome de la queue de cheval Autres neuropathies périphériques Méningo-radiculonévrite Poliomyélite Atteintes aiguës de la jonction neuro musculaire PRN chroniques Porphyrie aigue

Prise en charge Symptomatique Identification patients à admettre en réa Identification patients a ventiler Identification du moment adéquat de la ventilation Tt facteurs aggravant (déglutition, atélectasie, etc. . ) Douleurs Nutrition Rééducation Etiologique Ig. IV, échanges plasmatiques
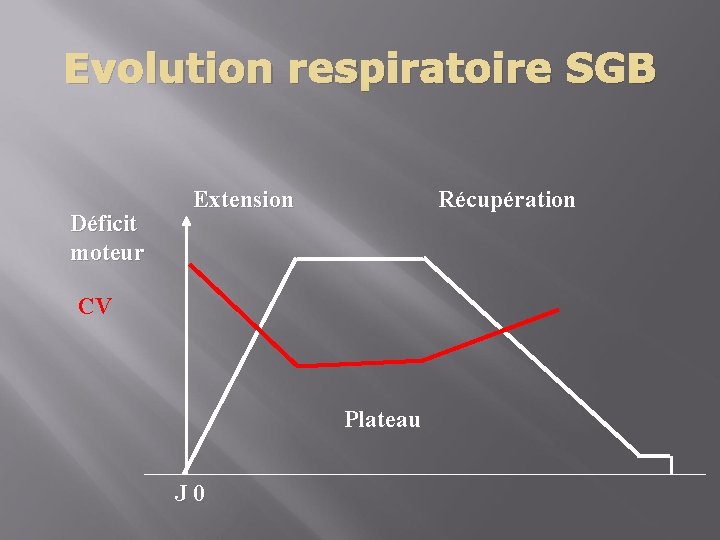
Evolution respiratoire SGB Déficit moteur Extension Récupération CV Plateau J 0
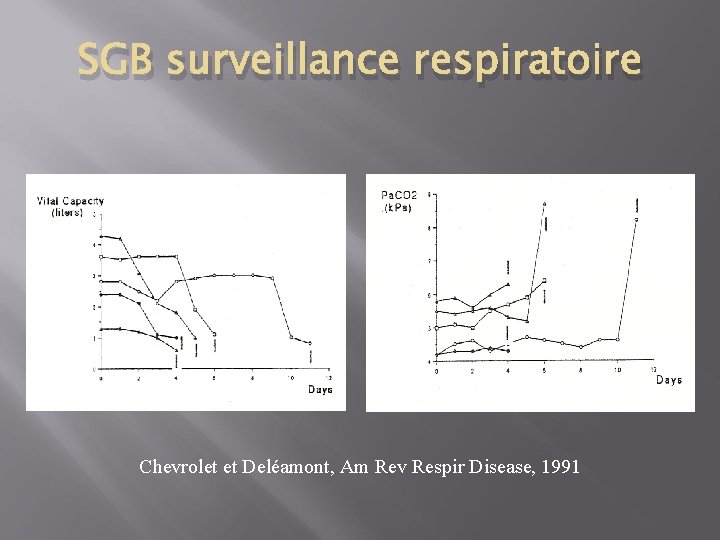
SGB surveillance respiratoire Chevrolet et Deléamont, Am Rev Respir Disease, 1991
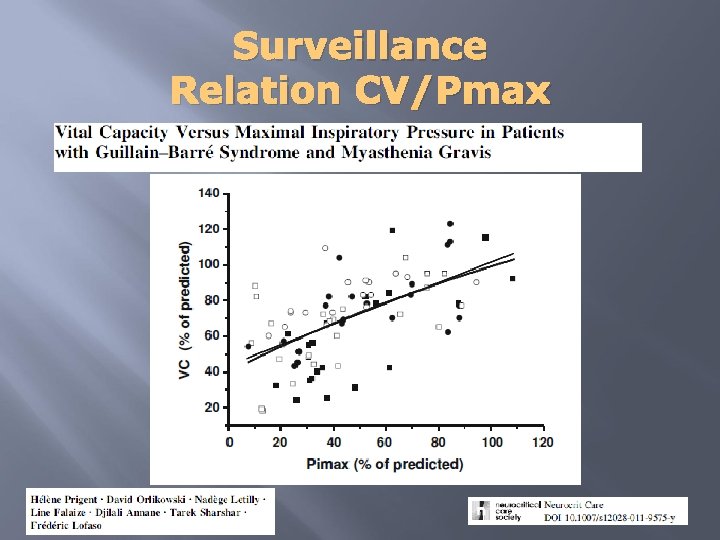
Surveillance Relation CV/Pmax

Orientation REA Facteurs de risques de ventilation mécanique A L’ADMISSION Sans CV Avec CV • Délai depuis l’admission < 7 J 7 J • Impossibilité de relever la tête • Impossibilité de tousser • Impossibilité de tenir debout • CV < 60 % • Impossibilité de relever les 3 présents= ventilation 85 % coudes • Impossibilité de relever la tête • Anomalies BHC 4 présents= ventilation 85 %
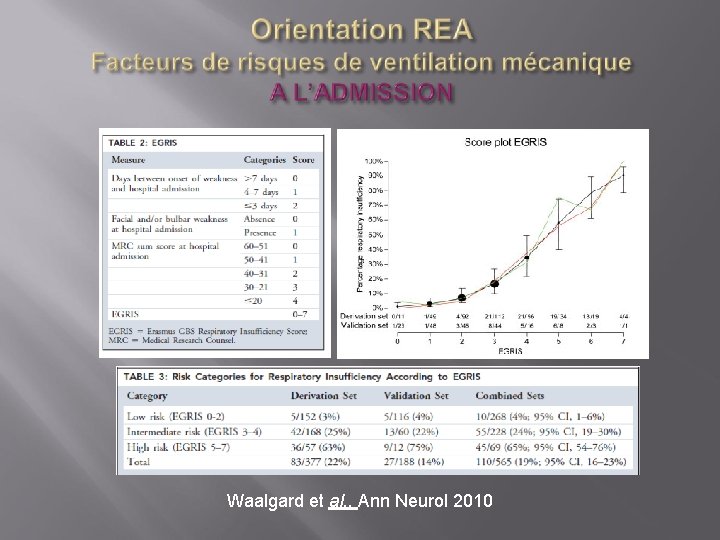
Waalgard et al. , Ann Neurol 2010

Facteurs de risques de ventilation Electrophysiologie Démyelinisation ++ Risque VM ++ Si ratio CPN p/d. CMAP < 55. 6 % Si VC < 80 % Durand MC et al. , Lancet Neurol 2006

Facteurs prédictifs de ventilation mécanique SGB lors du séjours en réanimation Troubles de déglutition CV < 20 ml/kg ou 30 % théorique PI max<30 et PE max<40 cm H 20 Lawn et al, Arch neurol, 2001

Vitesse évolutive Chute rapide de CV ou des pressions respiratoires de 50 % : risque de VM dans les 36 h de la CV en dessous d’ 1 L : risque de VM dans les 18 h de 30 % CV en cours d’hospitalisation Chevrolet et Deléamont, Am Rev Respir Disease, 1991 Lawn et al, Arch neurol, 2001
IRA d’origine neuromusculaire Pathologie neuromusculaire Aigue Intubation VNI ?

Critères d’intubation Critères majeurs 1. 2. 3. 4. Signes de détresse respiratoire VC< 15 ml/kg (20%), Pimax ou Pemax < 25 cm H 2 O Pa. CO 2 > 6, 4 k. Pa Pa. O 2 < 7. 5 k. Pa (Fi. O 2= 0, 21) Critères mineurs 1. Toux inefficace 2. Troubles de déglutition 3. Atélectasie Ropper Neurology 1985 - Wijdicks Neurology 1998
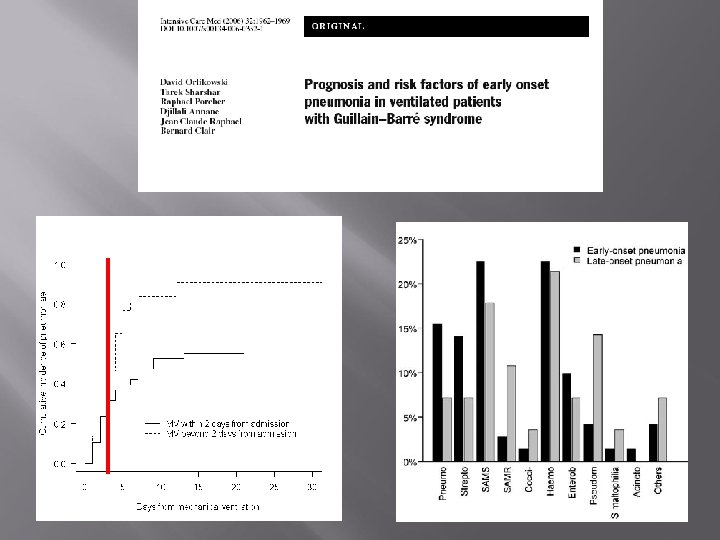

Immunotherapies et SGB Corticostéroïdes Introduit dans les années Effets négatifs Association avec IVIG? Echanges Plasmatiques Introduits en 1978 Démonstration efficacité 1950 IVIG Introduites en 1988 Effets similaires aux en 1985 EP 1992 Hughes et al. Brain 2007
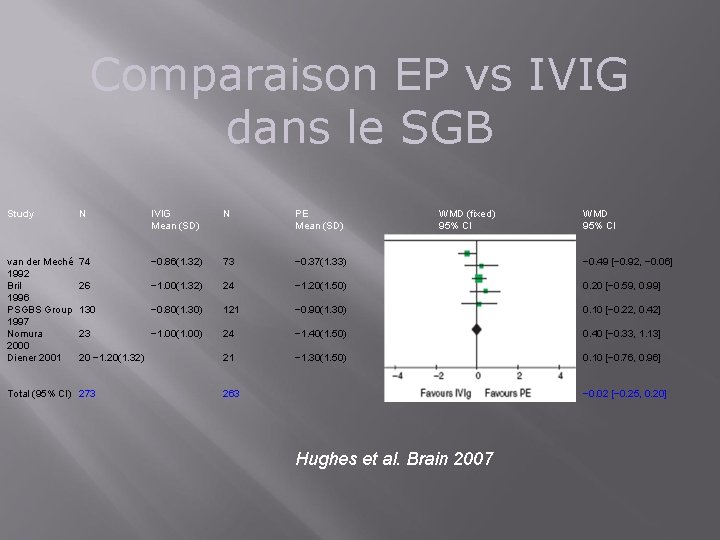
Comparaison EP vs IVIG dans le SGB Study N van der Meché 74 1992 Bril 26 1996 PSGBS Group 130 1997 Nomura 23 2000 Diener 2001 20 − 1. 20(1. 32) Total (95% CI) 273 IVIG Mean (SD) N PE Mean (SD) WMD (fixed) 95% CI − 0. 86(1. 32) 73 − 0. 37(1. 33) − 0. 49 [− 0. 92, − 0. 06] − 1. 00(1. 32) 24 − 1. 20(1. 50) 0. 20 [− 0. 59, 0. 99] − 0. 80(1. 30) 121 − 0. 90(1. 30) 0. 10 [− 0. 22, 0. 42] − 1. 00(1. 00) 24 − 1. 40(1. 50) 0. 40 [− 0. 33, 1. 13] 21 − 1. 30(1. 50) 0. 10 [− 0. 76, 0. 96] 263 WMD 95% CI − 0. 02 [− 0. 25, 0. 20] Hughes et al. Brain 2007

SGB Schéma thérapeutique
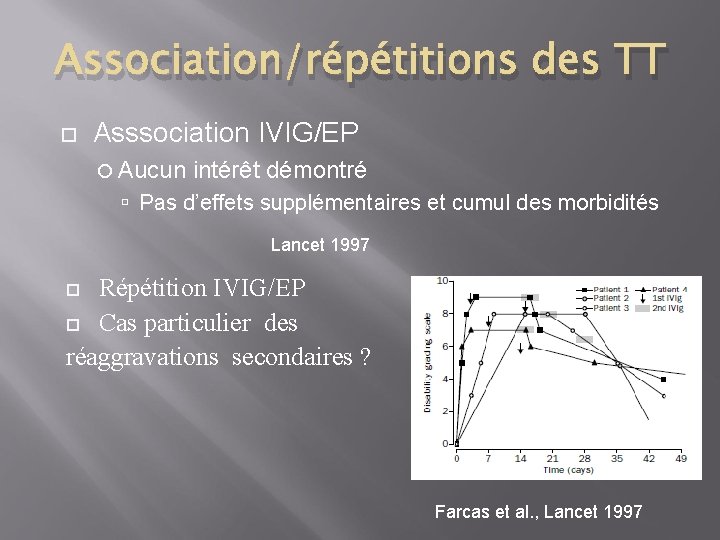
Association/répétitions des TT Asssociation IVIG/EP Aucun intérêt démontré Pas d’effets supplémentaires et cumul des morbidités Lancet 1997 Répétition IVIG/EP Cas particulier des réaggravations secondaires ? Farcas et al. , Lancet 1997

SGB contre-indications TT 1. 2. 3. 4. EP Infection Hypotension Hémorrhagie Troubles de l’hémostase Iv. Ig 1. Déficit en Ig. A 2. Allergie 3. Insuffisance rénale

SGB effets des traitements 1. Sur la ventilation A. Diminution du nombre de malades ventilés B. Diminution de la durée de ventilation 2. Au plan fonctionnel A. Diminution du délai de récupération de la marche B. Diminution du pourcentage de séquelles motrices

VENTILATION MECANIQUE Sevrage / Extubation Pré- requis § Amélioration du déficit musculaire (score) § Toux efficace - Déglutition ? Paramètres respiratoires § Début de sevrage : CV > 10 ml/kg (GBS 7 ml/kg) Pi max - 20 cm H 2 O Pe max 40 cm. H 2 O § Epreuves de RL sur pièce en T

VENTILATION MECANIQUE Sevrage / Extubation Paramètres respiratoires § Extubation § § CV 15 ml/kg- CV 4 ml/kg) Pi max : - 40 cm H 2 O (GBS - 50 cm H 2 O ) Pe max : 50 cm. H 2 O RL tolérée sans altération de la CV pendant 12 à 24 h L’hypercapnie en fin de RL Gaz du sang normaux en fin de RL = Echec Succès

SGB Trachéotomie • Durée moyenne de ventilation de 42 jours (médiane 25) • 2 Problèmes • Trachéotomiser trop vite des malades qui seront extubés rapidement • Laisser intubé des malades de façon prolongée avec des risques de complication • Délai habituel > 21 jours de ventilation • Sujets « à risques » = sujets âgés, maladie respiratoire sous jacente

SGB complications 1. 2. 3. 4. Mortalité globale environ 5% Morbidité essentiellement observée chez les patients ventilés Pneumopathies +++ (60 à 75 % des malades ventilés) Embolies pulmonaires, rares 3% Complication des traitements: 1. 2. EP (bradycardies, hypotensions, infections, thromboses, hématomes, liées à l’accès vasculaire) IVIG (sd grippal, dyspnée, insuffisance rénale, allergie)

Pronostic Long terme 10 à 20 % de séquelles motrices Sensitives ou PF>40% Séquelles motrices sévères C jejuni ++. Facteurs de risque de séquelles: âge +++, perte de la marche d’emblée et ventilation mécanique.

Myasthénie § § § Maladie auto-immune responsable d’ 1 atteinte de la jonction neuromusculaire Défaut de transmission neuromusculaire post- synaptique (cf figure) Lié à des anticorps dirigés contre le récepteur de l’acétylcholine Association fréquente a des anomalies thymiques Déficit des muscle volontaires Evolution : fluctuations et épisodes de décompensation (crises myasthéniques)

Myasthénie généralisée Clinique § § Fatigabilité musculaire fluctuante, apparaît ou s’aggrave lors de l’effort et diminue au repos Fatigabilité musculaire maximale le soir Tout les groupes musculaires peuvent être touché Variabilité +++

Clinique § § Atteinte de la musculature oculaire extrinsèque: ptôsis (à bascule), diplopie par atteinte des muscles oculomoteurs, ophtalmoplégie Atteinte de la musculature oro-pharyngolaryngée: troubles de mastication, troubles de la phonation (voix nasonnée), troubles de déglutition, atteinte faciale

Clinique § § § Atteinte axiale: muscle de la nuque (chute de la tête) Atteinte des membres (racine ++) Atteinte des muscles respiratoires inspiratoires et expiratoires (CV) Atteinte oculaire 50%, bulbaire 30%, membres et troncs 10 à 25% des cas Score de force musculaire /100

SCORE DE LA FORCE MUSCULAIRE (Total : 100 points) 1 Membres supérieurs étendus à l’horizontale en antéroposition 1 point pour 10 s Max. 15 Min. 0 Membres inférieurs, patient en décubitus dorsal, cuisses fléchies à 90° sur le bassin, jambes à 90° sur les cuisses 1 point pour 5 s Max. 15 Min. 0 Flexion de la tête en décubitus dorsal Contre résistance Sans résistance Impossible Passage de la position couchée à la position assise Possible sans l’aide des mains Impossible sans l’aide des mains Oculomotricité extrinsèque Normal Ptosis isolé Diplopie 10 5 0

SCORE DE LA FORCE MUSCULAIRE (Total : 100 points) 2 Occlusion palpébrale Complète Incomplète (mais avec recouvrement cornéen) Nulle (sans recouvrement cornéen) 10 5 0 Mastication Normale Diminuée Nulle 10 5 0 Déglutition Normale Dysphagie sans fausse route Dysphagie avecfausse route 10 5 0 Phonation Voix normale Voix nasonnée Aphonie 10 5 0

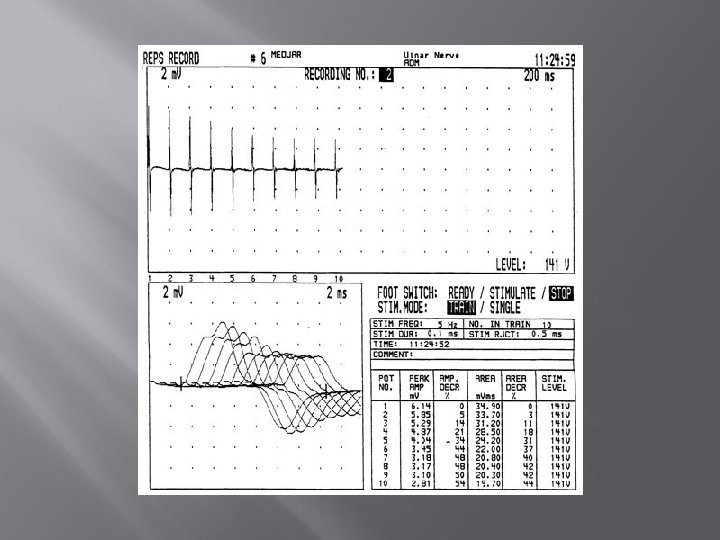
Diagnostic § Tests pharmacologiques: anticholinesterasique d’action rapide (Reversol, Enlon, etc. . ) § Examens électriques : décrément à la stimulation supramaximale de 2 à 5 Hz > 10 % § Dosages immunologiques et biologiques : anticorps anti-RACh (85 à 90 %), anti Mus. K

Pathologies associées § Auto-immune auto anticorps, bilan inflammatoire et ionique, CPK, TSH § Radio de thorax et scanner thoracique (thymome)

MYASTHENIE Evolution générale u Début : Signes oculaires Signes oropharyngés Déficit des membres u Aggravation progressive - irrégulière u Poussées et crises myasthéniques u Maximum des signes : 3ème année - 84% des cas u Rémission spontanée 15 à 20 %

MYASTHENIE Evolution par poussée ou crise myasthénique • Au - une crise myasthénique = 15 à 20 % des myasthéniques • Augmentation du déficit moteur Ø Troubles de la déglutition Ø Phonation Ø Dyspnée Ø Diaphragme • Crise révélatrice = Dg étiologique d’une IRA
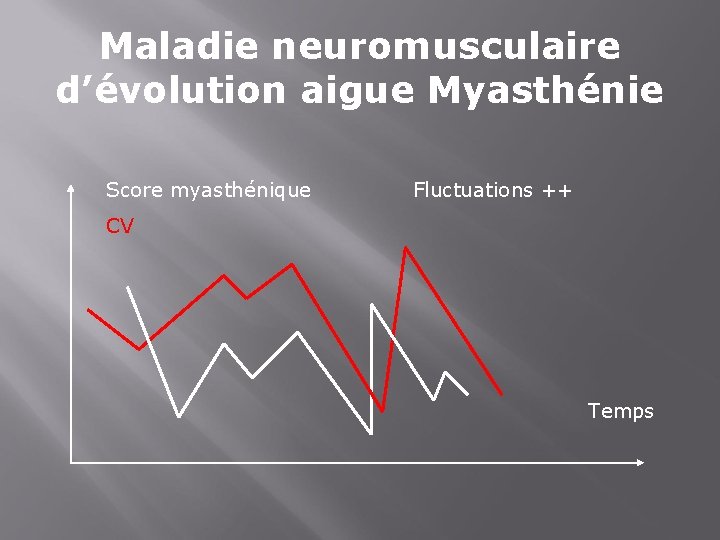
Maladie neuromusculaire d’évolution aigue Myasthénie Score myasthénique Fluctuations ++ CV Temps

Surveillance REA? Signes respiratoires Signes oropharyngés Encombrement Déficit axial CV < 60 % de la théorique Pathologie aggravante Fluctuations ++

TRAITEMENT DE LA CRISE MYASTHENIQUE • Symptomatique • Mesures de réanimation • Echanges plasmatiques • Immunoglobulines IV • Corticoides et immunosuppresseurs

TRAITEMENT SYMPTOMATIQUE EN REANIMATION ØRepos ØEliminer et traiter un facteur déclenchant ØSonde gastrique ØAnticholinestérasique Si myasthénie de novo : introduction Si myasthénie déjà traitée : diminution ou arrêt si suspicion de surdosage puis reprise progressive Pas de Prostigmine IVSE ØVentilation mécanique

RECHERCHE DE FACTEURS FAVORISANTS Infections Chirurgie Grossesse (post partum) Modifications thérapeutiques (corticoides, surdosage en anticholinesterasique) Médicaments contre-indiqués (cf liste)

MÉDICAMENTS CONTRE-INDIQUES Tableau IV. - Médicaments contre-indiqués au cours de la myasthénie. Médicaments à utiliser formellement contre-indiqués avec précaution Aminosides Colimycine® Polymyxine Cycline injectable Quinine - Chloroquine Quinidine Procaïnamide Diphénylhydantoïne Triméthadione Bêtabloquants Dantrolène D-pénicillamine Tous les curarisants Neuroleptiques Benzodiazépines Phénothiazines Carbamazépine !!!! Nouveaux médicaments
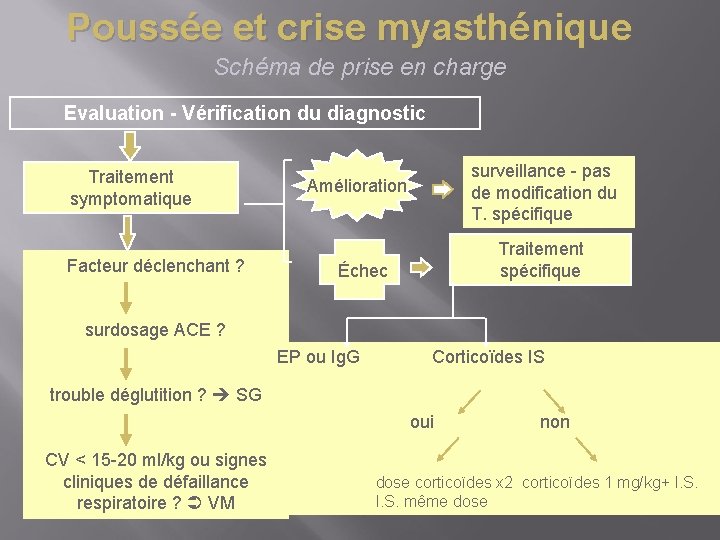
Poussée et crise myasthénique Schéma de prise en charge Evaluation - Vérification du diagnostic Traitement symptomatique Facteur déclenchant ? surveillance - pas de modification du T. spécifique Amélioration Traitement spécifique Échec surdosage ACE ? EP ou Ig. G Corticoïdes IS trouble déglutition ? SG oui CV < 15 -20 ml/kg ou signes cliniques de défaillance respiratoire ? VM non dose corticoïdes x 2 corticoïdes 1 mg/kg+ I. S. même dose
- Slides: 57