Switch pour DRVr RPV Etude PROBE 118 Etude

Switch pour DRV/r + RPV § Etude PROBE
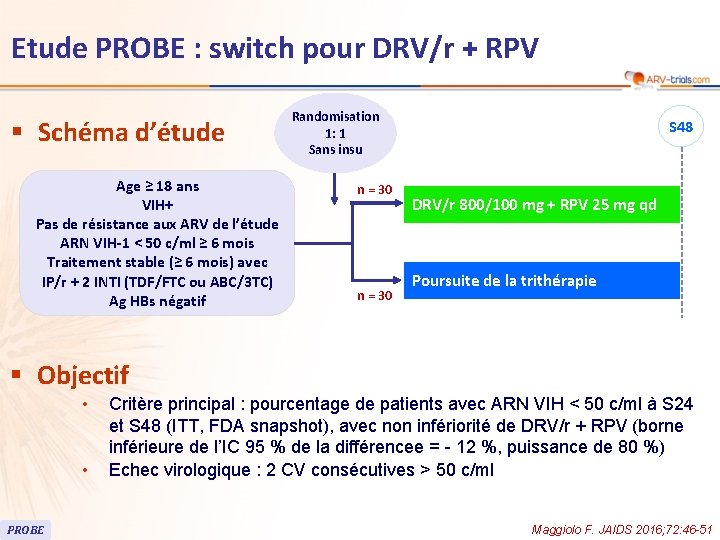
118 Etude PROBE : switch pour DRV/r + RPV § Schéma d’étude Age ≥ 18 ans VIH+ Pas de résistance aux ARV de l’étude ARN VIH-1 < 50 c/ml ≥ 6 mois Traitement stable (≥ 6 mois) avec IP/r + 2 INTI (TDF/FTC ou ABC/3 TC) Ag HBs négatif Randomisation 1: 1 Sans insu n = 30 S 48 DRV/r 800/100 mg + RPV 25 mg qd Poursuite de la trithérapie § Objectif • • PROBE Critère principal : pourcentage de patients avec ARN VIH < 50 c/ml à S 24 et S 48 (ITT, FDA snapshot), avec non infériorité de DRV/r + RPV (borne inférieure de l’IC 95 % de la différencee = - 12 %, puissance de 80 %) Echec virologique : 2 CV consécutives > 50 c/ml Maggiolo F. JAIDS 2016; 72: 46 -51
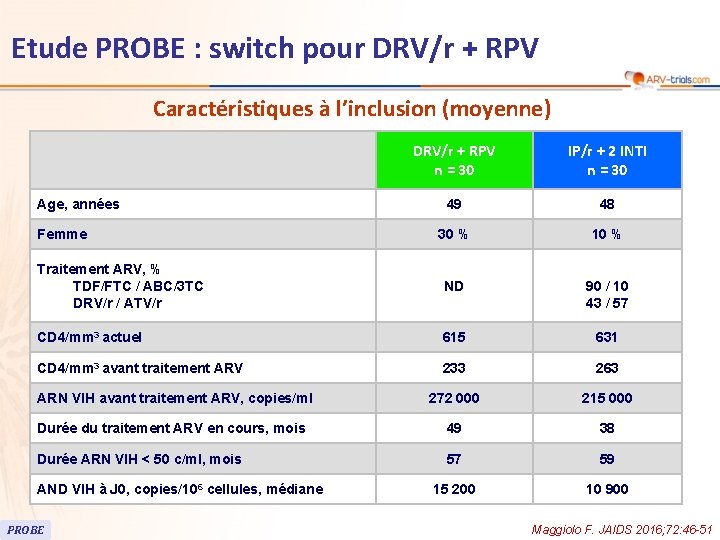
Etude PROBE : switch pour DRV/r + RPV Caractéristiques à l’inclusion (moyenne) DRV/r + RPV n = 30 IP/r + 2 INTI n = 30 49 48 30 % 10 % Traitement ARV, % TDF/FTC / ABC/3 TC DRV/r / ATV/r ND 90 / 10 43 / 57 CD 4/mm 3 actuel 615 631 CD 4/mm 3 avant traitement ARV 233 263 ARN VIH avant traitement ARV, copies/ml 272 000 215 000 Durée du traitement ARV en cours, mois 49 38 Durée ARN VIH < 50 c/ml, mois 57 59 15 200 10 900 Age, années Femme AND VIH à J 0, copies/106 cellules, médiane PROBE Maggiolo F. JAIDS 2016; 72: 46 -51
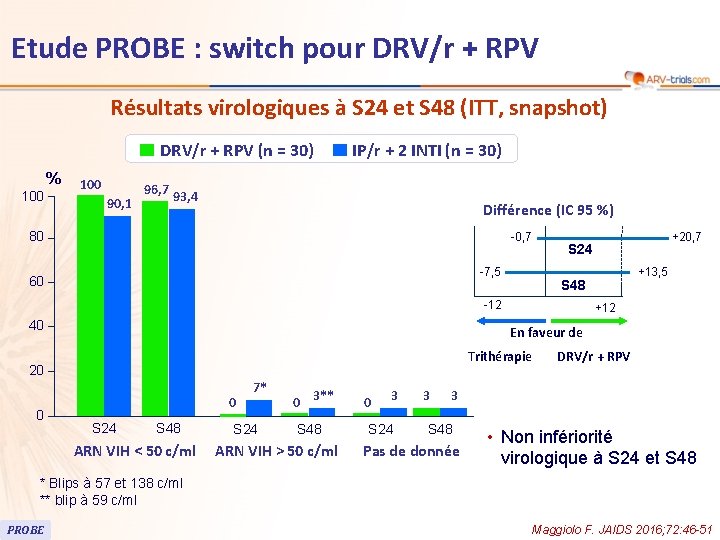
118 Etude PROBE : switch pour DRV/r + RPV Résultats virologiques à S 24 et S 48 (ITT, snapshot) DRV/r + RPV (n = 30) % 100 90, 1 IP/r + 2 INTI (n = 30) 96, 7 93, 4 Différence (IC 95 %) 80 -0, 7 -7, 5 60 +12 En faveur de Trithérapie 20 0 +13, 5 S 48 -12 40 +20, 7 S 24 0 S 24 S 48 ARN VIH < 50 c/ml 7* S 24 0 3** S 48 ARN VIH > 50 c/ml 0 3 S 24 3 DRV/r + RPV 3 S 48 Pas de donnée • Non infériorité virologique à S 24 et S 48 * Blips à 57 et 138 c/ml ** blip à 59 c/ml PROBE Maggiolo F. JAIDS 2016; 72: 46 -51
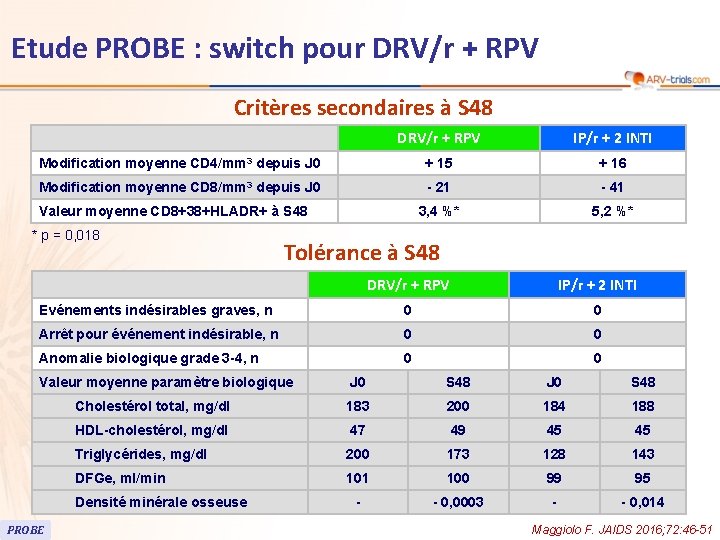
Etude PROBE : switch pour DRV/r + RPV Critères secondaires à S 48 DRV/r + RPV IP/r + 2 INTI Modification moyenne CD 4/mm 3 depuis J 0 + 15 + 16 Modification moyenne CD 8/mm 3 depuis J 0 - 21 - 41 3, 4 %* 5, 2 %* Valeur moyenne CD 8+38+HLADR+ à S 48 * p = 0, 018 Tolérance à S 48 DRV/r + RPV IP/r + 2 INTI Evénements indésirables graves, n 0 0 Arrêt pour événement indésirable, n 0 0 Anomalie biologique grade 3 -4, n 0 0 Valeur moyenne paramètre biologique J 0 S 48 Cholestérol total, mg/dl 183 200 184 188 HDL-cholestérol, mg/dl 47 49 45 45 Triglycérides, mg/dl 200 173 128 143 DFGe, ml/min 101 100 99 95 - - 0, 0003 - - 0, 014 Densité minérale osseuse PROBE Maggiolo F. JAIDS 2016; 72: 46 -51

Etude PROBE : switch pour DRV/r + RPV § Conclusion – La bithérapie rilpivirine plus DRV/ritonavir était non inférieure à 48 semaines à celle de la trithérapie standard à base d’IP/r – La bithérapie n’avait pas d’impact négatif sur le profil lipidique et la fonction rénale et avait un impact positif sur la densité minérale osseuse – Cette stratégie représente une alternative pour les patients ayant une toxicité avec les INTI – Limite • Faible taille d’étude PROBE Maggiolo F. JAIDS 2016; 72: 46 -51
- Slides: 6