Switch a ATVr RAL Estudio HARNESS Estudio HARNESS



- Slides: 7

Switch a ATV/r + RAL § Estudio HARNESS

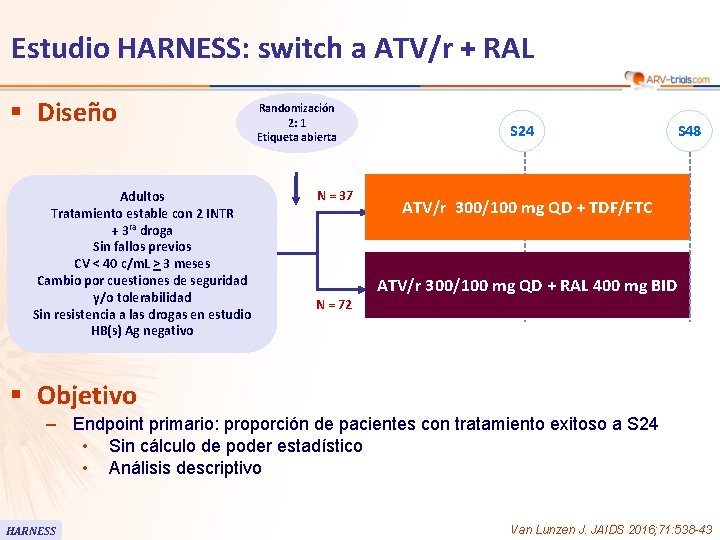
Estudio HARNESS: switch a ATV/r + RAL § Diseño Adultos Tratamiento estable con 2 INTR + 3 ra droga Sin fallos previos CV < 40 c/m. L > 3 meses Cambio por cuestiones de seguridad y/o tolerabilidad Sin resistencia a las drogas en estudio HB(s) Ag negativo Randomización 2: 1 Etiqueta abierta N = 37 S 24 S 48 ATV/r 300/100 mg QD + TDF/FTC ATV/r 300/100 mg QD + RAL 400 mg BID N = 72 § Objetivo – Endpoint primario: proporción de pacientes con tratamiento exitoso a S 24 • Sin cálculo de poder estadístico • Análisis descriptivo HARNESS Van Lunzen J. JAIDS 2016; 71: 538 -43

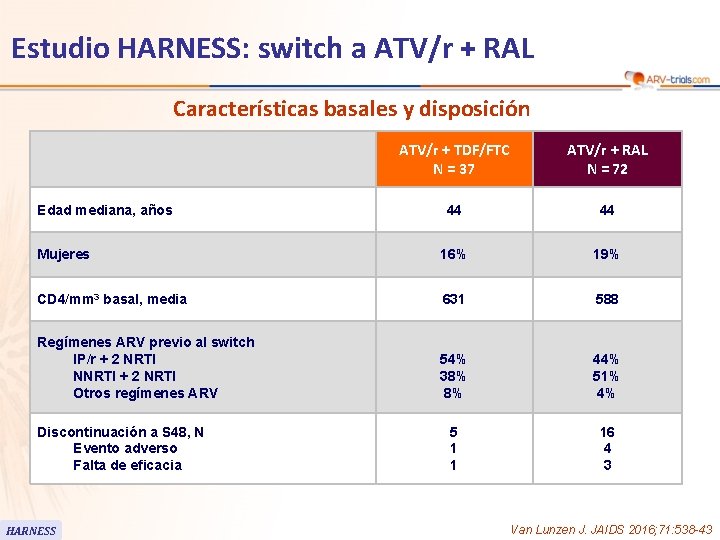
Estudio HARNESS: switch a ATV/r + RAL Características basales y disposición ATV/r + TDF/FTC N = 37 ATV/r + RAL N = 72 44 44 Mujeres 16% 19% CD 4/mm 3 basal, media 631 588 Regímenes ARV previo al switch IP/r + 2 NRTI NNRTI + 2 NRTI Otros regímenes ARV 54% 38% 8% 44% 51% 4% 5 1 1 16 4 3 Edad mediana, años Discontinuación a S 48, N Evento adverso Falta de eficacia HARNESS Van Lunzen J. JAIDS 2016; 71: 538 -43

Estudio HARNESS: switch a ATV/r + RAL Resultados de eficacia y seguridad CV < 40 c/m. L (ITT) ATV/r + TDF/FTC S 24 (endpoint primario) 100 % 80 60 40 94. 6 80. 6 Rebote virológico confirmado a semana 48, N ATV/r + RAL S 48 86. 5 69. 4 ATV/r + TDF/FTC ATV/r + RAL N 1 9 Muestras estudiadas 0 5 Resistencia a IP 1* L 10 V, G 16 Q, L 33 F, P 39 Q, M 46 L, G 48 V, Q 58 E, I 62 V, L 63 I/T, I 64 L, A 71 V, I 72 V, V 77 I, V 82 A, T 91 S, I 93 L Resistencia a INI 2* F 21 Y Y 143 C + N 155 H * 1 paciente con mutaciones a IP y INSTI § Rebote virologico 20 0 HARNESS 2 cargas virales consecutivas > 40 c/m. L Ultima CV en tratamiento > 40 c/m. L seguida por discontinuación Van Lunzen J. IAC 2014, Melbourne, Abs. LBPE 19, Van Lunzen J. JAIDS 2016; 71: 538 -43

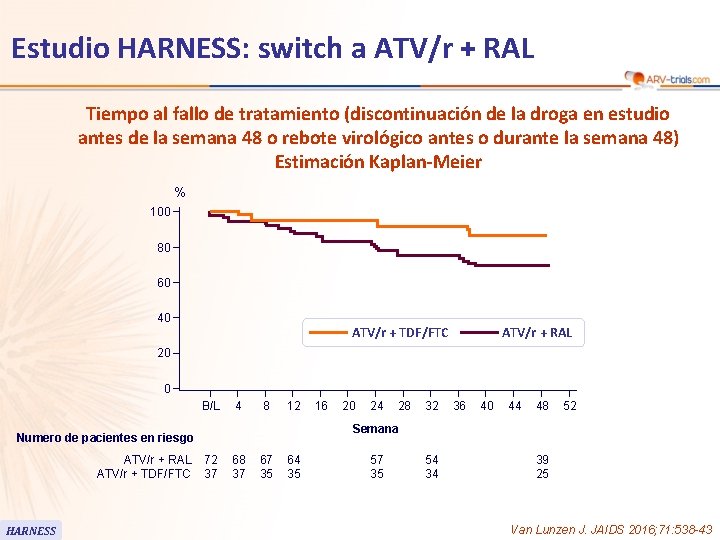
Estudio HARNESS: switch a ATV/r + RAL Tiempo al fallo de tratamiento (discontinuación de la droga en estudio antes de la semana 48 o rebote virológico antes o durante la semana 48) Estimación Kaplan-Meier % 100 80 60 40 ATV/r + TDF/FTC ATV/r + RAL 20 0 B/L 4 8 12 HARNESS 20 24 28 32 36 40 44 48 52 Semana Numero de pacientes en riesgo ATV/r + RAL ATV/r + TDF/FTC 16 72 37 68 37 67 35 64 35 57 35 54 34 39 25 Van Lunzen J. JAIDS 2016; 71: 538 -43

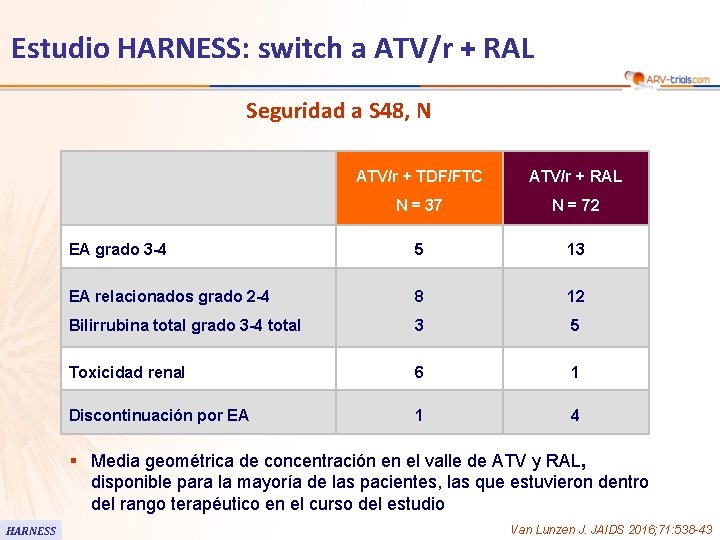
Estudio HARNESS: switch a ATV/r + RAL Seguridad a S 48, N ATV/r + TDF/FTC ATV/r + RAL N = 37 N = 72 EA grado 3 -4 5 13 EA relacionados grado 2 -4 8 12 Bilirrubina total grado 3 -4 total 3 5 Toxicidad renal 6 1 Discontinuación por EA 1 4 § Media geométrica de concentración en el valle de ATV y RAL, disponible para la mayoría de las pacientes, las que estuvieron dentro del rango terapéutico en el curso del estudio HARNESS Van Lunzen J. JAIDS 2016; 71: 538 -43

Estudio HARNESS: switch a ATV/r + RAL § Conclusión – En pacientes virológicamente suprimidos en triple régimen antiretroviral, el switch a ATV/r + RAL resultó en un menor mantenimiento de la supresión viral y mayor incidencia de rebote virológico que en el grupo que recibió ATV/r + TDF/FTC a S 24 y S 48 – Además, los problemas de tolerabilidad y discontinuación de tratamiento ocurrieron mas frecuentemente y la adherencia fue menor con ATV/r + RAL – Este estudio piloto no demostró evidencias sobre la conveniencia del switch a ATV/r + RAL por razones de seguridad y tolerabilidad en pacientes experimentados con supresión virológica HARNESS Van Lunzen J. JAIDS 2016; 71: 538 -43