Suren und Basen M Kresken 1 Suren und

Säuren und Basen M. Kresken 1

Säuren und Basen • Die Begriffe „Säure“ und „Base“ (früher Lauge) sind aus Beobachtungen entstanden: - Zitronen, Essig und saure Milch schmecken sauer, was auf den Gehalt an Citronensäure, Essigsäure bzw. Milchsäure zurückzuführen ist. - Dem gegenüber steht der bittere Geschmack von Seifenlaugen. Da Pflanzenasche durch den hohen K + -Gehalt die Basis für die Laugengewinnung (KOH) war, wurde später der Begriff „Base“ auf die ganze Stoffklasse angewendet. Wässrige Lösungen von Basen reagieren basisch oder alkalisch (arab. al-kaelie = Lauge). M. Kresken 2

Säuren und Basen • Wässrige Lösungen von Säuren und Basen leiten den elektrischen Strom. • Die gelösten Stoffe sind Elektrolyte, d. h. in der Lösung liegen Ionen vor. • Säuren und Basen bilden die Ionen meist erst unter dem Einfluss des Wassers. Der Vorgang wird als Dissoziation bezeichnet. M. Kresken 3
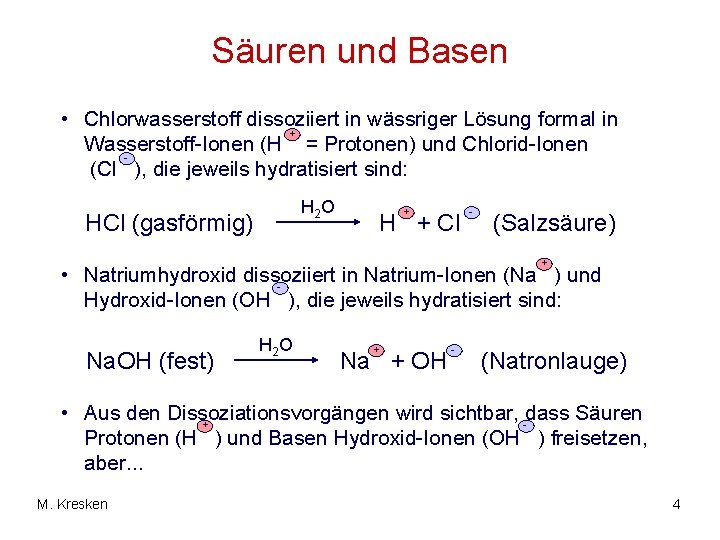
Säuren und Basen • Chlorwasserstoff dissoziiert in wässriger Lösung formal in + Wasserstoff-Ionen (H = Protonen) und Chlorid-Ionen (Cl ), die jeweils hydratisiert sind: H 2 O HCl (gasförmig) + H + Cl - (Salzsäure) + • Natriumhydroxid dissoziiert in Natrium-Ionen (Na ) und Hydroxid-Ionen (OH ), die jeweils hydratisiert sind: Na. OH (fest) H 2 O + Na + OH - (Natronlauge) • Aus den Dissoziationsvorgängen wird sichtbar, -dass Säuren + Protonen (H ) und Basen Hydroxid-Ionen (OH ) freisetzen, aber. . . M. Kresken 4
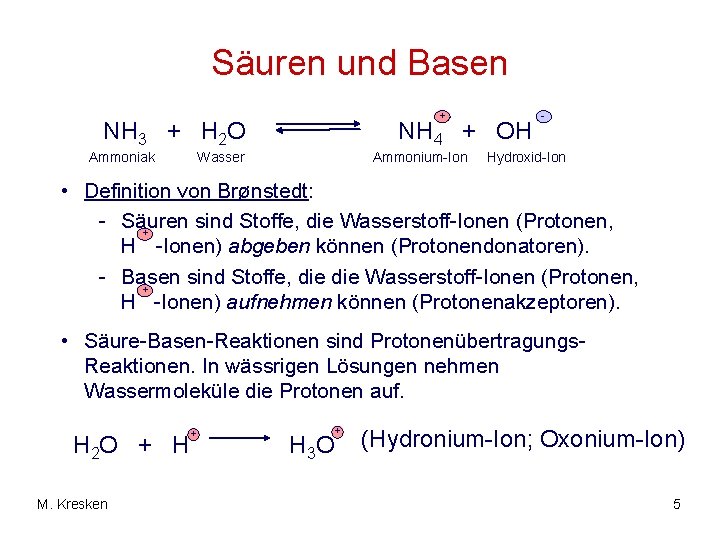
Säuren und Basen + NH 3 + H 2 O Ammoniak NH 4 + OH Wasser Ammonium-Ion - Hydroxid-Ion • Definition von Brønstedt: - Säuren sind Stoffe, die Wasserstoff-Ionen (Protonen, + H -Ionen) abgeben können (Protonendonatoren). - Basen sind Stoffe, die Wasserstoff-Ionen (Protonen, + H -Ionen) aufnehmen können (Protonenakzeptoren). • Säure-Basen-Reaktionen sind Protonenübertragungs. Reaktionen. In wässrigen Lösungen nehmen Wassermoleküle die Protonen auf. H 2 O + H M. Kresken + + H 3 O (Hydronium-Ion; Oxonium-Ion) 5
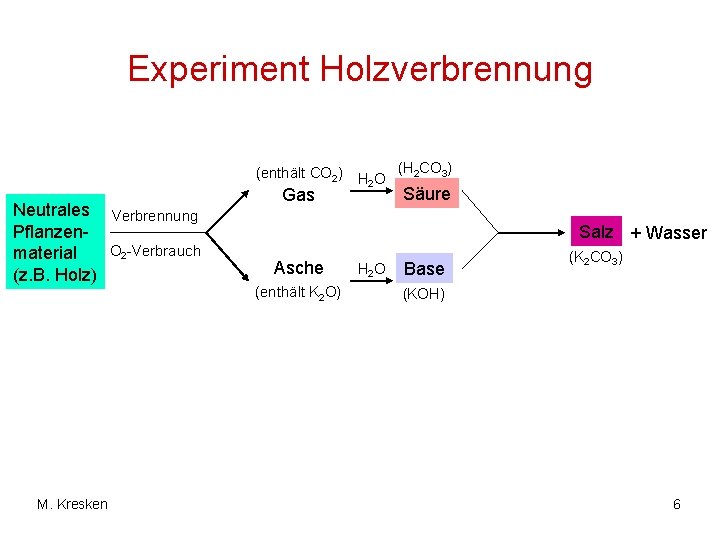
Experiment Holzverbrennung (enthält CO 2) H O (H 2 CO 3) 2 Neutrales Verbrennung Pflanzen. O 2 -Verbrauch material (z. B. Holz) M. Kresken Säure Gas Salz + Wasser Asche (enthält K 2 O) H 2 O Base (K 2 CO 3) (KOH) 6

Wasser • Wasser ist ein Ampholyt. In geringen, aber messbarem Umfang reagiert es mit sich selbst (Eigendissoziation, Autoprotolyse). H 2 O + H 3 O + OH - (H+ + OH–) • Ampholyte können als Säure oder Base reagieren. • Wie Wasser reagiert, hängt vom Reaktionspartner ab. - Reagiert es mit einem Stoff, der eine größere Protonendonatorstärke als es selbst hat, reagiert es als Base. - Gegenüber der Base Ammoniak überwiegt jedoch seine eigene Protonendonatorstärke. Wasser reagiert als Säure. M. Kresken 7

Massenwirkungsgesetz (MWG) • Im Gleichgewichtszustand der Reaktion A + B C + D sind die Gleichgewichtskonzentrationen der beteiligten Stoffe konstant, da Hin- und Rückreaktionen gleich schnell ablaufen. • Das Verhältnis der Konzentrationen der beteiligten Stoffe führt zu einer für die betrachtete Reaktion spezifischen Konstante, der Gleichgewichtskonstanten K, deren Wert von der Temperatur abhängt. M. Kresken 8
![Massenwirkungsgesetz (MWG) K= [C] • [D] [A] • [B] oder Kc = c(C) • Massenwirkungsgesetz (MWG) K= [C] • [D] [A] • [B] oder Kc = c(C) •](http://slidetodoc.com/presentation_image/52e1f907f2d47c55e7c27ae1222fbc91/image-9.jpg)
Massenwirkungsgesetz (MWG) K= [C] • [D] [A] • [B] oder Kc = c(C) • c(D) c(A) • c(B) • C und D sind die Produkte, A und B die Edukte, K die Gleichgewichtskonstante. • Das Produkt der Konzentrationen der Produkte dividiert durch das Produkt der Edukte ist konstant. • Die eckigen Klammern dokumentieren eine Konzentration, (z. B. [A] in mol/L). • Das MWG gibt Auskunft über die Lage eines Gleichgewichtes: - Ein Zahlenwert K > 1 zeigt an, dass die Reaktion auf der Seite der Produkte liegt, die Hinreaktion also überwiegt. - Bei einem Zahlenwert K < 1 überwiegen die Edukte im Gleichgewicht, d. h. die Rückreaktion überwiegt. M. Kresken 9
![Ionenprodukt des Wassers + K = - [H 3 O ] • [OH ] Ionenprodukt des Wassers + K = - [H 3 O ] • [OH ]](http://slidetodoc.com/presentation_image/52e1f907f2d47c55e7c27ae1222fbc91/image-10.jpg)
Ionenprodukt des Wassers + K = - [H 3 O ] • [OH ] [H 2 O]2 • Da Wasser im Überschuss vorliegt, ist seine Konzentration (1 L = 55, 55 mol) bei einer geringen Eigendissoziation praktisch konstant [1 mol Wasser wiegt 18 g; 1 L Wasser wiegt 1. 000 g; 55, 55 mol wiegen 1. 000 g]. + - [H 2 O]2 • K = [H 3 O ] • [OH ] + - Kw = [H 3 O ] • [OH ] Ionenprodukt des Wassers Kw = 1, 0 • 10 -14 mol 2/L 2 + - [H 3 O ] = 1, 0 • 10 -7 mol/L = [OH ] M. Kresken 10

p. H-Wert + • Der p. H-Wert ist der negative Zehnerlogarithmus von [H 3 O ]. + • In reinem Wasser (bei 22°C) ist [H 3 O ] = 10 -7 mol/L, daher ist der p. H-Wert 7. + • Gibt man eine Säure hinzu, wird [H 3 O ] > 1, 0 • 10 -7 mol/L. Entsprechend sinkt der p. H-Wert auf < 7 und man spricht von einer sauren Lösung. M. Kresken p. H, lat. pondus hydrogenii 11

p. OH-Wert • Neben dem p. H-Wert gibt es auch noch den p. OH-Wert. • Der p. OH-Wert ist der negative Zehnerlogarithmus von [OH ]. • In reinem Wasser (bei 22°C) ist [OH ] = 10 -7 mol/L, daher ist der p. OH-Wert 7. • Gibt man eine Base hinzu, wird [OH ] > 1, 0 • 10 -7 mol/L. Entsprechend sinkt der p. OH-Wert auf < 7 und man spricht von einer basischen Lösung. M. Kresken 12
![Ionenprodukt des Wassers + - Kw = [H 3 O ] • [OH ] Ionenprodukt des Wassers + - Kw = [H 3 O ] • [OH ]](http://slidetodoc.com/presentation_image/52e1f907f2d47c55e7c27ae1222fbc91/image-13.jpg)
Ionenprodukt des Wassers + - Kw = [H 3 O ] • [OH ] = 10 -14 mol 2/L 2 p. Kw = p. H + p. OH = 14 + + p. H = -log 10 [H 3 O ] = -lg [H 3 O ] - - p. OH = -log 10 [OH ] = -lg [OH ] M. Kresken 13
![Zusammenhang zwischen p. H-Wert und p. OH-Wert p. H-Wert [H 3 O+] in mol/L Zusammenhang zwischen p. H-Wert und p. OH-Wert p. H-Wert [H 3 O+] in mol/L](http://slidetodoc.com/presentation_image/52e1f907f2d47c55e7c27ae1222fbc91/image-14.jpg)
Zusammenhang zwischen p. H-Wert und p. OH-Wert p. H-Wert [H 3 O+] in mol/L [OH-] in mol/L p. OH-Wert 14 10 -14 100 0 13 10 -1 1 12 10 -2 2 11 10 -3 3 10 10 -4 4 9 10 -5 5 8 10 -6 6 7 10 -7 7 6 10 -8 8 5 10 -9 9 4 10 -10 10 3 10 -11 11 2 10 -12 12 1 10 -13 13 0 10 -14 14

p. H- / p. OH-Wert + • Die Konzentration an Hydronium-Ionen (H 3 O ) oder Hydroxid -Ionen (OH ) lässt sich bei allen verdünnten wässrigen Lösungen als Maß für die Azidität bzw. Basizität einer Lösung verwenden. + • In saurer Lösung überwiegt die Konzentration an H 3 O , in basischer die an OH. • Solange die Lösungen sehr verdünnt sind, gilt das Ionen+ produkt des Wassers (Kw), d. h. , wenn man H 3 O kennt, lässt sich OH berechnen und umgekehrt. Beispiel: OH - = 10 -5 mol/L; p. OH = 5 + [H 3 O ] • 10 -5 = 10 -14 mol 2/L 2; p. H + 5 = 14 + [H 3 O ] = M. Kresken 10 -14 10 -5 = 10 -9 mol/L; p. H = 14 – 5 = 9 15
![p. H- / p. OH-Wert Beispiele: + [H 3 O ] = 10 -6 p. H- / p. OH-Wert Beispiele: + [H 3 O ] = 10 -6](http://slidetodoc.com/presentation_image/52e1f907f2d47c55e7c27ae1222fbc91/image-16.jpg)
p. H- / p. OH-Wert Beispiele: + [H 3 O ] = 10 -6 mol/L; p. H = -lg-6 = 6 + [H 3 O ] = 2 • 10 -7 mol/L; p. H = -lg 2 + -lg 10 -7 = -0, 3 + 7 = 6, 7 + [H 3 O ] = 102 mol/L; p. H = -lg 102 = -2 M. Kresken 16
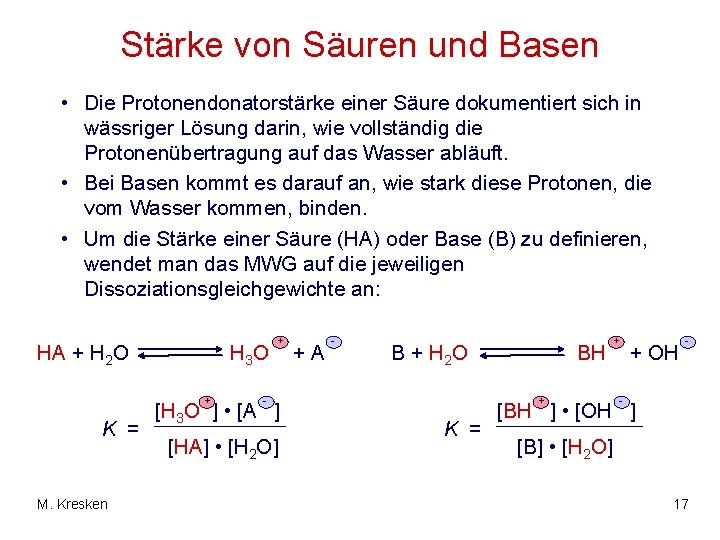
Stärke von Säuren und Basen • Die Protonendonatorstärke einer Säure dokumentiert sich in wässriger Lösung darin, wie vollständig die Protonenübertragung auf das Wasser abläuft. • Bei Basen kommt es darauf an, wie stark diese Protonen, die vom Wasser kommen, binden. • Um die Stärke einer Säure (HA) oder Base (B) zu definieren, wendet man das MWG auf die jeweiligen Dissoziationsgleichgewichte an: HA + H 2 O H 3 O + K = M. Kresken + +A - B + H 2 O - [H 3 O ] • [A ] [HA] • [H 2 O] BH + K = + + OH - - [BH ] • [OH ] [B] • [H 2 O] 17

Stärke von Säuren und Basen • Da sich die Konzentration an H 2 O durch die Dissoziation in verdünnter Lösung kaum verändert, wird H 2 O in die Gleichgewichtskonstante einbezogen. • Man erhält die Säurekonstante Ks bzw. die Basenkonstante Kb in mol/L. Die Werte sind temperaturabhängig. + Ks = M. Kresken - [H 3 O ] • [A ] [HA] + Kb = - [BH ] • [OH ] [B] 18

p. Ks-Wert / p. Kb-Wert • Findet man für die Säurekonstante (Ks) einen großen Wert, so liegt das Dissoziationsgleichgewicht weit rechts, d. h. die Säure ist stark. • Kleine Säurekonstanten (Ks-Werte) deuten auf eine schwache Säure hin. • Bildet man den negativen dekadischen Logarithmus der Ks- und Kb-Werte, so ergibt sich: p. Ks = – lg Ks p. Kb = – lg Kb • Der p. Ks einer Säure und der p. Kb-Wert ihrer konjugierten Base hängen in wässriger Lösung wie folgt zusammen: p. Ks + p. Kb = 14 • Der p. Ks- bzw. p. Kb-Wert ist das übliche Maß für die Stärke von Säuren und Basen. Kleine oder negative p. Ks-Werte zeigen an, dass die Säure stark ist, große Werte, dass sie schwach ist. M. Kresken 19
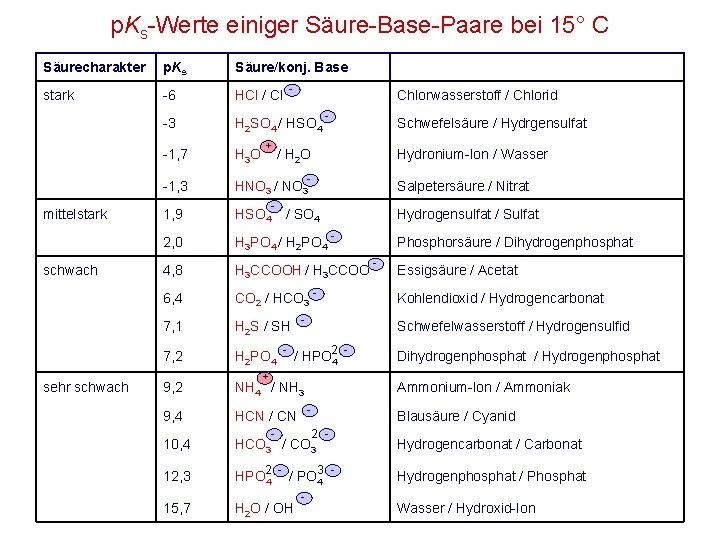
p. Ks-Werte einiger Säure-Base-Paare bei 15° C Säurecharakter p. Ks Säure/konj. Base stark -6 HCl / Cl - -3 H 2 SO 4 / HSO 4 -1, 7 H 3 O -1, 3 HNO 3 / NO 3 1, 9 HSO 4 2, 0 H 3 PO 4 / H 2 PO 4 4, 8 H 3 CCOOH / H 3 CCOO 6, 4 CO 2 / HCO 3 - 7, 1 H 2 S / SH 7, 2 H 2 PO 4 9, 2 NH 4 / NH 3 9, 4 HCN / CN 10, 4 HCO 3 / CO 3 12, 3 HPO 4 15, 7 H 2 O / OH mittelstark schwach sehr schwach + Chlorwasserstoff / Chlorid - Schwefelsäure / Hydrgensulfat / H 2 O Hydronium-Ion / Wasser - - Salpetersäure / Nitrat / SO 4 - Hydrogensulfat / Sulfat - 2 - / HPO 4 Dihydrogenphosphat / Hydrogenphosphat Ammonium-Ion / Ammoniak - Blausäure / Cyanid 2 3 - / PO 4 - Essigsäure / Acetat Schwefelwasserstoff / Hydrogensulfid + 2 - - Kohlendioxid / Hydrogencarbonat - - Phosphorsäure / Dihydrogenphosphat Hydrogencarbonat / Carbonat Hydrogenphosphat / Phosphat Wasser / Hydroxid-Ion

p. H-Werte im Organismus • Die p. H-Werte in Zellen und in der Extrazellulärflüssigkeit werden in engen Grenzen konstant gehalten. • Im Blut schwankt der p. H-Wert normalerweise nur zwischen 7, 35 + und 7, 45. Dies entspricht einer maximalen Änderung der H 3 O Ionen (H+-Ionen) um etwa 30%. • Der p. H-Wert des Cytoplasmas ist mit 7, 0 bis 7, 3 etwas niedriger als der des Blutes. • In Lysosomen (p. H 4, 5 - 5, 5) ist die H 3 O + -Konzentration einige hundertmal höher als im Cytoplasma. • Extreme Werte findet man im Magen (p. H 0, 8 - 2) und im Dünndarm (p. H > 8). • Da die Nieren Säuren oder Basen ausscheiden können, schwankt der p. H-Wert des Urins besonders stark (p. H 4, 8 bis 7, 5). M. Kresken 21

Puffer • Betrag und Konstanz des p. H-Wertes im Zytoplasma einer Zelle oder in bestimmten Körperflüssigkeiten wie z. B. dem Blut sind lebenswichtig. • Der p. H-Wert beeinflusst z. B. die Aktivität von Enzymen, an deren Aufbau Aminosäuren mit sauren und basischen Gruppen beteiligt sind. • Im Stoffwechsel laufen viele Reaktionen ab, bei denen Protonen freigesetzt oder verbraucht werden. • Dies birgt die Gefahr in sich, dass p. H-Änderungen im jeweiligen Milieu eintreten. • Zellflüssigkeiten müssen daher in der Lage sein, stoffwechselbedingte „p. H-Stöße“ abzufangen (= zu puffern). M. Kresken 22

Pufferlösungen • Pufferlösungen enthalten Stoffe (Puffersubstanzen), die dafür sorgen, dass sich bei Zugabe von Säuren oder Basen der p. HWert einer Lösung nur wenig ändert. • Geeignete Puffersubstanzen sind: - Das Gemisch aus einer schwachen Säure und der konjugierten Base dieser Säure (z. B. Essigsäure/Natriumacetat). - Das Gemisch aus einer schwachen Base und der konjugierten Säure dieser Base (z. B. Ammoniak/Ammoniumchlorid) M. Kresken 23

Acetat-Puffer • Beispiel: Ein äquimolarer 0, 2 M Acetat-Puffer liegt vor, wenn in 1 L einer wässrigen Pufferlösung 0, 1 mol Essigsäure und 0, 1 mol Natriumacetat enthalten sind. • Was passiert, wenn diese Lösung „p. H-Stößen“ ausgesetzt wird. - Zugabe von Säure: H 3 O + + H 3 CCOO - H 3 CCOOH + H 2 O - Zugabe von Base: OH - + H 3 CCOOH H 3 CCOO - + H 2 O • In beiden Fällen entsteht neutrales Wasser, daneben entweder Essigsäure oder deren Anion, die beide bereits schon in der Lösung vorhanden sind. • Die Zunahme der Konzentration des einen oder anderen Bestandteils in der Pufferlösung wirkt sich auf den p. H-Wert jedoch nur wenig aus. M. Kresken 24
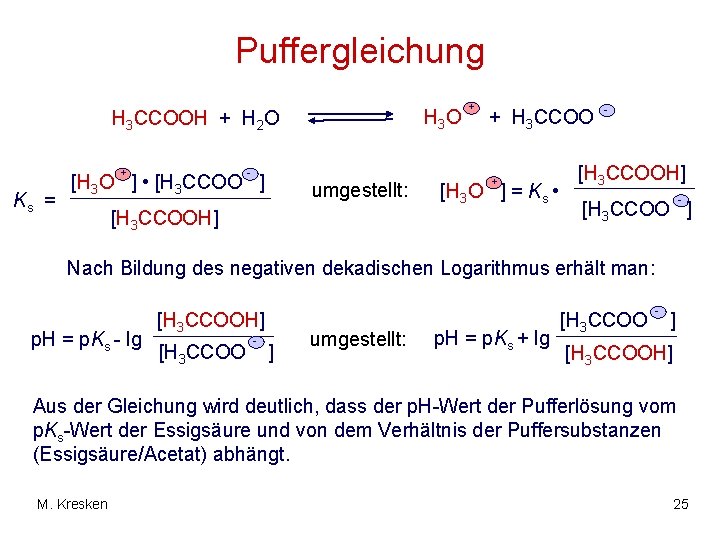
Puffergleichung H 3 O H 3 CCOOH + H 2 O + Ks = - [H 3 O ] • [H 3 CCOO ] umgestellt: + + H 3 CCOO + [H 3 O ] = Ks • [H 3 CCOOH] - [H 3 CCOO ] Nach Bildung des negativen dekadischen Logarithmus erhält man: p. H = p. Ks - lg [H 3 CCOOH] [H 3 CCOO - ] umgestellt: p. H = p. Ks + lg [H 3 CCOO - ] [H 3 CCOOH] Aus der Gleichung wird deutlich, dass der p. H-Wert der Pufferlösung vom p. Ks-Wert der Essigsäure und von dem Verhältnis der Puffersubstanzen (Essigsäure/Acetat) abhängt. M. Kresken 25
![Puffersysteme im Blut p. H = 6, 4 + lg [HCO 3 - ] Puffersysteme im Blut p. H = 6, 4 + lg [HCO 3 - ]](http://slidetodoc.com/presentation_image/52e1f907f2d47c55e7c27ae1222fbc91/image-26.jpg)
Puffersysteme im Blut p. H = 6, 4 + lg [HCO 3 - ] [CO 2] • Der Kohlensäure-Puffer ist daran beteiligt, den p. H-Wert bei 7, 4 konstant zu halten. • Bei Körpertemperatur (37°C) beträgt der p. Ks-Wert 6, 1. • Um den Blut-p. H-Wert (7, 4) zu erreichen, beträgt das Konzentrationsverhältnis der Puffersubstanzen: p. H = 6, 1 + lg H 3 O M. Kresken + - + HCO 3 20 1 = 7, 4 CO 2 + 2 H 2 O 26

Puffersysteme im Blut • Kohlensäure-Puffer • Phosphat-Puffer • Protein-Puffer M. Kresken 27
- Slides: 27