SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISIRADIKAL REAKSI

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER
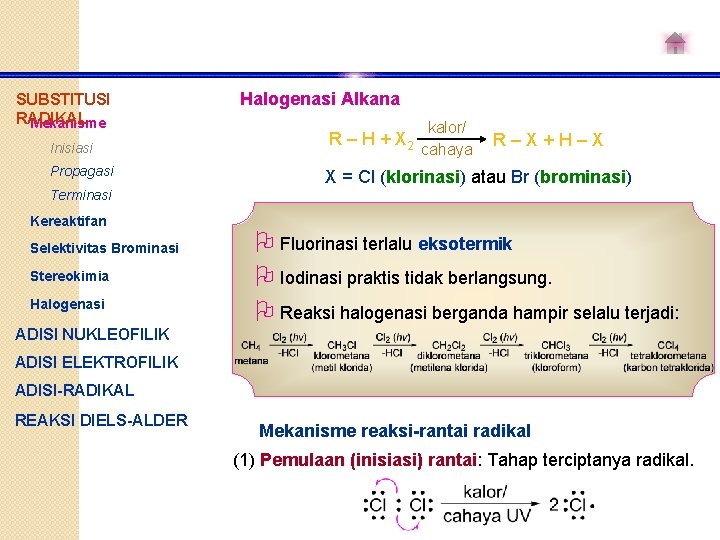
SUBSTITUSI RADIKAL Mekanisme Inisiasi Propagasi Halogenasi Alkana R – H + X 2 kalor/ cahaya R–X+H–X X = Cl (klorinasi) atau Br (brominasi) Terminasi Kereaktifan Selektivitas Brominasi Stereokimia Halogenasi Fluorinasi terlalu eksotermik Iodinasi praktis tidak berlangsung. Reaksi halogenasi berganda hampir selalu terjadi: ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER Mekanisme reaksi-rantai radikal (1) Pemulaan (inisiasi) rantai: Tahap terciptanya radikal.
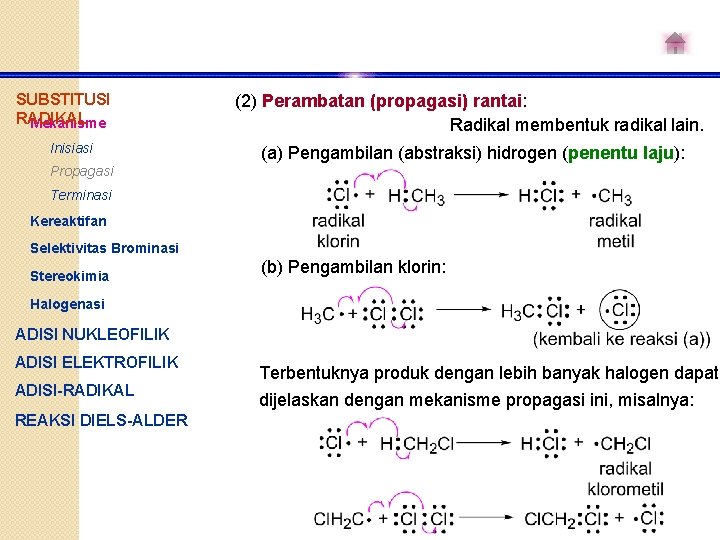
SUBSTITUSI RADIKAL Mekanisme Inisiasi (2) Perambatan (propagasi) rantai: Radikal membentuk radikal lain. (a) Pengambilan (abstraksi) hidrogen (penentu laju): Propagasi Terminasi Kereaktifan Selektivitas Brominasi Stereokimia (b) Pengambilan klorin: Halogenasi ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER Terbentuknya produk dengan lebih banyak halogen dapat dijelaskan dengan mekanisme propagasi ini, misalnya:

SUBSTITUSI RADIKAL Mekanisme (3) Penamatan (terminasi) rantai: Tahap hilangnya radikal bebas. Inisiasi Propagasi Terminasi reaksi kopling Kereaktifan Selektivitas Brominasi Stereokimia Halogenasi ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER (jarang terjadi)
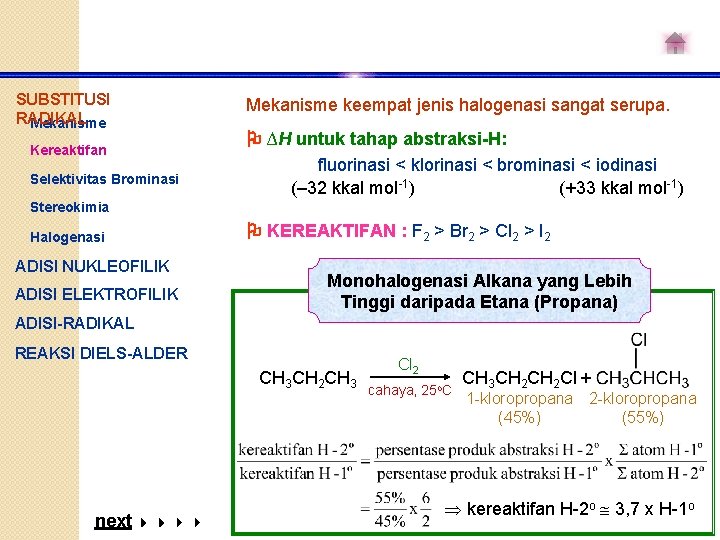
SUBSTITUSI RADIKAL Mekanisme Kereaktifan Selektivitas Brominasi Mekanisme keempat jenis halogenasi sangat serupa. ∆H untuk tahap abstraksi-H: fluorinasi < klorinasi < brominasi < iodinasi (– 32 kkal mol-1) (+33 kkal mol-1) Stereokimia Halogenasi ADISI NUKLEOFILIK ADISI ELEKTROFILIK KEREAKTIFAN : F 2 > Br 2 > Cl 2 > I 2 Monohalogenasi Alkana yang Lebih Tinggi daripada Etana (Propana) ADISI-RADIKAL REAKSI DIELS-ALDER CH 3 CH 2 CH 3 next Cl 2 cahaya, 25 o. C CH 3 CH 2 Cl + 1 -kloropropana 2 -kloropropana (45%) (55%) kereaktifan H-2 o 3, 7 x H-1 o
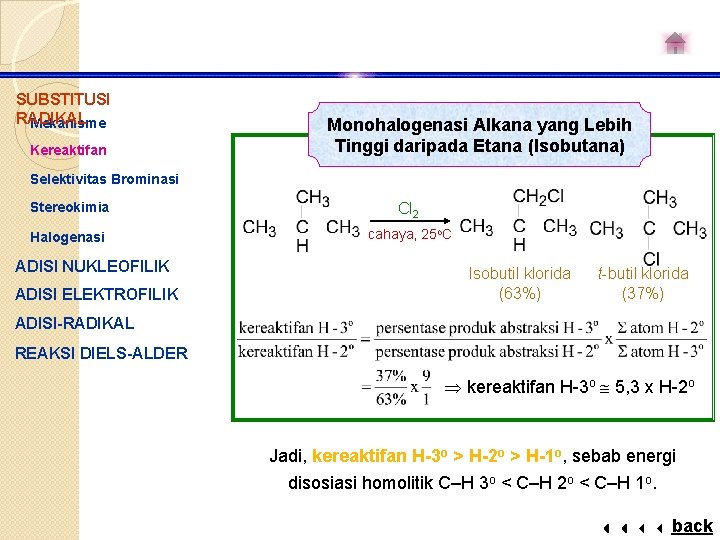
SUBSTITUSI RADIKAL Mekanisme Kereaktifan Monohalogenasi Alkana yang Lebih Tinggi daripada Etana (Isobutana) Selektivitas Brominasi Stereokimia Cl 2 Halogenasi cahaya, 25 o. C ADISI NUKLEOFILIK ADISI ELEKTROFILIK Isobutil klorida (63%) t-butil klorida (37%) ADISI-RADIKAL REAKSI DIELS-ALDER kereaktifan H-3 o 5, 3 x H-2 o Jadi, kereaktifan H-3 o > H-2 o > H-1 o, sebab energi disosiasi homolitik C–H 3 o < C–H 2 o < C–H 1 o. back

SUBSTITUSI RADIKAL Mekanisme Kereaktifan Selektivitas Brominasi Stereokimia Meskipun bromin tidak sereaktif klorin terhadap alkana, ia lebih selektif memilih tapak serangan saat bereaksi. Br 2 cahaya, 127 o. C Halogenasi ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER (sangat sedikit) (> 99%)

SUBSTITUSI RADIKAL Mekanisme Kereaktifan Stereokimia Selektivitas Brominasi Radikal bebas berhibridisasi sp 2 dengan orbital p memuat elektron yang tidak berpasangan Stereokimia n-pentana 2 -kloropentana Halogenasi serangan dari atas peluang sama besar ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER serangan dari bawah
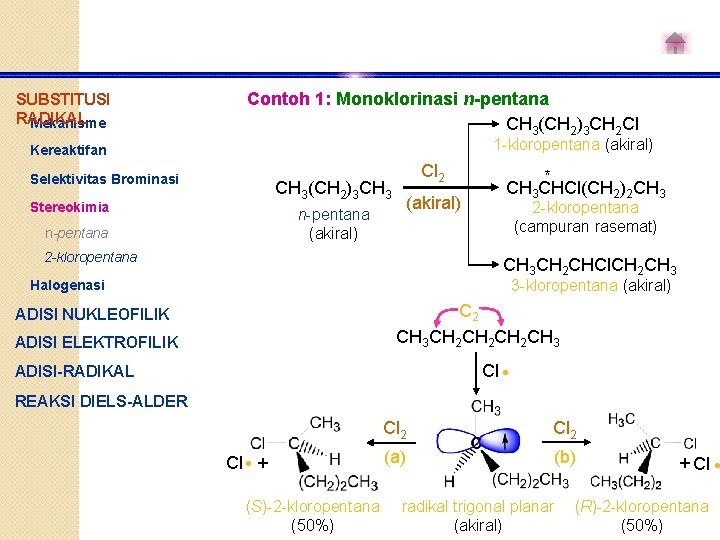
SUBSTITUSI RADIKAL Mekanisme Contoh 1: Monoklorinasi n-pentana CH 3(CH 2)3 CH 2 Cl 1 -kloropentana (akiral) Kereaktifan Selektivitas Brominasi Cl 2 CH 3(CH 2)3 CH 3 Stereokimia (akiral) n-pentana 2 -kloropentana * CH 3 CHCl(CH 2)2 CH 3 2 -kloropentana (campuran rasemat) CH 3 CH 2 CHCl. CH 2 CH 3 3 -kloropentana (akiral) Halogenasi C 2 CH 3 CH 2 CH 2 CH 3 ADISI NUKLEOFILIK ADISI ELEKTROFILIK Cl ADISI-RADIKAL REAKSI DIELS-ALDER Cl + (S)-2 -kloropentana (50%) Cl 2 (a) (b) radikal trigonal planar (akiral) + Cl (R)-2 -kloropentana (50%)

SUBSTITUSI RADIKAL Mekanisme Contoh 2: Monoklorinasi (S)-2 -kloropentana pada C-3 Kereaktifan Selektivitas Brominasi Stereokimia Cl 2 * * + * * n-pentana 2 -kloropentana Halogenasi ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER (2 S, 3 R)-dikloropentana (2 S, 3 S) (serangan kanan) (serangan kiri)
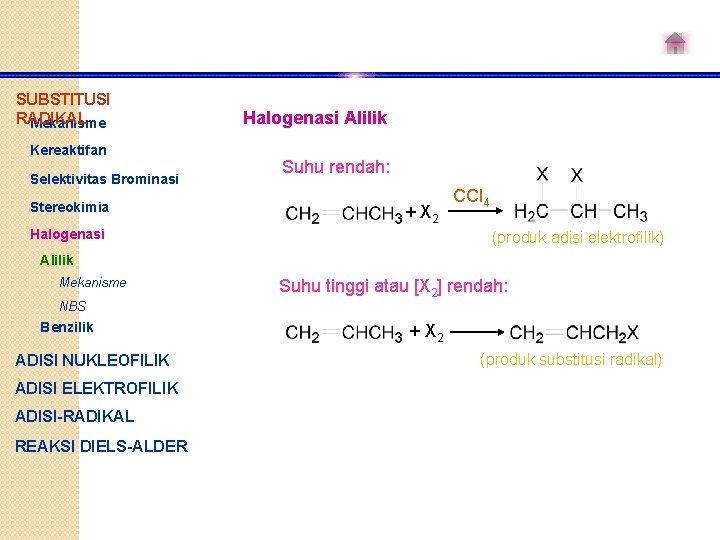
SUBSTITUSI RADIKAL Mekanisme Kereaktifan Selektivitas Brominasi Stereokimia Halogenasi Alilik Suhu rendah: + X 2 Halogenasi CCl 4 (produk adisi elektrofilik) Alilik Mekanisme Suhu tinggi atau [X 2] rendah: NBS Benzilik ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER + X 2 (produk substitusi radikal)

SUBSTITUSI RADIKAL Mekanisme Kereaktifan Selektivitas Brominasi (1) Pemulaan-rantai: (2) Perambatan-rantai: (a) Stereokimia Halogenasi Stabilisasi resonansi energi disosiasi homolitik C-H alil < C-H 3 o Alilik Mekanisme NBS Benzilik (b) ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER (3) Penamatan-rantai:

SUBSTITUSI RADIKAL Mekanisme Kereaktifan Propena juga melakukan brominasi alilik jika diperlakukan dengan N-bromosuksinimida (NBS) dalam CCl 4 dengan adanya peroksida atau cahaya. Selektivitas Brominasi Stereokimia Halogenasi Alilik Mekanisme NBS Benzilik ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER 1. Reaksi dimulai dengan pembentukan sejumlah kecil Br yang mungkin terbentuk dari disosiasi ikatan N–Br. 2. Perambatan rantai: (a) CH 2=CHCH 3 + Br CH 2=CHCH 2 + HBr (b) CH 2=CHCH 2 + Br 2 CH 2=CHCH 2 Br + Br 3. Pembentukan Br 2:
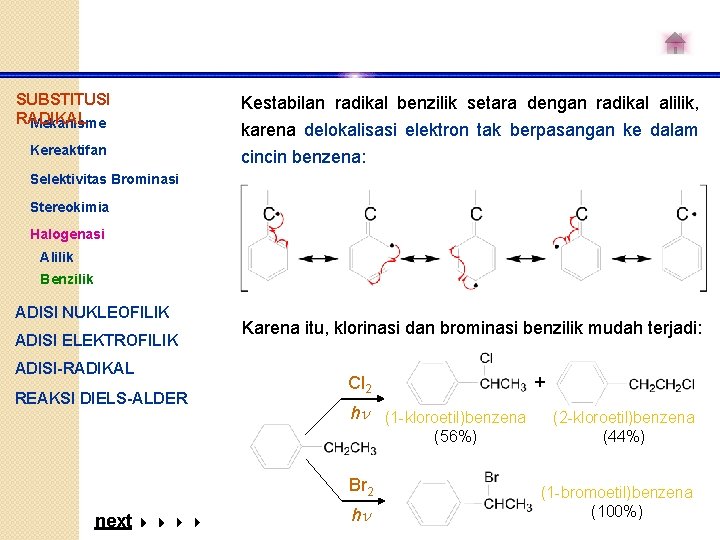
SUBSTITUSI RADIKAL Mekanisme Kereaktifan Kestabilan radikal benzilik setara dengan radikal alilik, karena delokalisasi elektron tak berpasangan ke dalam cincin benzena: Selektivitas Brominasi Stereokimia Halogenasi Alilik Benzilik ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER Karena itu, klorinasi dan brominasi benzilik mudah terjadi: + Cl 2 h (1 -kloroetil)benzena (56%) Br 2 next h (2 -kloroetil)benzena (44%) (1 -bromoetil)benzena (100%)

SUBSTITUSI RADIKAL Mekanisme Pereaksi NBS juga berguna untuk brominasi benzilik: Kereaktifan + NBS Selektivitas Brominasi Stereokimia Halogenasi Alilik 3 -bromo-1 -fenilpropana CCl 4 pemula 1, 3 -dibromo-1 -fenilpropana (~100%) Benzilik ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER back
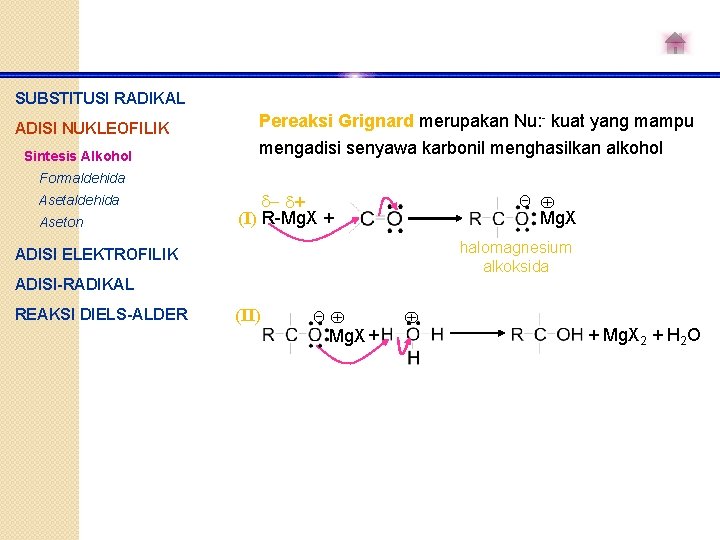
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Sintesis Alkohol Pereaksi Grignard merupakan Nu: - kuat yang mampu mengadisi senyawa karbonil menghasilkan alkohol Formaldehida Aseton - + (I) R-Mg. X + Θ Mg. X halomagnesium alkoksida ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER (II) Θ Mg. X + + Mg. X 2 + H 2 O

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK 1. Formaldehida Alkohol 1 o Sintesis Alkohol Formaldehida Aseton ADISI ELEKTROFILIK + formaldehida Θ Mg. Br ADISI-RADIKAL REAKSI DIELS-ALDER benzil alkohol (1 o) (90%)
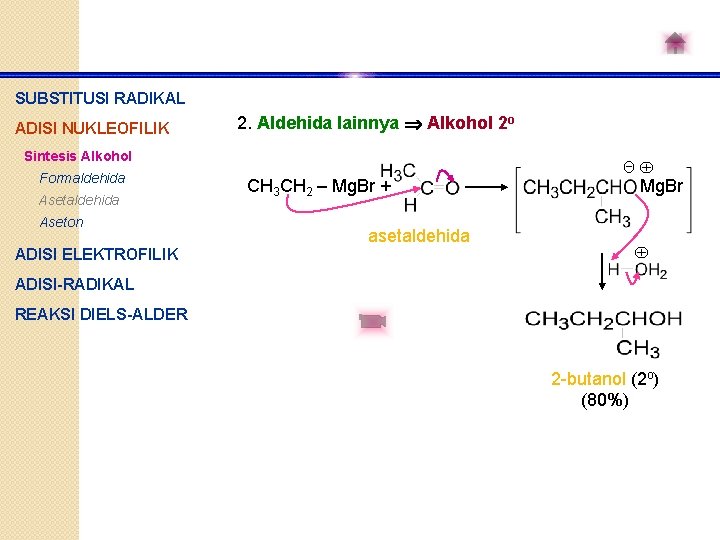
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK 2. Aldehida lainnya Alkohol 2 o Sintesis Alkohol Formaldehida Aseton ADISI ELEKTROFILIK CH 3 CH 2 – Mg. Br + asetaldehida Θ Mg. Br ADISI-RADIKAL REAKSI DIELS-ALDER 2 -butanol (2 o) (80%)
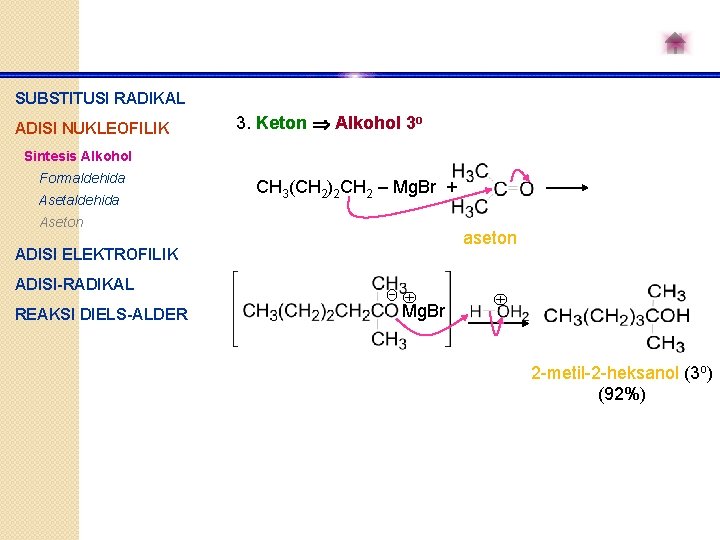
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK 3. Keton Alkohol 3 o Sintesis Alkohol Formaldehida Asetaldehida CH 3(CH 2)2 CH 2 – Mg. Br + Aseton aseton ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER Θ Mg. Br 2 -metil-2 -heksanol (3 o) (92%)

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Ikatan ADISI ELEKTROFILIK Alkena Alkuna ADISI-RADIKAL C C C C REAKSI DIELS-ALDER Elektron rentan terhadap serangan elektrofili (E ) “kation atau spesi netral tuna-elektron“ ADISI ELEKTROFILIK
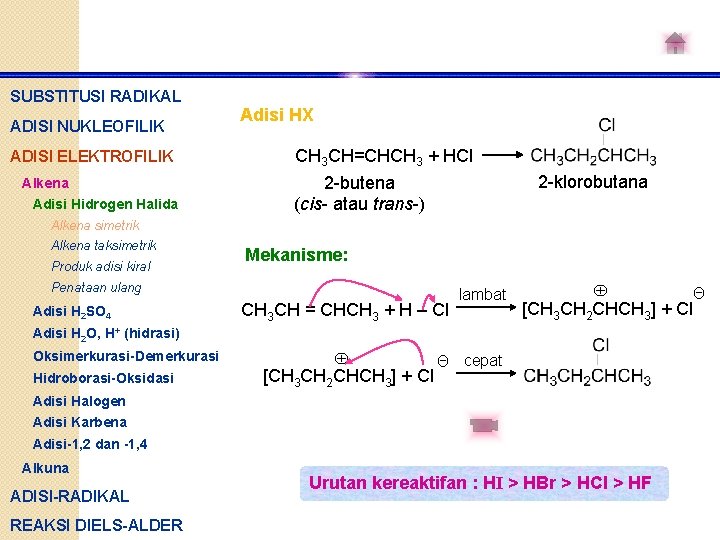
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Alkena simetrik Alkena taksimetrik Produk adisi kiral Adisi HX CH 3 CH=CHCH 3 + HCl 2 -butena (cis- atau trans-) Mekanisme: Penataan ulang Adisi H 2 SO 4 2 -klorobutana CH 3 CH = CHCH 3 + H – Cl lambat [CH 3 CH 2 CHCH 3] + Cl Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi [CH 3 CH 2 CHCH 3] + Cl Θ cepat Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER Urutan kereaktifan : HI > HBr > HCl > HF Θ

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Aturan Markovnikov (1870): Dalam adisi HX pada alkena, atom-H mengadisi ikatan rangkap pada atom-C yang memiliki lebih banyak atom-H. Adisi Hidrogen Halida Alkena simetrik Alkena taksimetrik Aturan Markovnikov Perluasan Markovnikov Produk adisi kiral Penataan ulang Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna CH 2 = CHCH 3 + H – Cl 2 -kloropropana karbon dengan lebih banyak atom H (produk adisi Markovnikov) Adisi Markovnikov reaksi regioselektif Ketika suatu reaksi dapat menghasilkan dua atau lebih isomer konstitusional secara nyata hanya dihasilkan salah satunya (atau salah satu produk dominan) ADISI-RADIKAL REAKSI DIELS-ALDER next
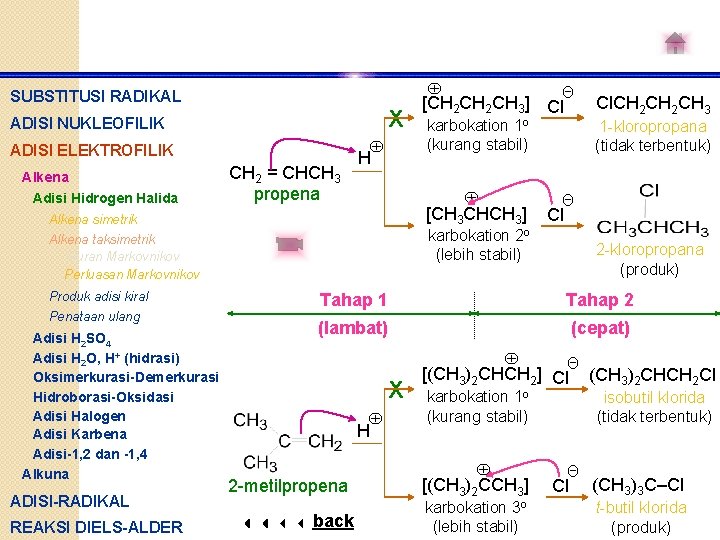
SUBSTITUSI RADIKAL X ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida CH 2 = CHCH 3 propena H Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER karbokation 1 o (kurang stabil) [CH 3 CHCH 3] Alkena simetrik Alkena taksimetrik Aturan Markovnikov Perluasan Markovnikov Produk adisi kiral Penataan ulang Θ [CH 2 CH 3] Cl Cl. CH 2 CH 3 1 -kloropropana (tidak terbentuk) Θ Cl karbokation 2 o (lebih stabil) 2 -kloropropana (produk) Tahap 1 Tahap 2 (lambat) (cepat) X H 2 -metilpropena back Θ [(CH 3)2 CHCH 2] Cl karbokation 1 o (kurang stabil) [(CH 3)2 CCH 3] karbokation 3 o (lebih stabil) (CH 3)2 CHCH 2 Cl isobutil klorida (tidak terbentuk) Θ Cl (CH 3)3 C–Cl t-butil klorida (produk)

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Perluasan aturan Markovnikov: ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Alkena simetrik Alkena taksimetrik Aturan Markovnikov Perluasan Markovnikov Dalam adisi ionik suatu pereaksi taksimetrik pada ikatan rangkap, bagian positif dari pereaksi itu akan melekatkan diri pada atom karbon dari ikatan rangkap sedemikian rupa sehingga dihasilkan karbokation yang lebih stabil sebagai zat antara. Produk adisi kiral Penataan ulang Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER Contoh: Θ Cl + + I – Cl pereaksi Wijs (elektronegativitas I < Cl) karbokation 3 o (lebih stabil) 2 -kloro-1 -iodo 2 -metilpropana

SUBSTITUSI RADIKAL Produk-adisi (adduct) kiral ADISI NUKLEOFILIK Cl ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Alkena simetrik Alkena taksimetrik CH 2 = CHCH 2 CH 3 Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) H 1 -butena Θ Produk adisi kiral Penataan ulang Θ Cl serangan atas (R)-2 -klorobutana (50%) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER serangan bawah (S)-2 -klorobutana (50%) (CAMPURAN RASEMAT)
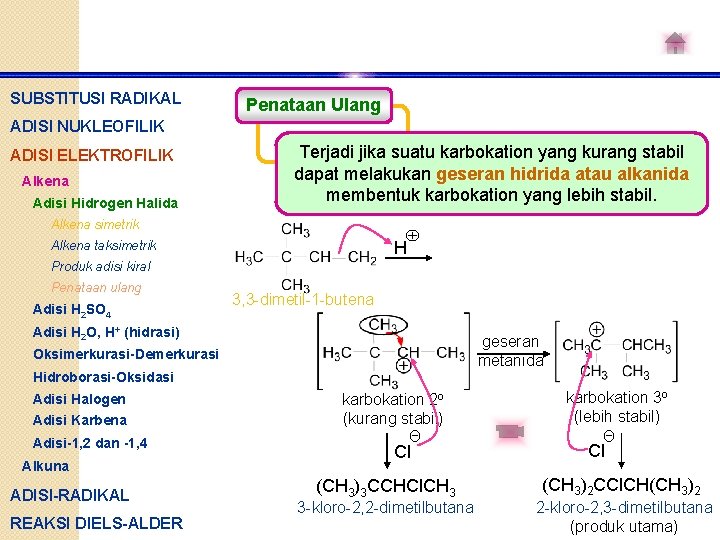
SUBSTITUSI RADIKAL Penataan Ulang ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Terjadi jika suatu karbokation yang kurang stabil dapat melakukan geseran hidrida atau alkanida membentuk karbokation yang lebih stabil. Alkena simetrik H Alkena taksimetrik Produk adisi kiral Penataan ulang Adisi H 2 SO 4 3, 3 -dimetil-1 -butena Adisi H 2 O, H+ (hidrasi) geseran metanida Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER karbokation 2 o (kurang stabil) Θ Cl (CH 3)3 CCHCl. CH 3 3 -kloro-2, 2 -dimetilbutana karbokation 3 o (lebih stabil) Θ Cl (CH 3)2 CCl. CH(CH 3)2 2 -kloro-2, 3 -dimetilbutana (produk utama)
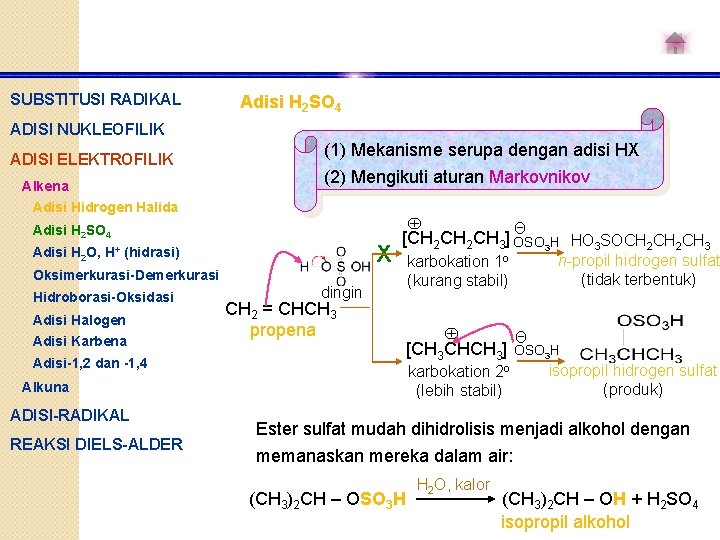
SUBSTITUSI RADIKAL Adisi H 2 SO 4 ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena (1) Mekanisme serupa dengan adisi HX (2) Mengikuti aturan Markovnikov Adisi Hidrogen Halida Adisi H 2 SO 4 X Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena dingin CH 2 = CHCH 3 propena Adisi-1, 2 dan -1, 4 REAKSI DIELS-ALDER n-propil hidrogen sulfat (tidak terbentuk) karbokation 1 o (kurang stabil) [CH 3 CHCH 3] karbokation 2 o (lebih stabil) Alkuna ADISI-RADIKAL Θ [CH 2 CH 3] OSO 3 H HO 3 SOCH 2 CH 3 Θ OSO 3 H isopropil hidrogen sulfat (produk) Ester sulfat mudah dihidrolisis menjadi alkohol dengan memanaskan mereka dalam air: (CH 3)2 CH – OSO 3 H H 2 O, kalor (CH 3)2 CH – OH + H 2 SO 4 isopropil alkohol

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Mekanisme reaksi Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi H 2 O dengan Katalis H+ (1) Mekanisme dan kondisi reaksinya berkebalikan dengan dehidrasi alkohol intramolekuler: umumnya (a) Dehidrasi: asam pekat, suhu tinggi H 2 SO 4/H 3 PO 4 (b) Hidrasi: asam encer, suhu rendah Adisi Halogen Adisi Karbena (2) Mengikuti aturan Markovnikov. Adisi-1, 2 dan -1, 4 (3) Penataan ulang, polimerisasi, serta rendemen yang rendah membuat reaksi ini kurang disukai untuk sintesis alkohol. Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER
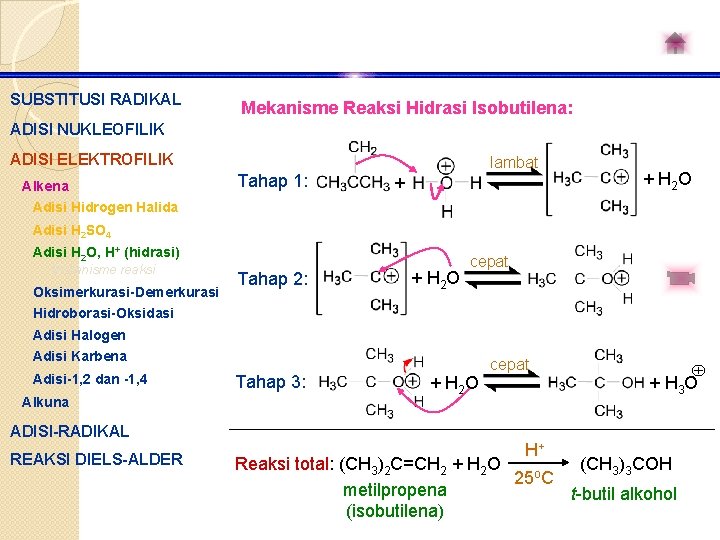
SUBSTITUSI RADIKAL Mekanisme Reaksi Hidrasi Isobutilena: ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Tahap 1: lambat + + H 2 O Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Mekanisme reaksi Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Tahap 2: + H 2 O cepat Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna Tahap 3: + H 2 O cepat + H 3 O ADISI-RADIKAL REAKSI DIELS-ALDER H+ Reaksi total: (CH 3)2 C=CH 2 + H 2 O (CH 3)3 COH 25 o. C metilpropena t-butil alkohol (isobutilena)

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Contoh reaksi Mekanisme reaksi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER Oksimerkurasi-Demerkurasi (1) Metode sintesis alkohol dari alkena dengan rendemen tinggi dan tanpa penataan ulang, yang terdiri atas: (a) Hidrasi alkena dengan merkuri asetat dalam sistem THF-air (Oksimerkurasi). (b) Reduksi dengan Na. BH 4 pada senyawa (hidroksialkil) merkuri yang terbentuk (Demerkurasi). (2) Mekanisme oksimerkurasi: adisi Markovnikov via zat antara karbokation bertitian-merkuri, maka tidak terjadi penataan-ulang. (3) Mekanisme demerkurasi belum sepenuhnya dipahami (diduga melibatkan radikal).
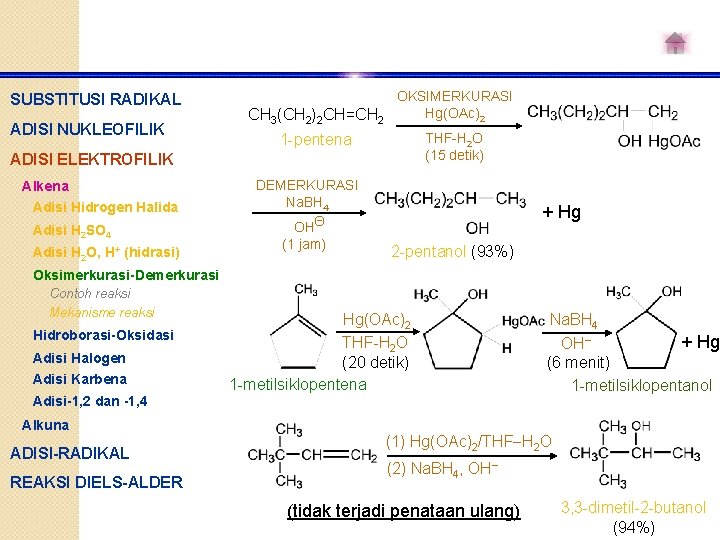
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK CH 3(CH 2)2 CH=CH 2 OKSIMERKURASI Hg(OAc)2 1 -pentena THF-H 2 O (15 detik) ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) DEMERKURASI Na. BH 4 OHΘ (1 jam) + Hg 2 -pentanol (93%) Oksimerkurasi-Demerkurasi Contoh reaksi Mekanisme reaksi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Hg(OAc)2 THF-H 2 O (20 detik) 1 -metilsiklopentena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER Na. BH 4 + Hg OH(6 menit) 1 -metilsiklopentanol (1) Hg(OAc)2/THF-H 2 O (2) Na. BH 4, OH- (tidak terjadi penataan ulang) 3, 3 -dimetil-2 -butanol (94%)
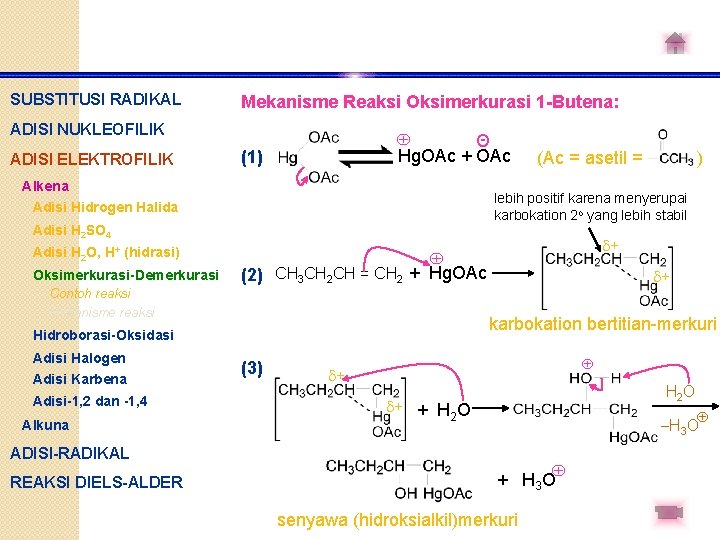
SUBSTITUSI RADIKAL Mekanisme Reaksi Oksimerkurasi 1 -Butena: ADISI NUKLEOFILIK ADISI ELEKTROFILIK Θ Hg. OAc + OAc (1) Alkena Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) (2) CH 3 CH 2 CH = CH 2 + Hg. OAc Alkuna + karbokation bertitian-merkuri Hidroborasi-Oksidasi Adisi-1, 2 dan -1, 4 + Contoh reaksi Mekanisme reaksi Adisi Halogen Adisi Karbena (3) + H 2 O + + H O 2 -H 3 O ADISI-RADIKAL REAKSI DIELS-ALDER ) lebih positif karena menyerupai karbokation 2 o yang lebih stabil Adisi Hidrogen Halida Oksimerkurasi-Demerkurasi (Ac = asetil = + H 3 O senyawa (hidroksialkil)merkuri

SUBSTITUSI RADIKAL Hidroborasi-Oksidasi ADISI NUKLEOFILIK (1) Metode sintesis alkohol dari alkena dengan rendemen tinggi dan tanpa penataan ulang, yang terdiri atas: (a) Adisi borana dalam THF pada alkena (Hidroborasi). (b) Oksidasi dan hidrolisis-basa pada zat antara organoboron dengan H 2 O 2. ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Mekanisme hidroborasi Mekanisme oksidasi Contoh reaksi lainnya Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER (2) Mekanisme hidroborasi: adisi anti-Markovnikov yang bersifat stereospesifik (adisi sin). (3) Mekanisme oksidasi: retensi konfigurasi. Berbeda dari adisi H 2 SO 4 + hidrolisis, adisi H 2 O terkatalisisasam, atau oksimerkurasi-demerkurasi, hidroborasi-oksidasi menghasilkan alkohol anti-Markovnikov sehingga berguna untuk sintesis alkohol 1 o. Contohnya CH 3(CH 2)3 CH = CH 2 1 -heksena (1) THF: BH 3 (2) H 2 O 2, OH Θ CH 3(CH 2)3 CH 2 OH 1 -heksanol (90%)
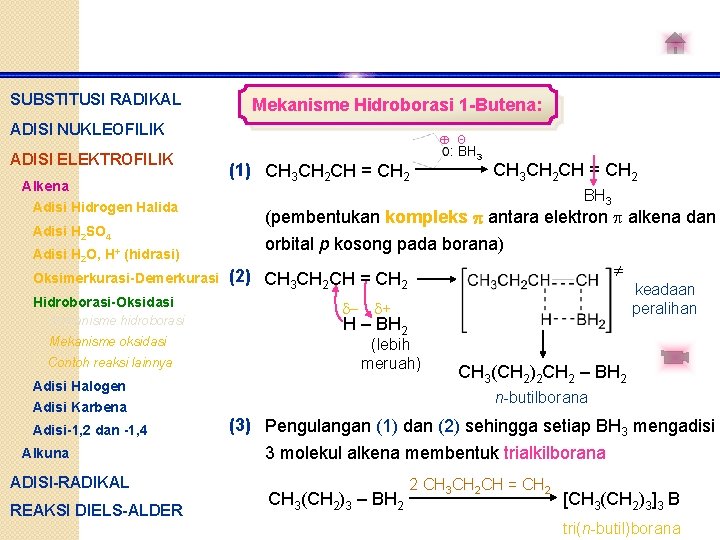
SUBSTITUSI RADIKAL Mekanisme Hidroborasi 1 -Butena: ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Mekanisme hidroborasi Mekanisme oksidasi Contoh reaksi lainnya Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER Θ (1) CH 3 CH 2 CH = CH 2 : BH 3 CH 3 CH 2 CH = CH 2 BH 3 (pembentukan kompleks antara elektron alkena dan orbital p kosong pada borana) (2) CH 3 CH 2 CH = CH 2 keadaan peralihan - + H – BH 2 (lebih meruah) CH 3(CH 2)2 CH 2 – BH 2 n-butilborana (3) Pengulangan (1) dan (2) sehingga setiap BH 3 mengadisi 3 molekul alkena membentuk trialkilborana CH 3(CH 2)3 – BH 2 2 CH 3 CH 2 CH = CH 2 [CH 3(CH 2)3]3 B tri(n-butil)borana
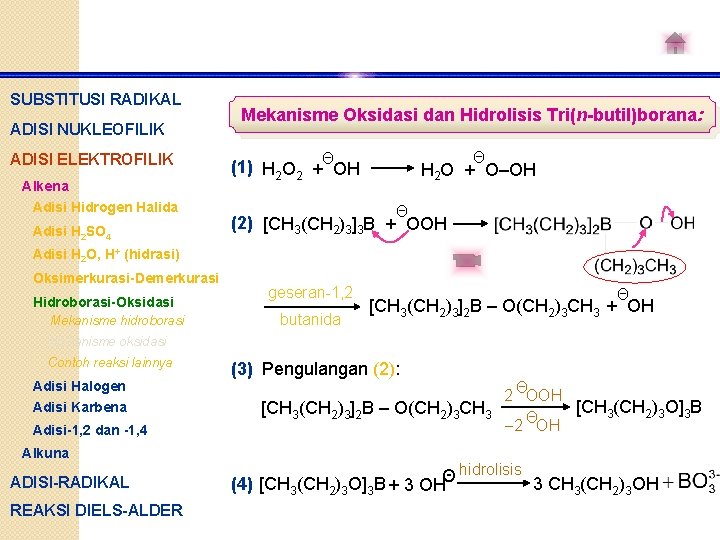
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Mekanisme Oksidasi dan Hidrolisis Tri(n-butil)borana: Θ Θ (1) H 2 O 2 + OH H 2 O + O–OH Θ (2) [CH 3(CH 2)3]3 B + OOH Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Mekanisme hidroborasi geseran-1, 2 butanida Θ [CH 3(CH 2)3]2 B – O(CH 2)3 CH 3 + OH Mekanisme oksidasi Contoh reaksi lainnya Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER (3) Pengulangan (2): [CH 3(CH 2)3]2 B – O(CH 2)3 CH 3 2 ΘOOH [CH 3(CH 2)3 O]3 B Θ -2 OH hidrolisis Θ (4) [CH 3(CH 2)3 O]3 B + 3 OH 3 CH 3(CH 2)3 OH
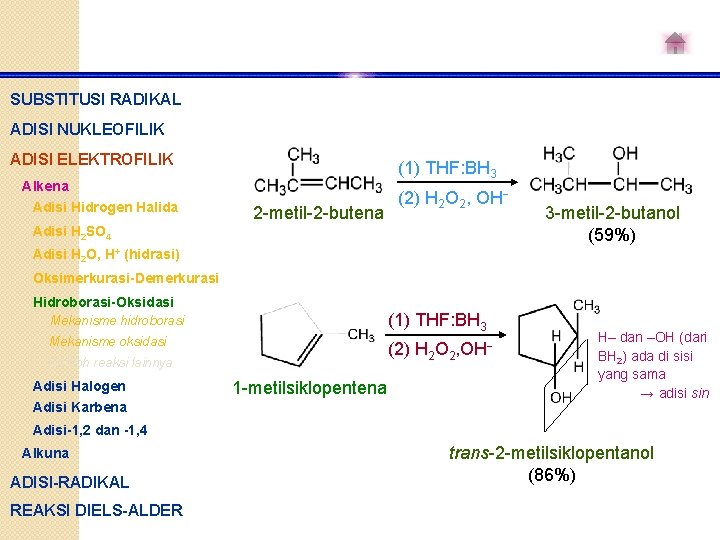
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK (1) THF: BH 3 Alkena Adisi Hidrogen Halida 2 -metil-2 -butena (2) H 2 O 2, OH- Adisi H 2 SO 4 3 -metil-2 -butanol (59%) Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Mekanisme hidroborasi (1) THF: BH 3 Mekanisme oksidasi (2) H 2 O 2, OH- Contoh reaksi lainnya Adisi Halogen Adisi Karbena 1 -metilsiklopentena H– dan –OH (dari BH 2) ada di sisi yang sama → adisi sin Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER trans-2 -metilsiklopentanol (86%)
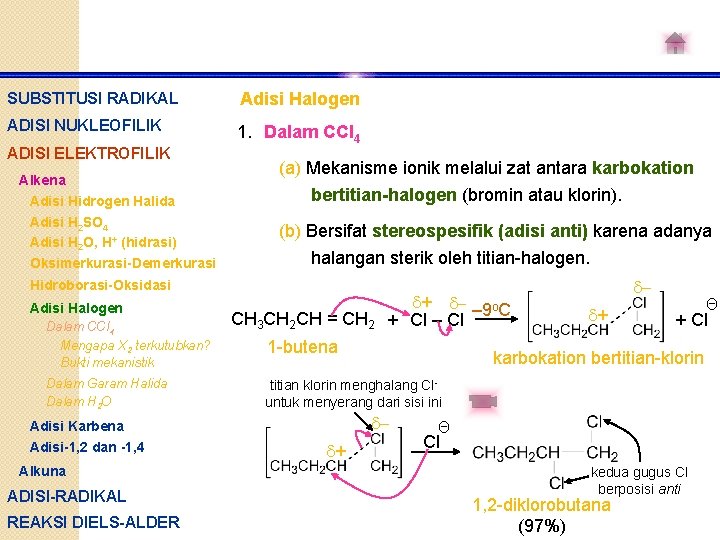
SUBSTITUSI RADIKAL Adisi Halogen ADISI NUKLEOFILIK 1. Dalam CCl 4 ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi (a) Mekanisme ionik melalui zat antara karbokation bertitian-halogen (bromin atau klorin). (b) Bersifat stereospesifik (adisi anti) karena adanya halangan sterik oleh titian-halogen. Hidroborasi-Oksidasi Adisi Halogen Dalam CCl 4 Mengapa X 2 terkutubkan? Bukti mekanistik Dalam Garam Halida Dalam H 2 O Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER CH 3 CH 2 CH = CH 2 + - – 9 o. C + Cl – Cl 1 -butena + + Cl karbokation bertitian-klorin titian klorin menghalang Cluntuk menyerang dari sisi ini + Θ Cl kedua gugus Cl berposisi anti 1, 2 -diklorobutana (97%) Θ
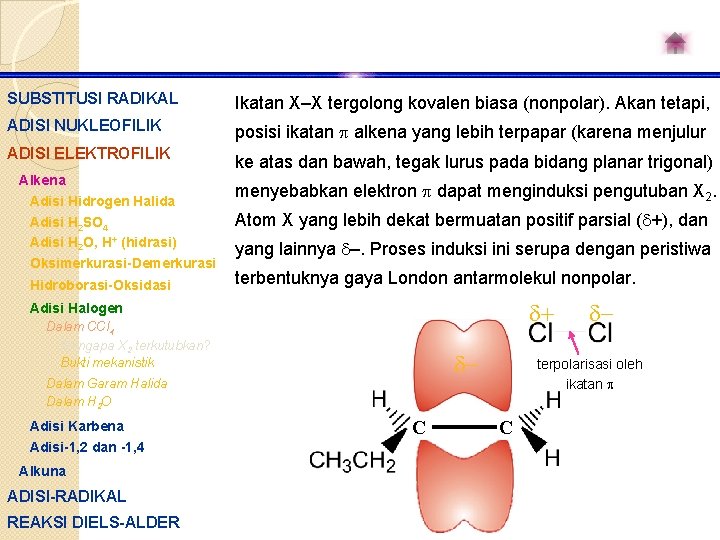
SUBSTITUSI RADIKAL Ikatan X–X tergolong kovalen biasa (nonpolar). Akan tetapi, ADISI NUKLEOFILIK posisi ikatan alkena yang lebih terpapar (karena menjulur ADISI ELEKTROFILIK ke atas dan bawah, tegak lurus pada bidang planar trigonal) Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi menyebabkan elektron dapat menginduksi pengutuban X 2. Atom X yang lebih dekat bermuatan positif parsial ( +), dan yang lainnya –. Proses induksi ini serupa dengan peristiwa terbentuknya gaya London antarmolekul nonpolar. + Adisi Halogen Dalam CCl 4 Mengapa X 2 terkutubkan? Bukti mekanistik - Dalam Garam Halida Dalam H 2 O Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER C - terpolarisasi oleh ikatan C
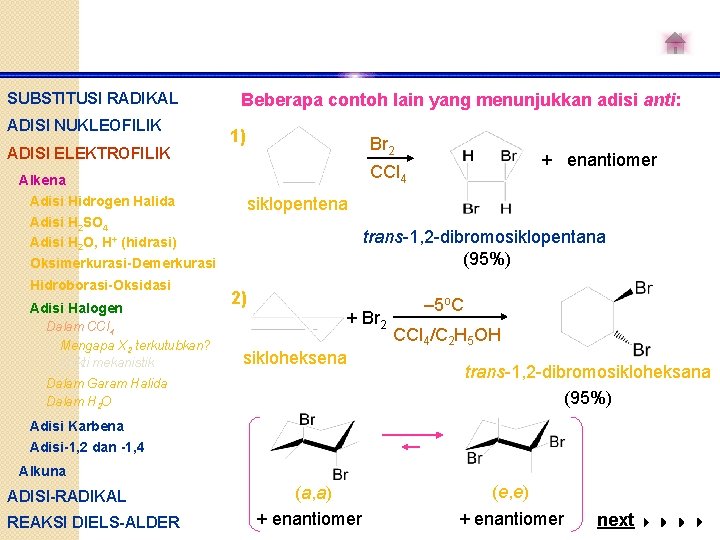
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Beberapa contoh lain yang menunjukkan adisi anti: 1) Br 2 Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Dalam CCl 4 Mengapa X 2 terkutubkan? Bukti mekanistik + enantiomer CCl 4 siklopentena trans-1, 2 -dibromosiklopentana (95%) 2) + Br 2 sikloheksena Dalam Garam Halida Dalam H 2 O – 5 o. C CCl 4/C 2 H 5 OH trans-1, 2 -dibromosikloheksana (95%) Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER (a, a) + enantiomer (e, e) + enantiomer next
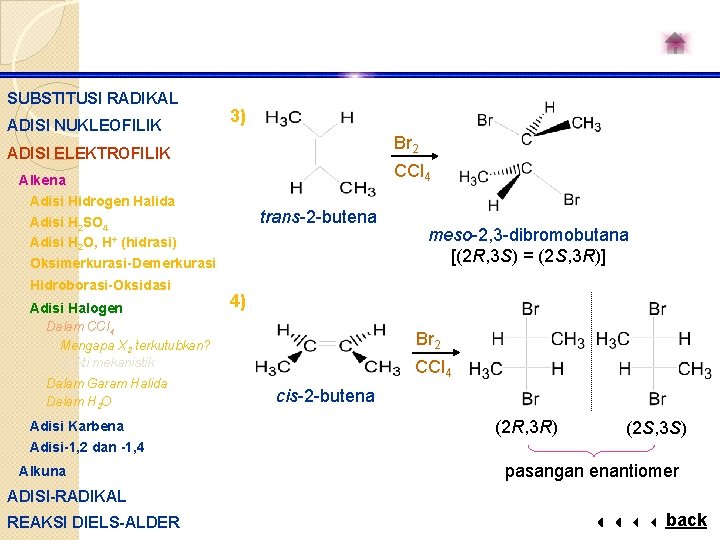
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK 3) Br 2 ADISI ELEKTROFILIK CCl 4 Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen trans-2 -butena 4) Dalam CCl 4 Mengapa X 2 terkutubkan? Bukti mekanistik Dalam Garam Halida Dalam H 2 O Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna meso-2, 3 -dibromobutana [(2 R, 3 S) = (2 S, 3 R)] Br 2 CCl 4 cis-2 -butena (2 R, 3 R) (2 S, 3 S) pasangan enantiomer ADISI-RADIKAL REAKSI DIELS-ALDER back
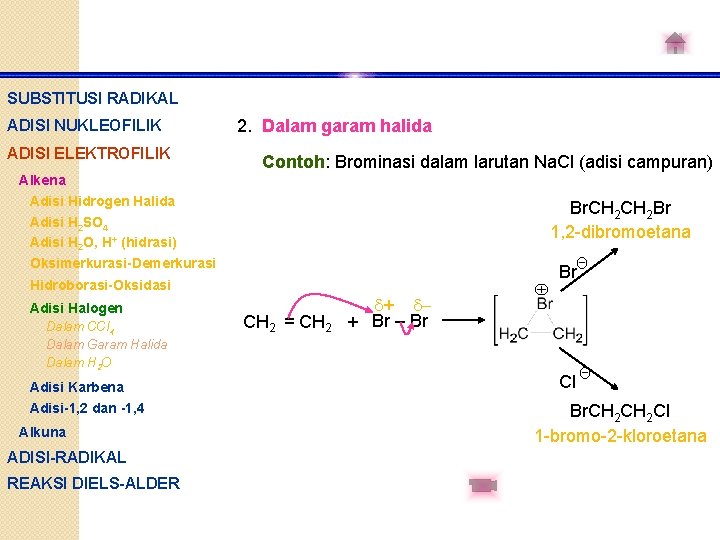
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK 2. Dalam garam halida Contoh: Brominasi dalam larutan Na. Cl (adisi campuran) Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Br. CH 2 Br 1, 2 -dibromoetana Hidroborasi-Oksidasi Adisi Halogen Dalam CCl 4 Dalam Garam Halida Dalam H 2 O Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER CH 2 = CH 2 + + Br – Br BrΘ Cl Θ Br. CH 2 Cl 1 -bromo-2 -kloroetana
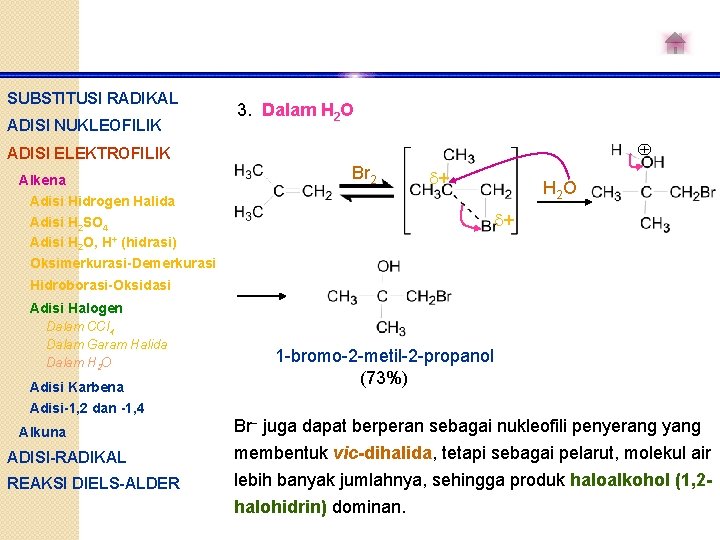
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK 3. Dalam H 2 O ADISI ELEKTROFILIK Alkena Br 2 Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi + H 2 O + Hidroborasi-Oksidasi Adisi Halogen Dalam CCl 4 Dalam Garam Halida Dalam H 2 O Adisi Karbena Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER 1 -bromo-2 -metil-2 -propanol (73%) Br- juga dapat berperan sebagai nukleofili penyerang yang membentuk vic-dihalida, tetapi sebagai pelarut, molekul air lebih banyak jumlahnya, sehingga produk haloalkohol (1, 2 halohidrin) dominan.
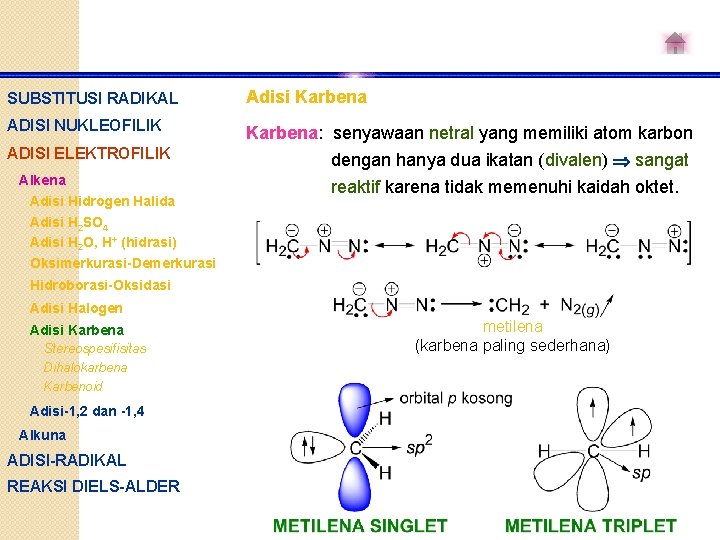
SUBSTITUSI RADIKAL Adisi Karbena ADISI NUKLEOFILIK Karbena: senyawaan netral yang memiliki atom karbon dengan hanya dua ikatan (divalen) sangat ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi reaktif karena tidak memenuhi kaidah oktet. Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Stereospesifisitas Dihalokarbena Karbenoid Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER metilena (karbena paling sederhana)
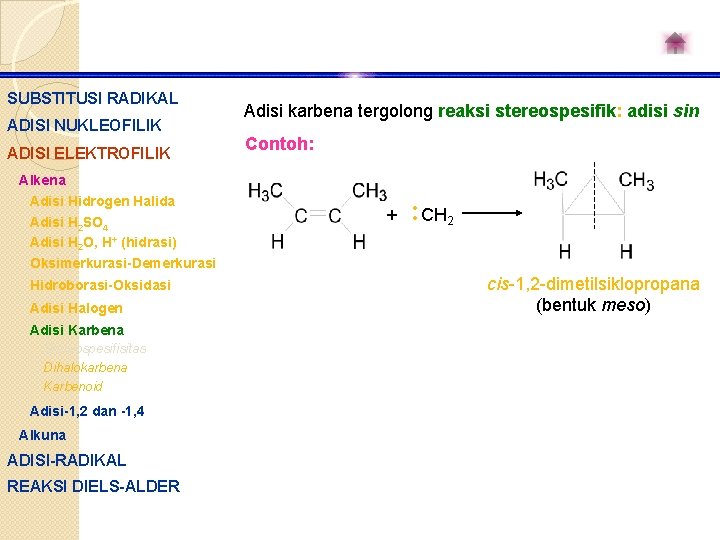
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Adisi karbena tergolong reaksi stereospesifik: adisi sin Contoh: Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Stereospesifisitas Dihalokarbena Karbenoid Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER + CH 2 cis-1, 2 -dimetilsiklopropana (bentuk meso)
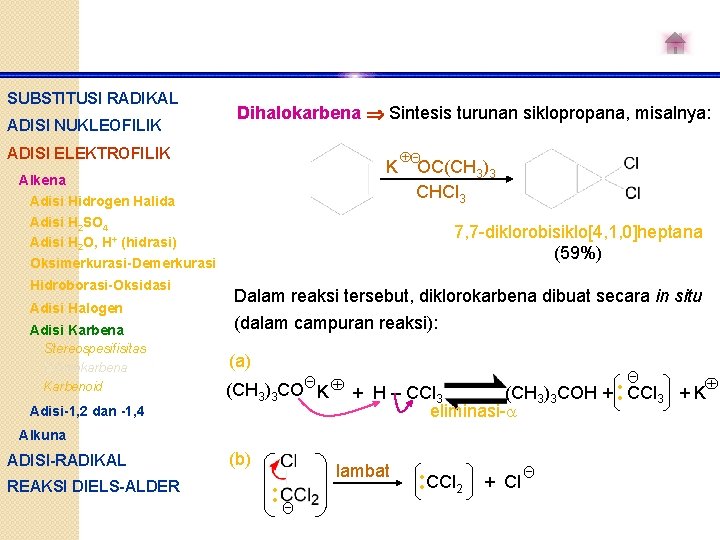
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Dihalokarbena Sintesis turunan siklopropana, misalnya: ADISI ELEKTROFILIK K Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Stereospesifisitas Dihalokarbena Karbenoid Adisi-1, 2 dan -1, 4 Θ OC(CH 3)3 CHCl 3 7, 7 -diklorobisiklo[4, 1, 0]heptana (59%) Dalam reaksi tersebut, diklorokarbena dibuat secara in situ (dalam campuran reaksi): (a) (CH 3)3 COΘ K + H – CCl 3 REAKSI DIELS-ALDER (CH 3)3 COH + CCl 3 + K eliminasi- Alkuna ADISI-RADIKAL Θ (b) lambat Θ CCl 2 + Cl Θ
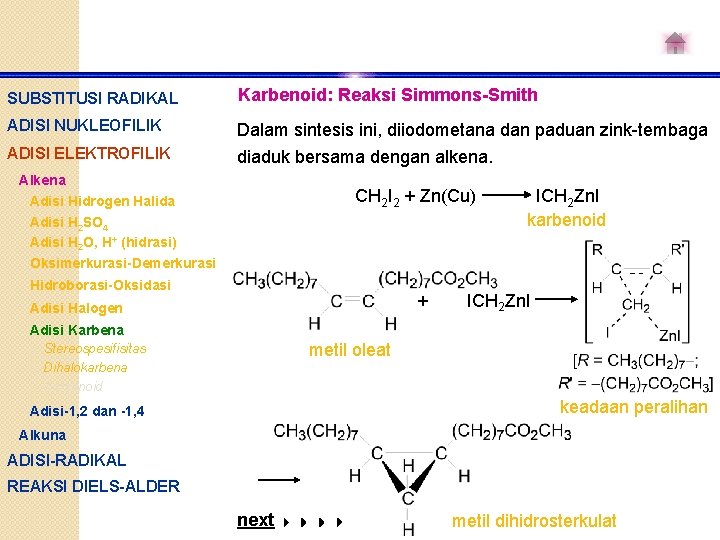
SUBSTITUSI RADIKAL Karbenoid: Reaksi Simmons-Smith ADISI NUKLEOFILIK Dalam sintesis ini, diiodometana dan paduan zink-tembaga ADISI ELEKTROFILIK diaduk bersama dengan alkena. Alkena CH 2 I 2 + Zn(Cu) Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi + Adisi Halogen ICH 2 Zn. I karbenoid ICH 2 Zn. I Adisi Karbena Stereospesifisitas Dihalokarbena Karbenoid metil oleat keadaan peralihan Adisi-1, 2 dan -1, 4 Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER next metil dihidrosterkulat
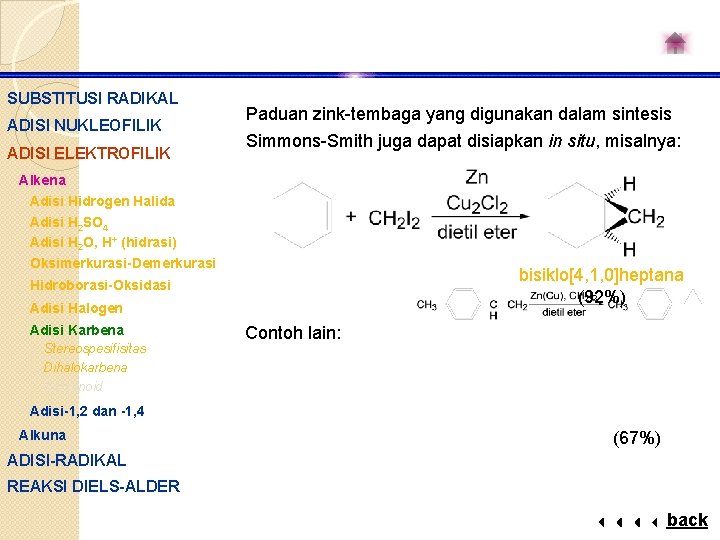
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Paduan zink-tembaga yang digunakan dalam sintesis Simmons-Smith juga dapat disiapkan in situ, misalnya: Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi bisiklo[4, 1, 0]heptana (92%) Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Stereospesifisitas Dihalokarbena Karbenoid Contoh lain: Adisi-1, 2 dan -1, 4 Alkuna (67%) ADISI-RADIKAL REAKSI DIELS-ALDER back

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Adisi-1, 2 dan -1, 4 pada Diena Terkonjugasi ADISI ELEKTROFILIK Contoh: Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi 1, 3 -butadiena Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Mekanisme Bukti mekanistik Pengaruh suhu Kinetika vs termodinamika Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER 3 -kloro-1 -butena (78%) 1 -kloro-2 -butena (22%) Jika mengikuti adisi elektrofilik biasa, reaksi 1, 3 -butadiena dengan 1 ekuivalen molar HCl hanya akan menghasilkan 3 -kloro-1 -butena. Turut dihasilkannya 1 -kloro-2 -butena dikarenakan kestabilan dan sifat terdelokalisasi dari karbokation alilik yang menjadi zat antara.
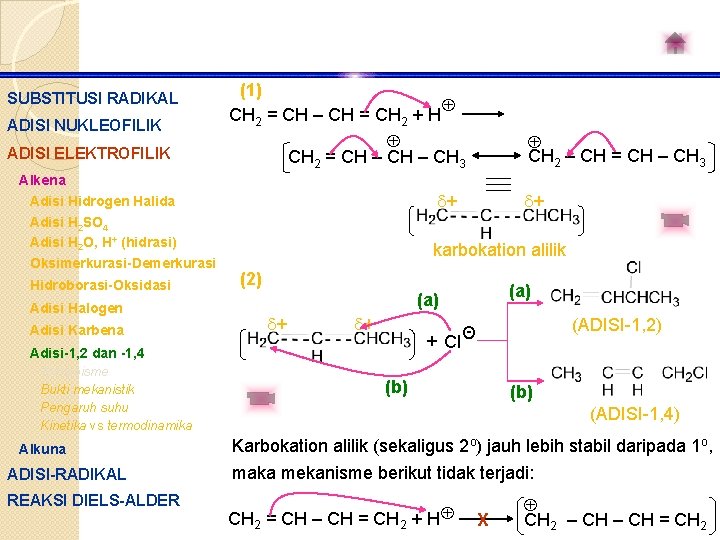
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK (1) CH 2 = CH – CH = CH 2 + H CH 2 = CH – CH 3 CH 2 – CH = CH – CH 3 Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena + karbokation alilik (2) Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER (a) + + (ADISI-1, 2) + Cl Θ Adisi-1, 2 dan -1, 4 Mekanisme Bukti mekanistik Pengaruh suhu Kinetika vs termodinamika + (b) (ADISI-1, 4) Karbokation alilik (sekaligus 2 o) jauh lebih stabil daripada 1 o, maka mekanisme berikut tidak terjadi: CH 2 = CH – CH = CH 2 + H X CH 2 – CH = CH 2
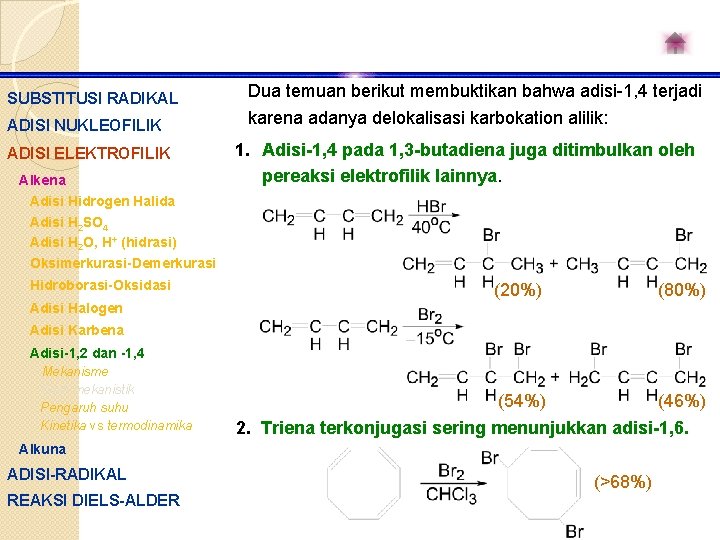
SUBSTITUSI RADIKAL Dua temuan berikut membuktikan bahwa adisi-1, 4 terjadi ADISI NUKLEOFILIK karena adanya delokalisasi karbokation alilik: ADISI ELEKTROFILIK Alkena 1. Adisi-1, 4 pada 1, 3 -butadiena juga ditimbulkan oleh pereaksi elektrofilik lainnya. Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi (20%) (80%) (54%) (46%) Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Mekanisme Bukti mekanistik Pengaruh suhu Kinetika vs termodinamika 2. Triena terkonjugasi sering menunjukkan adisi-1, 6. Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER (>68%)
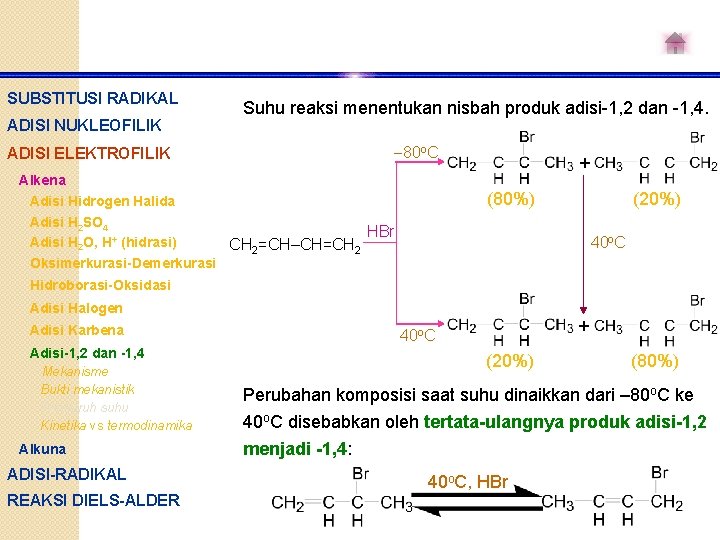
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Suhu reaksi menentukan nisbah produk adisi-1, 2 dan -1, 4. -80 o. C + Alkena (20%) (80%) Adisi Hidrogen Halida Adisi H 2 SO 4 HBr Adisi H 2 O, H+ (hidrasi) CH 2=CH–CH=CH 2 Oksimerkurasi-Demerkurasi 40 o. C Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Mekanisme Bukti mekanistik Pengaruh suhu Kinetika vs termodinamika Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER + 40 o. C (20%) (80%) Perubahan komposisi saat suhu dinaikkan dari – 80 o. C ke 40 o. C disebabkan oleh tertata-ulangnya produk adisi-1, 2 menjadi -1, 4: 40 o. C, HBr

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Suhu rendah: 1. relatif produk-produk adisi ditentukan oleh laju relatif berlangsungnya kedua reaksi adisi (faktor kinetika). 2. Adisi-1, 2 lebih cepat produknya menjadi produk utama. Suhu tinggi: 1. relatif produk ditentukan oleh posisi kesetimbangan mereka (faktor termodinamika). 2. Produk adisi-1, 4 lebih stabil dominan. Mekanisme Bukti mekanistik Pengaruh suhu Kinetika vs termodinamika Alkuna ADISI-RADIKAL REAKSI DIELS-ALDER next

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Adisi Hidrogen Halida Adisi H 2 SO 4 Adisi H 2 O, H+ (hidrasi) Oksimerkurasi-Demerkurasi Hidroborasi-Oksidasi Adisi Halogen Adisi Karbena Adisi-1, 2 dan -1, 4 Mekanisme Bukti mekanistik Pengaruh suhu Kinetika vs termodinamika Alkuna ADISI-RADIKAL DIAGRAM ENERGI POTENSIAL REAKSI DIELS-ALDER back
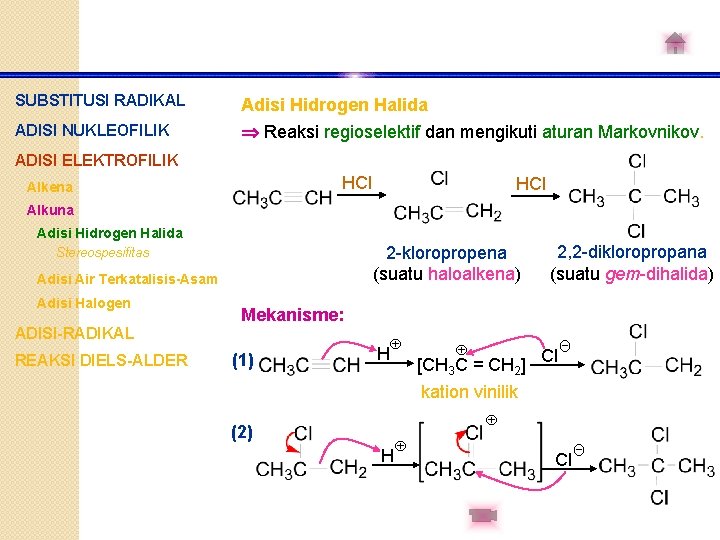
SUBSTITUSI RADIKAL Adisi Hidrogen Halida ADISI NUKLEOFILIK Reaksi regioselektif dan mengikuti aturan Markovnikov. ADISI ELEKTROFILIK HCl Alkena HCl Alkuna Adisi Hidrogen Halida 2 -kloropropena (suatu haloalkena) Stereospesifitas Adisi Air Terkatalisis-Asam Adisi Halogen ADISI-RADIKAL REAKSI DIELS-ALDER 2, 2 -dikloropropana (suatu gem-dihalida) Mekanisme: (1) H [CH 3 C = CH 2] Cl Θ kation vinilik (2) H Cl Θ

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK Alkena Alkuna Adisi Hidrogen Halida Stereospesifitas Tahap (1) biasanya berlangsung dengan adisi anti, terutama jika dalam campuran terdapat ion halida yang berhubungan dengan atom halogen pada hidrogen halida. Adisi Air Terkatalisis-Asam Adisi Halogen Contoh: ADISI-RADIKAL REAKSI DIELS-ALDER (97%)
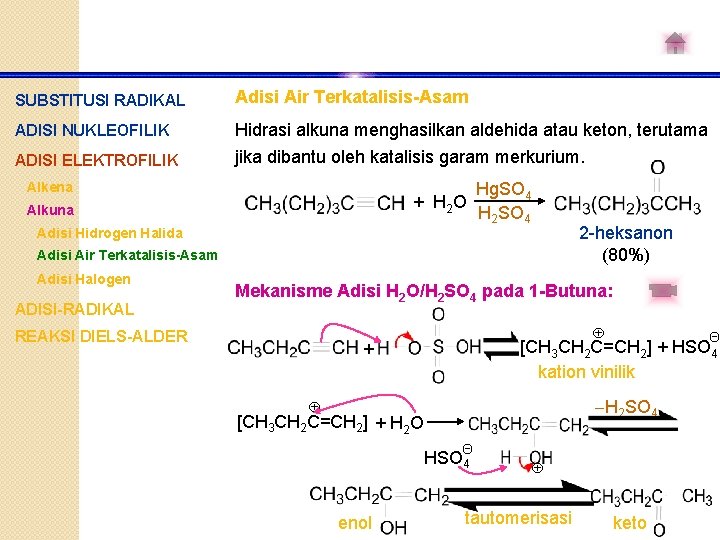
SUBSTITUSI RADIKAL Adisi Air Terkatalisis-Asam ADISI NUKLEOFILIK Hidrasi alkuna menghasilkan aldehida atau keton, terutama jika dibantu oleh katalisis garam merkurium. ADISI ELEKTROFILIK Hg. SO 4 + H 2 O H 2 SO 4 Alkena Alkuna Adisi Hidrogen Halida 2 -heksanon (80%) Adisi Air Terkatalisis-Asam Adisi Halogen ADISI-RADIKAL Mekanisme Adisi H 2 O/H 2 SO 4 pada 1 -Butuna: REAKSI DIELS-ALDER Θ [CH 3 CH 2 C=CH 2] + HSO 4 kation vinilik + -H 2 SO 4 [CH 3 CH 2 C=CH 2] + H 2 O Θ HSO 4 enol tautomerisasi keto
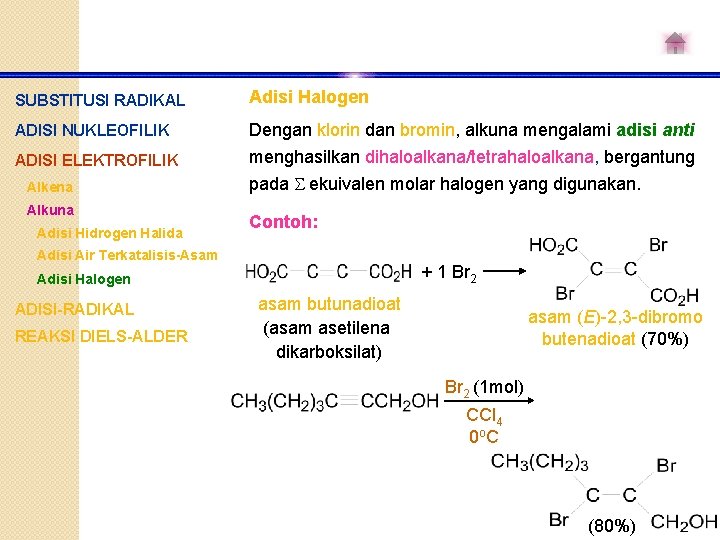
SUBSTITUSI RADIKAL Adisi Halogen ADISI NUKLEOFILIK Dengan klorin dan bromin, alkuna mengalami adisi anti menghasilkan dihaloalkana/tetrahaloalkana, bergantung pada ekuivalen molar halogen yang digunakan. ADISI ELEKTROFILIK Alkena Alkuna Adisi Hidrogen Halida Contoh: Adisi Air Terkatalisis-Asam + 1 Br 2 Adisi Halogen ADISI-RADIKAL REAKSI DIELS-ALDER asam butunadioat (asam asetilena dikarboksilat) asam (E)-2, 3 -dibromo butenadioat (70%) Br 2 (1 mol) CCl 4 0 o C (80%)

SUBSTITUSI RADIKAL Produk adisi HBr pada propena bergantung pada kondisi ADISI NUKLEOFILIK reaksi yang digunakan: ADISI ELEKTROFILIK ADISI-RADIKAL Adisi HBr Mekanisme Adisi Selain HBr Polimerisasi Etilena REAKSI DIELS-ALDER 1. Tanpa peroksida atau jika ada pemerangkap radikal: CH 3 CH=CH 2 + HBr → CH 3 CHBr. CH 3 [ADISI ELEKTROFILIK] 2 -bromopropana (Markovnikov) 2. Dengan adanya peroksida: CH 3 CH=CH 2 + HBr ROOR [ADISI RADIKAL] CH 3 CH 2 Br 1 -bromopropana (anti-Markovnikov) Adisi anti-Markovnikov juga dapat terjadi pada alkuna: HBr 1 -heksuna peroksida CH 3(CH 2)3 CH=CHBr 1 -bromo-1 -heksena (74%)
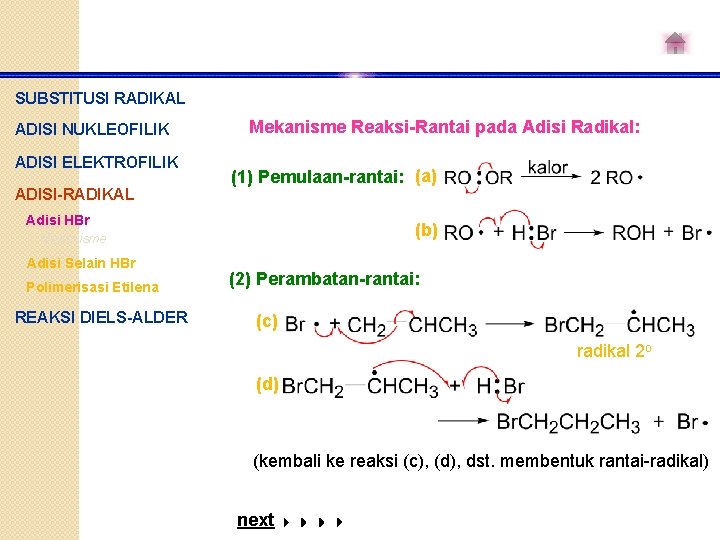
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL Mekanisme Reaksi-Rantai pada Adisi Radikal: (1) Pemulaan-rantai: (a) Adisi HBr (b) Mekanisme Adisi Selain HBr Polimerisasi Etilena REAKSI DIELS-ALDER (2) Perambatan-rantai: (c) radikal 2 o (d) (kembali ke reaksi (c), (d), dst. membentuk rantai-radikal) next
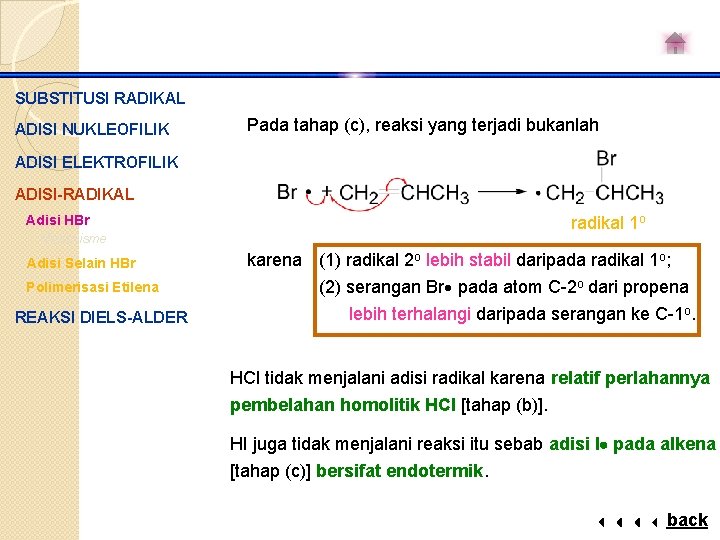
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Pada tahap (c), reaksi yang terjadi bukanlah ADISI ELEKTROFILIK ADISI-RADIKAL radikal 1 o Adisi HBr Mekanisme Adisi Selain HBr Polimerisasi Etilena REAKSI DIELS-ALDER karena (1) radikal 2 o lebih stabil daripada radikal 1 o; (2) serangan Br pada atom C-2 o dari propena lebih terhalangi daripada serangan ke C-1 o. HCl tidak menjalani adisi radikal karena relatif perlahannya pembelahan homolitik HCl [tahap (b)]. HI juga tidak menjalani reaksi itu sebab adisi I pada alkena [tahap (c)] bersifat endotermik. back
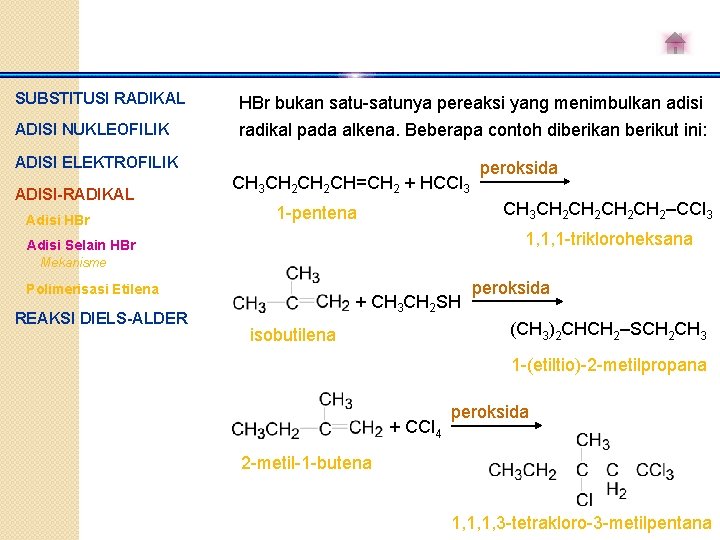
SUBSTITUSI RADIKAL HBr bukan satu-satunya pereaksi yang menimbulkan adisi ADISI NUKLEOFILIK radikal pada alkena. Beberapa contoh diberikan berikut ini: ADISI ELEKTROFILIK ADISI-RADIKAL Adisi HBr CH 3 CH 2 CH=CH 2 + HCCl 3 peroksida CH 3 CH 2 CH 2–CCl 3 1 -pentena 1, 1, 1 -trikloroheksana Adisi Selain HBr Mekanisme Polimerisasi Etilena REAKSI DIELS-ALDER + CH 3 CH 2 SH peroksida (CH 3)2 CHCH 2–SCH 2 CH 3 isobutilena 1 -(etiltio)-2 -metilpropana + CCl 4 peroksida 2 -metil-1 -butena 1, 1, 1, 3 -tetrakloro-3 -metilpentana
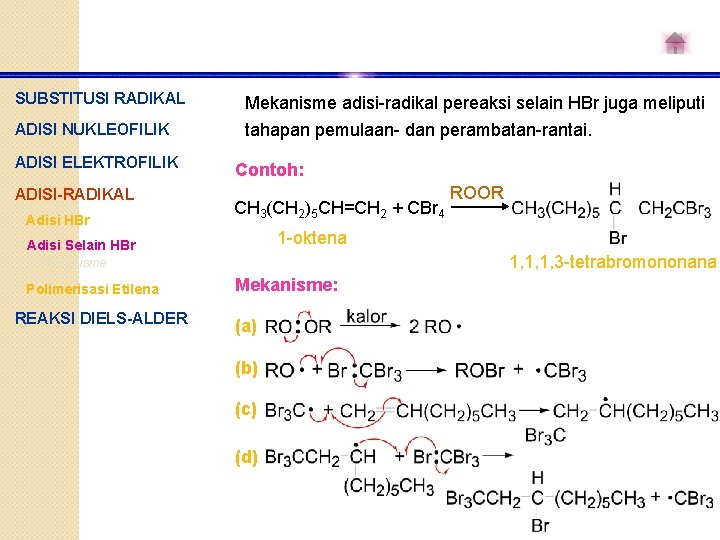
SUBSTITUSI RADIKAL Mekanisme adisi-radikal pereaksi selain HBr juga meliputi ADISI NUKLEOFILIK tahapan pemulaan- dan perambatan-rantai. ADISI ELEKTROFILIK ADISI-RADIKAL Adisi HBr Contoh: CH 3(CH 2)5 CH=CH 2 + CBr 4 1 -oktena Adisi Selain HBr 1, 1, 1, 3 -tetrabromononana Mekanisme Polimerisasi Etilena REAKSI DIELS-ALDER ROOR Mekanisme: (a) (b) (c) (d)
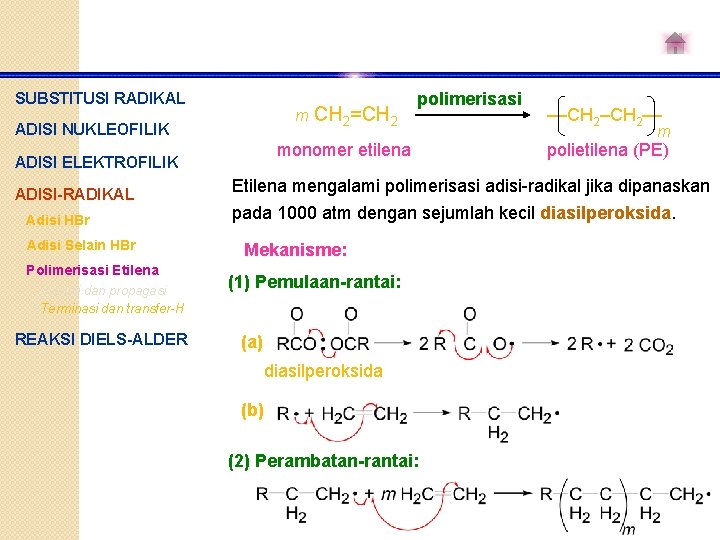
SUBSTITUSI RADIKAL m ADISI NUKLEOFILIK monomer etilena ADISI ELEKTROFILIK ADISI-RADIKAL Adisi HBr Adisi Selain HBr Polimerisasi Etilena Inisiasi dan propagasi Terminasi dan transfer-H REAKSI DIELS-ALDER CH 2=CH 2 polimerisasi ––CH 2–– m polietilena (PE) Etilena mengalami polimerisasi adisi-radikal jika dipanaskan pada 1000 atm dengan sejumlah kecil diasilperoksida. Mekanisme: (1) Pemulaan-rantai: (a) diasilperoksida (b) (2) Perambatan-rantai:
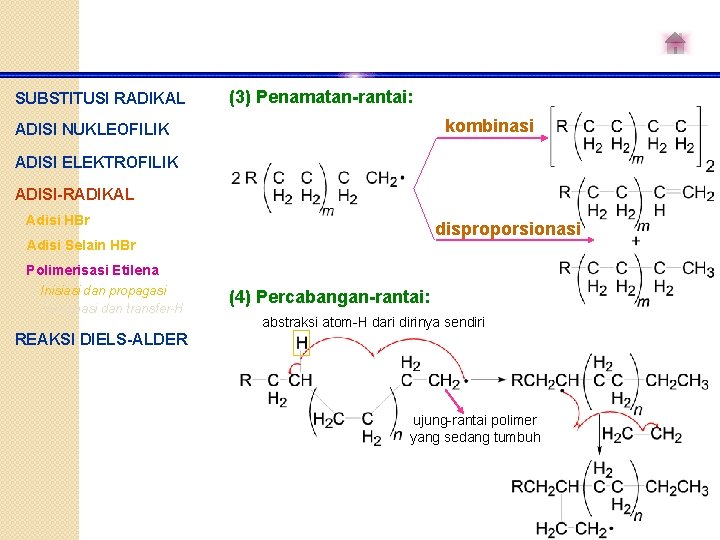
SUBSTITUSI RADIKAL (3) Penamatan-rantai: kombinasi ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL Adisi HBr disproporsionasi Adisi Selain HBr Polimerisasi Etilena Inisiasi dan propagasi Terminasi dan transfer-H (4) Percabangan-rantai: abstraksi atom-H dari dirinya sendiri REAKSI DIELS-ALDER ujung-rantai polimer yang sedang tumbuh
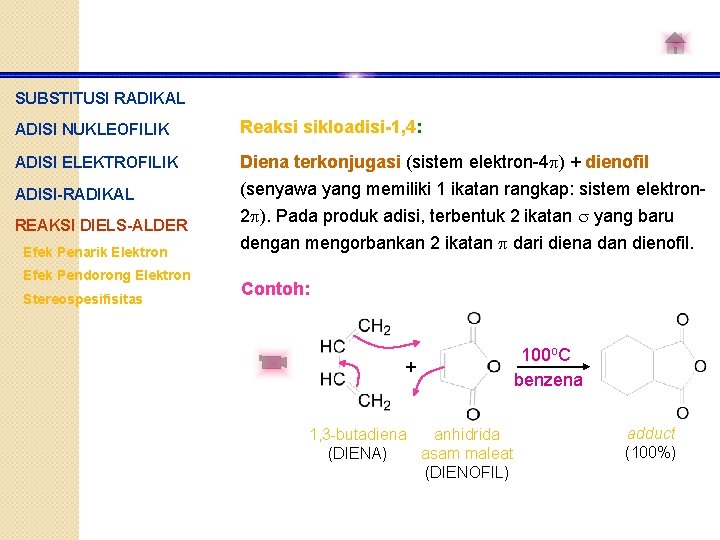
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Reaksi sikloadisi-1, 4: ADISI ELEKTROFILIK Diena terkonjugasi (sistem elektron-4 ) + dienofil ADISI-RADIKAL (senyawa yang memiliki 1 ikatan rangkap: sistem elektron 2 ). Pada produk adisi, terbentuk 2 ikatan yang baru REAKSI DIELS-ALDER Efek Penarik Elektron Efek Pendorong Elektron Stereospesifisitas dengan mengorbankan 2 ikatan dari diena dan dienofil. Contoh: + 1, 3 -butadiena anhidrida (DIENA) asam maleat (DIENOFIL) 100 o. C benzena adduct (100%)

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK Rendemen reaksi Diels-Alder meningkat jika terdapat ADISI ELEKTROFILIK 1. Gugus penarik-elektron pada dienofil. Buktinya, etena hanya bereaksi dengan 1, 3 -butadiena pada suhu yang lebih tinggi dan dengan rendemen yang jauh lebih rendah daripada anhidrida asam maleat. ADISI-RADIKAL REAKSI DIELS-ALDER Efek Penarik Elektron Efek Pendorong Elektron Stereospesifisitas 200 o. C + etena (20%)
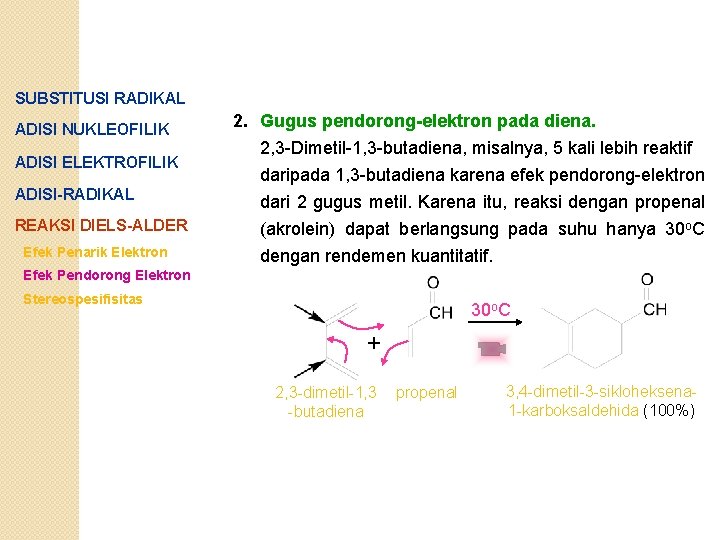
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER Efek Penarik Elektron 2. Gugus pendorong-elektron pada diena. 2, 3 -Dimetil-1, 3 -butadiena, misalnya, 5 kali lebih reaktif daripada 1, 3 -butadiena karena efek pendorong-elektron dari 2 gugus metil. Karena itu, reaksi dengan propenal (akrolein) dapat berlangsung pada suhu hanya 30 o. C dengan rendemen kuantitatif. Efek Pendorong Elektron Stereospesifisitas 30 o. C + 2, 3 -dimetil-1, 3 -butadiena propenal 3, 4 -dimetil-3 -sikloheksena 1 -karboksaldehida (100%)
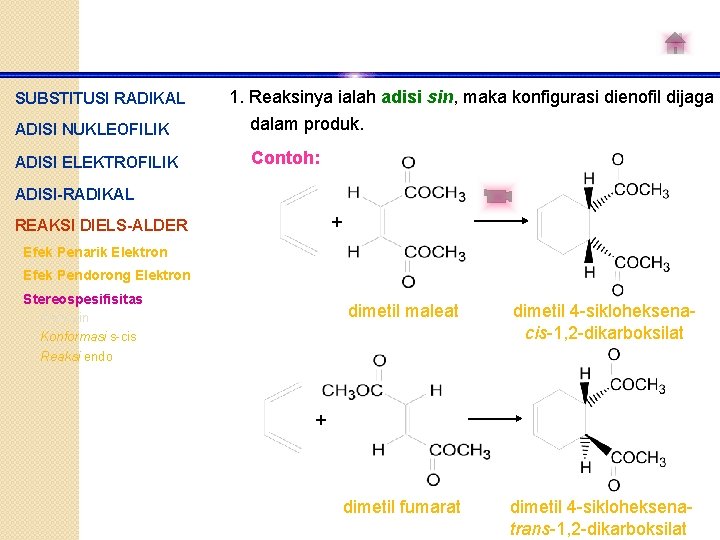
SUBSTITUSI RADIKAL 1. Reaksinya ialah adisi sin, maka konfigurasi dienofil dijaga ADISI NUKLEOFILIK dalam produk. ADISI ELEKTROFILIK Contoh: ADISI-RADIKAL + REAKSI DIELS-ALDER Efek Penarik Elektron Efek Pendorong Elektron Stereospesifisitas Adisi sin Konformasi s-cis dimetil maleat dimetil 4 -sikloheksenacis-1, 2 -dikarboksilat dimetil fumarat dimetil 4 -sikloheksenatrans-1, 2 -dikarboksilat Reaksi endo +
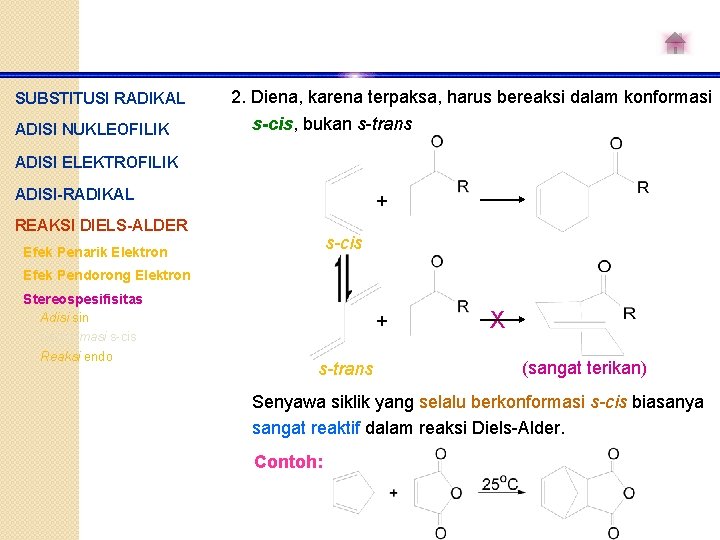
SUBSTITUSI RADIKAL ADISI NUKLEOFILIK 2. Diena, karena terpaksa, harus bereaksi dalam konformasi s-cis, bukan s-trans ADISI ELEKTROFILIK ADISI-RADIKAL + REAKSI DIELS-ALDER s-cis Efek Penarik Elektron Efek Pendorong Elektron Stereospesifisitas Adisi sin Konformasi s-cis Reaksi endo + s-trans X (sangat terikan) Senyawa siklik yang selalu berkonformasi s-cis biasanya sangat reaktif dalam reaksi Diels-Alder. Contoh:

SUBSTITUSI RADIKAL ADISI NUKLEOFILIK ADISI ELEKTROFILIK ADISI-RADIKAL REAKSI DIELS-ALDER 3. Reaksi Diels Alder berlangsung terutama secara endo dan bukan ekso ketika reaksi terkendali secara kinetik. endo = sin (pada sisi yang sama) terhadap titian terpanjang ekso = anti (pada sisi berlawanan) terhadap titian terpanjang Contoh: Efek Penarik Elektron titian 1 atom C Efek Pendorong Elektron Stereospesifisitas Adisi sin Konformasi s-cis + Reaksi endo titian 2 atom C (terpanjang) ENDO + EKSO ENDO (produk utama) (produk minor)
- Slides: 70