Substituio REAES DOS COMPOSTOS CARBONLICOS Adio nucleoflica Substituio
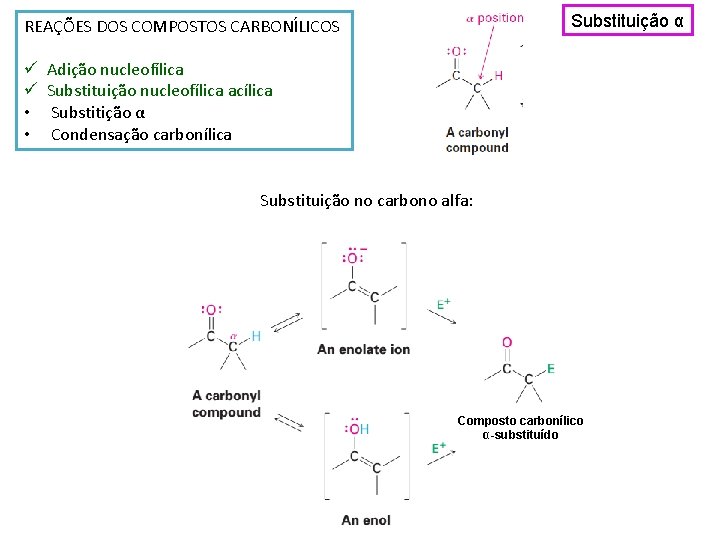
Substituição α REAÇÕES DOS COMPOSTOS CARBONÍLICOS ü ü • • Adição nucleofílica Substituição nucleofílica acílica Substitição α Condensação carbonílica Substituição no carbono alfa: Composto carbonílico α-substituído
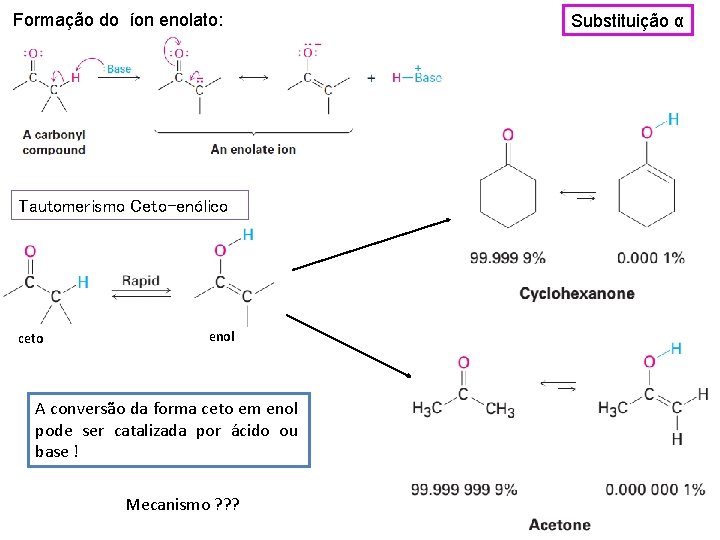
Formação do íon enolato: Tautomerismo Ceto-enólico ceto enol A conversão da forma ceto em enol pode ser catalizada por ácido ou base ! Mecanismo ? ? ? Substituição α
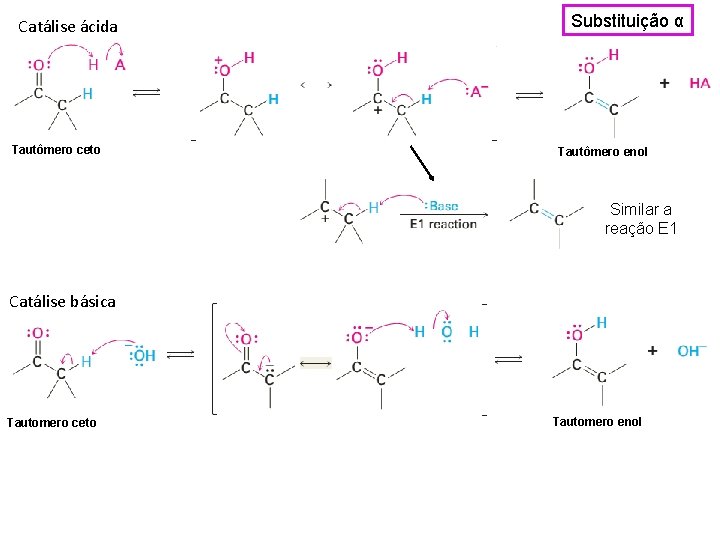
Catálise ácida Tautômero ceto Substituição α Tautômero enol Similar a reação E 1 Catálise básica Tautomero ceto Tautomero enol
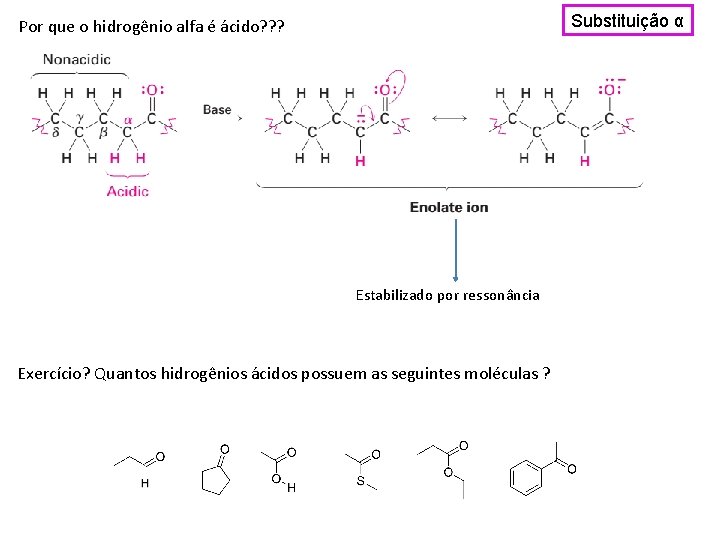
Substituição α Por que o hidrogênio alfa é ácido? ? ? Estabilizado por ressonância Exercício? Quantos hidrogênios ácidos possuem as seguintes moléculas ?
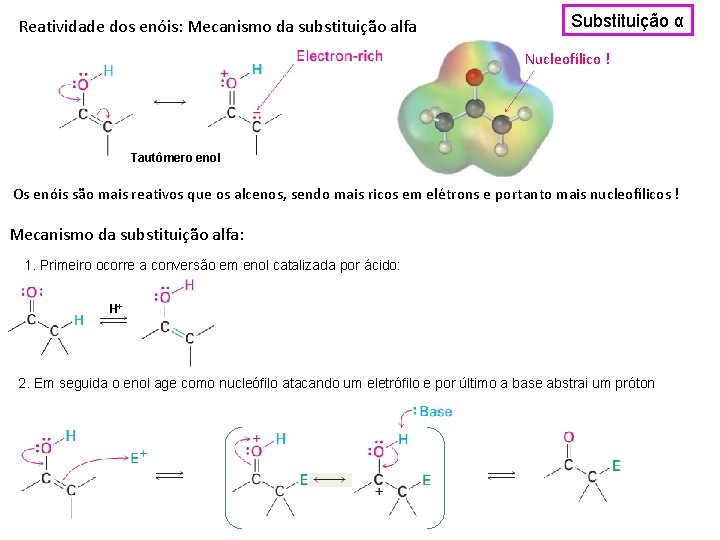
Reatividade dos enóis: Mecanismo da substituição alfa Substituição α Nucleofílico ! Tautômero enol Os enóis são mais reativos que os alcenos, sendo mais ricos em elétrons e portanto mais nucleofílicos ! Mecanismo da substituição alfa: 1. Primeiro ocorre a conversão em enol catalizada por ácido: H+ 2. Em seguida o enol age como nucleófilo atacando um eletrófilo e por último a base abstrai um próton
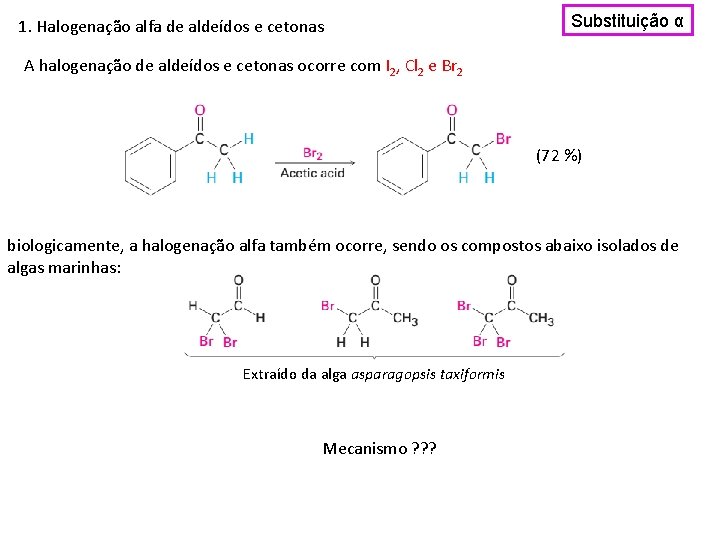
1. Halogenação alfa de aldeídos e cetonas Substituição α A halogenação de aldeídos e cetonas ocorre com I 2, Cl 2 e Br 2 (72 %) biologicamente, a halogenação alfa também ocorre, sendo os compostos abaixo isolados de algas marinhas: Extraído da alga asparagopsis taxiformis Mecanismo ? ? ?
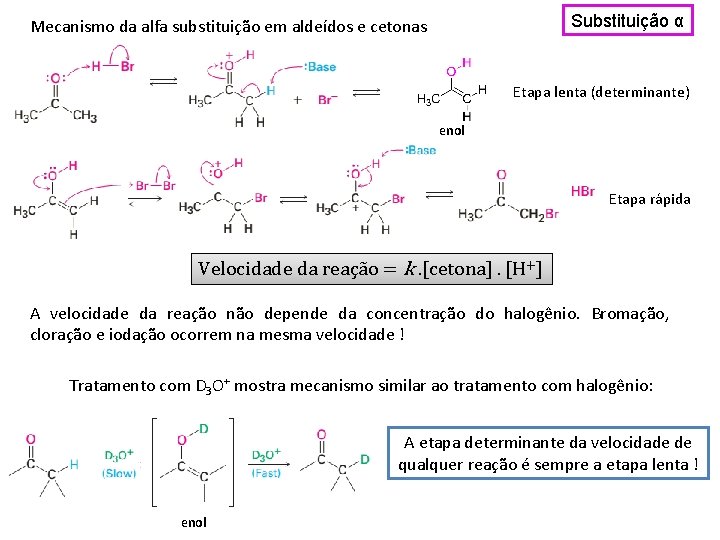
Substituição α Mecanismo da alfa substituição em aldeídos e cetonas Etapa lenta (determinante) enol Etapa rápida Velocidade da reação = k. [cetona]. [H+] A velocidade da reação não depende da concentração do halogênio. Bromação, cloração e iodação ocorrem na mesma velocidade ! Tratamento com D 3 O+ mostra mecanismo similar ao tratamento com halogênio: A etapa determinante da velocidade de qualquer reação é sempre a etapa lenta ! enol
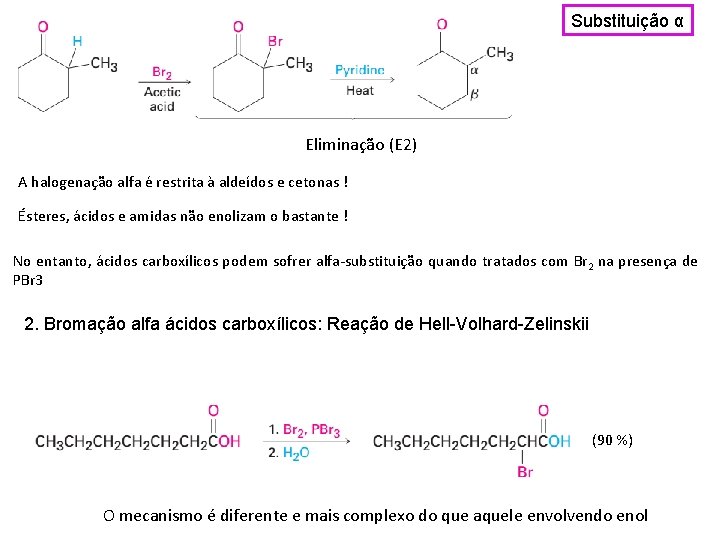
Substituição α Eliminação (E 2) A halogenação alfa é restrita à aldeídos e cetonas ! Ésteres, ácidos e amidas não enolizam o bastante ! No entanto, ácidos carboxílicos podem sofrer alfa-substituição quando tratados com Br 2 na presença de PBr 3 2. Bromação alfa ácidos carboxílicos: Reação de Hell-Volhard-Zelinskii (90 %) O mecanismo é diferente e mais complexo do que aquele envolvendo enol
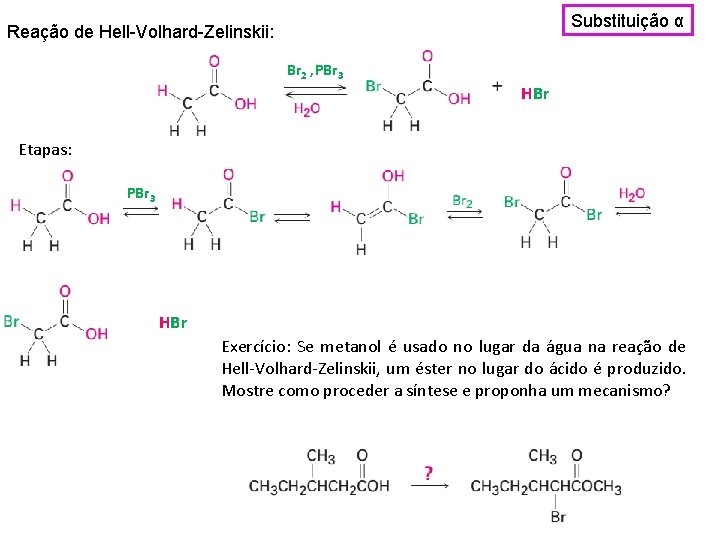
Substituição α Reação de Hell-Volhard-Zelinskii: Br 2 , PBr 3 HBr Etapas: PBr 3 HBr Exercício: Se metanol é usado no lugar da água na reação de Hell-Volhard-Zelinskii, um éster no lugar do ácido é produzido. Mostre como proceder a síntese e proponha um mecanismo?
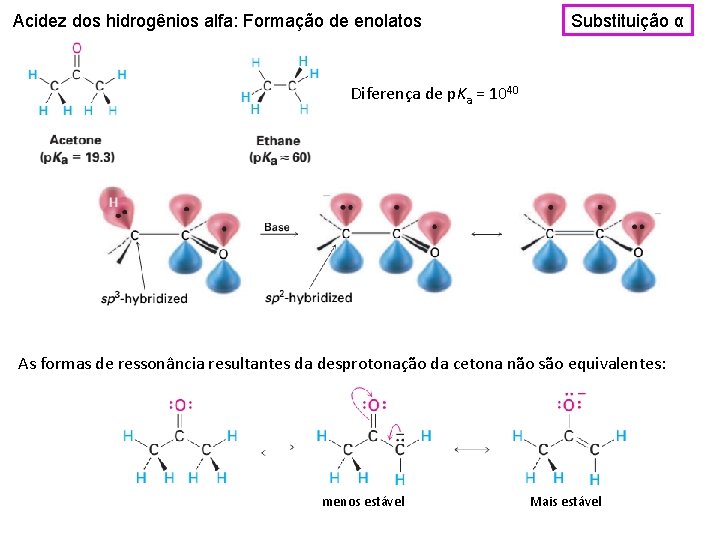
Acidez dos hidrogênios alfa: Formação de enolatos Substituição α Diferença de p. Ka = 1040 As formas de ressonância resultantes da desprotonação da cetona não são equivalentes: menos estável Mais estável
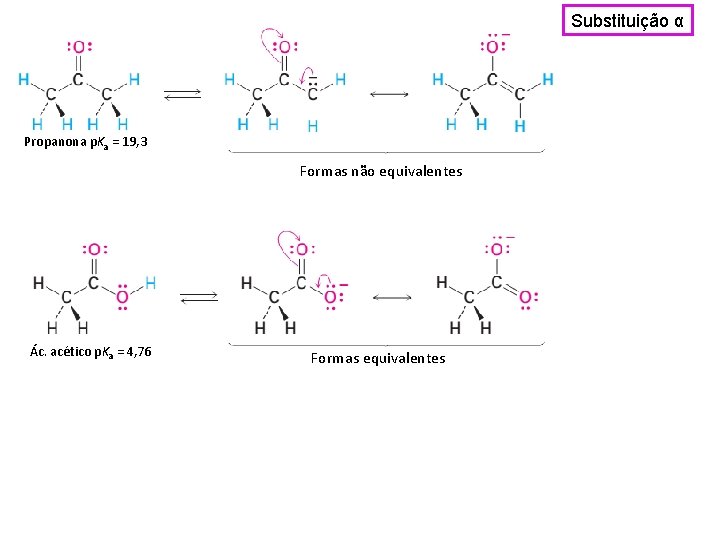
Substituição α Propanona p. Ka = 19, 3 Formas não equivalentes Ác. acético p. Ka = 4, 76 Formas equivalentes
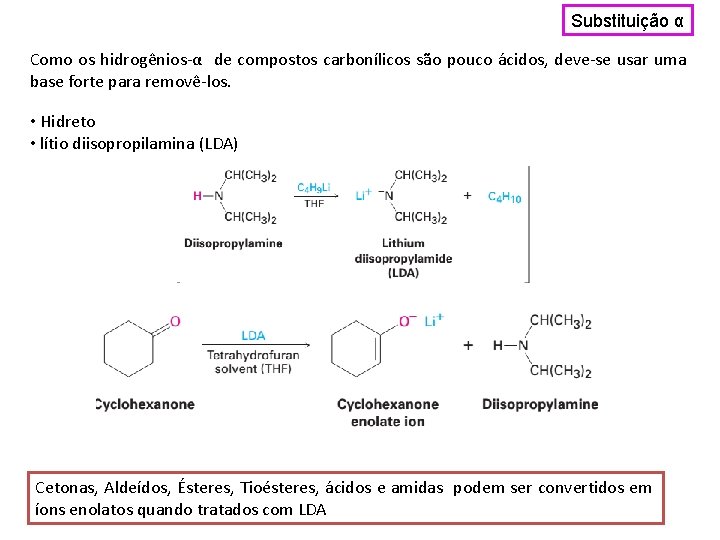
Substituição α Como os hidrogênios-α de compostos carbonílicos são pouco ácidos, deve-se usar uma base forte para removê-los. • Hidreto • lítio diisopropilamina (LDA) Cetonas, Aldeídos, Ésteres, Tioésteres, ácidos e amidas podem ser convertidos em íons enolatos quando tratados com LDA
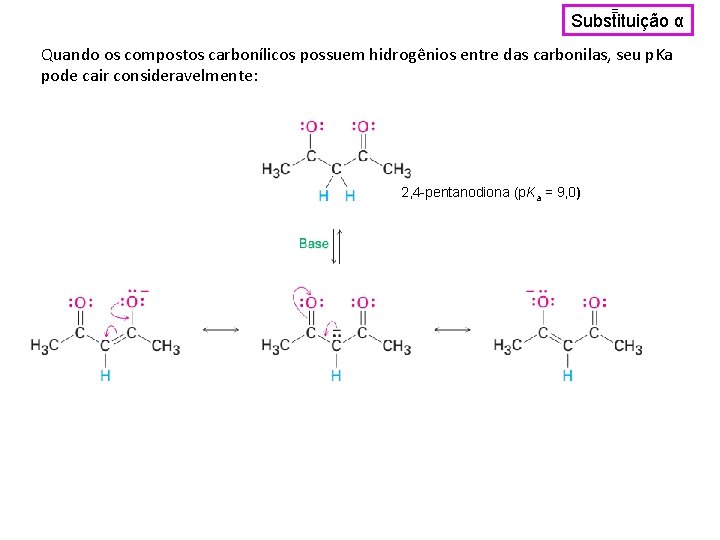
= Substituição α Quando os compostos carbonílicos possuem hidrogênios entre das carbonilas, seu p. Ka pode cair consideravelmente: 2, 4 -pentanodiona (p. Ka = 9, 0)
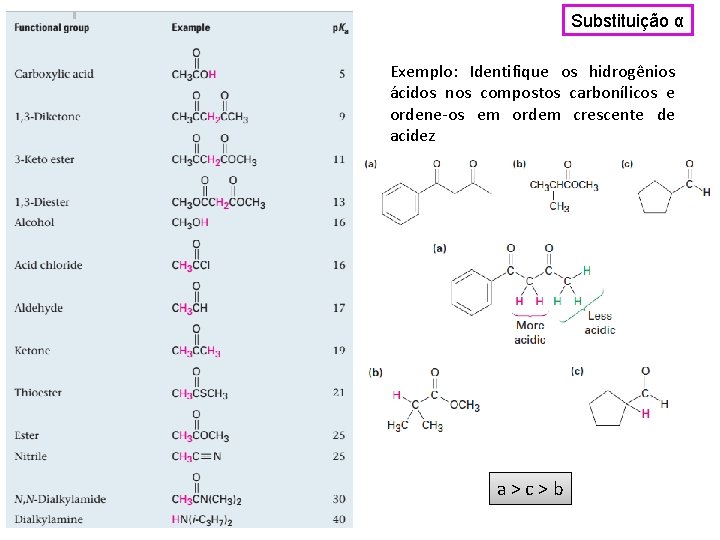
Substituição α Exemplo: Identifique os hidrogênios ácidos nos compostos carbonílicos e ordene-os em ordem crescente de acidez a>c>b
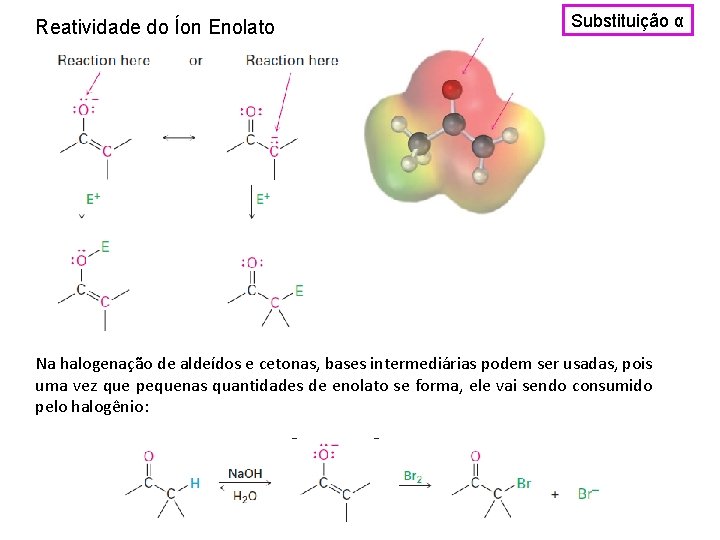
Reatividade do Íon Enolato Substituição α Na halogenação de aldeídos e cetonas, bases intermediárias podem ser usadas, pois uma vez que pequenas quantidades de enolato se forma, ele vai sendo consumido pelo halogênio:
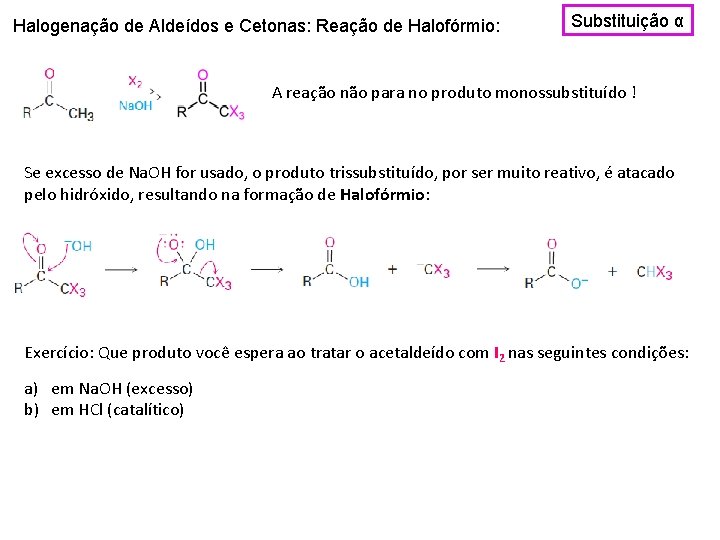
Halogenação de Aldeídos e Cetonas: Reação de Halofórmio: Substituição α A reação não para no produto monossubstituído ! Se excesso de Na. OH for usado, o produto trissubstituído, por ser muito reativo, é atacado pelo hidróxido, resultando na formação de Halofórmio: Exercício: Que produto você espera ao tratar o acetaldeído com I 2 nas seguintes condições: a) em Na. OH (excesso) b) em HCl (catalítico)
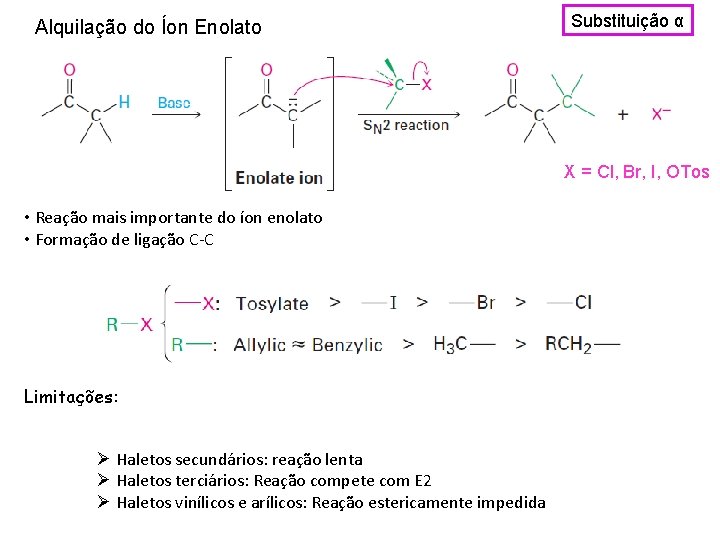
Alquilação do Íon Enolato Substituição α X = Cl, Br, I, OTos • Reação mais importante do íon enolato • Formação de ligação C-C Limitações: Ø Haletos secundários: reação lenta Ø Haletos terciários: Reação compete com E 2 Ø Haletos vinílicos e arílicos: Reação estericamente impedida
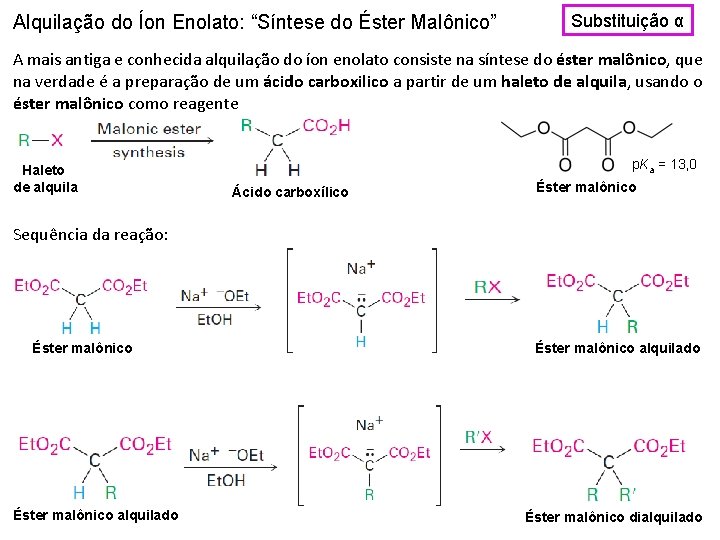
Alquilação do Íon Enolato: “Síntese do Éster Malônico” Substituição α A mais antiga e conhecida alquilação do íon enolato consiste na síntese do éster malônico, que na verdade é a preparação de um ácido carboxilico a partir de um haleto de alquila, usando o éster malônico como reagente Haleto de alquila p. Ka = 13, 0 Ácido carboxílico Éster malônico Sequência da reação: Éster malônico alquilado Éster malônico dialquilado
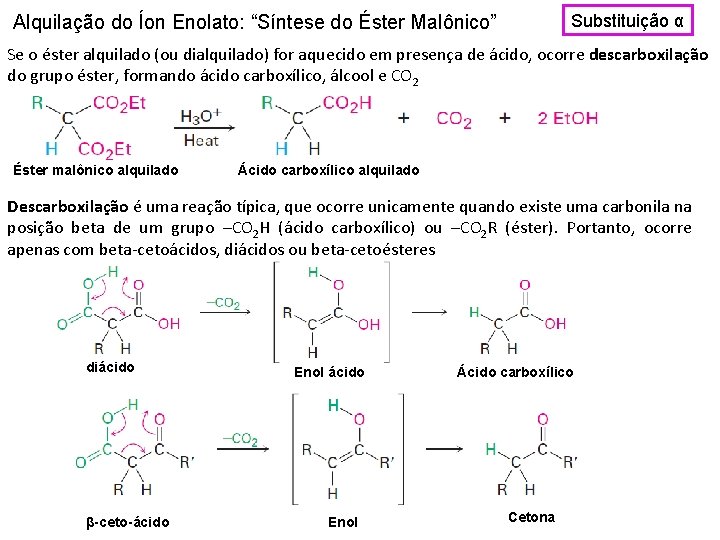
Substituição α Alquilação do Íon Enolato: “Síntese do Éster Malônico” Se o éster alquilado (ou dialquilado) for aquecido em presença de ácido, ocorre descarboxilação do grupo éster, formando ácido carboxílico, álcool e CO 2 Éster malônico alquilado Ácido carboxílico alquilado Descarboxilação é uma reação típica, que ocorre unicamente quando existe uma carbonila na posição beta de um grupo –CO 2 H (ácido carboxílico) ou –CO 2 R (éster). Portanto, ocorre apenas com beta-cetoácidos, diácidos ou beta-cetoésteres diácido β-ceto-ácido Enol Ácido carboxílico Cetona
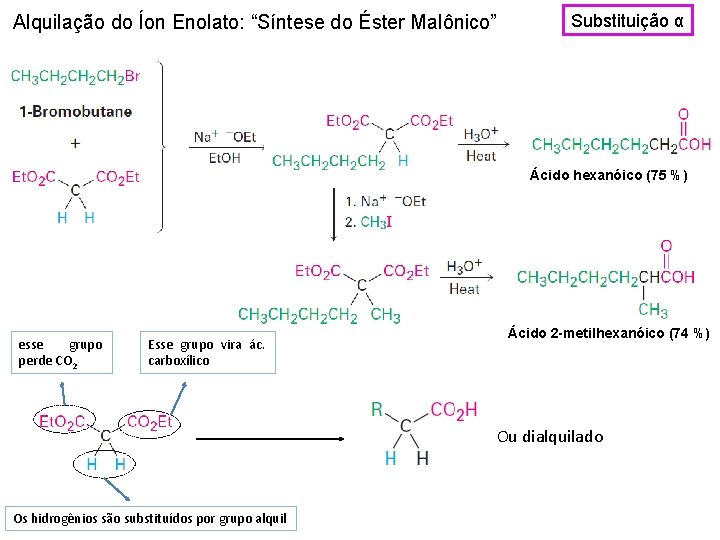
Alquilação do Íon Enolato: “Síntese do Éster Malônico” Substituição α Ácido hexanóico (75 %) esse grupo perde CO 2 Esse grupo vira ác. carboxílico Ácido 2 -metilhexanóico (74 %) Ou dialquilado Os hidrogênios são substituídos por grupo alquil
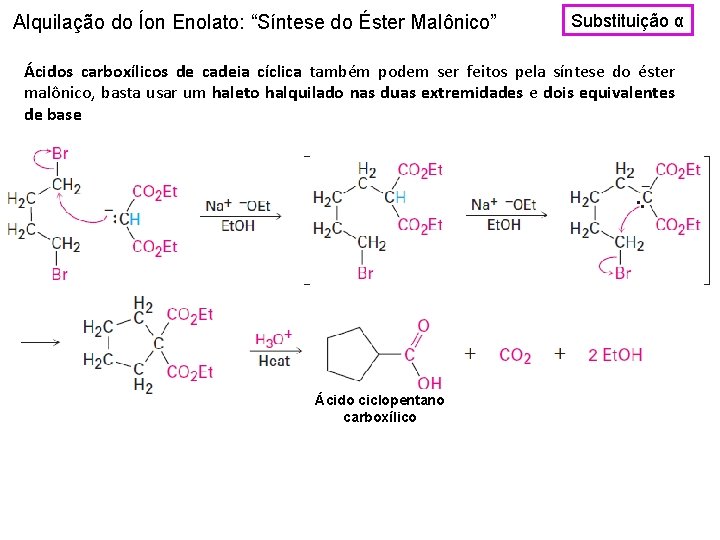
Alquilação do Íon Enolato: “Síntese do Éster Malônico” Substituição α Ácidos carboxílicos de cadeia cíclica também podem ser feitos pela síntese do éster malônico, basta usar um haleto halquilado nas duas extremidades e dois equivalentes de base Ácido ciclopentano carboxílico
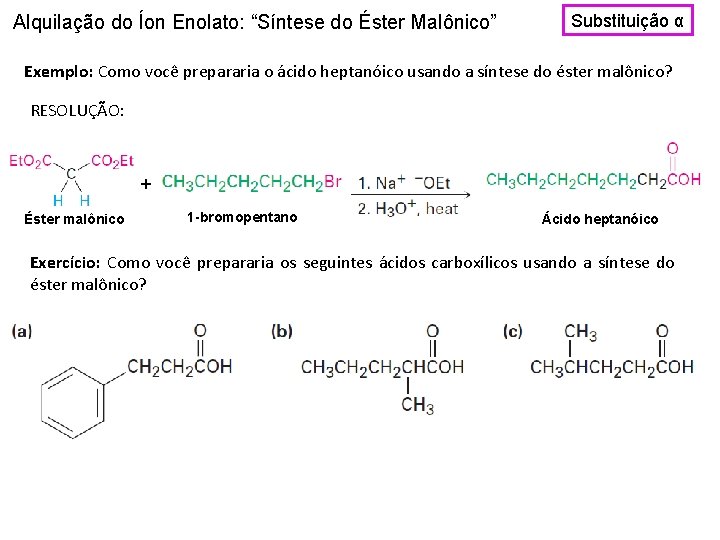
Alquilação do Íon Enolato: “Síntese do Éster Malônico” Substituição α Exemplo: Como você prepararia o ácido heptanóico usando a síntese do éster malônico? RESOLUÇÃO: + Éster malônico 1 -bromopentano Ácido heptanóico Exercício: Como você prepararia os seguintes ácidos carboxílicos usando a síntese do éster malônico?
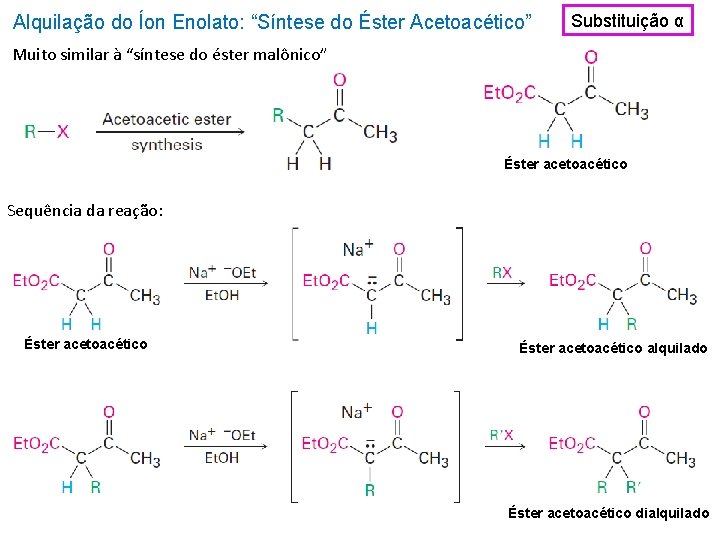
Alquilação do Íon Enolato: “Síntese do Éster Acetoacético” Substituição α Muito similar à “síntese do éster malônico” Éster acetoacético Sequência da reação: Éster acetoacético alquilado Éster acetoacético dialquilado
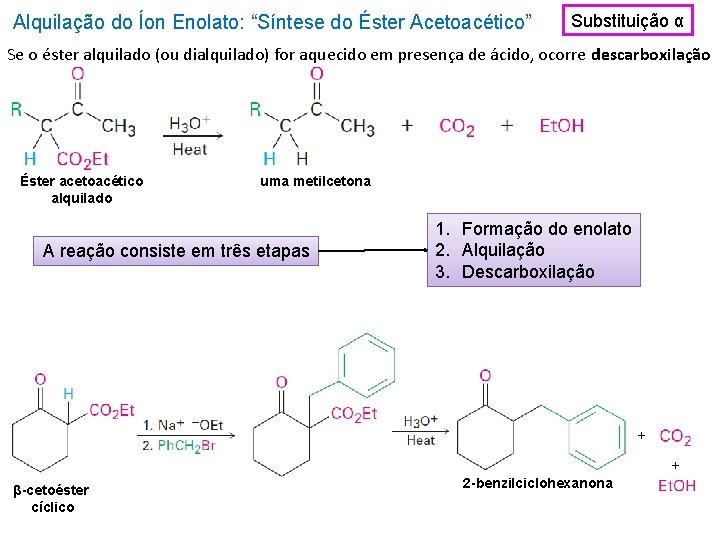
Alquilação do Íon Enolato: “Síntese do Éster Acetoacético” Substituição α Se o éster alquilado (ou dialquilado) for aquecido em presença de ácido, ocorre descarboxilação Éster acetoacético alquilado uma metilcetona A reação consiste em três etapas 1. Formação do enolato 2. Alquilação 3. Descarboxilação + + β-cetoéster cíclico 2 -benzilciclohexanona
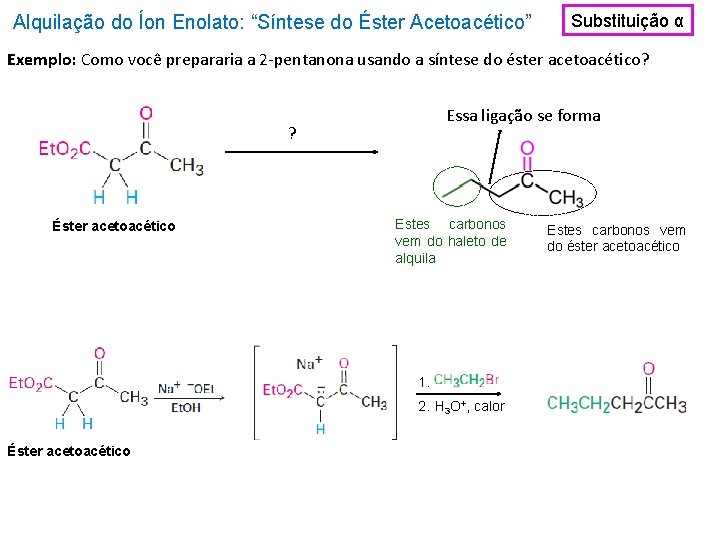
Alquilação do Íon Enolato: “Síntese do Éster Acetoacético” Substituição α Exemplo: Como você prepararia a 2 -pentanona usando a síntese do éster acetoacético? Essa ligação se forma ? Éster acetoacético Estes carbonos vem do haleto de alquila 1. 2. H 3 O+, calor Éster acetoacético Estes carbonos vem do éster acetoacético
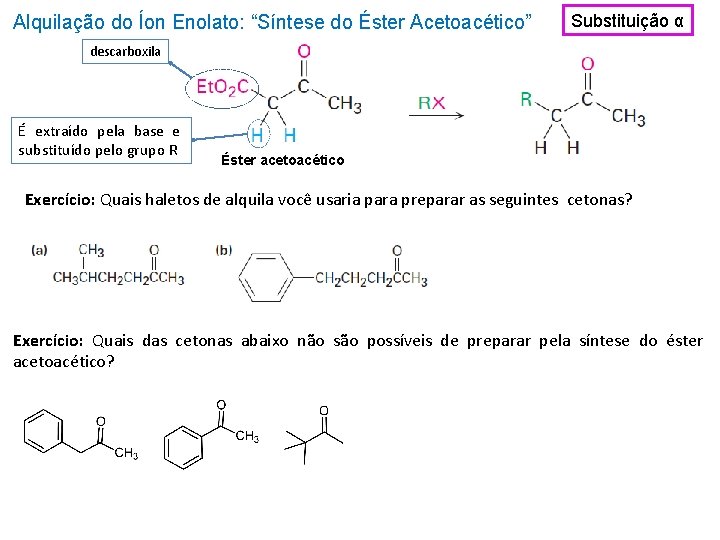
Alquilação do Íon Enolato: “Síntese do Éster Acetoacético” Substituição α descarboxila É extraído pela base e substituído pelo grupo R Éster acetoacético Exercício: Quais haletos de alquila você usaria para preparar as seguintes cetonas? Exercício: Quais das cetonas abaixo não são possíveis de preparar pela síntese do éster acetoacético?
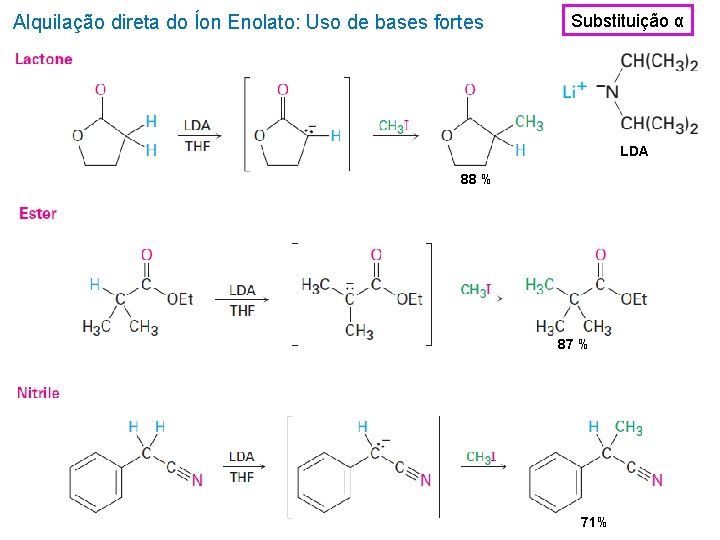
Alquilação direta do Íon Enolato: Uso de bases fortes Substituição α LDA 88 % 87 % 71%
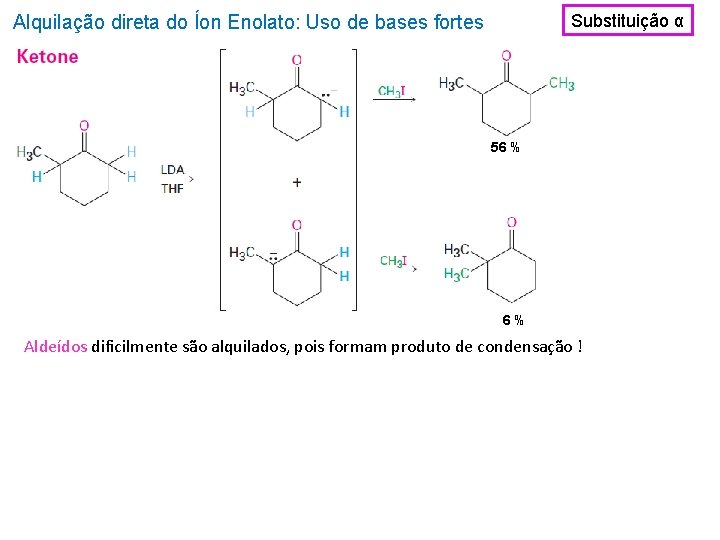
Substituição α Alquilação direta do Íon Enolato: Uso de bases fortes 56 % 6% Aldeídos dificilmente são alquilados, pois formam produto de condensação !
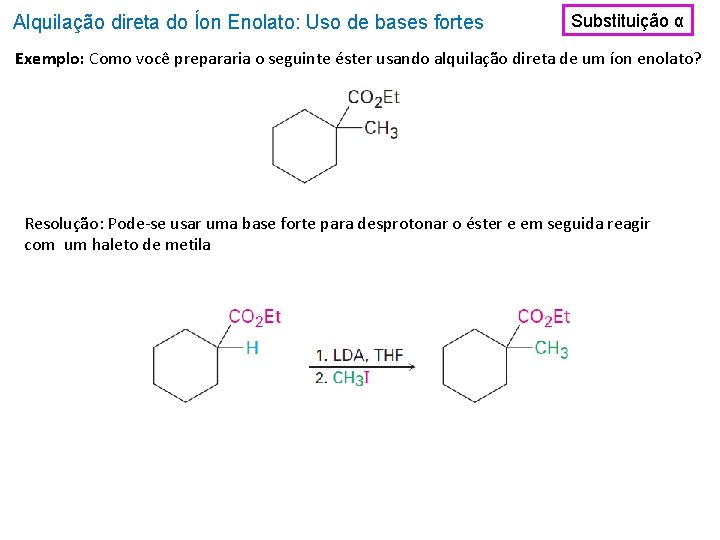
Alquilação direta do Íon Enolato: Uso de bases fortes Substituição α Exemplo: Como você prepararia o seguinte éster usando alquilação direta de um íon enolato? Resolução: Pode-se usar uma base forte para desprotonar o éster e em seguida reagir com um haleto de metila
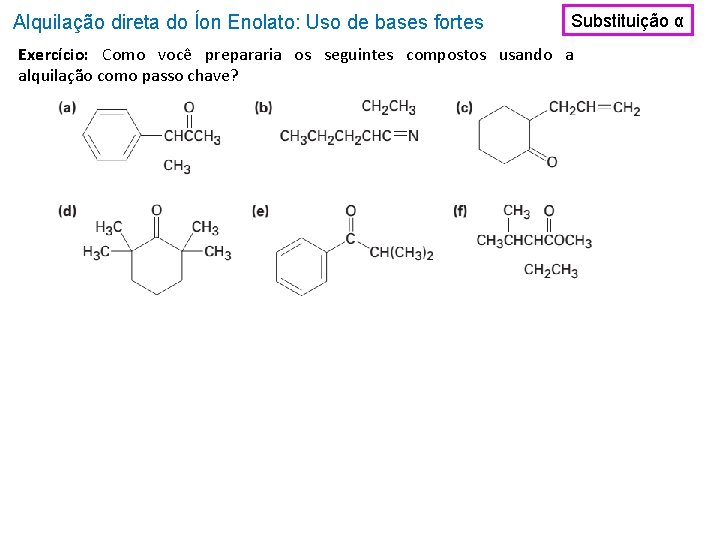
Alquilação direta do Íon Enolato: Uso de bases fortes Substituição α Exercício: Como você prepararia os seguintes compostos usando a alquilação como passo chave?
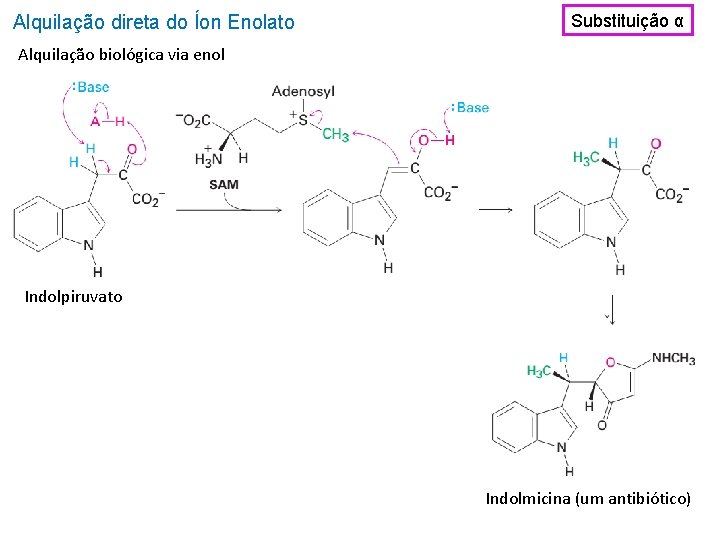
Alquilação direta do Íon Enolato Substituição α Alquilação biológica via enol Indolpiruvato Indolmicina (um antibiótico)
- Slides: 31