SUBST NCIAS E MISTURAS Sumrio Estrutura da matria

SUBST NCIAS E MISTURAS

Sumário Estrutura da matéria Elementos químicos Átomos e moléculas Substância química Misturas Soluções

ESTRUTURA DA MATÉRIA O termo matéria refere-se a todos os materiais ou coisas que compõem o universo. A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas chamadas de átomos.
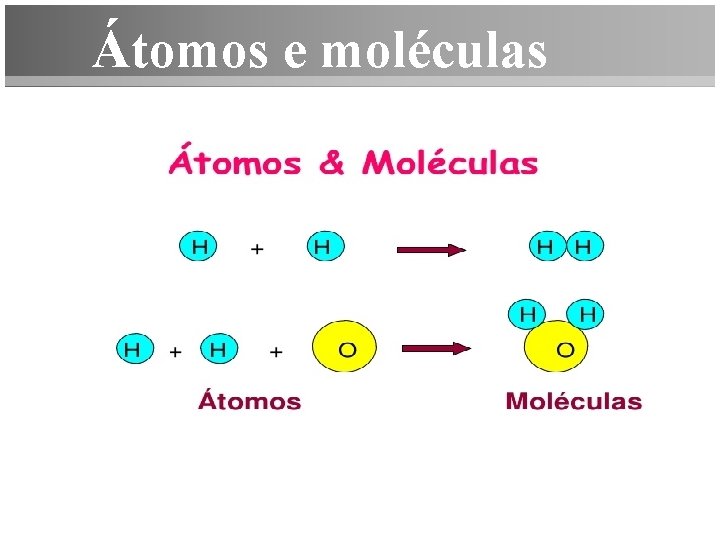
Átomos e moléculas

Substância química É uma porção de matéria que tem propriedades bem definidas e que lhe são característica.
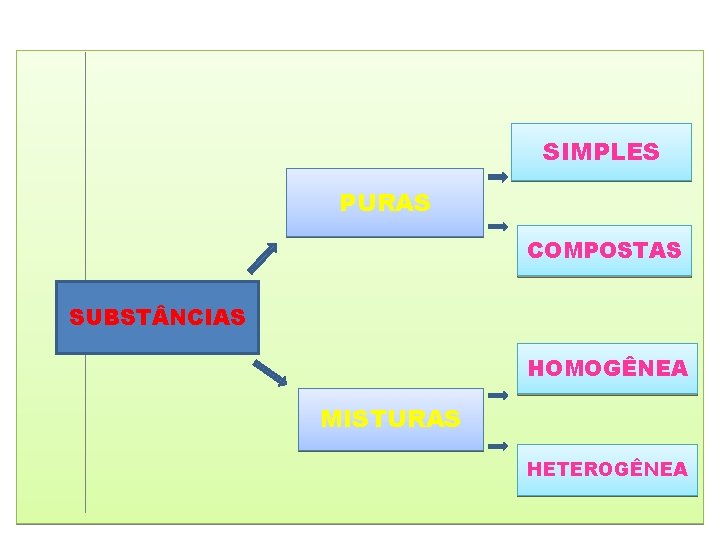
SIMPLES PURAS COMPOSTAS SUBST NCIAS HOMOGÊNEA MISTURAS HETEROGÊNEA
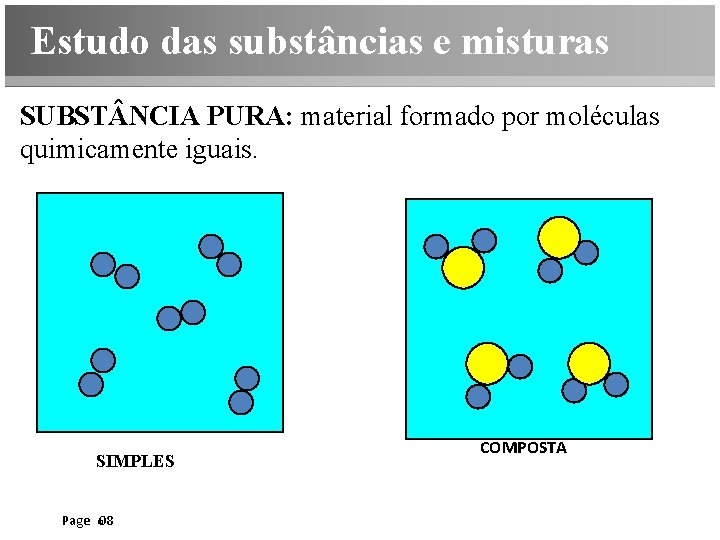
Estudo das substâncias e misturas SUBST NCIA PURA: material formado por moléculas quimicamente iguais. SIMPLES Page 08 COMPOSTA

Substância pura simples SUBST NCIA PURA SIMPLES: é constituída de uma molécula formada por átomos do mesmo elemento químico (mesmo tipo de átomo), como por exemplo o gás hidrogênio formado por dois átomos de hidrogênio ligados entre si; o ozônio formado por três átomos de oxigênio. Substância Fórmula Gás hidrogênio H 2 Gás oxigênio O 2 Gás ozônio O 3 Representação
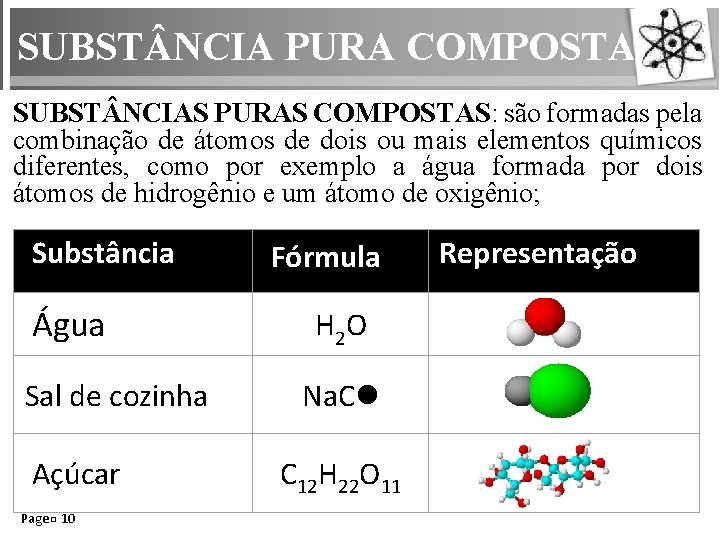
SUBST NCIA PURA COMPOSTA SUBST NCIAS PURAS COMPOSTAS: são formadas pela combinação de átomos de dois ou mais elementos químicos diferentes, como por exemplo a água formada por dois átomos de hidrogênio e um átomo de oxigênio; Substância Água Sal de cozinha Açúcar Page 10 Fórmula H 2 O Na. Cl C 12 H 22 O 11 Representação

Mistura É formada por duas, ou mais, substâncias, sendo cada uma destas denominada componente. CLASSIFICAÇÃO DAS MISTURAS Fase: em uma mistura, é cada uma das porções que apresenta aspecto homogêneo ou uniforme. Mistura homogênea: toda mistura que apresenta uma única fase. Mistura heterogênea: toda mistura que apresenta pelo menos duas fases.
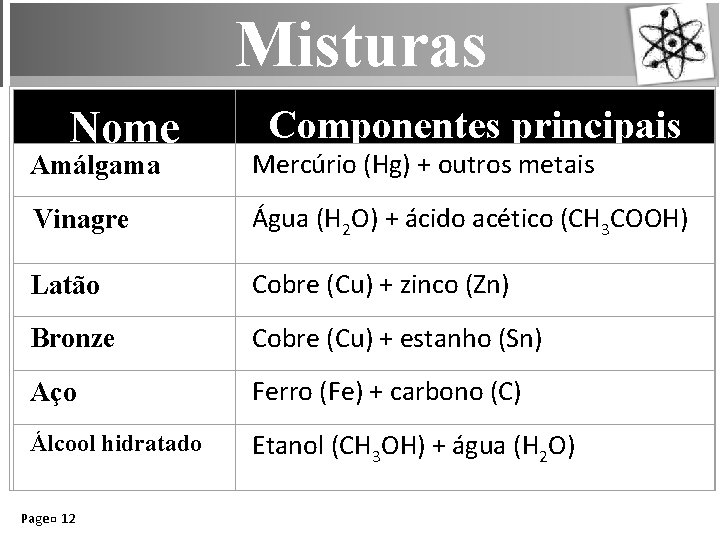
Misturas Nome Componentes principais Amálgama Mercúrio (Hg) + outros metais Vinagre Água (H 2 O) + ácido acético (CH 3 COOH) Latão Cobre (Cu) + zinco (Zn) Bronze Cobre (Cu) + estanho (Sn) Aço Ferro (Fe) + carbono (C) Álcool hidratado Etanol (CH 3 OH) + água (H 2 O) Page 12

Misturas • A matéria encontrada na natureza, na sua grande maioria, é formada por duas ou mais substâncias puras, portanto são misturas. • Uma maneira de classificar as misturas baseia-se em a sua composição ser uniforme, isto é, a mesma em qualquer zona da amostra, ou não. • Por exemplo, uma garrafa de álcool (etanol) tem sempre uma certa porção de água misturada; estas duas substâncias estão bem misturadas uma com a outra que não se pode dizer que a água está num lado e o álcool de outro, ou seja, a composição da mistura é a mesma em qualquer zona da garrafa - mistura homogênea. • Já o mesmo não acontece com uma mistura de água e areia; a areia fica em baixo separada da água. A composição desta mistura não é uniforme - mistura heterogênea.
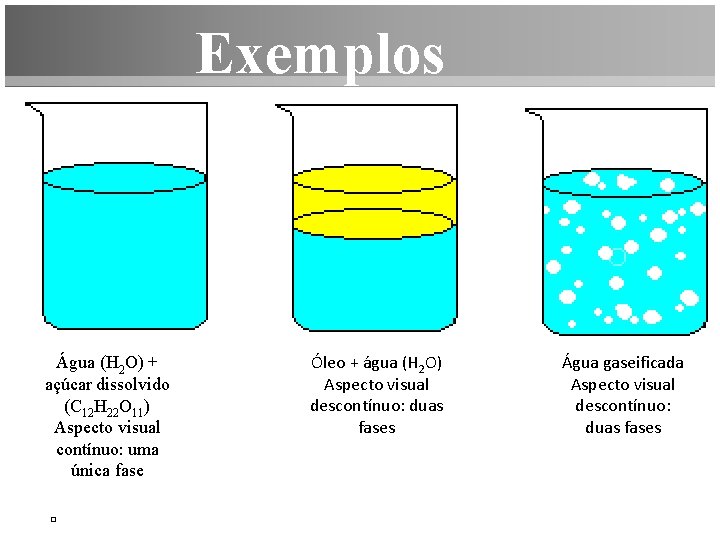
Exemplos Água (H 2 O) + açúcar dissolvido (C 12 H 22 O 11) Aspecto visual contínuo: uma única fase Óleo + água (H 2 O) Aspecto visual descontínuo: duas fases Água gaseificada Aspecto visual descontínuo: duas fases

Misturas Homogêneas e Heterogêneas SITEMA: É UMA PORÇÃO DE MATÉRIA ESCOLHIDA PARA SER ESTUDADA. OBSERVE A FIGURA E RESPONDA: 1) SÃO SUBST NCIAS PURAS (SIMPLES OU COMPOSTAS) OU MISTURAS (HOMOGÊNEA OU HETEROGÊNEA)? 2) QUANTAS FASES EXTENTES?

Misturas • É a união de duas ou mais substâncias químicas. • Uma das formas de diferenciação das substâncias puras e das misturas é através da temperatura, durante as mudanças de estado físico.
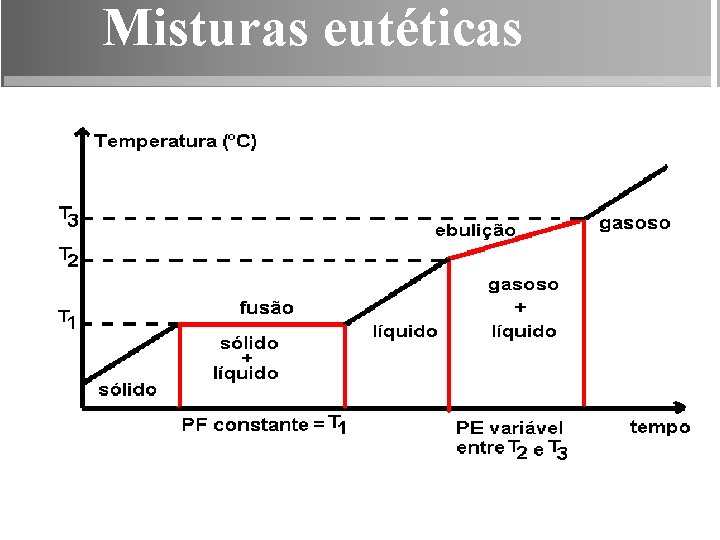
Misturas eutéticas
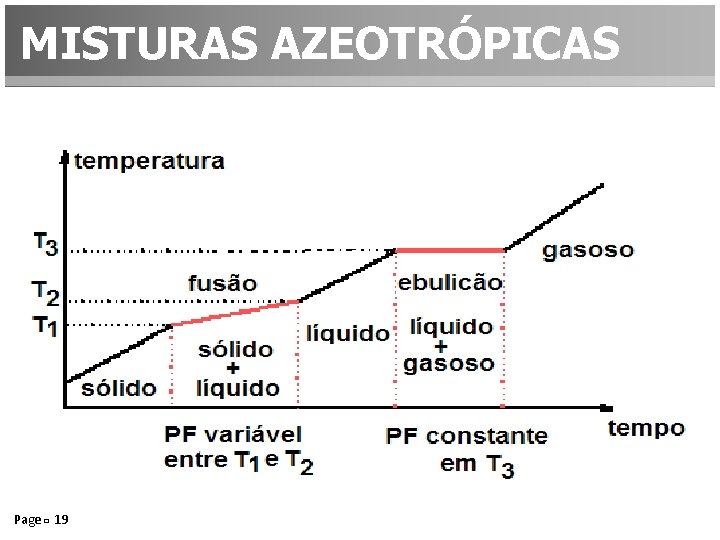
MISTURAS AZEOTRÓPICAS Page 19
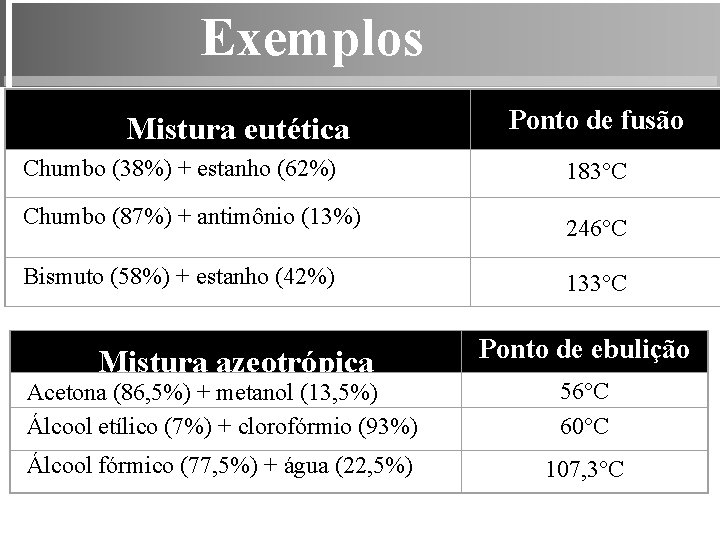
Exemplos Mistura eutética Ponto de fusão Chumbo (38%) + estanho (62%) 183°C Chumbo (87%) + antimônio (13%) 246°C Bismuto (58%) + estanho (42%) 133°C Mistura azeotrópica Ponto de ebulição Acetona (86, 5%) + metanol (13, 5%) Álcool etílico (7%) + clorofórmio (93%) 56°C 60°C Álcool fórmico (77, 5%) + água (22, 5%) 107, 3°C

Fases • Fases são as diferentes porções homogêneas, limitadas por superfícies de separação, que constituem um sistema heterogêneo. • Os sistemas homogêneos são monofásicos ou unifásicos. Os sistemas heterogêneos são polifásicos, podendo ser bifásicos, trifásicos, etc. • Sistema com n componentes sólidos como regra tem n fases. Sistema com n gases sempre tem uma única fase. Não existe sistema heterogêneo de dois ou mais gases. • Sistema heterogêneo ou é uma mistura (heterogênea) ou é uma substância pura em mudança de estado físico. • Sistema homogêneo ou é uma mistura (homogênea) ou é uma substância pura num único estado físico Page 21

Soluções Por quê um ovo cru incha ou murcha quando colocado em diferentes soluções?
Soluções Uma solução é uma mistura HOMOGÊNEA de 2 ou mais substâncias em uma única fase. Um dos constituintes é o SOLVENTE os outros são os SOLUTOS.

Separação de Misturas Ø Na natureza, raramente encontramos substâncias puras. Em função disso, é necessário usarmos métodos de separação para obtermos determinada substância. Ø Na separação dos componentes de uma mistura (obtenção separada de cada uma das substâncias puras que deram origem à mistura) usa-se um conjunto de processos físicos denominados análise imediata. Ø Esses processos não alteram a composição das substâncias que formam a mistura. Ø Nem sempre apenas um método de separação é suficiente para separar todos os componentes de uma mistura. Page 23

Separação de Misturas Ø A escolha dos melhores métodos para a separação de misturas exige um conhecimento anterior de algumas das propriedades das substâncias presentes. Ø Assim, se tivermos uma mistura de açúcar com areia, é útil sabermos que o açúcar se dissolve na água, enquanto a areia não. Ø Muitas vezes, dependendo da complexidade da mistura, será necessário usar vários processos diferentes em uma sequência baseada nas propriedades das substâncias presentes na mistura.

Separação de Misturas SÓLIDO – SÓLIDO: - Catação - Ventilação - Levigação - Separação magnética - Cristalização fracionada - Dissolução fracionada - Sublimação • SÓLIDO – LÍQUIDO: – Decantação – Centrifugação – Filtração simples – Filtração à vácuo • LÍQUIDO – LÍQUIDO: – Decantação • GÁS – SÓLIDO: – Decantação – Filtração

Separação de Misturas SÓLIDO – SÓLIDO:

Separação de Misturas heterogênea Ø Catação: método utilizado para separar misturas heterogêneas de sólido – sólido, onde é necessário que os componentes da mistura sejam aparentemente distintos. Um exemplo é a catação de pedra no feijão, onde se retira, catando, as pedras, que são diferentes do feijão.

Separação de Misturas heterogênea Ø Peneiração: Método de separação para sistemas sólido, no qual o sólido menos denso é arrastado por uma corrente de ar. Ø Um bom exemplo é a separação das cascas de grãos de arroz, amendoim torrado, etc.

Separação de Misturas heterogênea Ø Levigação: A água corrente arrasta o componente menos denso e o mais denso deposita-se no fundo do recipiente. Ø É usada, por exemplo, para separar areia e ouro: a areia é menos densa e, por isso, é arrastada pela água corrente; o ouro, por ser mais denso, permanece no fundo da bateia.

Separação de Misturas heterogênea Ø Separação Magnética: Também chamado de Imantação, nesse método de separação, um dos sólidos é atraído por um ímã. Ø Esse processo é usado em larga escala para separar alguns minérios de ferro de suas impurezas, como, por exemplo, separar do lixo objetos de metal que serão reciclados. Outro exemplo simples é a separação de linha e agulha através de um imã.

Separação de Misturas heterogênea Ø Cristalização fracionada: A mistura de sólidos é dissolvida em água e a solução é submetida à evaporação. Quando a solução ficar saturada em relação à um componente, o prosseguimento da evaporação do solvente acarretará a cristalização gradativa do referido componente, que se separará da solução. A solução, contendo o componente cuja saturação ainda não foi atingida, fica sobre os cristais do outro e é chamada água-mãe de cristalização.
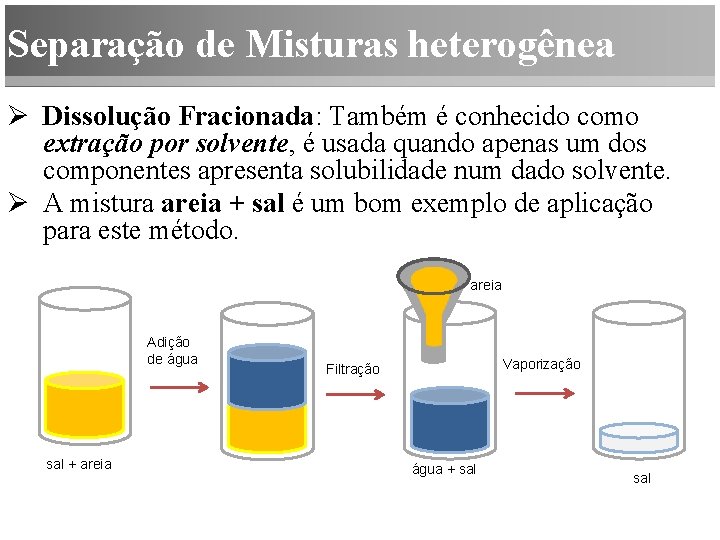
Separação de Misturas heterogênea Ø Dissolução Fracionada: Também é conhecido como extração por solvente, é usada quando apenas um dos componentes apresenta solubilidade num dado solvente. Ø A mistura areia + sal é um bom exemplo de aplicação para este método. areia Adição de água sal + areia Vaporização Filtração água + sal

Separação de Misturas heterogênea Ø Sublimação: Usado quando apenas um dos sólidos sublima (passa para o estado gasoso) quando aquecido. Ø São substâncias que podem ser separadas por sublimação: iodo, enxofre e naftaleno (naftalina). Ø Mais recentemente, tal propriedade passou a ser usada na impressão de camisetas. Ø Com uma impressora especial é preparado um desenho em uma folha de papel e, através de uma prensa térmica, a tinta sublima e se transfere para o tecido. Ø Tem a vantagem de não desbotar, mantendo a tonalidade original.

Separação de Misturas SÓLIDO – LÍQUIDO:

Separação de Misturas heterogênea Sedimentação ou decantação: Separação de dois ou mais componentes devido à diferença de densidade, seguida do escoamento da fase líquida.

Separação de Misturas GÁS – SÓLIDO:
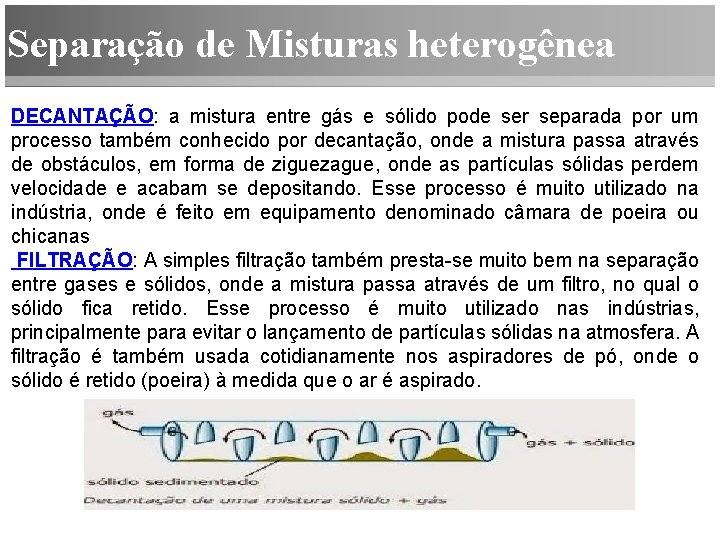
Separação de Misturas heterogênea DECANTAÇÃO: a mistura entre gás e sólido pode ser separada por um processo também conhecido por decantação, onde a mistura passa através de obstáculos, em forma de ziguezague, onde as partículas sólidas perdem velocidade e acabam se depositando. Esse processo é muito utilizado na indústria, onde é feito em equipamento denominado câmara de poeira ou chicanas FILTRAÇÃO: A simples filtração também presta-se muito bem na separação entre gases e sólidos, onde a mistura passa através de um filtro, no qual o sólido fica retido. Esse processo é muito utilizado nas indústrias, principalmente para evitar o lançamento de partículas sólidas na atmosfera. A filtração é também usada cotidianamente nos aspiradores de pó, onde o sólido é retido (poeira) à medida que o ar é aspirado.
- Slides: 36