STRUTTURA 3 D ENZIMI RNA polimerasi Piruvato carbossilasi
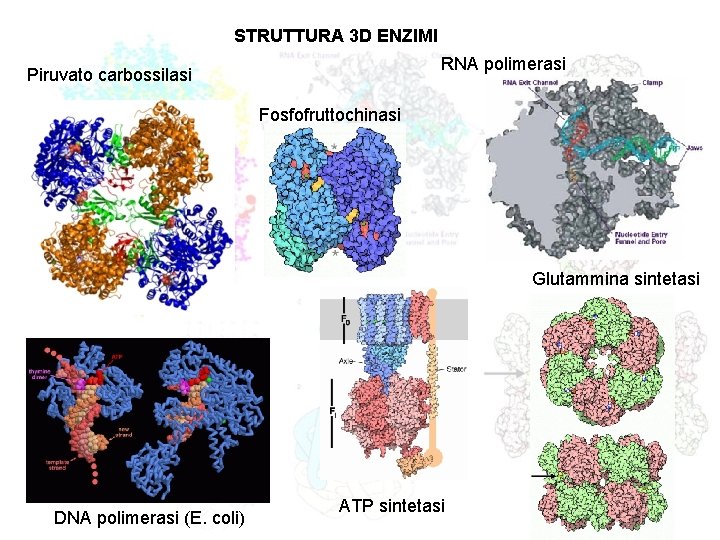
STRUTTURA 3 D ENZIMI RNA polimerasi Piruvato carbossilasi Fosfofruttochinasi Glutammina sintetasi DNA polimerasi (E. coli) ATP sintetasi

CLASSIFICAZIONE ENZIMI Alcuni tra i principali meccanismi di catalisi enzimatica: • acido base • covalente • elettrostatica e da ione metallico
Effetto del mezzo sulla velocità delle reazioni catalizzate da enzimi: temperatura, forza ionica e p. H Le proteine, quindi anche gli enzimi, hanno conformazioni 3 D complesse strettamente legate alla loro funzionalità: le strutture secondaria e terziaria sono dovute ad interazioni deboli tra atomi coinvolti nel legame peptidico e tra i gruppi –R degli AA costituenti ( idrofobiche, elettrostatiche, legami idrogeno, forze van Der Waals), in relazione al mezzo acquoso e all’ambiente. Vengono studiate le interazioni tra enzimi, proteine, e il mezzo. Queste interazioni stabilizzano o meno la struttura dell’enzima in studio, influenzando la catalisi. Temperatura Forza ionica p. H Saggio enzimatico in vitro: concentrazioni di sali e p. H del tampone di dosaggio; temperatura di dosaggio – parametri che devono essere standardizzati.
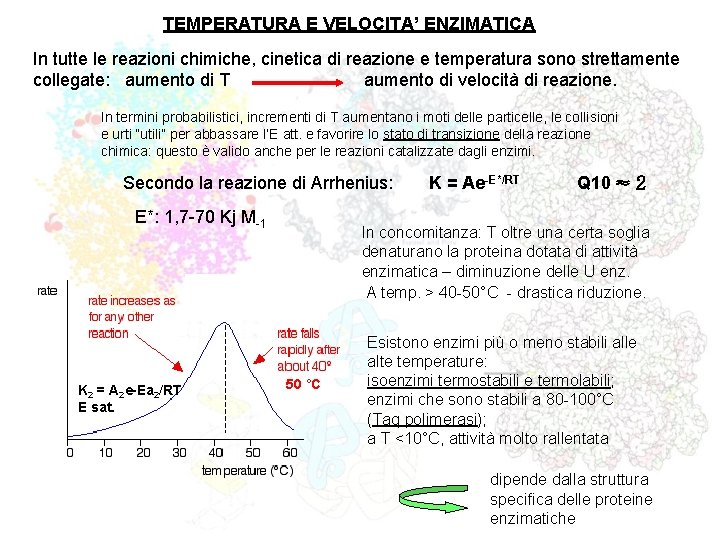
TEMPERATURA E VELOCITA’ ENZIMATICA In tutte le reazioni chimiche, cinetica di reazione e temperatura sono strettamente collegate: aumento di T aumento di velocità di reazione. In termini probabilistici, incrementi di T aumentano i moti delle particelle, le collisioni e urti “utili” per abbassare l’E att. e favorire lo stato di transizione della reazione chimica: questo è valido anche per le reazioni catalizzate dagli enzimi. Secondo la reazione di Arrhenius: E*: 1, 7 -70 Kj M-1 K 2 = A 2 e-Ea 2/RT E sat. K = Ae-E*/RT Q 10 ≈ 2 In concomitanza: T oltre una certa soglia denaturano la proteina dotata di attività enzimatica – diminuzione delle U enz. A temp. > 40 -50°C - drastica riduzione. 50 °C Esistono enzimi più o meno stabili alle alte temperature: isoenzimi termostabili e termolabili; enzimi che sono stabili a 80 -100°C (Taq polimerasi); a T <10°C, attività molto rallentata dipende dalla struttura specifica delle proteine enzimatiche

SALI E VELOCITA’ ENZIMATICA In generale: effetto simile a quello dato dalla concentrazione di sali sulle macromolecole biologiche e, in particolare, le proteine: la solubilità di una proteina a bassa forza ionica aumenta con l’aumentare della forza ionica (salting in). Ad alta forza ionica, la proteina precipita, si separa dal mezzo acquoso (salting out). Forza ionica, I = ½ cizi 2 -Gli ioni dei sali sciolti in una soluzione acquosa interferiscono con i legami a idrogeno tra H 2 O (mezzo acquoso) e proteine : modificano le interazioni intramolecolari che stabilizzano le proteine, quindi la loro conformazione e/o solubilità: -Ioni “cosmotropici” o stabilizzanti (Cl-, Br-): aumentano e stabilizzano le interazioni H 2 O-enzima; aumentano la solubilità nel mezzo acquoso. Ad alte concentrazioni ammonio solfato, salting-out, proteine non denaturate. Effetti relativi che dipendono dal tipo di sale (specie ionica) , dal tipo di proteina- principio base della precipitazione frazionata -Ioni “chaotropici” o denaturanti (Cl. O 4 -; SCN-): alterano le interazioni H 2 O-enzima (proteina) sottraggono H 2 O all’enzima e quindi ne diminuiscono la solubilità ma ne alterano anche la conformazione 3 D (denaturanti).
![p. H E VELOCITA’ ENZIMATICA La [H+] può influire significativamente sulla catalisi enzimatica. Un p. H E VELOCITA’ ENZIMATICA La [H+] può influire significativamente sulla catalisi enzimatica. Un](http://slidetodoc.com/presentation_image_h2/f6e712d2b4d10c54845154a90bb49069/image-6.jpg)
p. H E VELOCITA’ ENZIMATICA La [H+] può influire significativamente sulla catalisi enzimatica. Un enzima proteico è suscettibile sia ai cambiamenti conformazionali legati al grado di ionizzazione e carica, a diversi p. H, dei gruppi –R ionizzabili degli AA che lo compongono sia al grado di protonazione di gruppi –R ionizzabili presenti sul sito attivo e determinanti per la catalisi enzimatica. A p. H estremi le proteine perdono la conformazione 3 D , precipitano e quindi molti enzimi si denaturano. Esempio: Se un enzima esplica la sua azione catalitica grazie alla presenza di un’ istidina e di una Lisina nel sito attivo svolgendo un attacco nucleofilo sul substrato in trasformazione oppure se un altro enzima trasforma S in P mediante un’interazione di tipo elettrostatico attraverso un aspartato o una lisina, opportunamente dislocati sul sito attivo, comprendiamo subito che il grado di protonazione dei gruppi in gioco alterano la catalisi: esisteranno solo stretti intervalli di p. H permettere l’interazione ES ottimale. Forma attiva dell’enzima a intervalli di p. H che vengono definiti sperimentalmente. Esistono intervalli di p. H ottimale. Il p. H influenza i parametri cinetici Vmax e Km dell’enzima e può variare anche lo stato di ionizzazione del substrato S e di eventuali coenzimi.
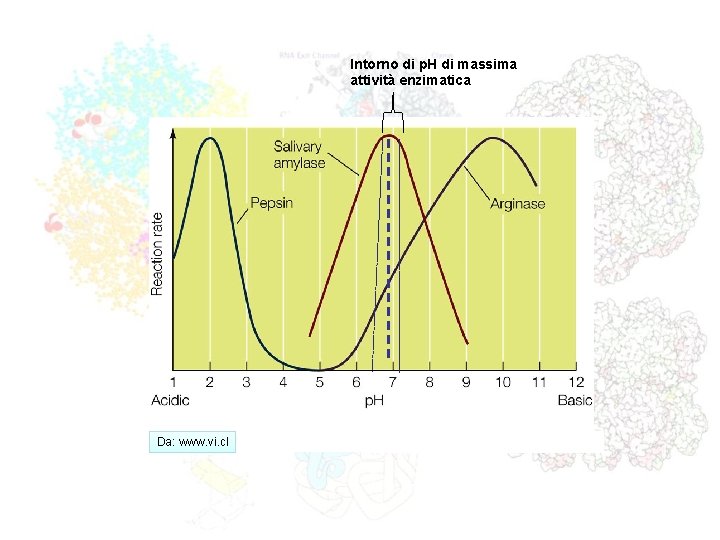
Intorno di p. H di massima attività enzimatica Da: www. vi. cl
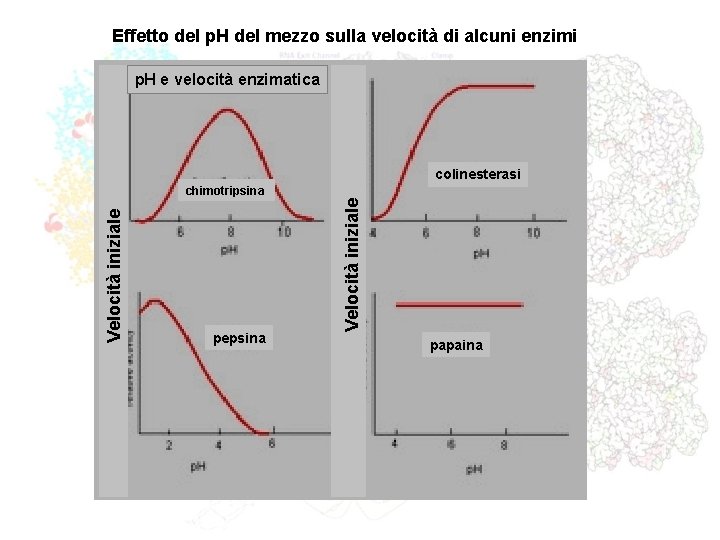
Effetto del p. H del mezzo sulla velocità di alcuni enzimi p. H e velocità enzimatica colinesterasi pepsina Velocità iniziale chimotripsina papaina
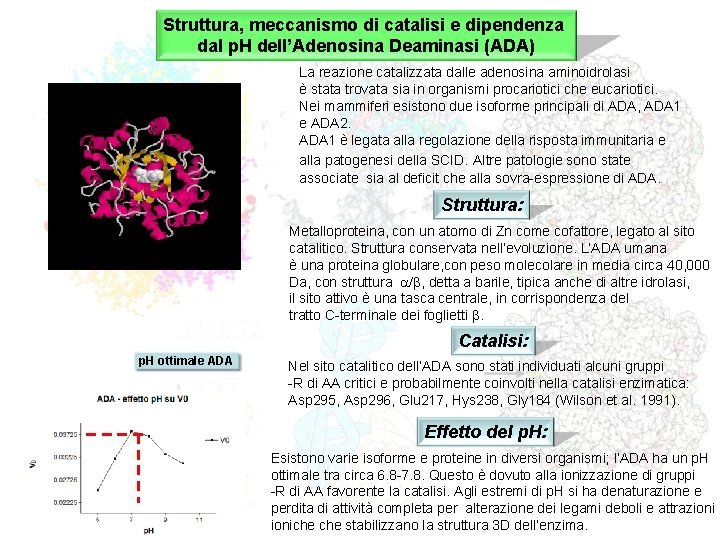
Struttura, meccanismo di catalisi e dipendenza dal p. H dell’Adenosina Deaminasi (ADA) La reazione catalizzata dalle adenosina aminoidrolasi è stata trovata sia in organismi procariotici che eucariotici. Nei mammiferi esistono due isoforme principali di ADA, ADA 1 e ADA 2. ADA 1 è legata alla regolazione della risposta immunitaria e alla patogenesi della SCID. Altre patologie sono state associate sia al deficit che alla sovra-espressione di ADA. Struttura: Metalloproteina, con un atomo di Zn come cofattore, legato al sito catalitico. Struttura conservata nell’evoluzione. L’ADA umana è una proteina globulare, con peso molecolare in media circa 40, 000 Da, con struttura a/b, detta a barile, tipica anche di altre idrolasi, il sito attivo è una tasca centrale, in corrispondenza del tratto C-terminale dei foglietti b. Catalisi: p. H ottimale ADA Nel sito catalitico dell’ADA sono stati individuati alcuni gruppi -R di AA critici e probabilmente coinvolti nella catalisi enzimatica: Asp 295, Asp 296, Glu 217, Hys 238, Gly 184 (Wilson et al. 1991). Effetto del p. H: Esistono varie isoforme e proteine in diversi organismi; l’ADA ha un p. H ottimale tra circa 6. 8 -7. 8. Questo è dovuto alla ionizzazione di gruppi -R di AA favorente la catalisi. Agli estremi di p. H si ha denaturazione e perdita di attività completa per alterazione dei legami deboli e attrazioniche stabilizzano la struttura 3 D dell’enzima.

Riepilogo Esercitazioni Enzimi Saggio enzimatico in condizioni saturanti della LDH in surnatante di omogenato di tessuto muscolare e in siero (confronto): Valutazione della concentrazione di LDH serica e muscolare, UE/ml nei due campioni a confronto. (UE/100 ml) – UI: UE/lt. Substrato: sodio piruvato Coenzima : NADH Tampone fosfato p. H 7, temperatura e forza ionica costanti; Enzima a concentrazione costante, campione diluito opportunamente. Lettura 340 nm (NADH) per 2 min, calcolo ΔA/min e UE per volume. Att. Specifica: UE/mg proteine totali Determinazione dei parametri cinetici Km e Vmax dell’enzima ADA: Calcolo della V 0 a varie concentrazioni di S (adenosina) sia al di sotto che al di sopra della Km attesa. S (adenosina) a concentrazioni crescenti: 5, 10, 20, 40, 60, 80 m. M. Tampone fosfato p. H 7, temperatura e forza ionica costanti; Enzima alla stessa concentrazione in tutto il dosaggio: costante. Lettura 265 nm (adenosina, no inosina). Dipendenza dal p. H della V 0 dell’ADA: Calcolo della V 0 a p. H variabile nel mezzo. Substrato a concentrazione costante S ≈ Km, 40 m. M; V 0= Vmax/2 Tampone fosfato a p. H variabile: p. H 5, 6, 7, 8, 9, 10. Temperatura e forza ionica costanti; Enzima a concentrazione costante. Lettura 265 nm (adenosina, no inosina).
- Slides: 10