Struktura ltek a stavba hmoty STAVBA HMOTY zkladn

Struktura látek a stavba hmoty

STAVBA HMOTY základní údaje o charakterů atomů a vnitřní stavbě dle vědeckých výzkumů z konce 19. a počátku 20. stol. - průchod el. proudu zředěnými plyny, - radioaktivita, - spektrální analýza § atomy složeny z elementárních (základních) částic společné všem prvkům § poznání struktury atomu – vliv na klasifikaci prvků z hlediska period. zákona – odhalení vnitřních příčin periodického opakování vlastností prvků – základ pro vybudování moderní teorie chemické vazby a struktury látek
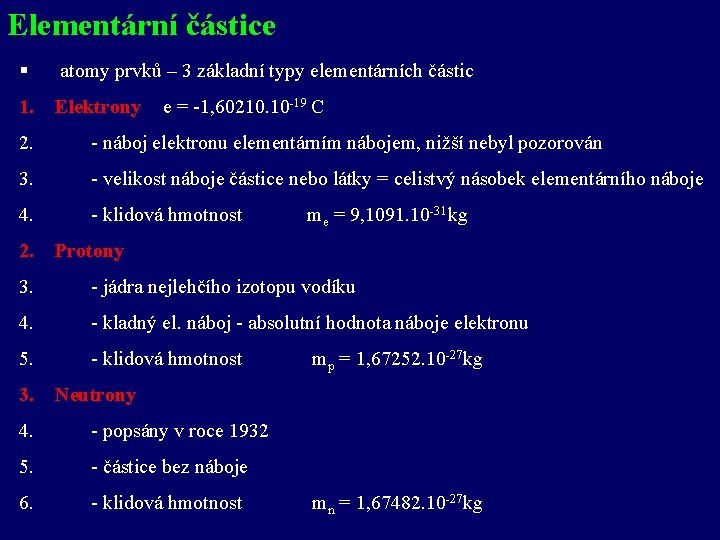
Elementární částice § atomy prvků – 3 základní typy elementárních částic 1. Elektrony e = -1, 60210. 10 -19 C 2. - náboj elektronu elementárním nábojem, nižší nebyl pozorován 3. - velikost náboje částice nebo látky = celistvý násobek elementárního náboje 4. - klidová hmotnost 2. me = 9, 1091. 10 -31 kg Protony 3. - jádra nejlehčího izotopu vodíku 4. - kladný el. náboj - absolutní hodnota náboje elektronu 5. - klidová hmotnost 3. mp = 1, 67252. 10 -27 kg Neutrony 4. - popsány v roce 1932 5. - částice bez náboje 6. - klidová hmotnost mn = 1, 67482. 10 -27 kg

Ostatní částice Lehké částice, leptony - neutrino, positron, elektron Středně těžké částice, mezony - π a K Težké částice, baryony - proton, neutron a hyperony Kvantová mechanika – popis jevů v atomovém měřítku 1. Energie mikročástic je kvantována (např. energie elektronu v atomu) 2. - může nabývat pouze určitých hodnot na rozdíl od makroskopických těles (spojitě) 2. Pro mikročástice je charakteristický korpuskulárně vlnový dualismus 3. (chovají se jako korpuskule nepatrných rozměrů nebo jako vlnění) 3. - princip neurčitosti – nelze současně určit polohu a hybnost mikročástic (pouze pravděpodobnost výskytu)

Atomy § základní stavební částice látek § sloučení atomů – molekuly § jádro (kladný náboj) + obal (záporný náboj, v absolutní hodnotě = náboji jádra) § atomy jsou navenek elektroneutrální § jádro = protony + neutrony - prakticky veškerá hmotnost koncentrována v jádře i přes relativně malé rozměrové zastoupení v atomu Protonové (atomové) číslo Z: levý dolní index, počet protonů, základní veličinou charakterizující atom, určuje pořadí (postavené) v Mendělejově per. s. p. Nukleonové (hmotnostní) číslo A: levý horní index, součet protonů a neutronů (souhrnně označovány jako nukleony) Neutronové číslo N: počet neutronů v jádře, odečtením počtu protonů Z od součtu nukleonů A

Nuklidy, izotopy a izobary - chemický prvek je vždy tvořen souborem atomů mající stejný počet protonů (Z) - v přírodě prvky směsí izotopů (izotopických nuklidů) lišící se počtem neutronů Nuklidy soubory totožných atomů mající shodné trojice čísel Z, A a N, např soubor atomů 32 S 16 Izotopické nuklidy - nuklidy příslušející témuž prvku, tedy se shodným počtem protonů (Z) 84 Sr, 86 Sr, 87 Sr 38 Izobarické nuklidy (izobary) - nuklidy mající stejné nukleonové číslo 40 K, 40 Ca 19 20 Vazebná energie jádra - jádro = protony + neutrony, hmotnost jádra není přesný součet hmotností - při vzniku jádra z volných nukleonů se uvolňuje energie, která se vyzáří (v opačném případě nutno dodat) - uvolněná energie je získána na úkor hmotnosti vzniklého jádra 38 38
- Slides: 6