Struktura i ewolucja genomw rolinnych Liczba chromosomw Metody

Struktura i ewolucja genomów roślinnych

Liczba chromosomów • Metody ustalania: analiza w mikroskopie świetlnym gniecionych preparatów komórek. • Rośliny nasienne: od 2 n=4 (np. Haplopappus gracilis) USA do 2 n=ok. 600 (Voanioala gerardii) Madagaskar • •
Rozmiar genomów Metody ustalania: Kinetyka reasocjacji DNA; Pomiary objętości jądra komórkowego; Oceny na podstawie próbek klonów z bibliotek genomowych; Mikrodesytometria jąder po barwieniu odcz. Feulgena; Cytometria przepływowa izolowanych jąder po barwieniu jodkiem propidyny. • • Na podstawie analiz >2800 gatunków roślin nasiennych: Haploidalny genom od 0. 1 pg do 125 pg. Ok. 50% roślin kwiatowych: 0. 1 – 3. 5 pg. Arabidopsis 125 Mb DNA – Fritillaria assyriaca – 120 000 Mb. • (Szachownica lisia) • Różnice także miedzy gatunkami z jednej rodziny: np. Poaceae (Wiechlinowate, d. trawy) : 450 Mb (ryż), 750 Mb (sorgo), 2500 Mb (kukurydza), 5000 Mb (jęczmień), 16 000 Mb (pszenica)
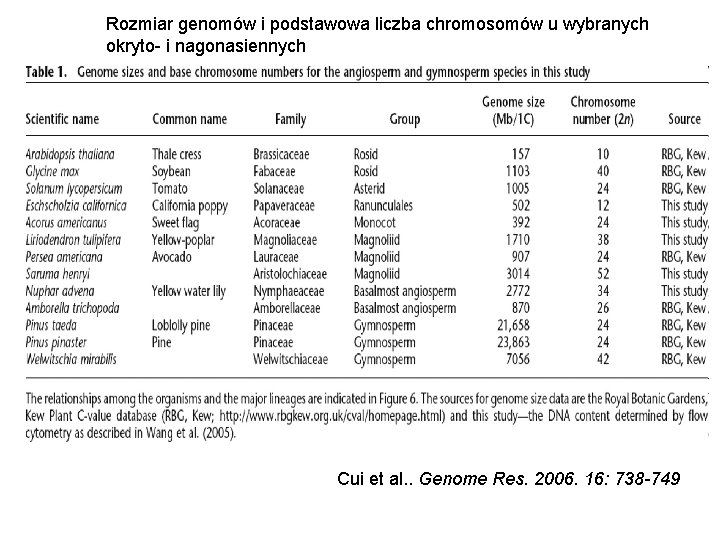
Rozmiar genomów i podstawowa liczba chromosomów u wybranych okryto- i nagonasiennych Cui et al. . Genome Res. 2006. 16: 738 -749

Poliploidy - wnioski na podstawie analizy kariotypów • 50 -70% roślin kwiatowych przeszło podwojenie liczby chromosomów co najmniej raz w swojej historii ewolucyjnej. • Poliploidy częste wśród roślin użytkowych: pszenica, rzepak, ziemniak, bawełna. • Autopoliploidy (ten sam gatunek) i allopolidy (hybrydy miedzygat. )
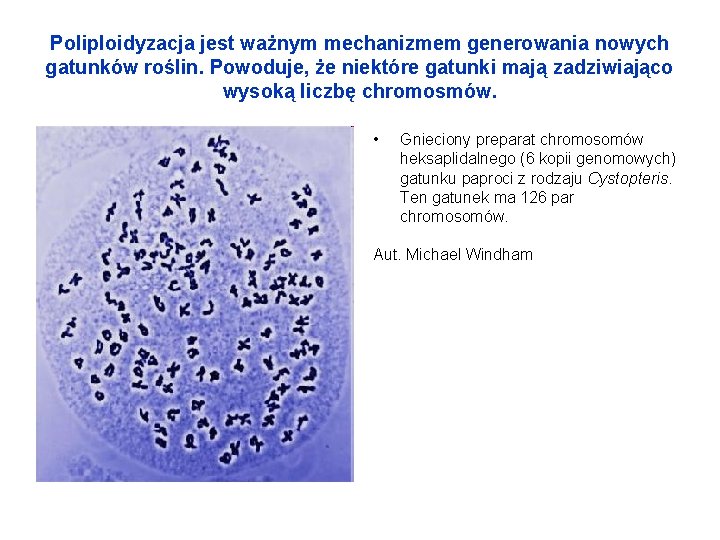
Poliploidyzacja jest ważnym mechanizmem generowania nowych gatunków roślin. Powoduje, że niektóre gatunki mają zadziwiająco wysoką liczbę chromosmów. • Gnieciony preparat chromosomów heksaplidalnego (6 kopii genomowych) gatunku paproci z rodzaju Cystopteris. Ten gatunek ma 126 par chromosomów. Aut. Michael Windham

Paradoks wartości C i jego przyczyny • Genomy eukariotyczne mają bardzo różne rozmiary, co nie ma związku ze stopniem złożoności organizmu. • Różnice w wielkości genomów wynikają przede wszystkim z różnic w poliploidalności i w zawartości niekodującego DNA, w szczególności transpozonów (TEs). • Poliploidyzacja i akumulacja elementów transpozonowych to główne siły napędowe ekspansji genomów roślinnych. • Główne mechanizmy utraty DNA to nierównomierny ‘crossing-over’, i nieuprawniona rekombinacja – przeciwdziałają one nieograniczonej ekspansji genomów. • W ewolucji roślin obserwuje się faworyzowanie większych genomów. • Poliploidyzacja: przystosowawczo neutralna? (Wood, T. et al. . PNAS 2009)

WEWNĘTRZNA STRUKTURA GENOMÓW • Paralogia – bliskie podobieństwo nie allelicznych segmentów chromosomów lub sekwencji DNA w obrębie gatunku, wskazuje na bliskie pokrewieństwo ewolucyjne. Paralogami są np. dwa różne ludzkie geny α-globinowe. • Ortologia – bliskie podobieństwo segmentów chromosomów lub sekwencji DNA pomiędzy gatunkami. Ortologami są np. główny ludzki gen determinujący płeć SRY i jego odpowiednik (ortolog) u myszy – gen Sry. • Homologia – ogólny termin określający podobieństwa sekwencji wskazujące na wspólne pochodzenie ewolucyjne (wewnątrz- lub pomiędzy gatunkami).
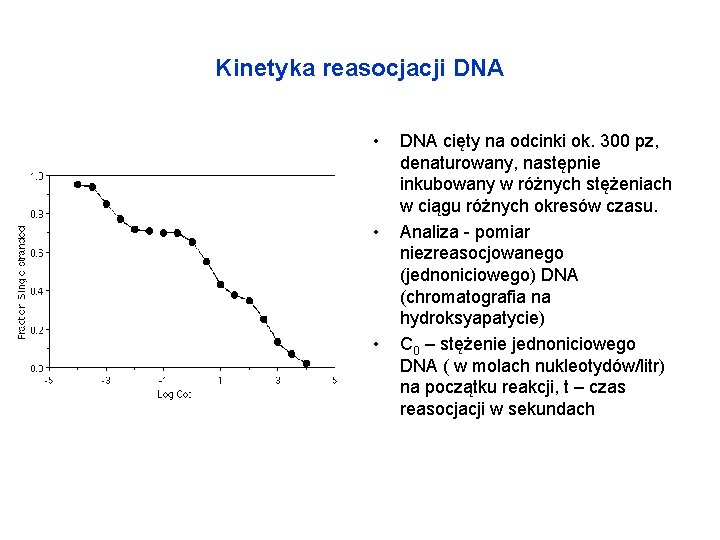
Kinetyka reasocjacji DNA • • • DNA cięty na odcinki ok. 300 pz, denaturowany, następnie inkubowany w różnych stężeniach w ciągu różnych okresów czasu. Analiza - pomiar niezreasocjowanego (jednoniciowego) DNA (chromatografia na hydroksyapatycie) C 0 – stężenie jednoniciowego DNA ( w molach nukleotydów/litr) na początku reakcji, t – czas reasocjacji w sekundach

Złożoność sekwencyjna genomów roślinnych na podstawie analizy kinetyk reasocjacji • Złożone z sekwencji powtarzalnych i jednokopijnych • Różnice w rozmiarach genomów głównie z powodu różnej ilości sekwencji powtarzalnych (istotny także poziom ploidalności). • Podział sekwencji powtarzalnych: a) ułożone tandemowe (większość w centromerach, telomerach) i b) rozrzucone po genomie. • W klasie b) najczęściej transpozony. W Arabidopsis stanowią ok. 10% genomu, w kukurydzy - 50%
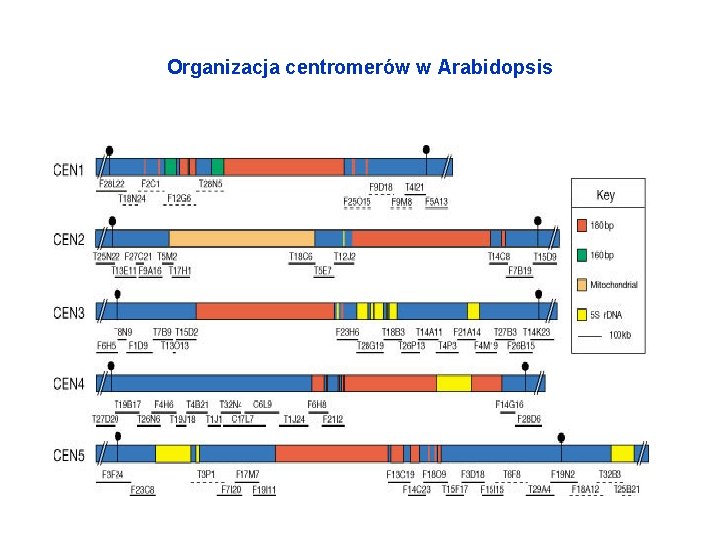
Organizacja centromerów w Arabidopsis

Rodzaje sekwencji w genomach roślin elementy transpozonowe: (na przykładzie Arabidopsis) • • • - copia- i gypsy-like long terminal repeat (LTR) retrotransposons, long interspersed nuclear elements (LINEs); short interspersed nuclear elements (SINEs), hobo/Activator /Tam 3 (h. AT)-like elements, CACTA-like elements miniature inverted-repeat transposable elements (MITEs).

Model obszarów genowych w genomach roślin • • Strzałki = geny (eksony zaznaczone na czarno) MITE =miniature inverted transposable elements • • LTR = long terminal repeat SSR = simple sequence repeat
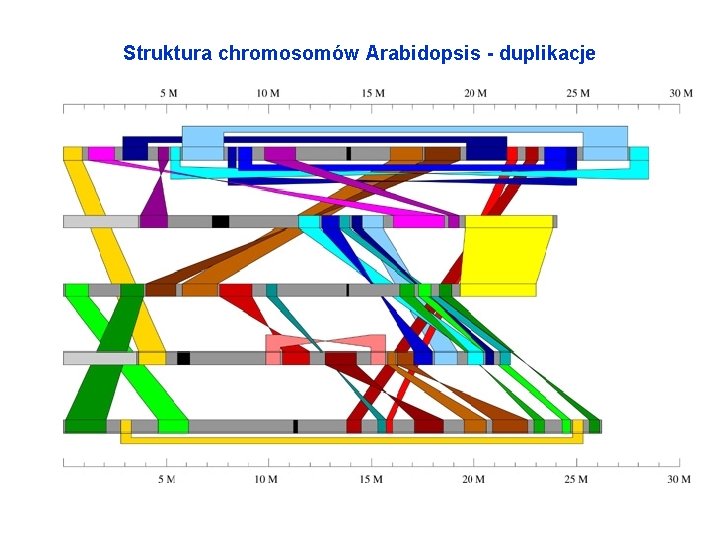
Struktura chromosomów Arabidopsis - duplikacje
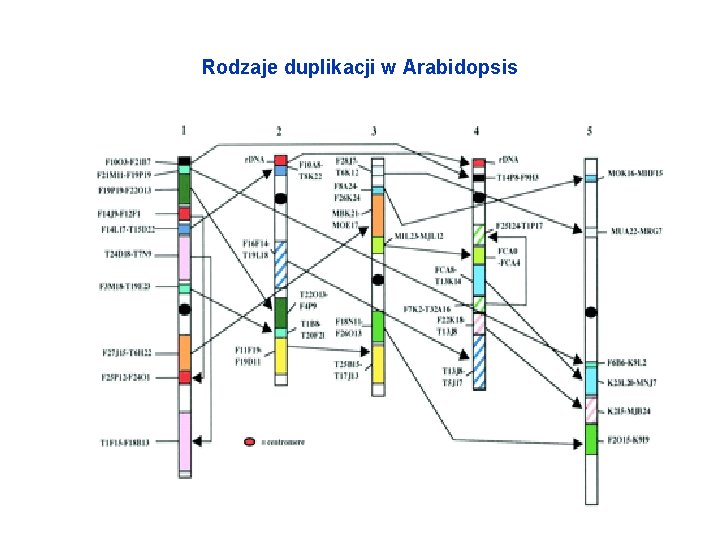
Rodzaje duplikacji w Arabidopsis

Relacje między gatunkowe/syntenia • Syntenia = podobieństwo genów i ich ułożenia w chromosomach
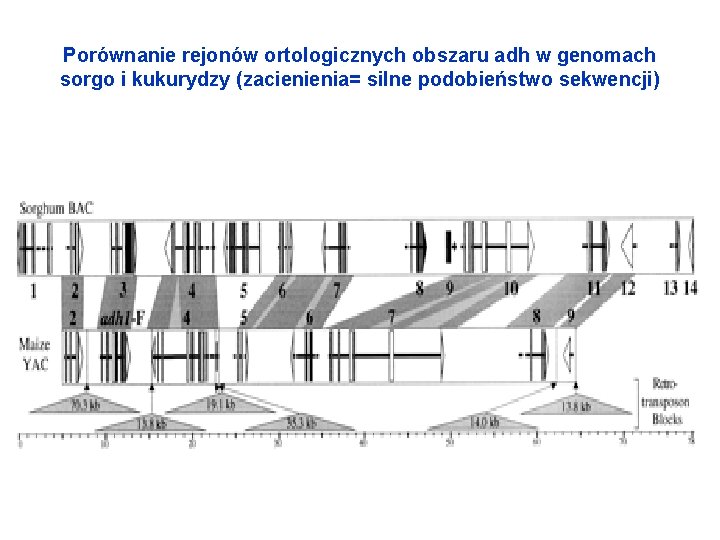
Porównanie rejonów ortologicznych obszaru adh w genomach sorgo i kukurydzy (zacienienia= silne podobieństwo sekwencji)
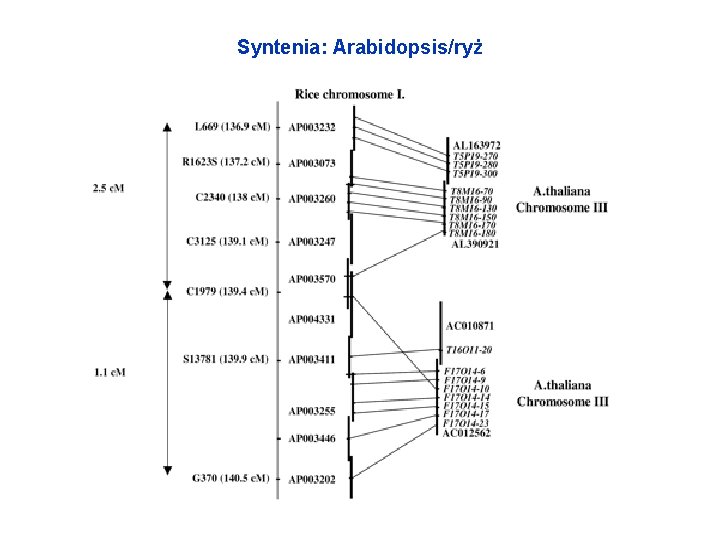
Syntenia: Arabidopsis/ryż

• • • • • • • • • • • • Genome sequencing and analysis of the model grass Brachypodium distachyon The International Brachypodium Initiative* The International Brachypodium Initiative Principal investigators John P. Vogel 1, David F. Garvin 2, Todd C. Mockler 3, Jeremy Schmutz 4, Dan Rokhsar 5, 6, Michael W. Bevan 7; DNA sequencing and assembly Kerrie Barry 5, Susan Lucas 5, Miranda Harmon-Smith 5, Kathleen Lail 5, Hope Tice 5, Jeremy Schmutz 4 (Leader), Jane Grimwood 4, Neil Mc. Kenzie 7, Michael W. Bevan 7; Pseudomolecule assembly and. BACend sequencing. Naxin. Huo 1, Yong Q. Gu 1, Gerard. R. Lazo 1, Olin. D. Anderson 1, John P. Vogel 1 (Leader), Frank M. You 8, Ming-Cheng Luo 8, Jan Dvorak 8, Jonathan Wright 7, Melanie Febrer 7, Michael W. Bevan 7, Dominika Idziak 9, Robert Hasterok 9, David F. Garvin 2; Transcriptome sequencing and analysis Erika Lindquist 5, Mei Wang 5, Samuel E. Fox 3, Henry D. Priest 3, Sergei A. Filichkin 3, Scott A. Givan 3, Douglas W. Bryant 3, Jeff. H. Chang 3, Todd. C. Mockler 3 (Leader), Haiyan. Wu 10, 24, Wei Wu 10, An-Ping Hsia 10, Patrick S. Schnable 10, 24, Anantharaman Kalyanaraman 11, Brad Barbazuk 12, Todd P. Michael 13, Samuel P. Hazen 14, Jennifer. N. Bragg 1, Debbie Laudencia-Chingcuanco 1, John P. Vogel 1, David F. Garvin 2, Yiqun Weng 15, Neil Mc. Kenzie 7, Michael W. Bevan 7; Gene analysis and annotation Georg Haberer 16, Manuel Spannagl 16, Klaus Mayer 16 (Leader), Thomas Rattei 17, Therese. Mitros 6, Dan Rokhsar 6, Sang-Jik Lee 18, Jocelyn K. C. Rose 18, Lukas A. Mueller 19, Thomas L. York 19; Repeats analysis Thomas Wicker 20 (Leader), Jan P. Buchmann 20, Jaakko Tanskanen 21, Alan H. Schulman 21 (Leader), Heidrun Gundlach 16, Jonathan Wright 7, Michael Bevan 7, Antonio Costa de Oliveira 22, Luciano da C. Maia 22, William Belknap 1, Yong Q. Gu 1, Ning Jiang 23, Jinsheng Lai 24, Liucun Zhu 25, Jianxin. Ma 25, Cheng Sun 26, Ellen Pritham 26; Comparative genomics Jerome Salse 27 (Leader), Florent Murat 27, Michael Abrouk 27, Georg Haberer 16, Manuel Spannagl 16, Klaus Mayer 16, Remy Bruggmann 13, Joachim Messing 13, Frank M. You 8, Ming-Cheng Luo 8, Jan Dvorak 8; Small RNA analysis Noah Fahlgren 3, Samuel E. Fox 3, Christopher M. Sullivan 3, Todd C. Mockler 3, James C. Carrington 3, Elisabeth J. Chapman 3, 28, Greg D. May 29, Jixian Zhai 30, Matthias Ganssmann 30, Sai Guna Ranjan Gurazada 30, Marcelo German 30, Blake C. Meyers 30, Pamela J. Green 30 (Leader); Manual annotation and gene family analysis Jennifer N. Bragg 1, Ludmila Tyler 1, 6, Jiajie Wu 1, 8, Yong Q. Gu 1, Gerard R. Lazo 1, Debbie Laudencia-Chingcuanco 1, James Thomson 1, John P. Vogel 1 (Leader), Samuel P. Hazen 14, Shan Chen 14, Henrik V. Scheller 31, Jesper. Harholt 32, Peter Ulvskov 32, Samuel E. Fox 3, Sergei A. Filichkin 3, Noah Fahlgren 3, Jeffrey A. Kimbrel 3, Jeff H. Chang 3, Christopher M. Sullivan 3, Elisabeth J. Chapman 3, 27, James C. Carrington 3, Todd C. Mockler 3, Laura E. Bartley 8, 31, Peijian Cao 8, 31, Ki-Hong Jung 8, 31{, Manoj K Sharma 8, 31, Miguel Vega-Sanchez 8, 31, Pamela Ronald 8, 31, Christopher D. Dardick 33, Stefanie. De Bodt 34, Wim Verelst 34, Dirk Inze´ 34, Maren Heese 35, Arp Schnittger 35, Xiaohan Yang 36, Udaya C. Kalluri 36, Gerald. A. Tuskan 36, Zhihua. Hua 37, Richard D. Vierstra 37, David F. Garvin 3, Yu Cui 24, Shuhong Ouyang 24, Qixin Sun 24, Zhiyong Liu 24, Alper Yilmaz 38, Erich Grotewold 38, Richard Sibout 39, Kian Hematy 39, Gregory Mouille 39, Herman Ho¨fte 39, Todd Michael 13, Je´rome Pelloux 40, Devin O’Connor 41, James Schnable 41, Scott Rowe 41, Frank Harmon 41, Cynthia L. Cass 42, John C. Sedbrook 42, Mary E. Byrne 7, Sean. Walsh 7, Janet Higgins 7, Michael Bevan 7, Pinghua. Li 19, Thomas. Brutnell 19, Turgay. Unver 43, Hikmet Budak 43, Harry Belcram 44, Mathieu Charles 44, Boulos Chalhoub 44, Ivan Baxter 45 NATURE| Vol 463| 11 February 2010 ARTICLES 767 JP Vogel et al. Nature 463, 763 -768 (2010) doi: 10. 1038/nature 08747 Kłosownica leśna

Problem badania genomów traw użytkowych • • • Trawy (Poaceae – ponad 600 rodzajów obejmujących ponad 10 000 gatunków, dominują w wielu systemach ekologicznych i rolniczych) dostarczają podstawowej masy żywności dla ludności Ziemi. Wysoce produktywne trawy są także poważnym źródłem odnawialnej energii Trzy podrodziny traw: Ehrartoideae (ryż), Panicoideae (kurkurydza, sorgo, trzcina cukrowa) i Pooideae (zboża stefy chłodnej, np. pszenica) – zawierają główne rośliny uprawne na Ziemi. Sekwencje genomów ryżu, kukurydzy, sorgo zostały ustalone – porównania wykazały silna konserwatywność liniowego porządku genów a także odległe i niedawne wydarzenia poliploidyzacyjne. Genomy większości użytkowych traw z podrodziny Pooideae są zbyt wielkie i skomplikowane, by nadawały się do szybkiego sekwencjonowania. Np. . Genom pszenicy (17 000 Mb) zawiera aż trzy niezależne genomy. Brachypodium (Pooideae; Kłosownica leśna) – diploid, jest dziką jednoroczną trawą z okolic Morza Śródziemnego i Bliskiego Wschodu, o niedużym genomie. Stanowi doskonały model do badania pszenicy i innych zbóż strefy chłodnej. ,
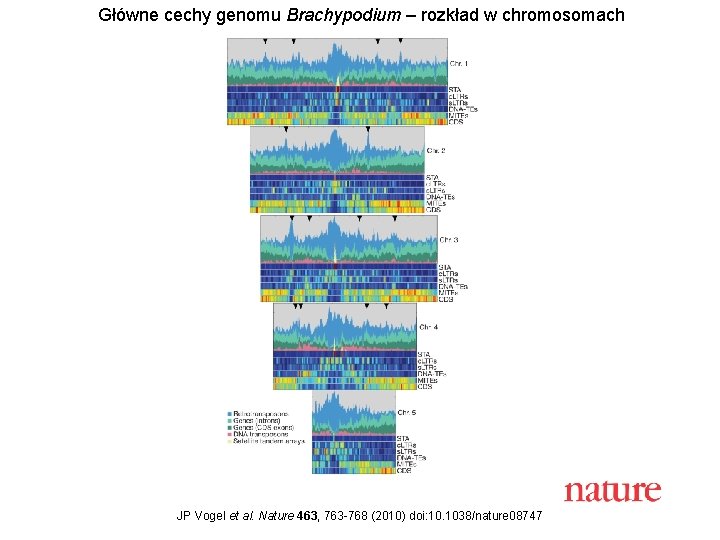
Główne cechy genomu Brachypodium – rozkład w chromosomach JP Vogel et al. Nature 463, 763 -768 (2010) doi: 10. 1038/nature 08747
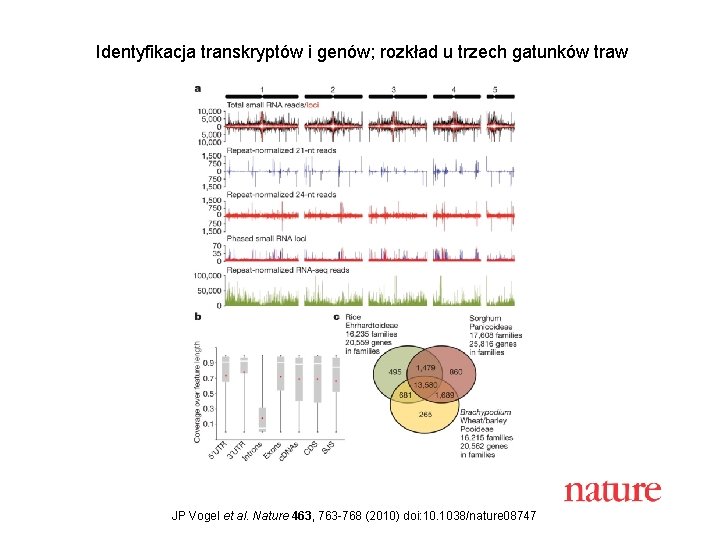
Identyfikacja transkryptów i genów; rozkład u trzech gatunków traw JP Vogel et al. Nature 463, 763 -768 (2010) doi: 10. 1038/nature 08747

Porównanie genomów trzech różnych traw • • • Pokrewieństwa ewolucyjne pomiędzy Brachypodium, sorgo i ryżem oceniono mierząc średnią szybkość podstawień synonimicznych (Ks) w parach genów ortologicznych. Na tej podstawie ustalono, że Brachypodium dzieli 32 -39 MYR (millions of years) od pszenicy, 40 -53 MYR od ryżu i 45 -60 MYR od sorgo. Paralogie między chromosomami Brachypodium wskazują, że w przeszłości nastąpiło 6 głównych duplikacji chromosomowych obejmujących 92, 1% genomu. Pokrewieństwa ortologiczne są zgodne z modelem ewolucyjnym, według którego 5 chromosomów Brachypodium powstało z 5 -chromosomowego genomu pierwotnego poprzez stadium 12 -chromosomowe i obejmowało 7 głównych fuzji chromosomowych.
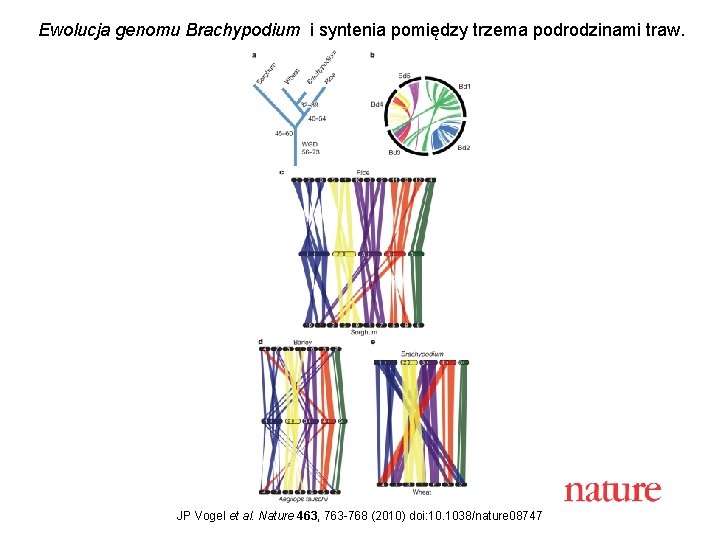
Ewolucja genomu Brachypodium i syntenia pomiędzy trzema podrodzinami traw. JP Vogel et al. Nature 463, 763 -768 (2010) doi: 10. 1038/nature 08747

Powtarzający się wzór fuzji chromosomowych u traw • • a Pięć chromosomów Brachypodium pokolorowano wg. kolorów odpowiadających homologiom z 12 -ma chromosomami ryżu. Czerwona linia nad chromosomami – gęstość genów Główne nieciągłości w gęstości genów (czarne romby) wskazują punkty rozdzielające obszary synteniczne Białe romby – miejsca fuzji zawierajace pozostałości powtórzeń centromerowych b. Wzór zagnieżdżonych insercji całych chromosomów w rejony centromerowe wyjaśniający obserwowane rozdzielenia obszarów syntenii c. , d. Przykłady zagnieżdżonych insercji chromosomowych u sorgo i jęczmienia

Powtarzający się wzór fuzji chromosomowych u traw. JP Vogel et al. Nature 463, 763 -768 (2010) doi: 10. 1038/nature 08747

Znacznie badań porównawczych genomów traw użytkowych • Zrozumienie mechanizmu dywersyfikacji traw poprzez wytłumaczenie, jak zróżnicowanie liczby chromosomów u różnych rodzajów ewoluowało z pierwotnego zbioru 5 chromosomów poprzez zagnieżdżone w centromerach insercje całych chromosomów. • Cel: Inżynieriach genomów traw w celu poprawy wydajności i jakości zbiorów (żywność i paliwa).
Genomy organelli komórkowych

Założenia teorii endosymbiotycznej • • • Mitochondria eukariontów ewoluowały z bakterii tlenowych żyjących, jako symbionty, w komórkach pra-eukariotycznego gospodarza. Chloroplasty eukariontów ewoluowały z endosymbiotycznych sinic. Dowody: Mitochondria i chloroplasty powstają wyłącznie z istniejących mitochodriów i chloroplastów. mitochondria and chloroplasts. Nie mogą powstać w komórce, która nie zawiera tych organelli ponieważ geny jądrowe kodują tylko niektóre białka organellarne. Zarówno mitochondria jak i chloroplasty mają własne genomy, które przypominaja genomy bakterii, a nie genomy jądrowe: – – • Oba składają się z kolistej cząsteczki DNA. Z DNA organelli nie są zasocjowane histony. Zarówno mitochondria jak i chloroplasty mają własny system translacji, który przypomina system prokariotyczny, a nie eukariotyczny. – – Pierwszym aminokwasem w transkryptach jest f. Met jak u bakterii (a nie metionina [Met], która jest pierwszym aminokwasem w białkach eukariotycznych). Antybiotyki (np. , streptomycyna) hamujace biosynteze białka u bakterii (lecz nie u eukarintów), hamuja także biiosyntezę białka w organellach. Inhibitory translacji eukariotycznej (np. . Toksyna dyfterytu) nie hamuja translacji w organellach. Antybiotyk rifampicina, który wybiórczo hamuje RNA polimrazę u bakterii, hamuje także RNA polimertqazę w organellach. ,

NCBI Organelle Genomes section at NCBI. L. Cui, N. Veeraraghavan, A. Richter, K. Wall, R. K. Jansen, J. Leebens-Mack, I. Makalowska, and C. W. de. Pamphilis. Chloroplast. DB: the chloroplast genome database. Nucleic Acids Research, 2006, vol. 34, pp. D 692 -696.
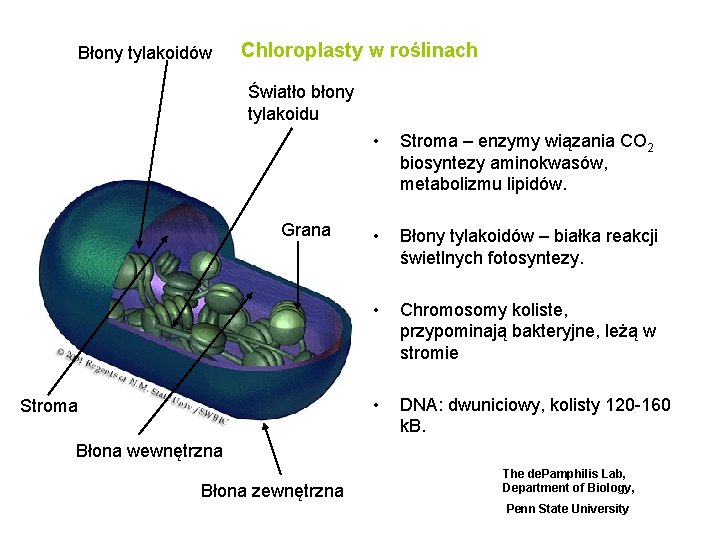
Błony tylakoidów Chloroplasty w roślinach Światło błony tylakoidu Grana Stroma • Stroma – enzymy wiązania CO 2 biosyntezy aminokwasów, metabolizmu lipidów. • Błony tylakoidów – białka reakcji świetlnych fotosyntezy. • Chromosomy koliste, przypominają bakteryjne, leżą w stromie • DNA: dwuniciowy, kolisty 120 -160 k. B. Błona wewnętrzna Błona zewnętrzna The de. Pamphilis Lab, Department of Biology, Penn State University
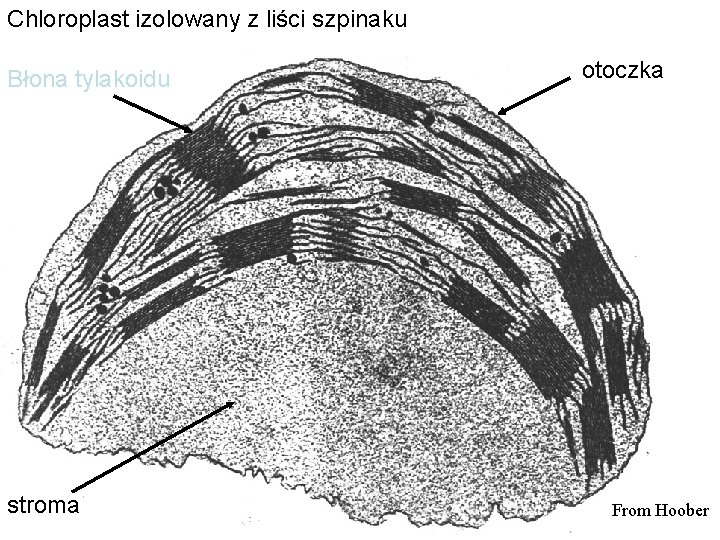
Chloroplast izolowany z liści szpinaku Błona tylakoidu stroma otoczka From Hoober
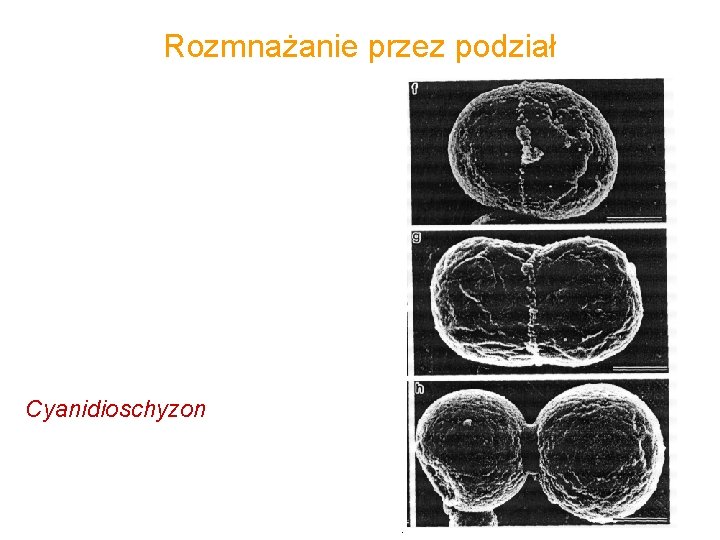
Rozmnażanie przez podział • all plant and eukaryotic algal cells have plastids • chloroplasts form by division; semi-autonomous • Involves proteins (Fts) similar to those that mediate cell division in bacteria Cyanidioschyzon chloroplast dividing From Miyagishima et al.
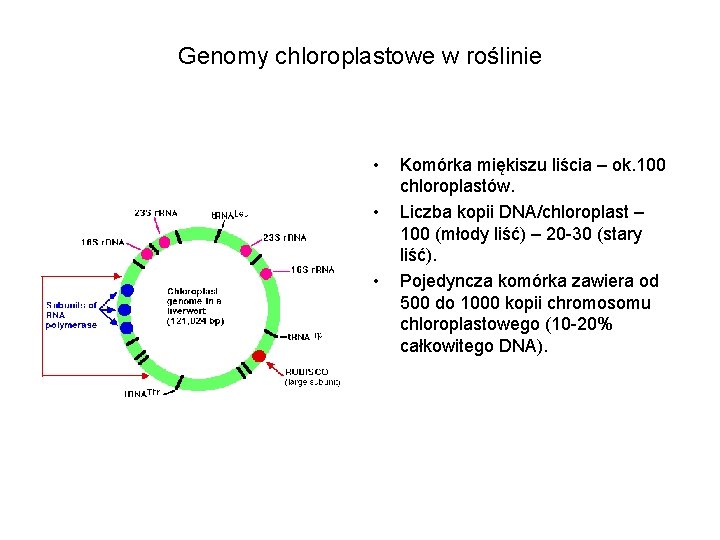
Genomy chloroplastowe w roślinie • • • Komórka miękiszu liścia – ok. 100 chloroplastów. Liczba kopii DNA/chloroplast – 100 (młody liść) – 20 -30 (stary liść). Pojedyncza komórka zawiera od 500 do 1000 kopii chromosomu chloroplastowego (10 -20% całkowitego DNA).
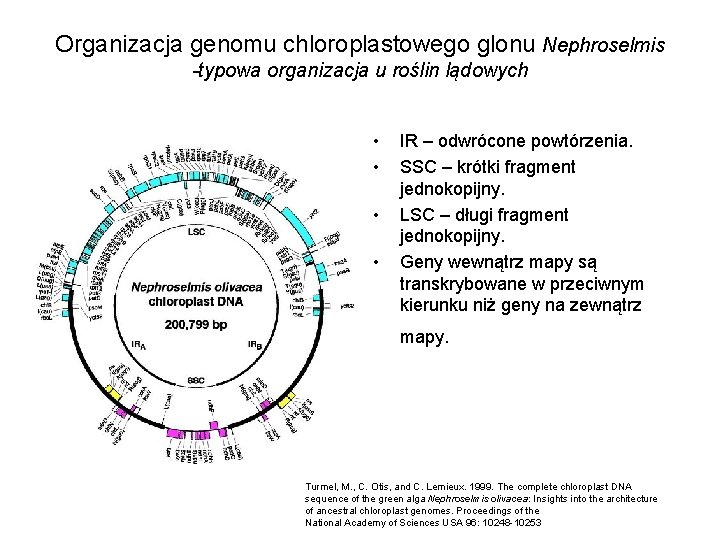
Organizacja genomu chloroplastowego glonu Nephroselmis -typowa organizacja u roślin lądowych • • IR – odwrócone powtórzenia. SSC – krótki fragment jednokopijny. LSC – długi fragment jednokopijny. Geny wewnątrz mapy są transkrybowane w przeciwnym kierunku niż geny na zewnątrz mapy. Turmel, M. , C. Otis, and C. Lemieux. 1999. The complete chloroplast DNA sequence of the green alga Nephroselmis olivacea: Insights into the architecture of ancestral chloroplast genomes. Proceedings of the National Academy of Sciences USA 96: 10248 -10253

Genom chloroplastowy u wątrobowca Marchantia polymorpha • Liczy 121 024 par zasad w postaci kolistego DNA. Odpowiada to 128 genom, które zawierają: • Zduplikowane geny kodujące każdą z czterech podjednostek (23 S, 16 S, 4. 5 S, i 5 S) rybosomalnego RNA (r. RNA) wykorzystywanego w chloroplaście • 37 genów kodujących wszystkie t. RNA używane do translacji w chloroplaście. • 4 geny kodujące niektóre podjednostki RNA polimerazy używanej do transkrypcji w chloroplaście. • Gen kodujący większą podjednostkę RUBISCO (ribulose bisphosphate carboxylase oxygenase) • 9 genów kodujących podjednstki składowe fotosystemu I i II • 6 genów kodujących składniki ATP syntazy • geny kodujące 19 z ~60 białek rybosomu chloroplastowego

• Struktury i funkcjonowanie chloroplastów zależy od genów jądrowych, których rozliczne produkty muszą być importowane do chloroplastu
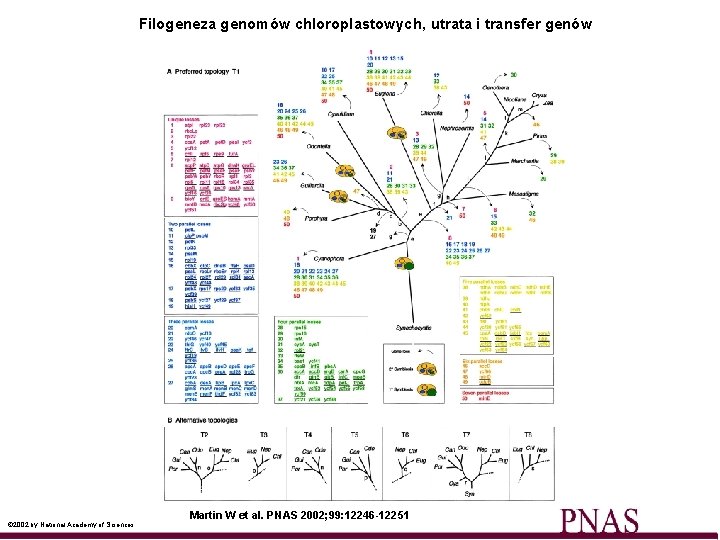
Filogeneza genomów chloroplastowych, utrata i transfer genów © 2002 by National Academy of Sciences Martin W et al. PNAS 2002; 99: 12246 -12251

• Wymiana genów między jądrem a chloroplastem jest stale zachodzącym dynamicznym procesem
- Slides: 39