Struktura atomovho obalu VY32 INOVACECHE12 AUTOR Ing Ladislava

Struktura atomového obalu VY-32 -INOVACE-CHE-12 AUTOR: Ing. Ladislava Semerádová ANOTACE: Výukový materiál, který může být použit při výkladu struktury elektronového obalu a významu kvantových čísel. Určeno pro studenty 1. ročníku SŠ. KLÍČOVÁ SLOVA: atomový orbital, kvantová čísla, popis atomových orbitalů pomocí kvantových čísel

Struktura atomového obalu, kvantová čísla

Atomový orbital • elektrony se nenacházejí v obale nahodile, ale v určitém prostoru • tento prostor nazýváme atomový orbital • uspořádání elektronů v obalu je důležité pro fyzikální a chemické vlastnosti látek
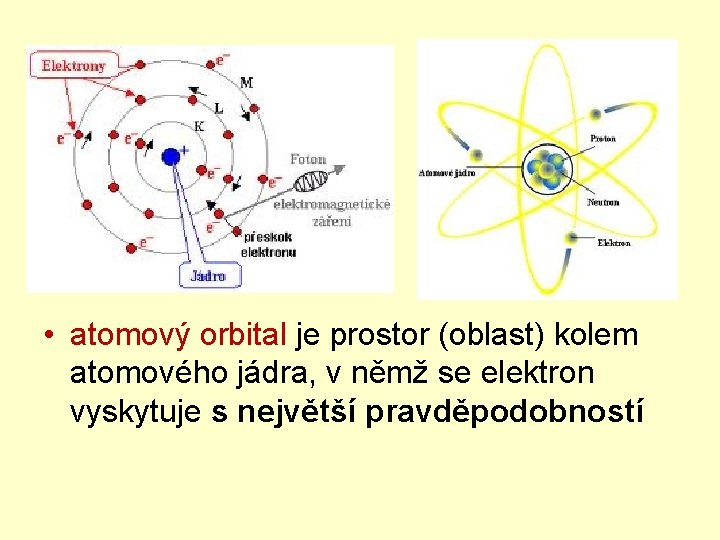
• atomový orbital je prostor (oblast) kolem atomového jádra, v němž se elektron vyskytuje s největší pravděpodobností

Kvantová čísla • podobně jako zeměpisné souřadnice přesně definují polohu na povrchu Země • tak i kvantová čísla nám pomáhají popsat orbital, ve kterém se elektron vyskytuje • Kvantová čísla jsou čtyři: • 1. Hlavní kvantové číslo n – popisuje celkovou velikost orbitalu • 2. Vedlejší kvantové číslo l- popisuje prostorový tvar orbitalu • 3. Magnetické kvantové číslo m – popisuje orientaci orbitalu v prostoru • 4. Spinové kvantové číslo s- popisuje směr pohybu elektronu
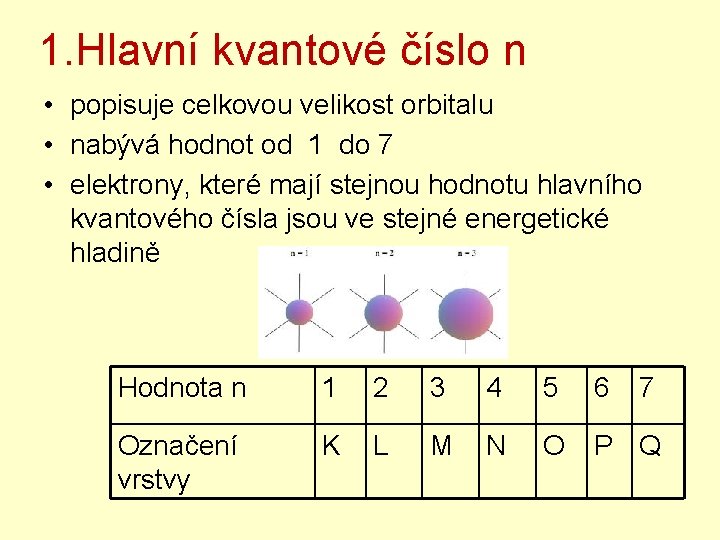
1. Hlavní kvantové číslo n • popisuje celkovou velikost orbitalu • nabývá hodnot od 1 do 7 • elektrony, které mají stejnou hodnotu hlavního kvantového čísla jsou ve stejné energetické hladině Hodnota n 1 2 3 4 5 6 7 Označení vrstvy K L M N O P Q
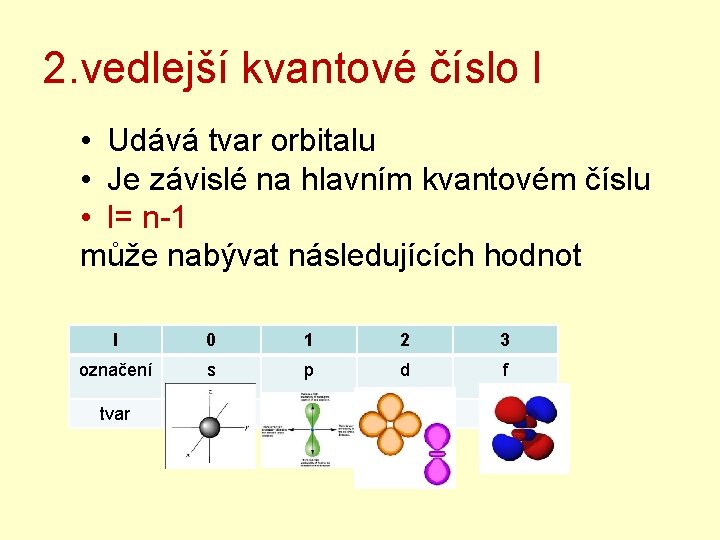
2. vedlejší kvantové číslo l • Udává tvar orbitalu • Je závislé na hlavním kvantovém číslu • l= n-1 může nabývat následujících hodnot l 0 1 2 3 označení s p d f tvar

3. Magnetické kvantové číslo m • Určuje polohu orbitalu v prostoru ( např. k osám x, y, z) • Je závislé na vedlejším kvantovém číslu l • Nabývá hodnot –l až +l (včetně 0)
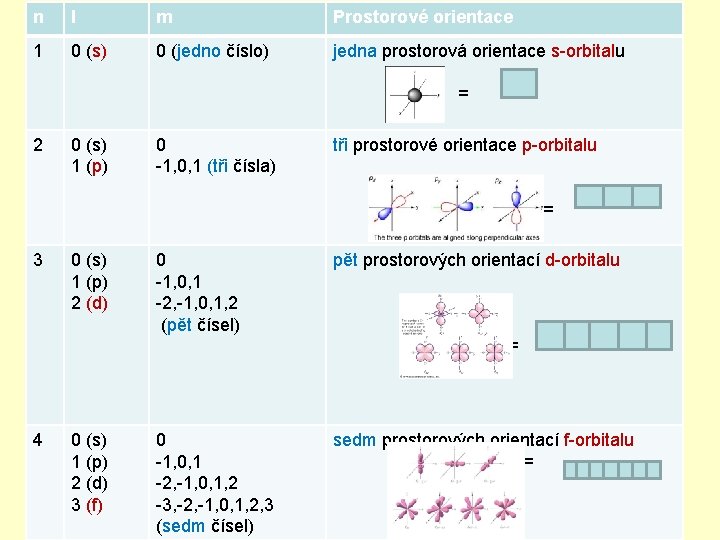
n l m Prostorové orientace 1 0 (s) 0 (jedno číslo) jedna prostorová orientace s-orbitalu = 2 0 (s) 1 (p) 0 -1, 0, 1 (tři čísla) tři prostorové orientace p-orbitalu = 3 0 (s) 1 (p) 2 (d) 0 -1, 0, 1 -2, -1, 0, 1, 2 (pět čísel) pět prostorových orientací d-orbitalu = 4 0 (s) 1 (p) 2 (d) 3 (f) 0 -1, 0, 1 -2, -1, 0, 1, 2 -3, -2, -1, 0, 1, 2, 3 (sedm čísel) sedm prostorových orientací f-orbitalu =
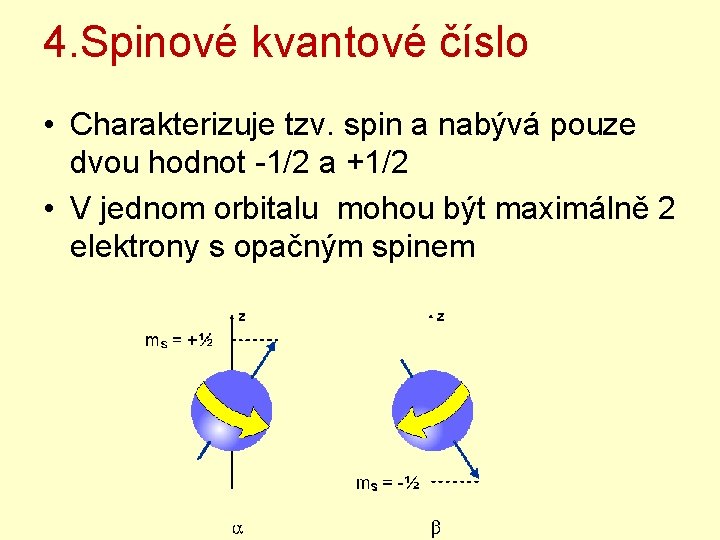
4. Spinové kvantové číslo • Charakterizuje tzv. spin a nabývá pouze dvou hodnot -1/2 a +1/2 • V jednom orbitalu mohou být maximálně 2 elektrony s opačným spinem
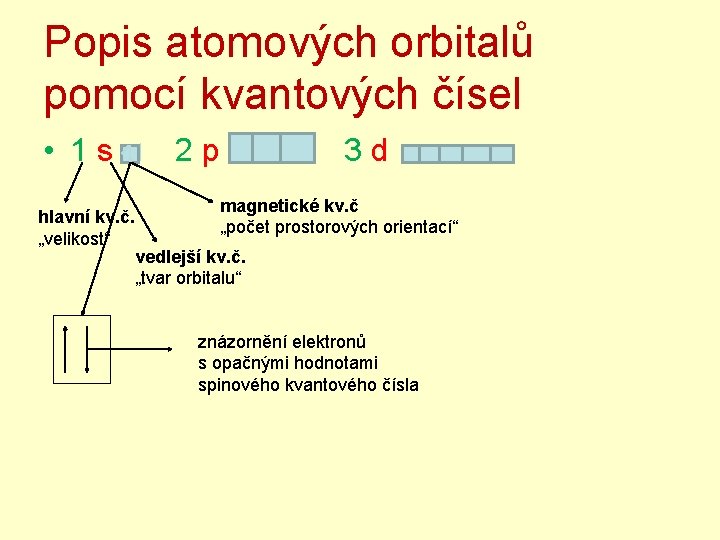
Popis atomových orbitalů pomocí kvantových čísel • 1 s 2 p 3 d magnetické kv. č hlavní kv. č. „počet prostorových orientací“ „velikost“ vedlejší kv. č. „tvar orbitalu“ znázornění elektronů s opačnými hodnotami spinového kvantového čísla

POUŽITÉ ZDROJE: MAREČEK, Aleš a Jaroslav HONZA. Chemie pro čtyřletá gymnázia. 3. , přeprac. vyd. Olomouc: Nakladatelství Olomouc, 2005, 240 s. ISBN 80 -7182 -055 -51. [online]. [cit. 2013 -02 -03]. Dostupné z: http: //images. google. com/ www. glassschool. cz
- Slides: 12