Struktur dan tata nama senyawa karbon OLEH M

Struktur dan tata nama senyawa karbon OLEH: M. NURISSALAM, S. Si SMA MUHAMMADIYAH I METRO • SK: Memahami senyawa organik dan reaksinya, benzena dan turunannya, dan makromolekul. • KD: 4. 1. Mendeskripsikan struktur, cara penulisan, tata nama, sifat, kegunaan, dan identifikasi senyawa karbon (halo alkana, alkanol, alkoksi alkana, alkanal, alkanon, alkanoat, dan alkil alkanoat)

INDIKATOR • Mengidentifikasi gugus fungsi senyawa karbon. • Menuliskan struktur dan nama senyawa karbon berdasarkan gugus fungsinya. • Menentukan isomer-isomer senyawa karbon. • Menjelaskan sifat fisik senyawa karbon. • Mendeskripsikan kegunaan senyawa karbon
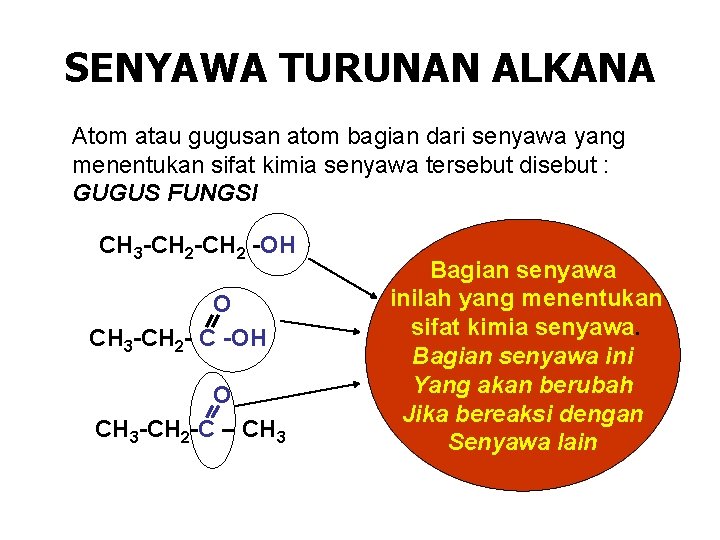
SENYAWA TURUNAN ALKANA Atom atau gugusan atom bagian dari senyawa yang menentukan sifat kimia senyawa tersebut disebut : GUGUS FUNGSI CH 3 -CH 2 -OH O CH 3 -CH 2 - C -OH O CH 3 -CH 2 -C – CH 3 Bagian senyawa inilah yang menentukan sifat kimia senyawa. Bagian senyawa ini Yang akan berubah Jika bereaksi dengan Senyawa lain
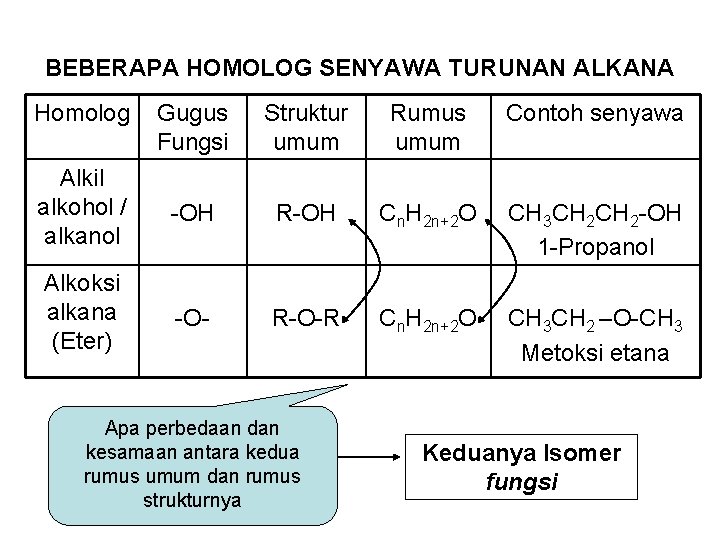
BEBERAPA HOMOLOG SENYAWA TURUNAN ALKANA Homolog Gugus Fungsi Struktur umum Rumus umum Contoh senyawa Alkil alkohol / alkanol -OH R-OH Cn. H 2 n+2 O CH 3 CH 2 -OH 1 -Propanol Alkoksi alkana (Eter) -O- R-O-R Cn. H 2 n+2 O CH 3 CH 2 –O-CH 3 Metoksi etana Apa perbedaan dan kesamaan antara kedua rumus umum dan rumus strukturnya Keduanya Isomer fungsi
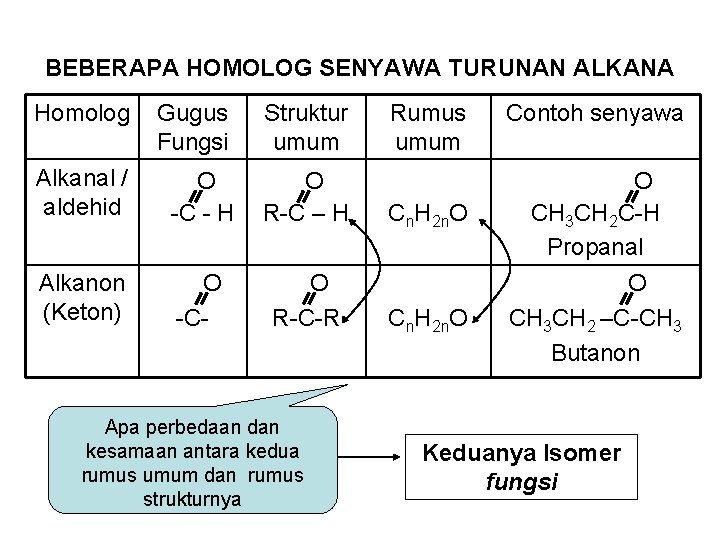
BEBERAPA HOMOLOG SENYAWA TURUNAN ALKANA Homolog Gugus Fungsi Struktur umum Alkanal / aldehid O -C - H O R-C – H Alkanon (Keton) O -C- O R-C-R Apa perbedaan dan kesamaan antara kedua rumus umum dan rumus strukturnya Rumus umum Contoh senyawa Cn. H 2 n. O O CH 3 CH 2 C-H Propanal Cn. H 2 n. O O CH 3 CH 2 –C-CH 3 Butanon Keduanya Isomer fungsi
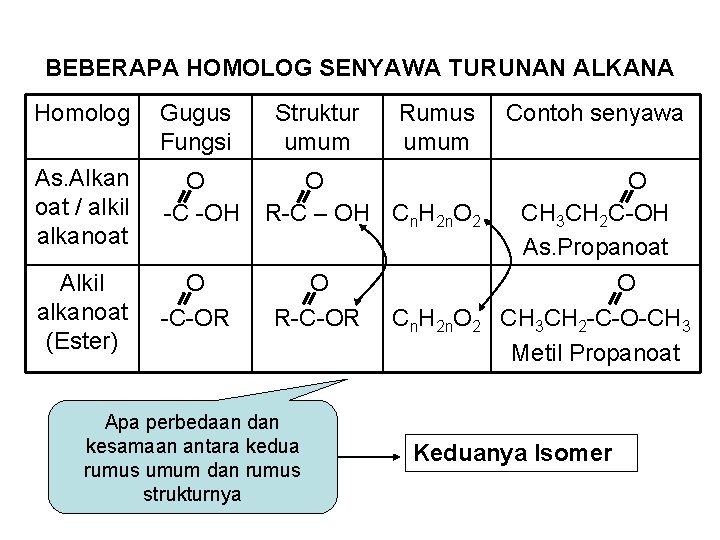
BEBERAPA HOMOLOG SENYAWA TURUNAN ALKANA Homolog Gugus Fungsi As. Alkan oat / alkil alkanoat O -C -OH Alkil alkanoat (Ester) O -C-OR Struktur umum Rumus umum O R-C – OH Cn. H 2 n. O 2 O R-C-OR Apa perbedaan dan kesamaan antara kedua rumus umum dan rumus strukturnya Cn. H 2 n. O 2 Contoh senyawa O CH 3 CH 2 C-OH As. Propanoat O CH 3 CH 2 -C-O-CH 3 Metil Propanoat Keduanya Isomer

Tata nama Alkanol/alkil alkohol 1. Alkohol monovalen 1. Tentukan rantai utama dan berikan penomoran atom C dimulai dari atom C yang paling dekat dengan gugus OH 2. Tuliskan nama alkana dengan akhiran nol dengan letak OH dinyatakan dengan bilangan yang ditulis didepan nama alkanol. R - OH Alkana + akhiran nol 3 2 1 CH 3 -CH 2 -OH 1 -Propanol
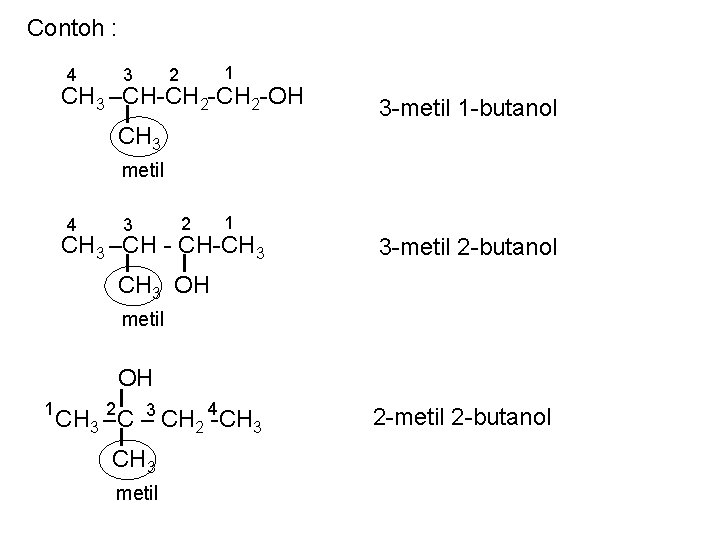
Contoh : 4 3 1 2 CH 3 –CH-CH 2 -OH 3 -metil 1 -butanol CH 3 metil 4 3 2 1 CH 3 –CH - CH-CH 3 3 -metil 2 -butanol CH 3 OH metil OH 1 2 CH 3 –C – 3 CH 2 4 -CH 3 metil 2 -butanol
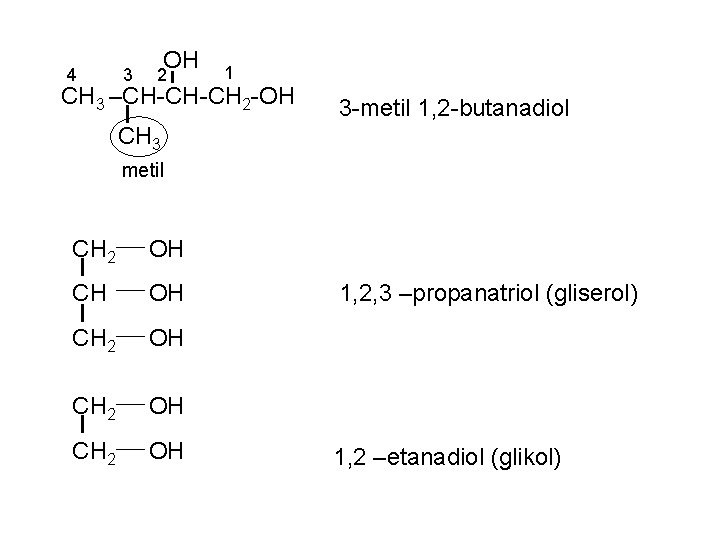
4 3 OH 2 1 CH 3 –CH-CH-CH 2 -OH 3 -metil 1, 2 -butanadiol CH 3 metil CH 2 OH CH 2 OH 1, 2, 3 –propanatriol (gliserol) 1, 2 –etanadiol (glikol)
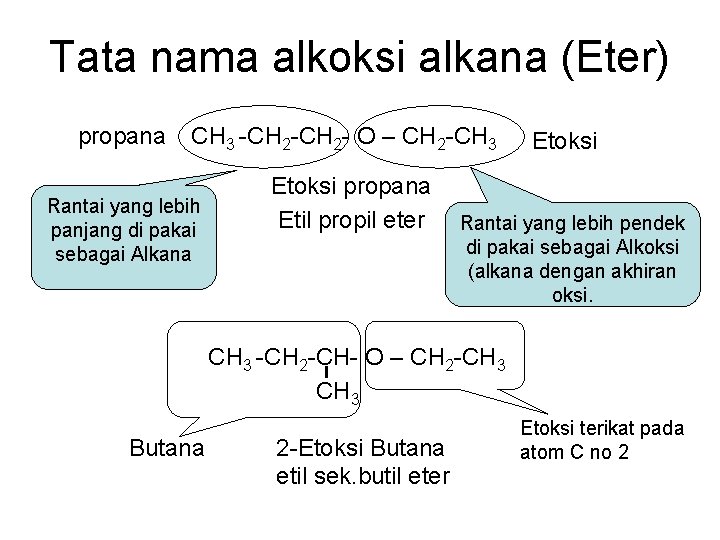
Tata nama alkoksi alkana (Eter) propana CH 3 -CH 2 - O – CH 2 -CH 3 Rantai yang lebih panjang di pakai sebagai Alkana Etoksi propana Etil propil eter Etoksi Rantai yang lebih pendek di pakai sebagai Alkoksi (alkana dengan akhiran oksi. CH 3 -CH 2 -CH- O – CH 2 -CH 3 Butana 2 -Etoksi Butana etil sek. butil eter Etoksi terikat pada atom C no 2
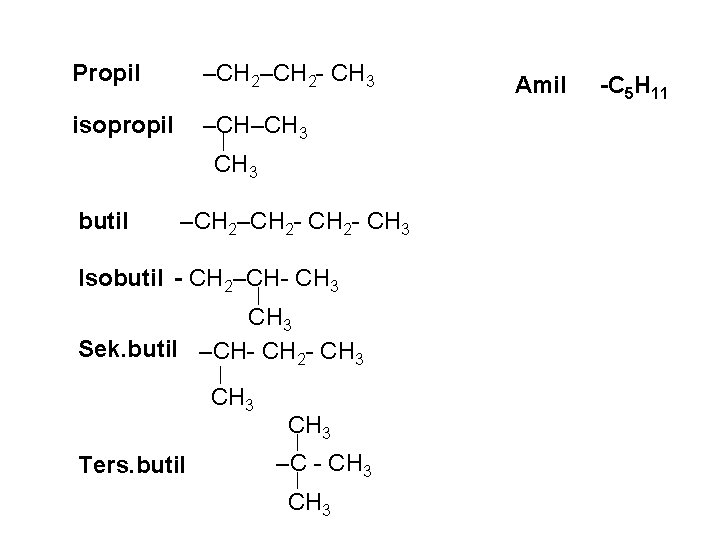
Propil –CH 2 - CH 3 isopropil –CH–CH 3 butil –CH 2 - CH 3 Isobutil - CH 2–CH- CH 3 Sek. butil –CH- CH 2 - CH 3 Ters. butil CH 3 –C - CH 3 Amil -C 5 H 11
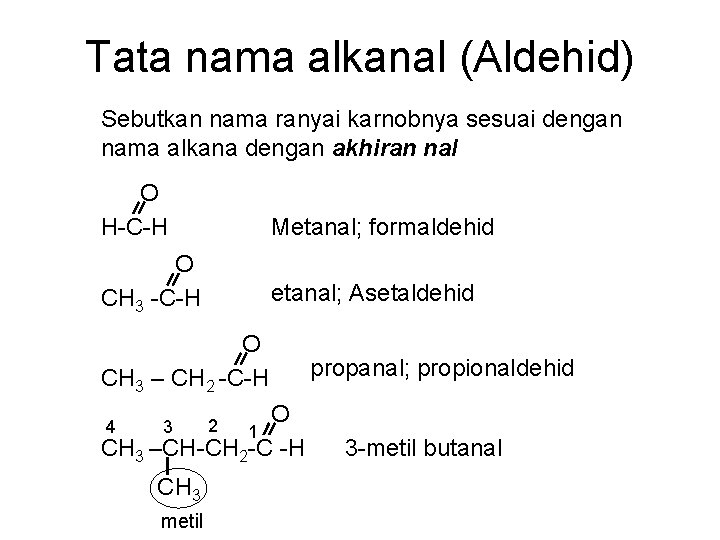
Tata nama alkanal (Aldehid) Sebutkan nama ranyai karnobnya sesuai dengan nama alkana dengan akhiran nal O H-C-H Metanal; formaldehid O CH 3 -C-H etanal; Asetaldehid O CH 3 – CH 2 -C-H O 1 CH 3 –CH-CH 2 -C -H 4 3 CH 3 metil 2 propanal; propionaldehid 3 -metil butanal
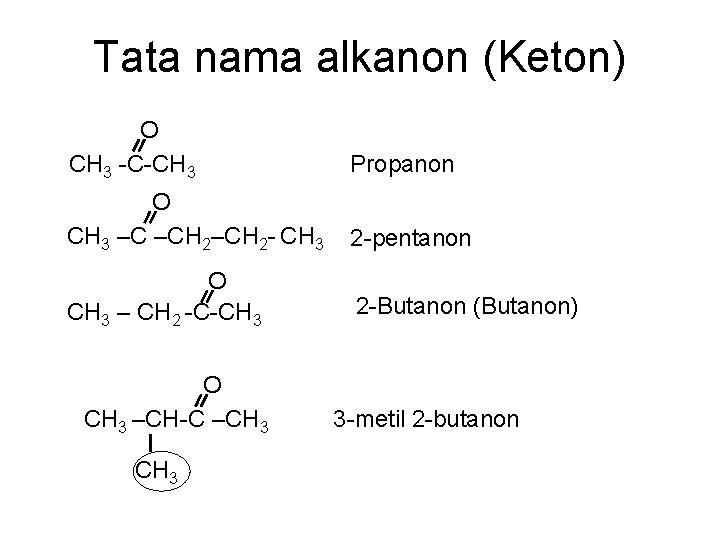
Tata nama alkanon (Keton) O CH 3 -C-CH 3 Propanon O CH 3 –C –CH 2 - CH 3 2 -pentanon O CH 3 – CH 2 -C-CH 3 2 -Butanon (Butanon) O CH 3 –CH-C –CH 3 3 -metil 2 -butanon
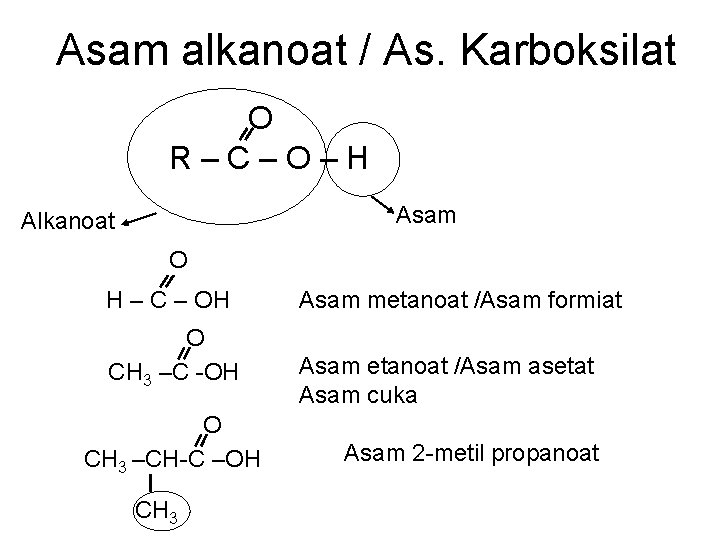
Asam alkanoat / As. Karboksilat O R–C–O–H Asam Alkanoat O H – C – OH O CH 3 –C -OH O CH 3 –CH-C –OH CH 3 Asam metanoat /Asam formiat Asam etanoat /Asam asetat Asam cuka Asam 2 -metil propanoat
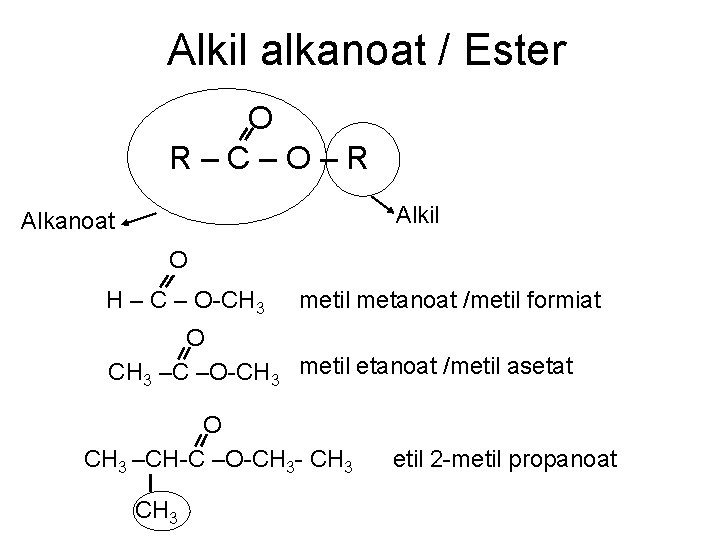
Alkil alkanoat / Ester O R–C–O–R Alkil Alkanoat O H – C – O-CH 3 metil metanoat /metil formiat O CH 3 –C –O-CH 3 metil etanoat /metil asetat O CH 3 –CH-C –O-CH 3 - CH 3 etil 2 -metil propanoat
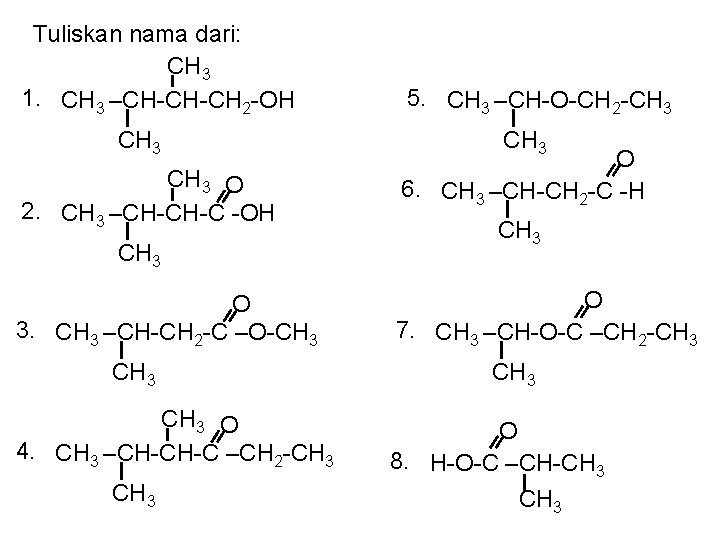
Tuliskan nama dari: CH 3 1. CH 3 –CH-CH-CH 2 -OH CH 3 O 2. CH 3 –CH-CH-C -OH CH 3 O 3. CH 3 –CH-CH 2 -C –O-CH 3 O 4. CH 3 –CH-CH-C –CH 2 -CH 3 5. CH 3 –CH-O-CH 2 -CH 3 O 6. CH 3 –CH-CH 2 -C -H CH 3 O 7. CH 3 –CH-O-C –CH 2 -CH 3 O 8. H-O-C –CH-CH 3

Tuliskan rumus struktur dari : a. 2 -metil 2 butanol b. 2, 4 -dimeti 3 pentanol c. Isopropil alkohol d. Etil butil eter e. Etoksi butana f. Isopropil butanoat g. Metil asetat h. Asam 2 -metil pentanoat i. 2, 4 -dimeti 3 -pentanon j. Butil asetat.
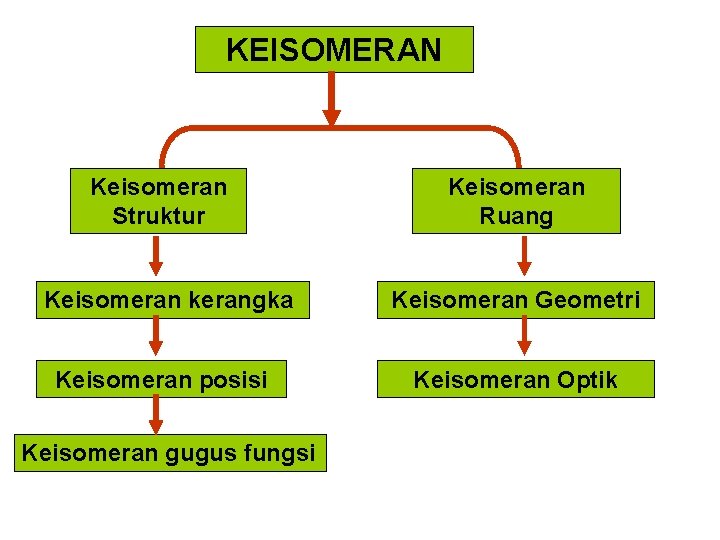
KEISOMERAN Keisomeran Struktur Keisomeran Ruang Keisomeran kerangka Keisomeran Geometri Keisomeran posisi Keisomeran Optik Keisomeran gugus fungsi
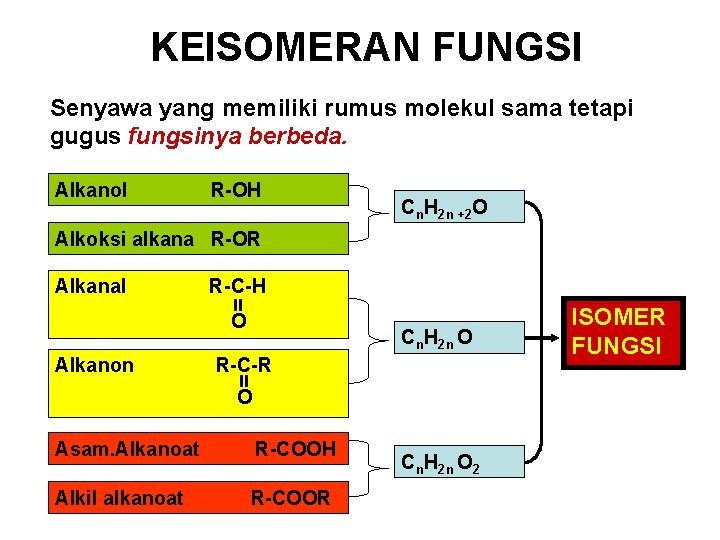
KEISOMERAN FUNGSI Senyawa yang memiliki rumus molekul sama tetapi gugus fungsinya berbeda. Alkanol R-OH Cn. H 2 n +2 O Alkoksi alkana R-OR Alkanal R-C-H O Alkanon Cn. H 2 n O R-C-R O Asam. Alkanoat R-COOH Alkil alkanoat R-COOR Cn. H 2 n O 2 ISOMER FUNGSI
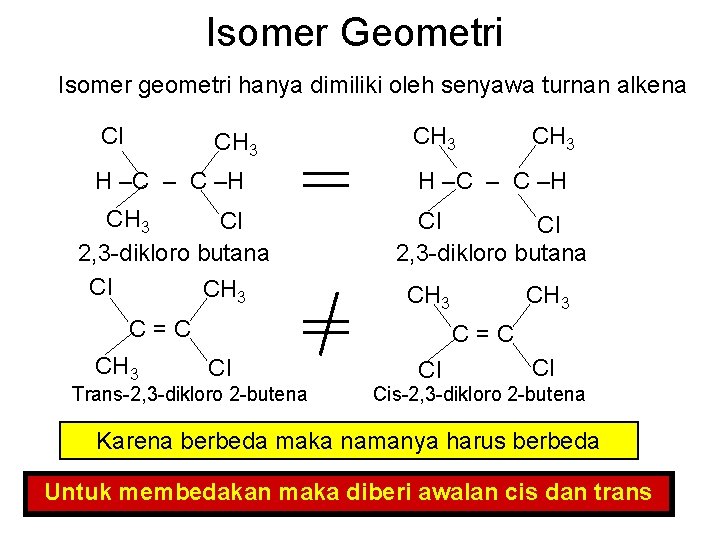
Isomer Geometri Isomer geometri hanya dimiliki oleh senyawa turnan alkena Cl CH 3 H –C – C –H CH 3 Cl 2, 3 -dikloro butana Cl CH 3 Cl Cl 2, 3 -dikloro butana CH 3 C=C Cl Trans-2, 3 -dikloro 2 -butena Cl Cl Cis-2, 3 -dikloro 2 -butena Karena berbeda maka namanya harus berbeda Untuk membedakan maka diberi awalan cis dan trans
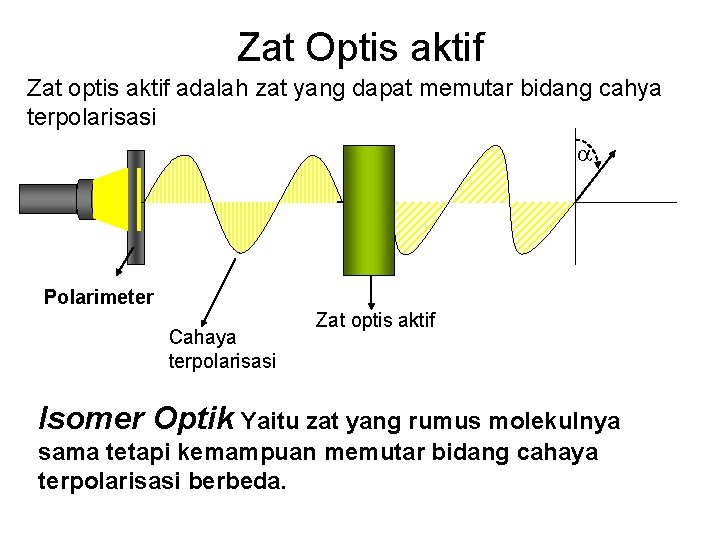
Zat Optis aktif Zat optis aktif adalah zat yang dapat memutar bidang cahya terpolarisasi Polarimeter Cahaya terpolarisasi Zat optis aktif Isomer Optik Yaitu zat yang rumus molekulnya sama tetapi kemampuan memutar bidang cahaya terpolarisasi berbeda.
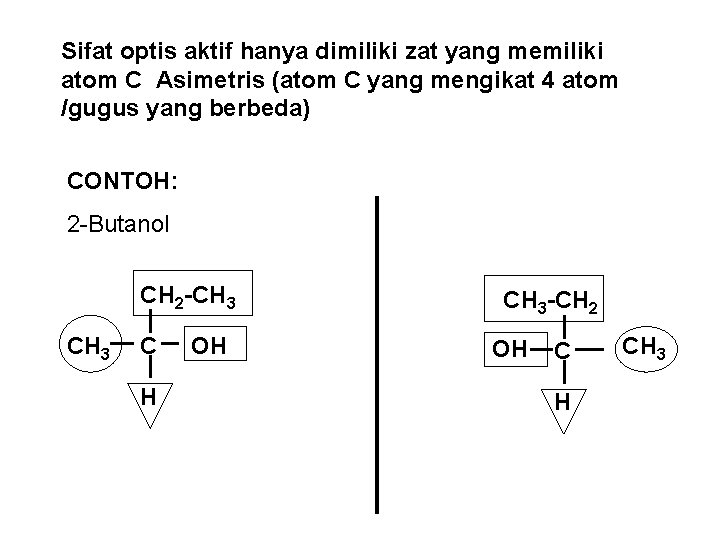
Sifat optis aktif hanya dimiliki zat yang memiliki atom C Asimetris (atom C yang mengikat 4 atom /gugus yang berbeda) CONTOH: 2 -Butanol CH 2 -CH 3 C H OH CH 3 -CH 2 OH C H CH 3
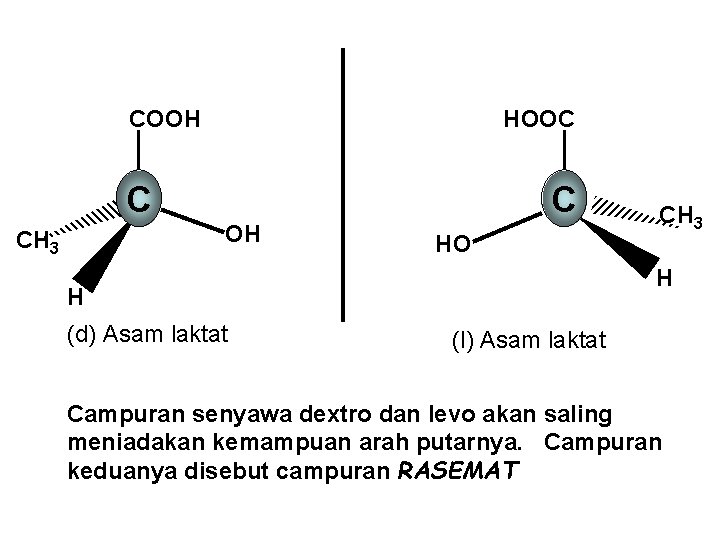
COOH HOOC C C OH CH 3 HO H H (d) Asam laktat CH 3 (l) Asam laktat Campuran senyawa dextro dan levo akan saling meniadakan kemampuan arah putarnya. Campuran keduanya disebut campuran RASEMAT
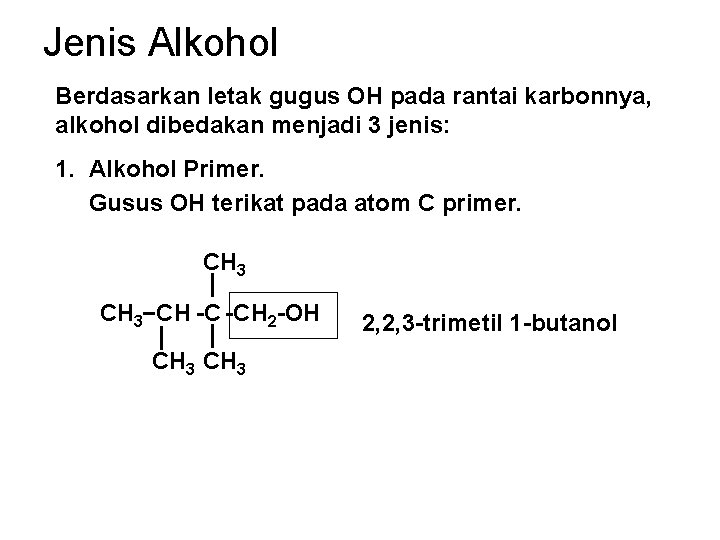
Jenis Alkohol Berdasarkan letak gugus OH pada rantai karbonnya, alkohol dibedakan menjadi 3 jenis: 1. Alkohol Primer. Gusus OH terikat pada atom C primer. CH 3 CH -C -CH 2 -OH CH 3 2, 2, 3 -trimetil 1 -butanol
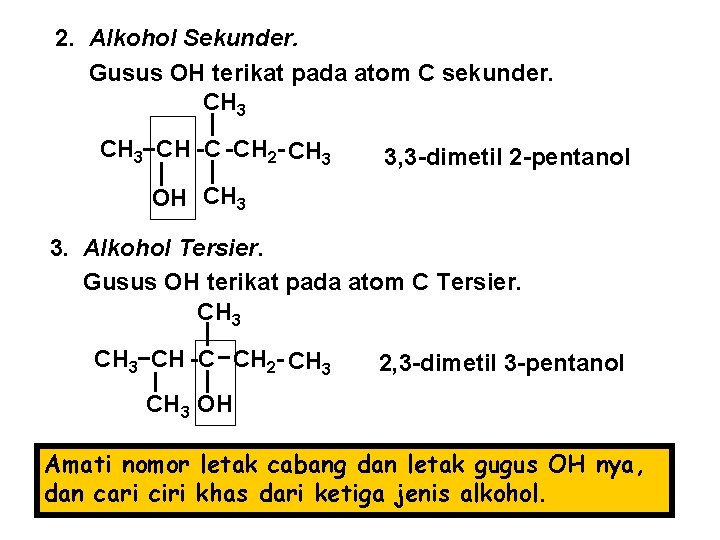
2. Alkohol Sekunder. Gusus OH terikat pada atom C sekunder. CH 3 CH -C -CH 2 - CH 3 3, 3 -dimetil 2 -pentanol OH CH 3 3. Alkohol Tersier. Gusus OH terikat pada atom C Tersier. CH 3 CH -C CH 2 - CH 3 2, 3 -dimetil 3 -pentanol CH 3 OH Amati nomor letak cabang dan letak gugus OH nya, dan cari ciri khas dari ketiga jenis alkohol.
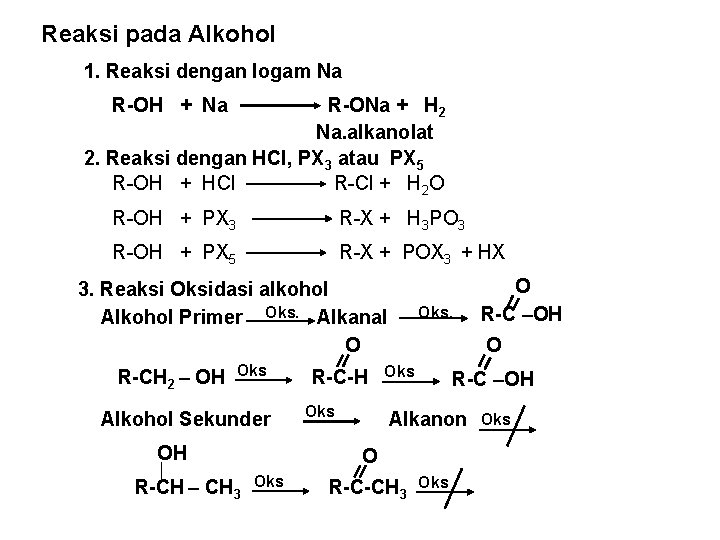
Reaksi pada Alkohol 1. Reaksi dengan logam Na R-OH + Na R-ONa + H 2 Na. alkanolat 2. Reaksi dengan HCl, PX 3 atau PX 5 R-OH + HCl R-Cl + H 2 O R-OH + PX 3 R-X + H 3 PO 3 R-OH + PX 5 R-X + POX 3 + HX 3. Reaksi Oksidasi alkohol Alkohol Primer Oks. Alkanal O R-CH 2 – OH Oks Alkohol Sekunder OH R-CH – CH 3 R-C-H Oks. O Oks R-C –OH Alkanon O Oks O R-C –OH R-C-CH 3 Oks
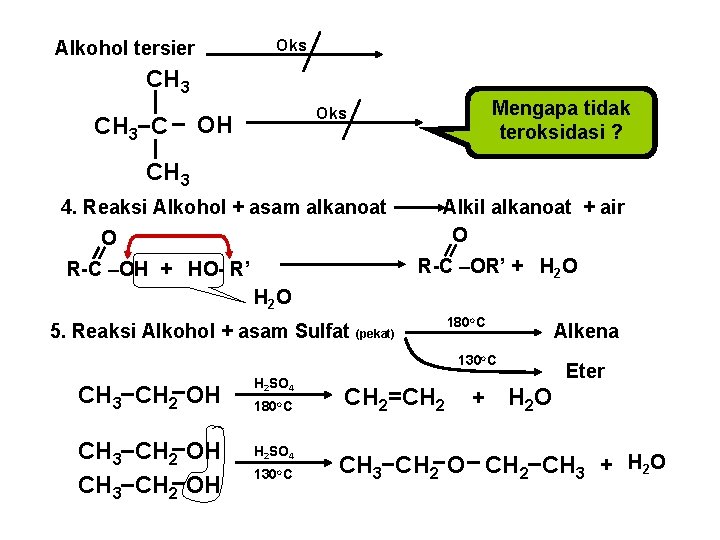
Oks Alkohol tersier CH 3 C Mengapa tidak teroksidasi ? Oks OH CH 3 4. Reaksi Alkohol + asam alkanoat O Alkil alkanoat + air O R-C –OR’ + H 2 O R-C –OH + HO- R’ H 2 O 5. Reaksi Alkohol + asam Sulfat (pekat) 180 o. C 130 o. C CH 3 CH 2 OH H 2 SO 4 180 o. C 130 o. C CH 2=CH 2 Alkena Eter + H 2 O CH 3 CH 2 O CH 2 CH 3 + H 2 O
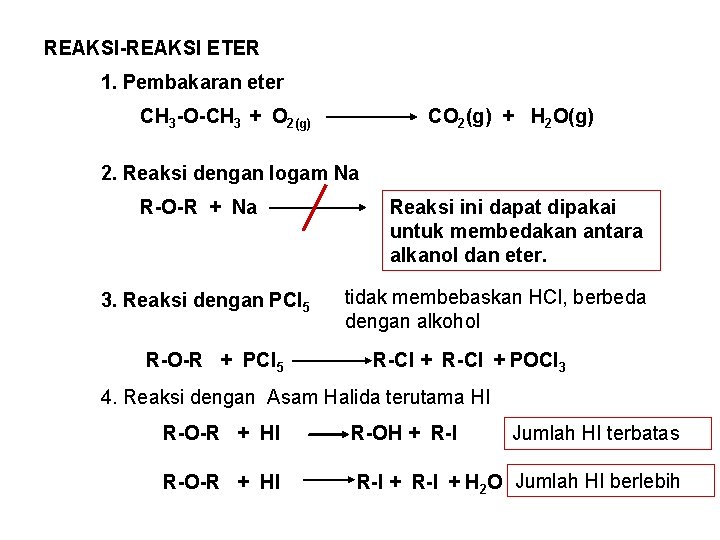
REAKSI-REAKSI ETER 1. Pembakaran eter CH 3 -O-CH 3 + O 2(g) CO 2(g) + H 2 O(g) 2. Reaksi dengan logam Na R-O-R + Na 3. Reaksi dengan PCl 5 R-O-R + PCl 5 Reaksi ini dapat dipakai untuk membedakan antara alkanol dan eter. tidak membebaskan HCl, berbeda dengan alkohol R-Cl + POCl 3 4. Reaksi dengan Asam Halida terutama HI R-O-R + HI R-OH + R-I R-O-R + HI R-I + H 2 O Jumlah HI berlebih Jumlah HI terbatas
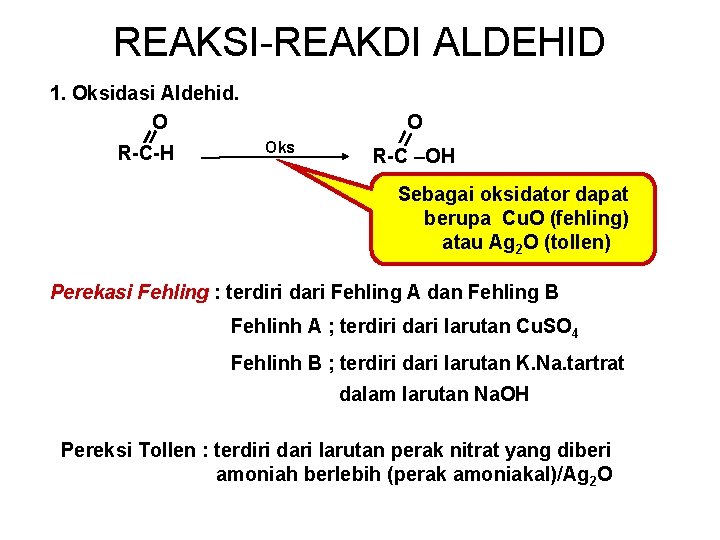
REAKSI-REAKDI ALDEHID 1. Oksidasi Aldehid. O R-C-H O Oks R-C –OH Sebagai oksidator dapat berupa Cu. O (fehling) atau Ag 2 O (tollen) Perekasi Fehling : terdiri dari Fehling A dan Fehling B Fehlinh A ; terdiri dari larutan Cu. SO 4 Fehlinh B ; terdiri dari larutan K. Na. tartrat dalam larutan Na. OH Pereksi Tollen : terdiri dari larutan perak nitrat yang diberi amoniah berlebih (perak amoniakal)/Ag 2 O
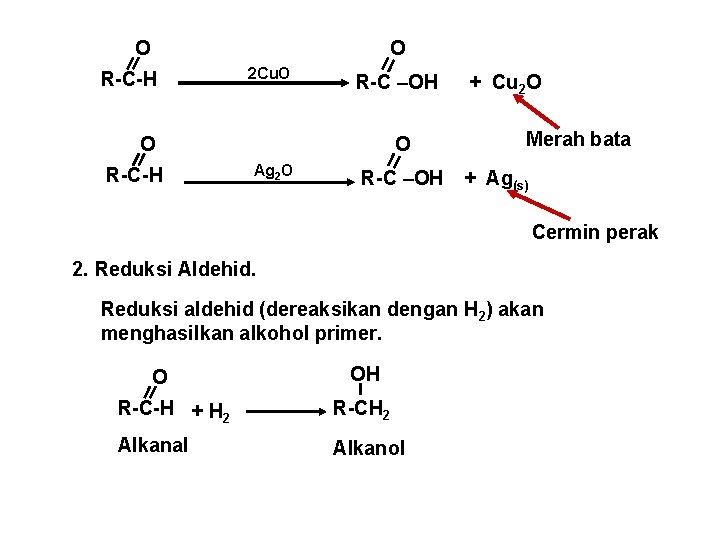
O O R-C-H 2 Cu. O R-C –OH O R-C-H O Ag 2 O + Cu 2 O Merah bata R-C –OH + Ag(s) Cermin perak 2. Reduksi Aldehid. Reduksi aldehid (dereaksikan dengan H 2) akan menghasilkan alkohol primer. O OH R-C-H + H 2 R-CH 2 Alkanal Alkanol

- Slides: 31