STRUKTUR ATOM q Model atom Thomson q Percobaan

STRUKTUR ATOM q Model atom Thomson q Percobaan Geiger & Marsden q Model atom Rutherford q Spektral atom q Model atom Bohr q Eksitasi atom
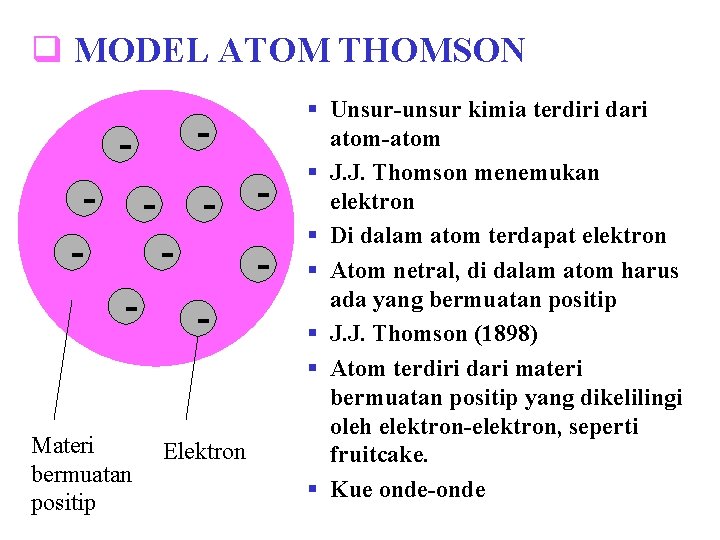
q MODEL ATOM THOMSON - - - Materi bermuatan positip - Elektron § Unsur-unsur kimia terdiri dari atom-atom § J. J. Thomson menemukan elektron § Di dalam atom terdapat elektron § Atom netral, di dalam atom harus ada yang bermuatan positip § J. J. Thomson (1898) § Atom terdiri dari materi bermuatan positip yang dikelilingi oleh elektron-elektron, seperti fruitcake. § Kue onde-onde

q PERCOBAAN GEIGER & MARSDEN § Cara langsung untuk mengetahui apa isi fruitcake, masukkan jari tangan ke dalamnya, sebagai probe § Ernest Rutherford mengusulkan menggunakan partikel alpha sebagai probe § Partikel alpha = inti Helium bermuatan + 2 e § Massa partikel alpha = 8000 massa elektron § Hans Geiger dan Ernest Marsden (1911) menggunakan partikel alpha cepat (2 x 107 m/s) § Hamburan partikel alpha akibat tumbukan dengan lapisan tipis emas diamati dan diukur
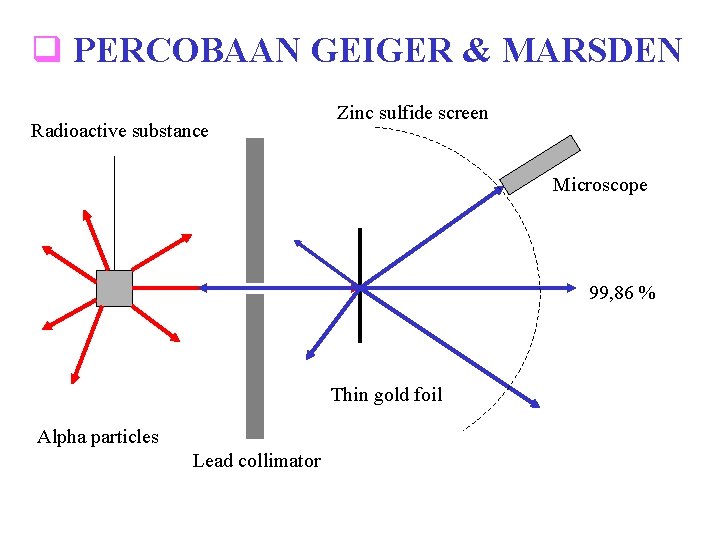
q PERCOBAAN GEIGER & MARSDEN Radioactive substance Zinc sulfide screen Microscope 99, 86 % Thin gold foil Alpha particles Lead collimator
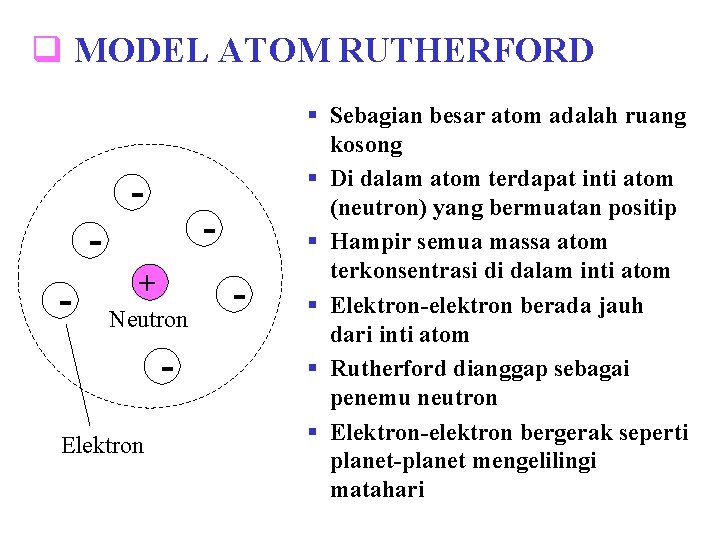
q MODEL ATOM RUTHERFORD - - - + Neutron Elektron - § Sebagian besar atom adalah ruang kosong § Di dalam atom terdapat inti atom (neutron) yang bermuatan positip § Hampir semua massa atom terkonsentrasi di dalam inti atom § Elektron-elektron berada jauh dari inti atom § Rutherford dianggap sebagai penemu neutron § Elektron-elektron bergerak seperti planet-planet mengelilingi matahari
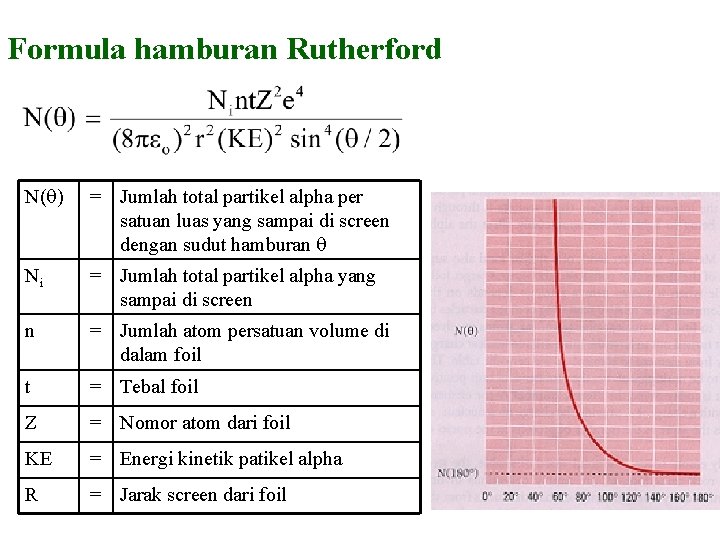
Formula hamburan Rutherford N( ) = Jumlah total partikel alpha per satuan luas yang sampai di screen dengan sudut hamburan Ni = Jumlah total partikel alpha yang sampai di screen n = Jumlah atom persatuan volume di dalam foil t = Tebal foil Z = Nomor atom dari foil KE = Energi kinetik patikel alpha R = Jarak screen dari foil
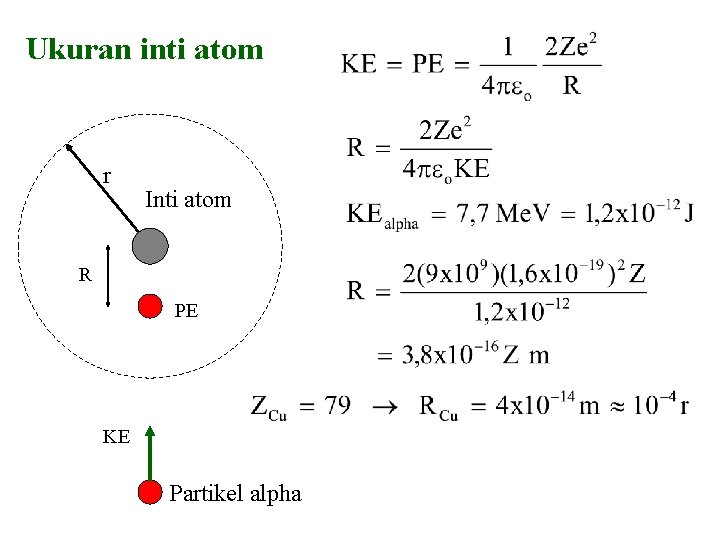
Ukuran inti atom r Inti atom R PE KE Partikel alpha
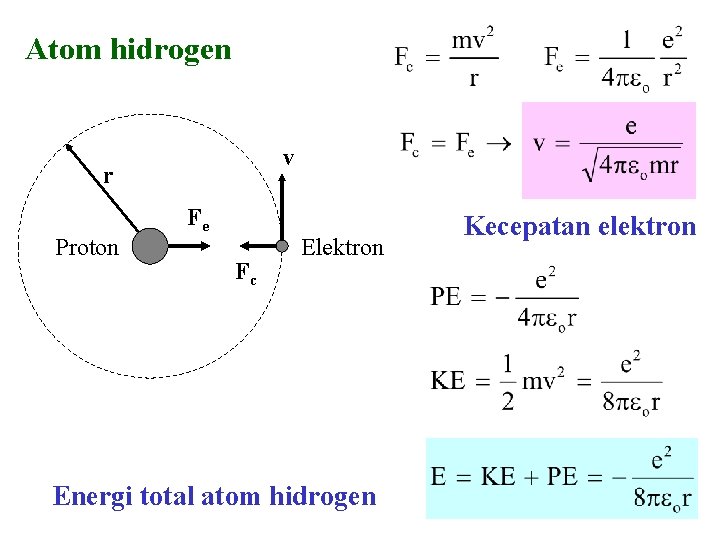
Atom hidrogen v r Proton Fe Fc Elektron Energi total atom hidrogen Kecepatan elektron

Contoh Soal 3. 1 Dari percobaan-percobaan diperoleh bahwa diperlukan energi sebesar 13, 6 e. V untuk memisahkan atom hidrogen menjadi sebuah proton dan sebuah elektron. Ini berarti bahwa energi total atom hidrogen adalah E = - 13, 6 e. V. Tentukan kecepatan dan jari-jari orbit elektron dari atom hidrogen. Jawab :

Kegagalan model atom klasik § Mekanik : Hukum Newton § Listrik : Hukum Coulomb § Elektromagnetik : partikel bermuatan yang sedang bergerak akan meradiasikan energi dalam bentuk gelombang elektromagnetik § Energi berkurang, sambil berputar elektron bergerak menuju proton § Kenyataannya atom selalu stabil § Fisika klasik gagal karena menggunakan pendekatan partikel murni dan gelombang murni

q SPEKTRAL ATOM § Atom dalam fasa gas diberi arus listrik § Setiap atom ternyata mengemisikan gelombang-gelombang dengan panjang gelombang tertentu (emission line spectra)

q SPEKTRAL ATOM § Setiap atom juga menyerap gelombang-gelombang dengan panjang gelombang tertentu (absorption line spectra) § Panjang gelombang yang diemisikan ternyata sama dengan panjang gelombang yang diserap § Diperlukan model atom yang dapat menerangkan kestabilan atom dan adanya garis-garis spektrum
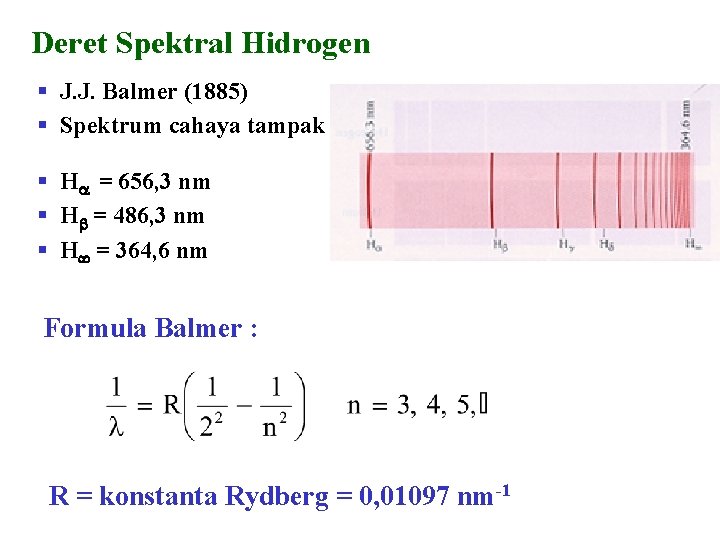
Deret Spektral Hidrogen § J. J. Balmer (1885) § Spektrum cahaya tampak § H = 656, 3 nm § H = 486, 3 nm § H = 364, 6 nm Formula Balmer : R = konstanta Rydberg = 0, 01097 nm-1
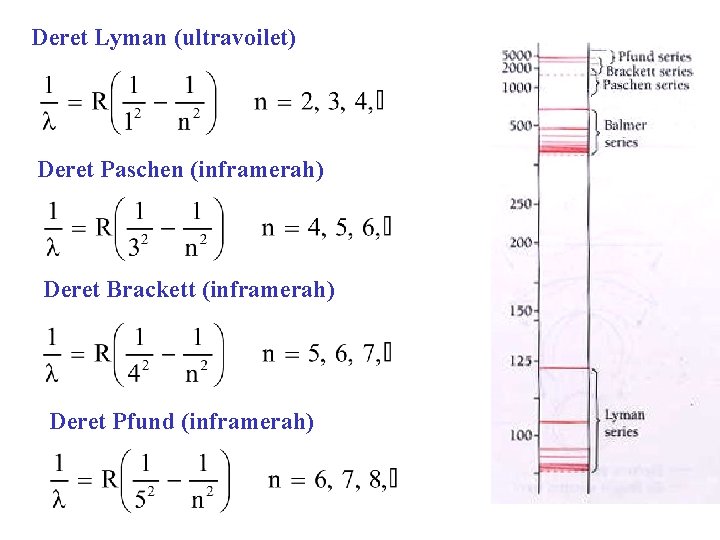
Deret Lyman (ultravoilet) Deret Paschen (inframerah) Deret Brackett (inframerah) Deret Pfund (inframerah)

q MODEL ATOM BOHR § Niels Bohr (1913) § Konsep gelombang materi § Menggunakan pendekatan yang lain, tetapi hasilnya sama dengan Broglie § Keliling orbit elektron yang mengelilingi inti atom hidrogen (proton) ternyata sama dengan panjang gelombangnya § Terdapat analogi dengan vibrasi/gelombang pada tali/kawat

Sebuah elektron hanya dapat mengelilingi inti atom bila lintasan orbitnya merupakan kelipatan bulat dari panjang gelombang Broglie-nya n=2 n=4 n = bilangan kuantum Jari-jari Bohr = ao = r 1 = 5, 292 x 10 -11 m n=8

Tingkat Energi Atom Hidrogen Ground state Excited states
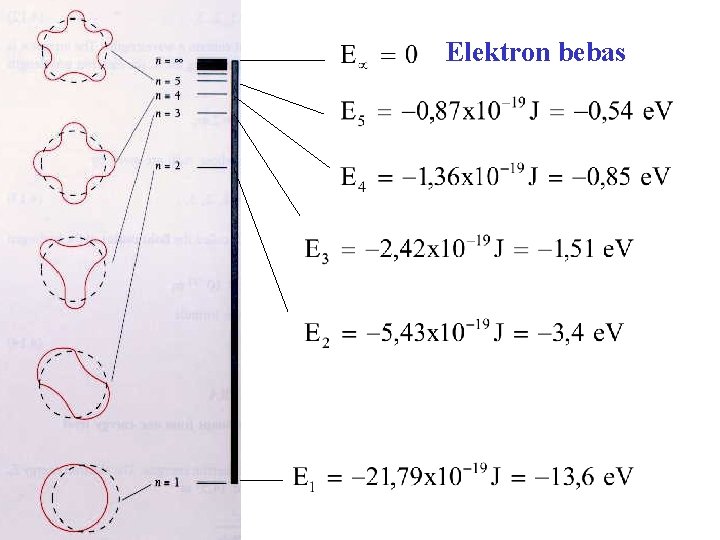
Elektron bebas

Contoh Soal 3. 2 Sebuah elektron bertumbukan dengan sebuah atom hidrogen yang sedang berada pada tinggat dasar (ground state). Bila atom hidrogen ini sekarang berada pada tingkat terekstasi (n = 3), berapa energi yang telah diberikan oleh elektron kepada atom hidrogen dalam tumbukan tersebut ? Jawab :

Contoh Soal 3. 3 Atom-atom hidrogen pada bilangan kuantum yang sangat tinggi dapat dibuat di laboratorium dan diamati di ruang angkasa. a). Tentukan bilangan kuantum dimana orbit Bohr = 0, 01 mm b). Hitung energi atom hidrogen tersebut Jawab : a). b).

Garis-garis Spektrum § Setelah mendapat energi, tingkat energi atom naik § Bila tingkat energinya turun, maka tentunya atom akan mengeluarkan (mengemisikan) energi § Energi yang diemisikan atom berupa foton Energi awal – Energi akhir = Energi foton

Deret Lyman Deret Balmer Deret Paschen Deret Brackett Deret Pfund

Contoh Soal 3. 4 Hitung panjang gelombang terbesar yang terdpat pada deret Balmer dari atom hidrogen (H ). Jawab : Deret Balmer :
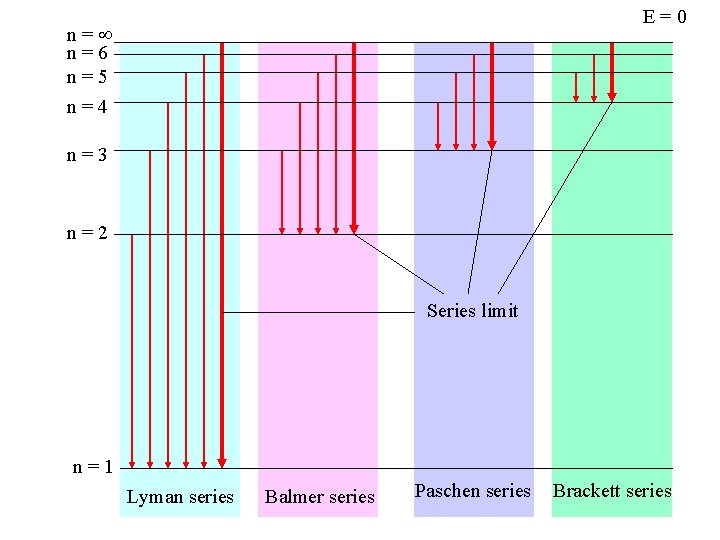
E=0 n= n=6 n=5 n=4 n=3 n=2 Series limit n=1 Lyman series Balmer series Paschen series Brackett series

q EKSITASI ATOM § Atom akan mampu meradiasikan energi bila berada dalam keadaan tereksitasi § Mekanisme 1: Tumbukan dengan partikel lain § Atom akan menyerap sebagian energi kinetik dari partikel yang menumbuknya § Atom akan kembali kekeadaan semula dengan mengemisikan satu atau lebih foton dalam waktu singkat (10 -8 s) § Mekanisme 2 : Interaksi dengan cahaya pada panjang gelombang tertentu § Atom akan kembali kekeadaan semula sambil mengemisikan foton dengan panjang gelombang yang sama
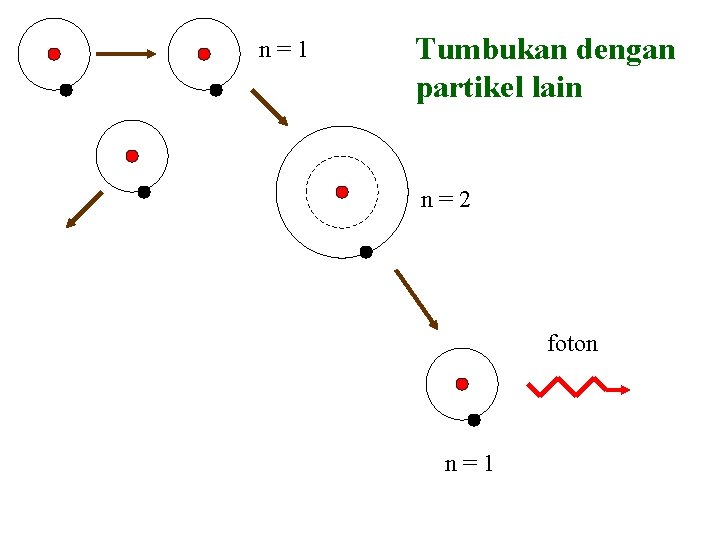
n=1 Tumbukan dengan partikel lain n=2 foton n=1
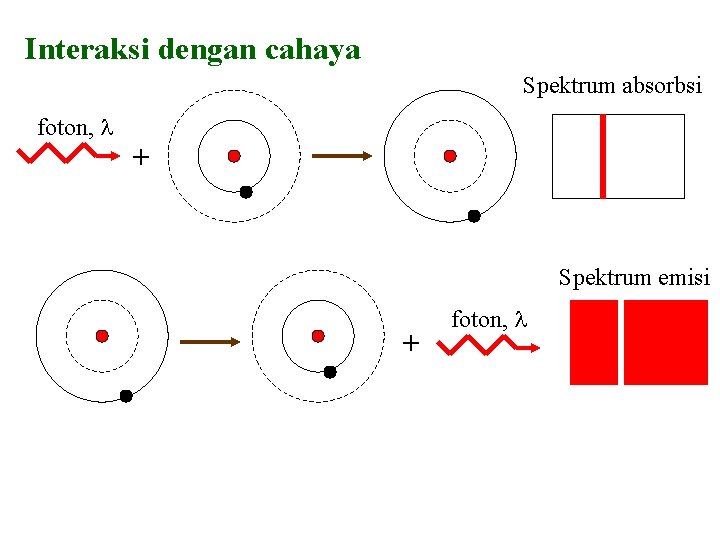
Interaksi dengan cahaya Spektrum absorbsi foton, + Spektrum emisi + foton,
- Slides: 27