STRUKTUR ATOM dan SISTEM PERIODIK TEORI ATOM 1










- Slides: 26

STRUKTUR ATOM dan SISTEM PERIODIK

TEORI ATOM

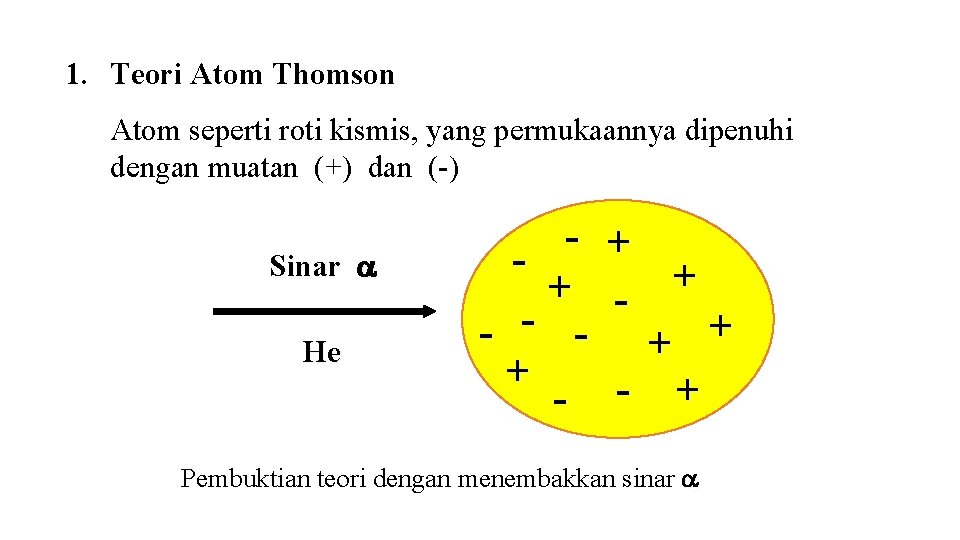
1. Teori Atom Thomson Atom seperti roti kismis, yang permukaannya dipenuhi dengan muatan (+) dan (-) Sinar He + + - + Pembuktian teori dengan menembakkan sinar

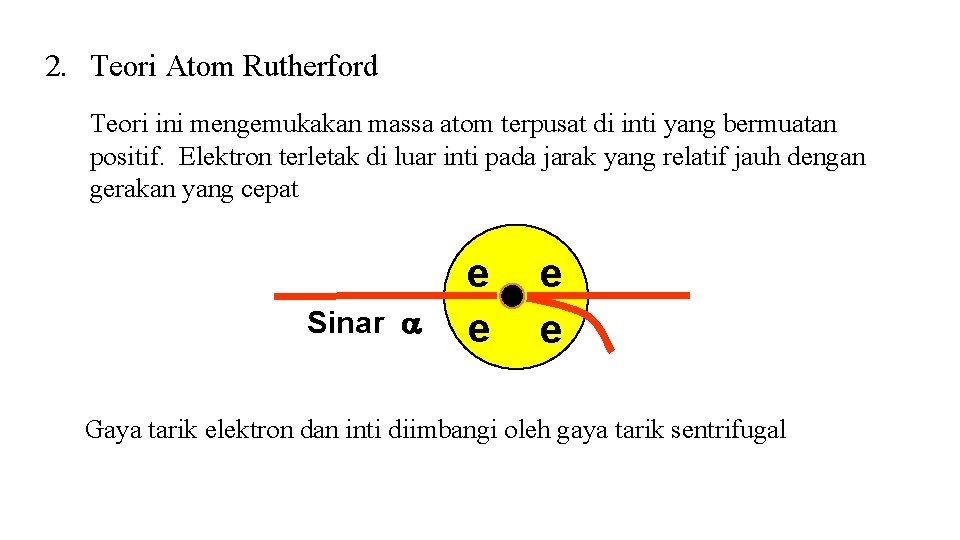
2. Teori Atom Rutherford Teori ini mengemukakan massa atom terpusat di inti yang bermuatan positif. Elektron terletak di luar inti pada jarak yang relatif jauh dengan gerakan yang cepat Sinar e e Gaya tarik elektron dan inti diimbangi oleh gaya tarik sentrifugal

Menurut hukum fisika klasik, partikel bermuatan yang bergerak selalu kehilangan energi, dengan demikian gerakan elektron makin mendekati inti dan terjadi gerakan spiral dengan kecepatan menurun. Pada suatu saat elektron bergabung dengan inti dan atom akan musnah. Dalam kenyataannya atom tidak musnah.

3. Teori Atom Bohr Kesukaran pada teori atom Rutherford diatasi oleh Bohr. Gerakan elektron mengelilingi inti harus dengan momentum sudut tertentu. a. Elektron dalam lintasannya mempunyai energi tertentu dan tetap selama dalam lintasan b. Elektron dapat pindah dari lintasan yang energinya lebih tinggi ke lintasan yang energinya lebih rendah. Bila hal ini terjadi, energi yang terbebas diubah menjadi sinar dengan frekuensi 5

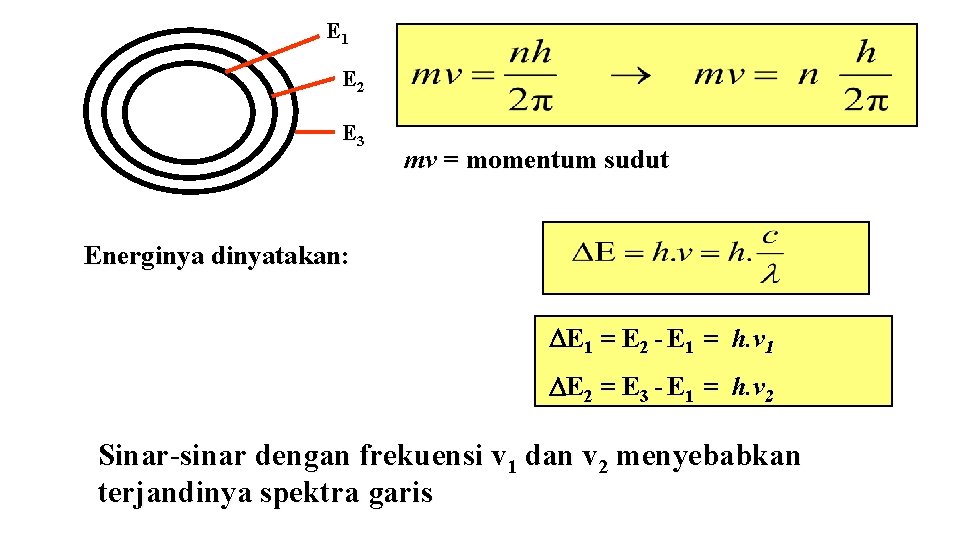
E 1 E 2 E 3 mv = momentum sudut Energinya dinyatakan: E 1 = E 2 - E 1 = h. v 1 E 2 = E 3 - E 1 = h. v 2 Sinar-sinar dengan frekuensi v 1 dan v 2 menyebabkan terjandinya spektra garis

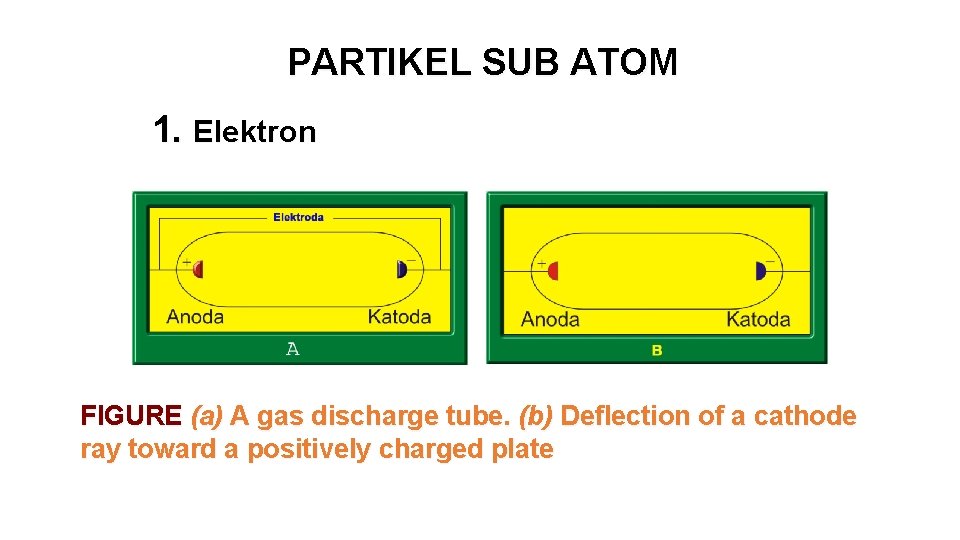
PARTIKEL SUB ATOM 1. Elektron FIGURE (a) A gas discharge tube. (b) Deflection of a cathode ray toward a positively charged plate

2. Percobaan Millikan: Penentuan Massa Elektron FIGURE Millikan’s famous oil drop experiment e = - 1, 60 x 1019 C

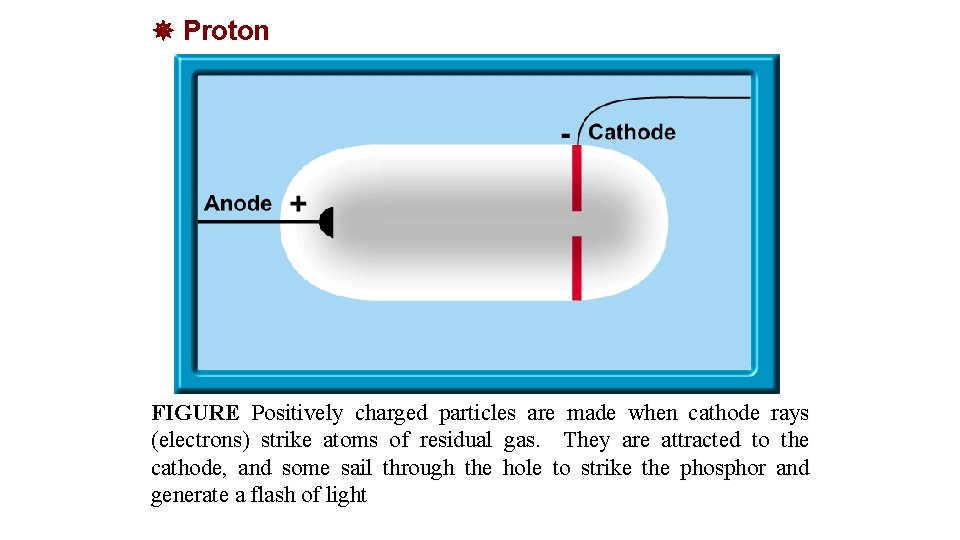
Proton FIGURE Positively charged particles are made when cathode rays (electrons) strike atoms of residual gas. They are attracted to the cathode, and some sail through the hole to strike the phosphor and generate a flash of light

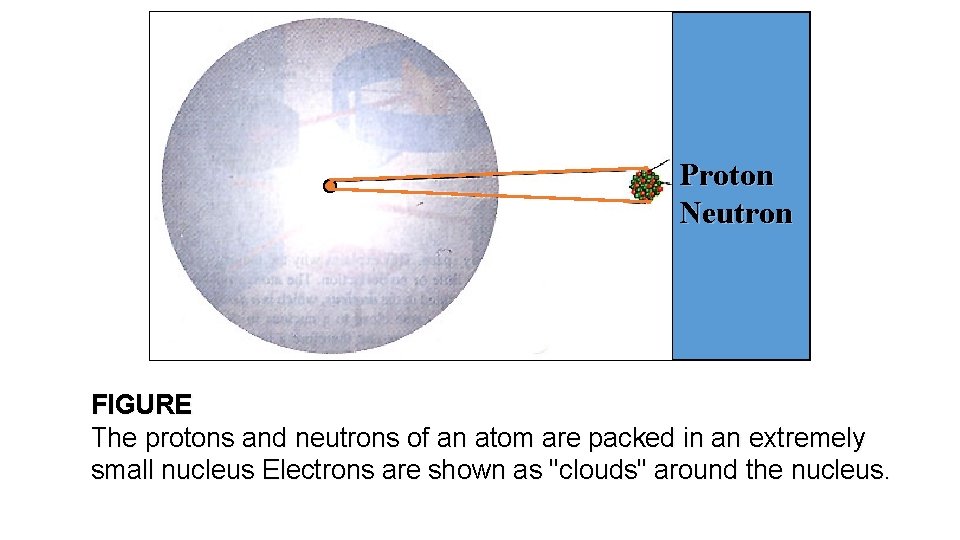
Proton Neutron FIGURE The protons and neutrons of an atom are packed in an extremely small nucleus Electrons are shown as "clouds" around the nucleus.

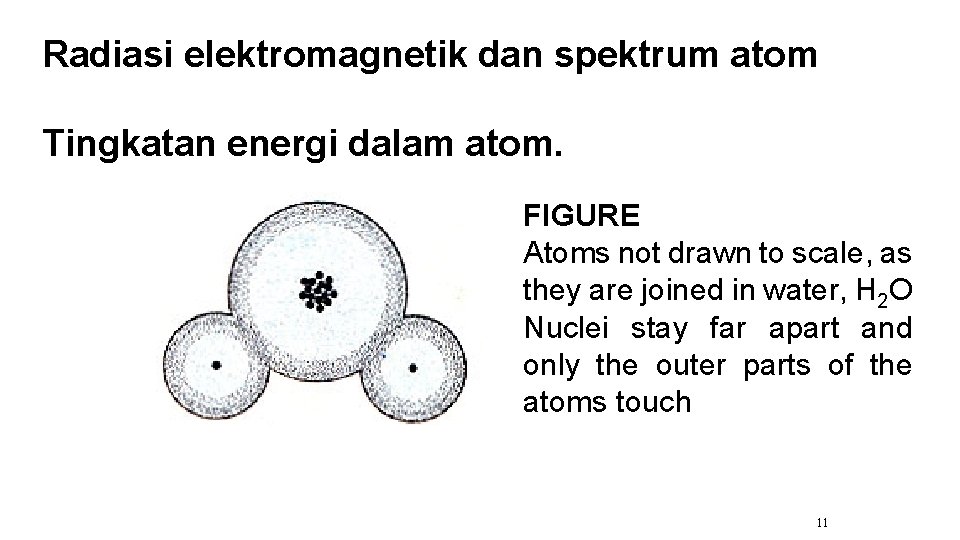
Radiasi elektromagnetik dan spektrum atom Tingkatan energi dalam atom. FIGURE Atoms not drawn to scale, as they are joined in water, H 2 O Nuclei stay far apart and only the outer parts of the atoms touch 11

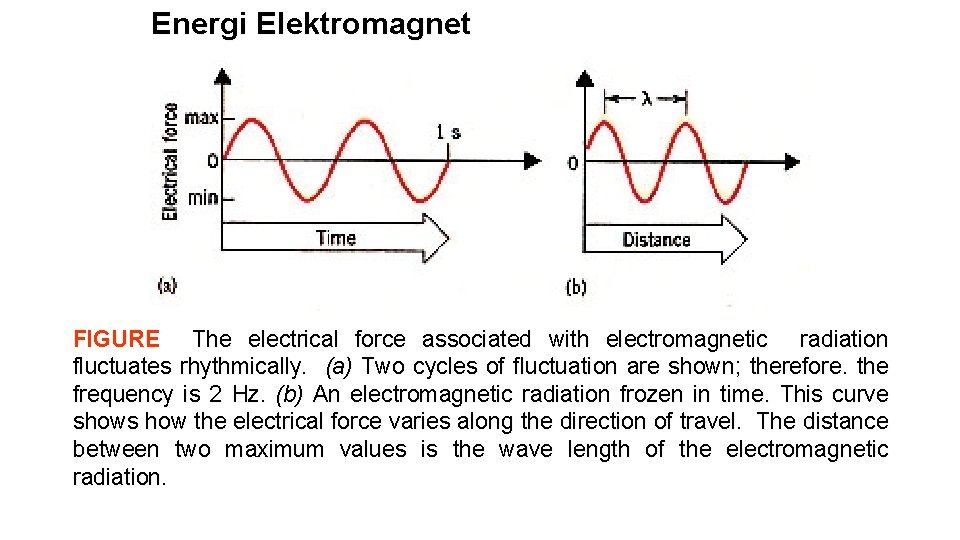
Energi Elektromagnet FIGURE The electrical force associated with electromagnetic radiation fluctuates rhythmically. (a) Two cycles of fluctuation are shown; therefore. the frequency is 2 Hz. (b) An electromagnetic radiation frozen in time. This curve shows how the electrical force varies along the direction of travel. The distance between two maximum values is the wave length of the electromagnetic radiation.

The SI symbol for the second is s. S-1 = 1/s For any wave, the product of its wavelength and its frequency equals the velocity of the wave. Hertz 1 Hz Lamda Kec. Cahaya . = = = (Hz) 1 s-1 = Panjang Gelombang c = 3, 00 x 108 ms-1

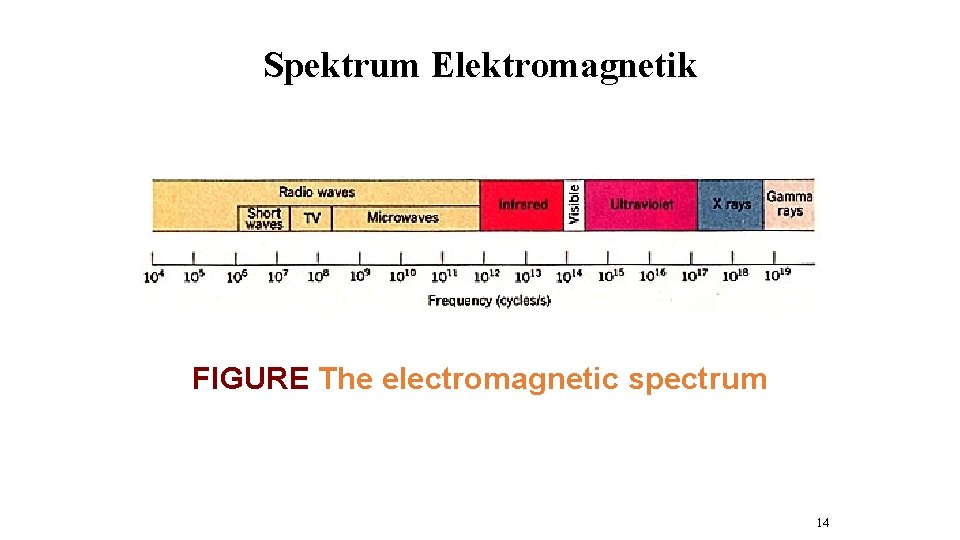
Spektrum Elektromagnetik FIGURE The electromagnetic spectrum 14

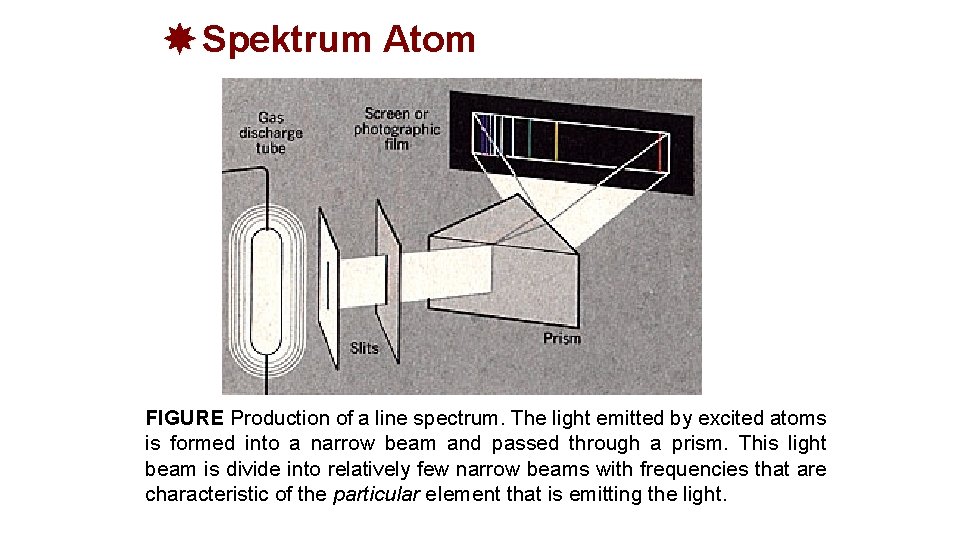
Spektrum Atom FIGURE Production of a line spectrum. The light emitted by excited atoms is formed into a narrow beam and passed through a prism. This light beam is divide into relatively few narrow beams with frequencies that are characteristic of the particular e. Iement that is emitting the light.

Spektrum Unsur

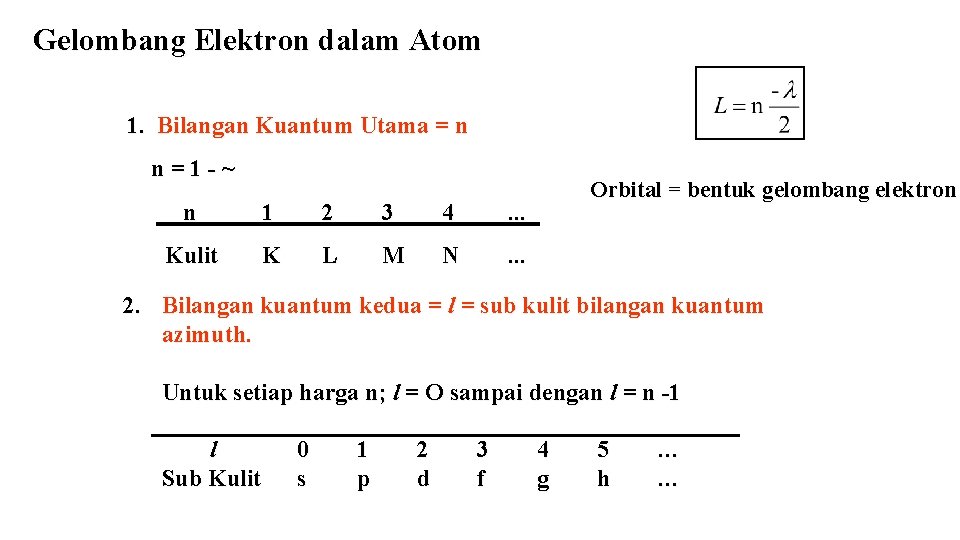
Gelombang Elektron dalam Atom 1. Bilangan Kuantum Utama = n n=1 -~ n 1 2 3 4 . . . Kulit K L M N . . . Orbital = bentuk gelombang elektron 2. Bilangan kuantum kedua = l = sub kulit bilangan kuantum azimuth. Untuk setiap harga n; l = O sampai dengan l = n -1 l Sub Kulit 0 s 1 p 2 d 3 f 4 g 5 h … …

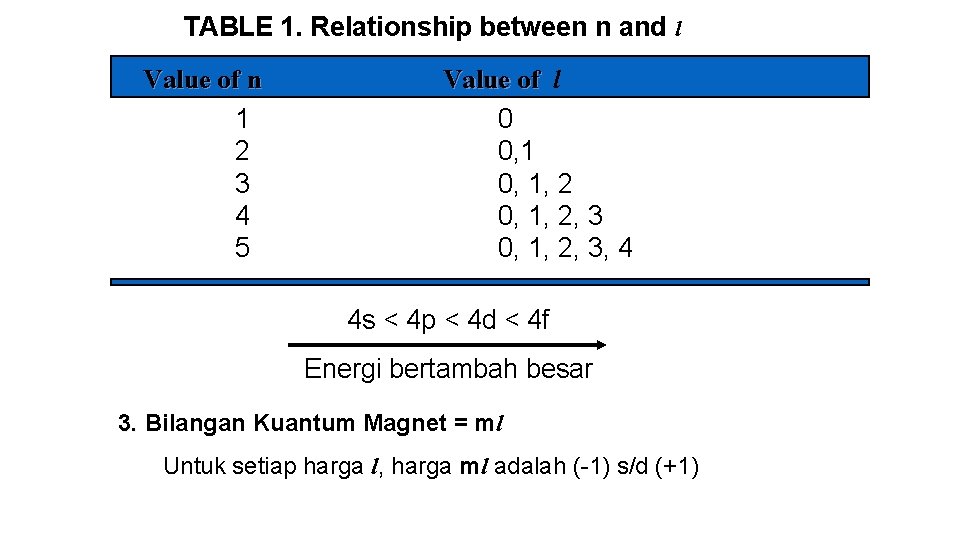
TABLE 1. Relationship between n and l Value of n 1 2 3 4 5 Value of l 0 0, 1, 2, 3, 4 4 s < 4 p < 4 d < 4 f Energi bertambah besar 3. Bilangan Kuantum Magnet = ml Untuk setiap harga l, harga ml adalah (-1) s/d (+1)

Spin Elektron = ms ms = + ½ atau – ½ (Prinsip Pauli)

20

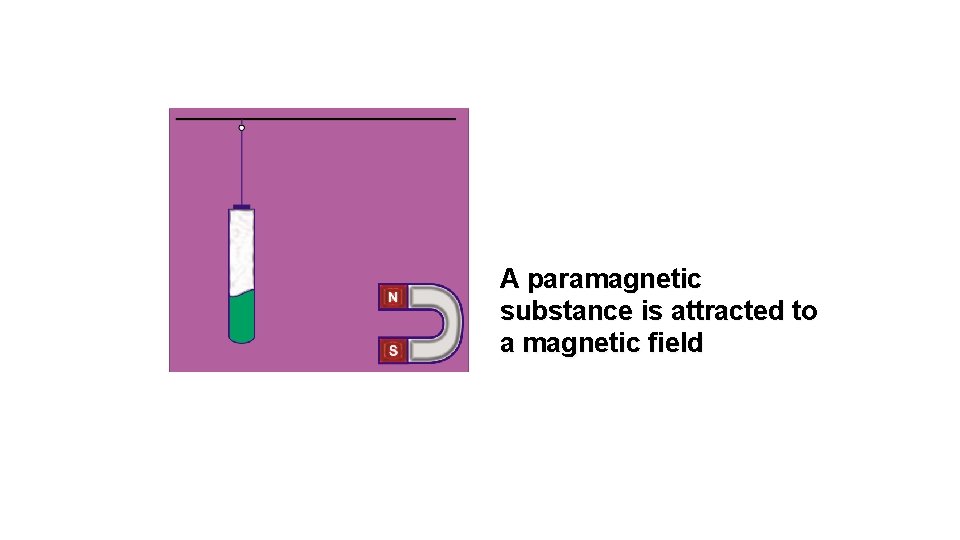
A paramagnetic substance is attracted to a magnetic field

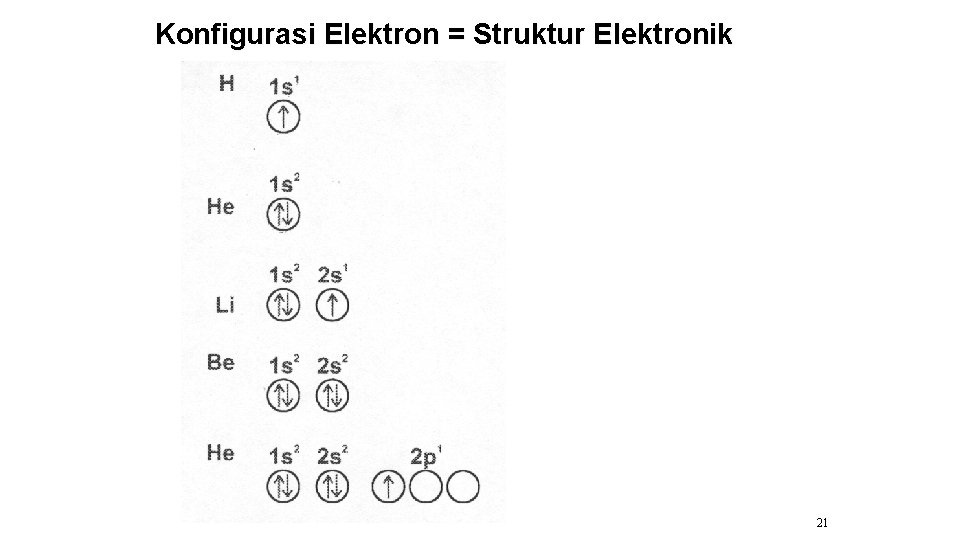
Konfigurasi Elektron = Struktur Elektronik 21

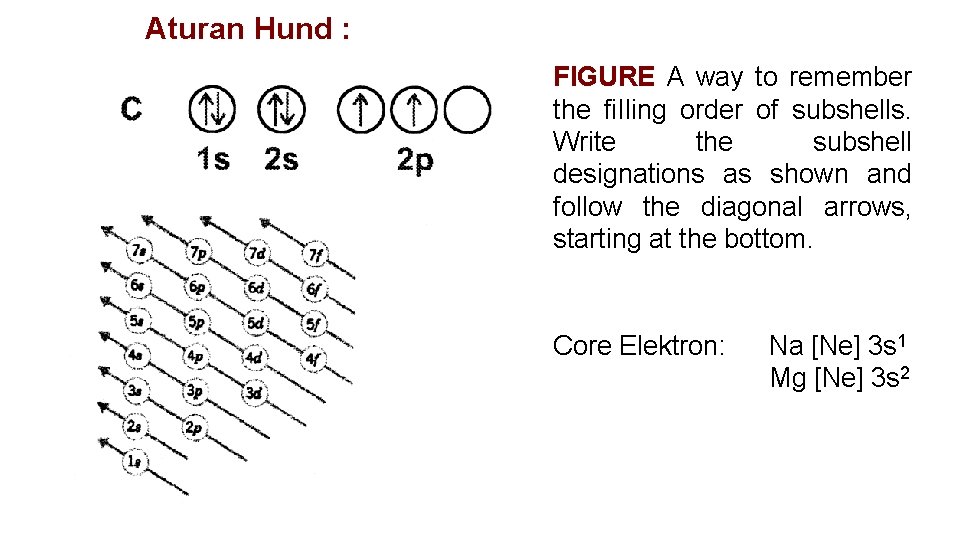
Aturan Hund : FIGURE A way to remember the fi. Iling order of subshells. Write the subshell designations as shown and follow the diagonal arrows, starting at the bottom. Core Elektron: Na [Ne] 3 s 1 Mg [Ne] 3 s 2

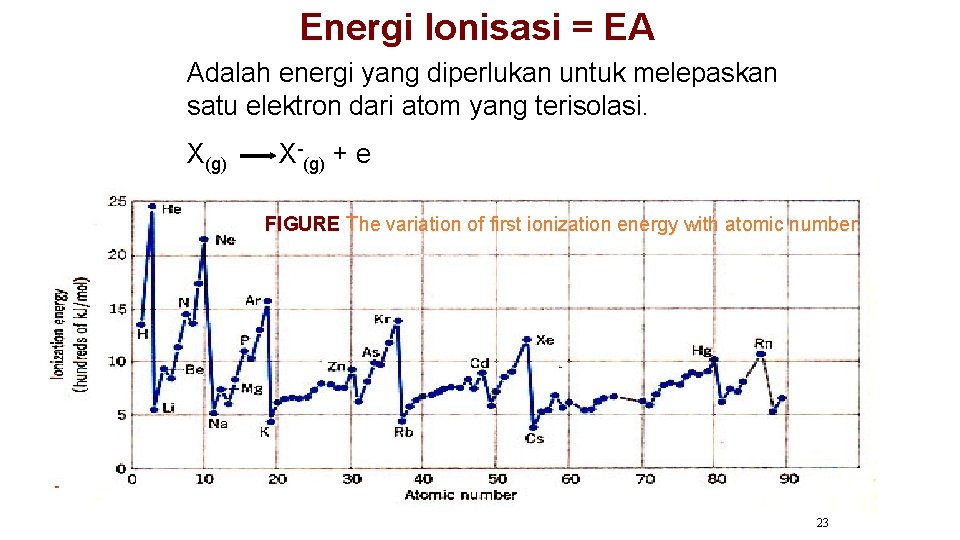
Energi lonisasi = EA Adalah energi yang diperlukan untuk melepaskan satu elektron dari atom yang terisolasi. X(g) X-(g) + e FIGURE The variation of first ionization energy with atomic number 23

Afinitas Elektron = EA Adalah energi yang dilepaskan untuk menerima satu elektron dari atom yang terisolasi. X(g) + e- X-(g) 24