Structural Biochemistry Molecular Biophysics Laboratory yjjungspin yonsei ac

Structural Biochemistry & Molecular Biophysics Laboratory 정영진 yjjung@spin. yonsei. ac. kr

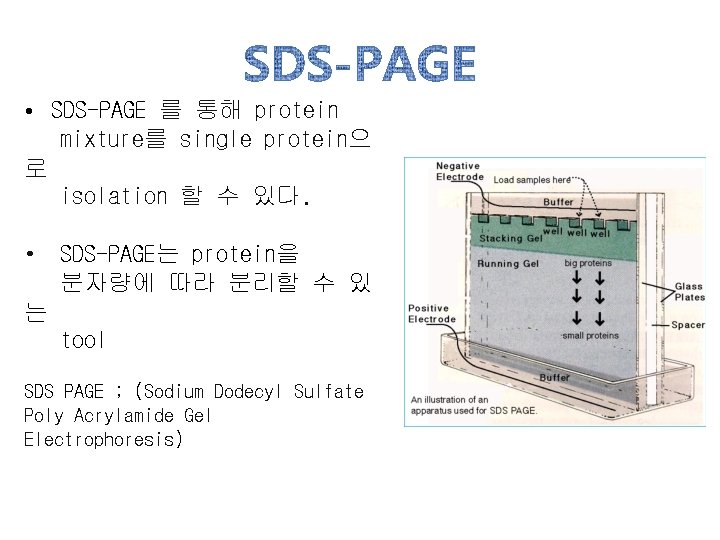
• SDS-PAGE 를 통해 protein mixture를 single protein으 로 isolation 할 수 있다. • SDS-PAGE는 protein을 분자량에 따라 분리할 수 있 는 tool SDS PAGE ; (Sodium Dodecyl Sulfate Poly Acrylamide Gel Electrophoresis)

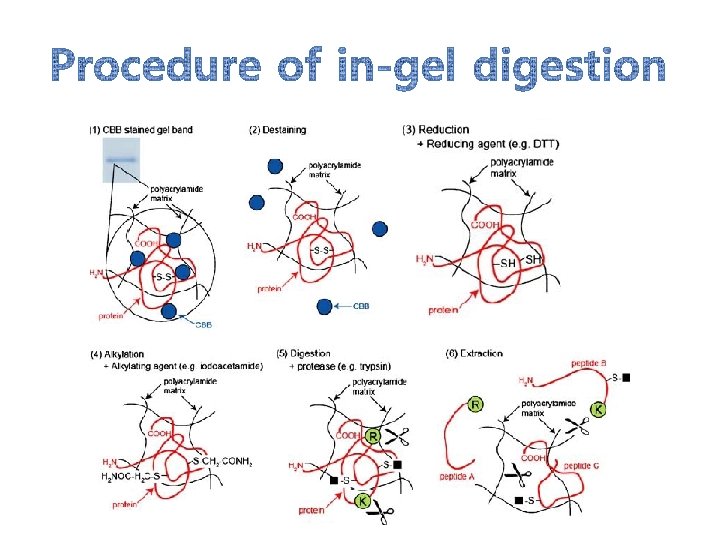
In-gel digestion procedure은 peptide를 fragmentation 후, mass analyzer를 통하여 fragment를 분석 할 수 있 다.

• Mass spectra의 quality는 sample의 amount나 purity 에 의존한다. • Peptide의 concentration이 signal intensity나 spectra를 해석하는데 직접적으로 연관 되어진다. • Sample의 양이 많을수록 얻어지는 information은 증가 하고 이러한 information을 통하여 일치하는 protein 을 찾을 수 있다.

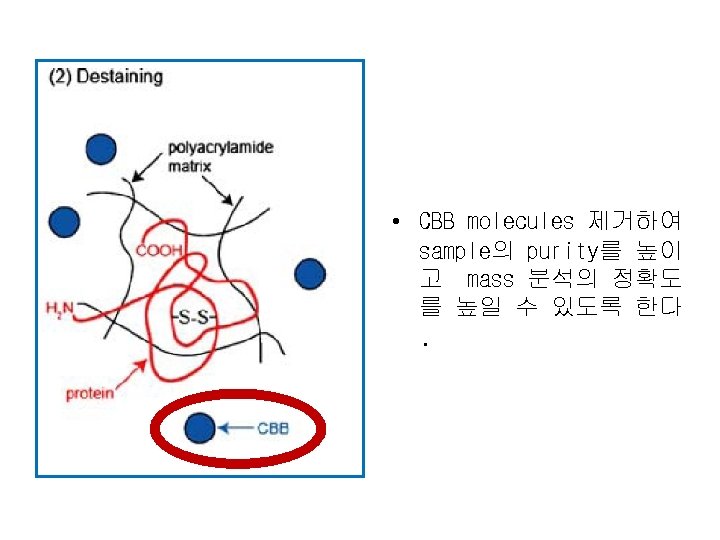
• Protein preparation, separation, purification, and in-gel digestion 과정 중 많은 protein의 loss가 발 생할 수 있다. • Protein or peptide loss가 destaining과정 중에 발생 할 수 있다. (by adsorption on surfaces of pipette tips and digestion tubes, during drying of samples in a vacuum concentrator) 결과적으로 gel로부터 완 벽하게 peptide를 extraction 할 수 없다. • In-gel digestion과정을 최소화 하는 것이 peptide loss를 최소화 할 수 있다.
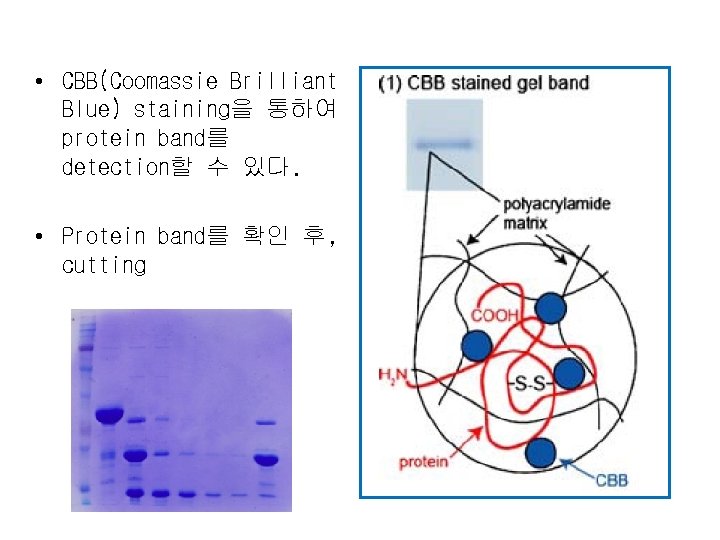
• CBB(Coomassie Brilliant Blue) staining을 통하여 protein band를 detection할 수 있다. • Protein band를 확인 후, cutting
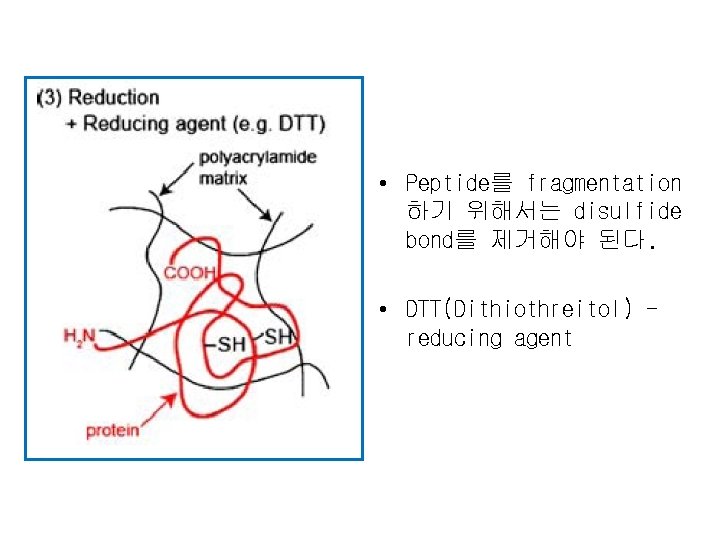
• Peptide를 fragmentation 하기 위해서는 disulfide bond를 제거해야 된다. • DTT(Dithiothreitol) reducing agent
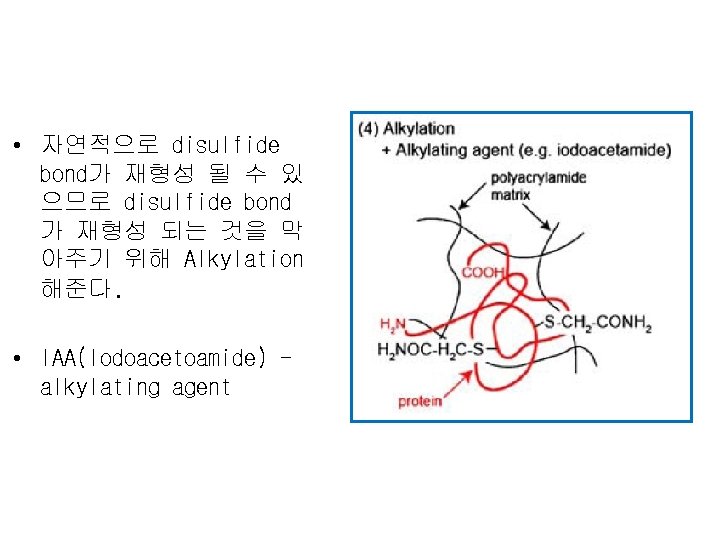
• 자연적으로 disulfide bond가 재형성 될 수 있 으므로 disulfide bond 가 재형성 되는 것을 막 아주기 위해 Alkylation 해준다. • IAA(Iodoacetoamide) alkylating agent
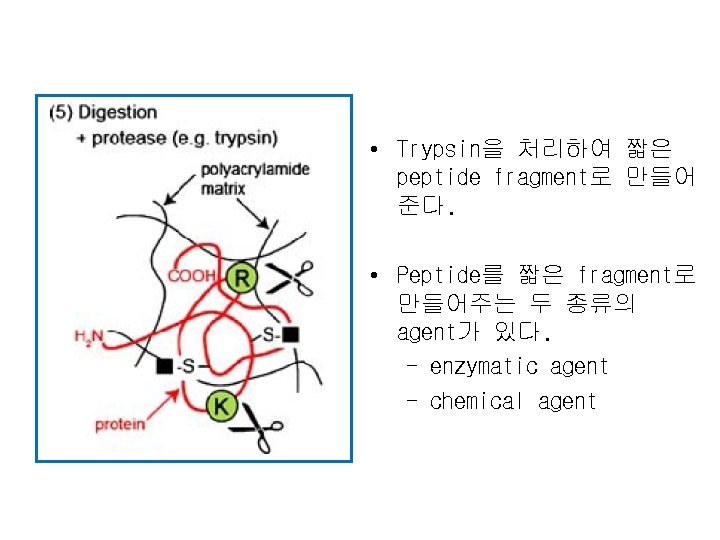
• Trypsin을 처리하여 짧은 peptide fragment로 만들어 준다. • Peptide를 짧은 fragment로 만들어주는 두 종류의 agent가 있다. - enzymatic agent - chemical agent



- Wash buffer : 100% acetonitrile + 50 m. M NH 4 HCO 3(Ammonium Bicarbonate) 4 : 6으로 mix - 0. 01㎍/㎕ trypsin : trypsin 10㎕(0. 1㎍/㎕ stock) + 50 m. M NH 4 HCO 3 90 ㎕ 1. Gel에서 protein band를 확인한 뒤, 칼을 이용하여 gel을 잘라 1. 5 ml tube에 넣는다. 2. 각 Tube에 wash buffer 200㎕를 넣는다. 3. 호일로 tube를 덮고 37℃ shaking incubator에서 incubation한다. (15분) 4. Wash buffer를 제거한 후, 새로운 wash buffer 200㎕ 를 넣어준 뒤 incubation(5분). (dye가 완전히 빠질때까지 이 과정을 반복해 준다. ) 5. Dye가 완전히 빠지면 wash buffer를 제거한 후 Acetonitrile 100% 200 ul넣고, 37℃ shaking incubator에서 incubation한다. (3분) Gel

- Slides: 16