Strategie zum Aufstellen von Redoxgleichungen Th Bse Chrom
Strategie zum Aufstellen von Redoxgleichungen © Th. Böse

Chrom (III)-salzlösung wird im alkalischen Milieu mit Wasserstoffperoxid versetzt, so dass Chromat-Ionen entstehen. Kein Problem für Professor Theo Retisch. Pass mal auf……. . …… © Th. Böse
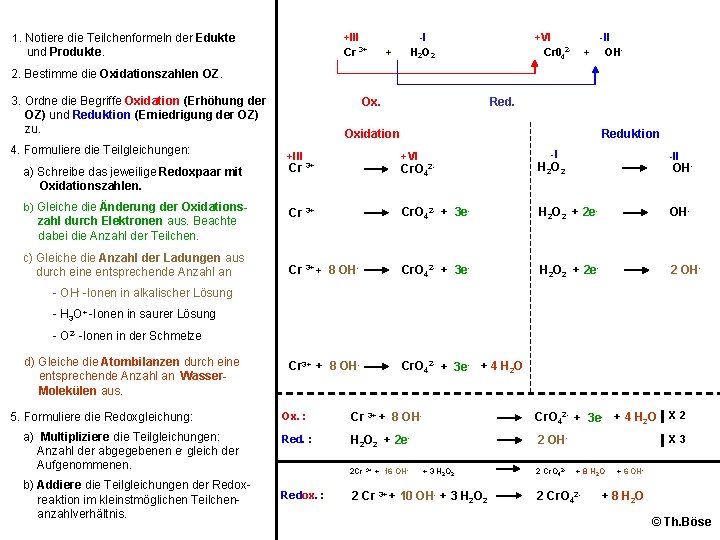
+III Cr 3+ 1. Notiere die Teilchenformeln der Edukte und Produkte. -I H 2 O 2 + +VI Cr 042 - + -II OH- 2. Bestimme die Oxidationszahlen OZ. 3. Ordne die Begriffe Oxidation (Erhöhung der OZ) und Reduktion (Erniedrigung der OZ) zu. 4. Formuliere die Teilgleichungen: a) Schreibe das jeweilige Redoxpaar mit Oxidationszahlen. b) Gleiche die Änderung der Oxidations- zahl durch Elektronen aus. Beachte dabei die Anzahl der Teilchen. c) Gleiche die Anzahl der Ladungen aus durch eine entsprechende Anzahl an Ox. Red. Oxidation Reduktion -I +III +VI Cr. O 42 - H 2 O 2 Cr 3+ Cr. O 42 - + 3 e- H 2 O 2 + 2 e- OH- Cr 3+ + 8 OH- Cr. O 42 - + 3 e- H 2 O 2 + 2 e- 2 OH- Cr 3+ + 8 OH- Cr. O 42 - + 3 e- + 4 H 2 O Cr 3+ -II OH- -Ionen in alkalischer Lösung - H 3 O+ -Ionen in saurer Lösung - O 2 - -Ionen in der Schmelze d) Gleiche die Atombilanzen durch eine entsprechende Anzahl an Wasser. Molekülen aus. 5. Formuliere die Redoxgleichung: a) Multipliziere die Teilgleichungen: Anzahl der abgegebenen e- gleich der Aufgenommenen. b) Addiere die Teilgleichungen der Redoxreaktion im kleinstmöglichen Teilchenanzahlverhältnis. Ox. : Cr 3+ + 8 OH- Cr. O 42 - + 3 e- + 4 H 2 O X 2 Red. : H 2 O 2 + 2 e- 2 OH- X 3 2 Cr Redox. : 3+ + 16 OH- + 3 H 2 O 2 2 Cr 3+ + 10 OH- + 3 H 2 O 2 2 Cr. O 42 - + 8 H 2 O 2 Cr. O 42 - + 6 OH- + 8 H 2 O © Th. Böse
- Slides: 3