STOIKIOMETRI Tim Dosen Pengampu MK Kimia Dasar FTPUB

STOIKIOMETRI Tim Dosen Pengampu MK Kimia Dasar FTPUB

Outlines : � � � � Pengertian Konsep mol Hubungan koefisien dalam persamaan reaksi dengan hitungan Kadar zat Pereaksi pembatas Reaksi yang melibatkan campuran Reaksi pengendapan Reaksi-reaksi pembuatan gas

Pengertian… Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) � Stoikiometri adalah hitungan kimia �
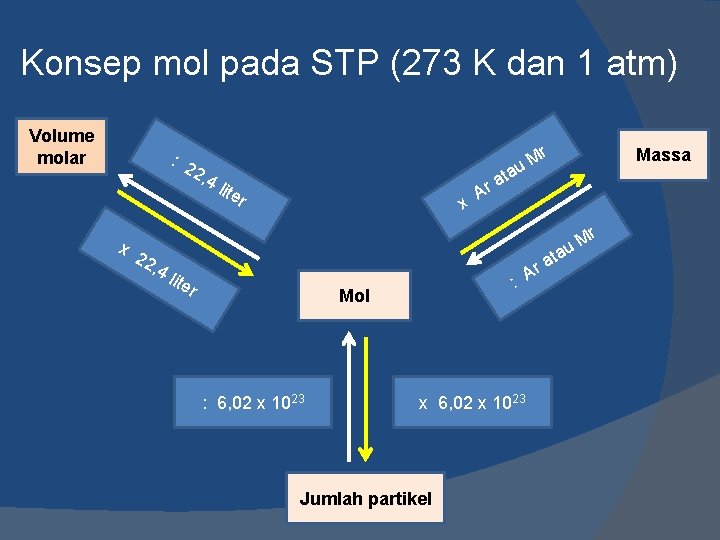
Konsep mol pada STP (273 K dan 1 atm) Volume molar r M u : 2 2, 4 lite r x 22 , 4 x Massa ta a r A ta r M u lite r : Mol : 6, 02 x 1023 x 6, 02 x 1023 Jumlah partikel a Ar

Hubungan koefisien dalam persamaan reaksi dengan hitungan a. Perbandingan koefisien pada persamaan reaksi sebanding dengan volume gas (T, P sama) Contoh: N 2(g) + 3 H 2(g) 2 NH 3(g) 3 liter ? ? Jawab: Perbandingan volum 3 lt : 3/1 x 3 lt : 2/1 x 3 lt : 9 lt : 6 lt 1 : 3 : 2

Hubungan koefisien dalam persamaan reaksi dengan hitungan b. Perbandingan koefisien pada persamaan reaksi sebanding dengan perbandingan mol Contoh: N 2(g) + 3 H 2(g) 2 NH 3(g) 2, 8 g ? ? Ø mol N 2 = 2, 8 / 28 = 0, 1 mol Ø mol H 2 = 3/1 x 0, 1 mol = 0, 3 mol massa H 2 = 0, 3 x 2 = 0, 6 g Ø mol NH 3 = 2/1 x 0, 1 = 0, 2 mol massa NH 3 = 0, 2 x 17 = 3, 4 g

Hubungan koefisien dalam persamaan reaksi dengan hitungan Perbandingan koefisien pada persamaan reaksi sebanding dengan perbandingan jumlah partikel Contoh: N 2(g) + 3 H 2(g) 2 NH 3(g) 6, 022 x 1023 Molekul ? Jawab: perbandingan koef 1 : 3 : 2 Ø Jumlah molekul H 2 = 3 x 6, 022 x 1023 = 18, 07 x 1023 Ø Jumlah molekul NH 3 = 2 x 6, 022 x 1023 = 12, 04 x 1023 c.

KADAR ZAT Massa Ax. By = p gram Massa A = x. Ar A. p Mr Ax. By Massa B = y. Ar B. p Mr Ax. By % A = x. Ar A. 100% Mr Ax. By % B = y. Ar B. 100% Mr Ax. By

Contoh… Misalkan massa Al 2 O 3 = 50 g, maka berapakah persentase masing-masing logam tersebut? Jawab: Mr Al 2 O 3 = (2. 27) + (3. 16) = 102 g/mol % Al = 2. Ar Al. 100% = 2. 27. 100% = 52, 94% Mr Al 2 O 3 102 Massa Al = 52, 94% x 50 g = 26, 47 g % O = 3. Ar O. 100% = 3. 16. 100% = 47, 06% Mr Al 2 O 3 102 Massa O = 47, 06% x 50 g = 25, 53 g

Latihan Soal Semua logam alkali bereaksi dengan air menghasilkan gas hidrogen dan hidroksida logam alkali yang bersesuaian. Contoh reaksi antara lithium dan air : 2 Li(s) + 2 H 2 O(l) 2 Li. OH(aq) + H 2(g) � (a) Berapa mol H 2 akan terbentuk dari reaksi sempurna antara 6, 23 mol Li dengan air? � (b) Berapa gr H 2 akan terbentuk dari reaksi sempurna antara 80, 57 g Li dengan air? �

PEREAKSI PEMBATAS Adalah pereaksi yang habis terlebih dahulu dalam suatu reaksi kimia Cara menentukan pereaksi pembatas: membagi jumlah mol masing-masing pereaksi dengan koefisiennya, kemudian hasil terkecil itulah yang merupakan pereaksi pembatas

Contoh Soal � 2 NH 3(g) + CO 2(g) (NH 2)2 CO(aq)+H 2 O(l) � Pada satu proses, 637, 2 gr NH 3 bereaksi dengan 1142 g CO 2 � (a) Reaktan manakah yang merupakan pereaksi pembatas? � (b) Hitung massa (NH 2)2 CO yang terbentuk � © Berapa banyak pereaksi berlebih (dalam gram) yang tersisa pada akhir reaksi? � Ar C=12, O=16, N=14, H=1

Contoh: 4 Al(s) + 3 O 2(g) 2 Al 2 O 3(s) Mula-mula : 4 mol Bereaksi : 4 mol Sisa/stlh : - 4 mol 3/4 x 4 mol 2/4 x 4 mol 1 mol Jadi, setelah reaksi: - Terdapat sisa O 2(g) = 1 mol - Terdapat hasil Al 2 O 3(s) = 2 mol

Contoh: 1. Sebanyak 1, 8 g Mg bereaksi dengan 1, 4 g gas N 2 membentuk magnesium nitrida (Mg 3 N 2). Tentukan persamaan reaksinya dan massa zat setelah reaksi! (Ar Mg = 24 g/mol; Ar N= 14 g/mol) Jawab: Mol Mg = 1, 8/24 = 0, 075 mol Mol N 2 = 1, 4/28 = 0, 050 mol

Lanjutan… 3 Mg + N 2 Mg 3 N 2 Mula-mula Bereaksi : : 0, 075 mol 0, 050 mol 0, 025 mol Sisa / setelah : - 0, 025 mol Massa N 2 setelah bereaksi = n x Mr = 0, 025 x 28 = 0, 7 g Massa Mg 3 N 2 = n x Mr = 0, 025 x 100 = 2, 5 g

Latihan… 1. Sebanyak 38, 8 g senyawa Zn. S dibakar dengan 30 liter gas oksigen (pada 0 o. C, 1 atm) dengan reaksi: Zn. S + O 2 Zn. O + SO 2 Tentukan: - penyetaraan reaksinya! - volume SO 2 setelah reaksi berlangsung! Ar Zn=32, S=65, O=16

Latihan (homework) 2. Etilena, C 2 H 4 terbakar di udara membentuk CO 2 dan H 2 O sesuai dengan reaksi berikut: C 2 H 4 + O 2 CO 2 + H 2 O Tentukan: a. Penyetaraan reaksinya! b. Massa CO 2 yang terbentuk jika campuran ini mengandung 1, 93 g C 2 H 4 dan 5, 92 g O 2 yang terbakar!

REAKSI YANG MELIBATKAN CAMPURAN Jika suatu campuran direaksikan, maka masing-masing komponen mempunyai persamaan reaksi sendiri. Pada umumnya hitungan yang melibatkan campuran diselesaikan dengan pemisalan.

Contoh: Suatu campuran sejumlah 7, 8 g yang terdiri dari logam aluminium dan logam magnesium direaksikan dengan asam sulfat. Reaksi tersebut menghasilkan total gas hidrogen sebanyak 8, 96 l (STP). Berapakah komposisi persen massa masing-masing logam tersebut? Jawab: I. Mg + H 2 SO 4 Mg. SO 4 + H 2 II. 2 Al + 3 H 2 SO 4 Al 2(SO 4)3 + 3 H 2 Misal : Al = x gram (x / 27) mol Mg = (7, 8 – x) gram (7, 8 – x) / 24 mol

Jika diketahui bahwa volum total gas hidrogen = 8, 96 l, maka n H 2= 8, 96/22, 4 = 0, 4 mol (mol H 2 I + mol H 2 II) I. Mg + H 2 SO 4 Mg. SO 4 + H 2 mol H 2 = [(7, 8 – x) / 24] mol II. 2 Al + 3 H 2 SO 4 Al 2(SO 4)3 + 3 H 2 Mol H 2 = (3/2. x/27) mol = (x/18) mol Mol H 2 I + mol H 2 II = 0, 4 mol [(7, 8 – x) / 24] + x/18 = 0, 4 ………(1)

Dari persamaan (1), diperoleh: x = 5, 4 g (Massa Al) Maka massa Mg = 7, 8 – x = 7, 8 – 5, 4 = 2, 4 g Sehingga persentase masing-masing logam: % Al = (5, 4 / 7, 8) x 100% = 69, 23% % Mg = (2, 4 / 7, 8) x 100% = 30, 77%

REAKSI PENGENDAPAN Adalah reaksi yang dapat menghasilkan endapan padat Contoh: Reaksi antara timbal(II) nitrat dengan natrium klorida sesuai reaksi: Pb(NO 3)2(aq) + 2 Na. Cl(aq) Pb. Cl 2(s) + 2 Na. NO 3(aq)

REAKSI-REAKSI PEMBUATAN GAS a. Reaksi pembuatan gas H 2 Logam + HCl / H 2 SO 4 encer H 2 + senyawa ion (garam) Contoh: Mg(s) + 2 HCl(aq) H 2(g) + Mg. Cl 2(aq) 2 Al(s) + 3 H 2 SO 4(aq) Al 2(SO 4)3(aq) + 3 H 2(g)

REAKSI-REAKSI PEMBUATAN GAS b. Reaksi pembuatan gas CO 2 Seny. Karbonat + HCl / H 2 SO 4 encer CO 2 + H 2 O + senyawa ion (garam) Contoh: Na 2 CO 3 + H 2 SO 4 CO 2 + H 2 O + Na 2 SO 4

REAKSI-REAKSI PEMBUATAN GAS c. Reaksi pembuatan gas NH 3 Seny. Amonia + seny. Hidroksida NH 3 + H 2 O + garam Contoh: 3(NH 4)SO 4(s) + 2 Al(OH)3(aq) 6 NH 3(g) + 6 H 2 O + Al 2(SO 4)3(aq)

Terima kasih

QUIZ

SOAL 1. Asetilen, yang digunakan sebagai api pembakar dalam mengerjakan las, dibuat dari reaksi antara kalsium karbida dengan air : Ca. C 2 + H 2 O Ca(OH)2 + C 2 H 2 (g) a. Setarakan persamaan reaksi di atas terlebih dahulu b. Berapa mol C 2 H 2 yang terbentuk dari 2, 50 mol Ca. C 2? www. themegallery. com

c. Berapa mol air yang dibutuhkan jika 3, 20 mol C 2 H 2 yang terbentuk? d. Berapa gram Ca(OH)2 yang dihasilkan jika 28, 0 gram C 2 H 2 yang terbentuk? Ar C=12, H=1, O=16, Ca=40 www. themegallery. com

SOAL 2. Setarakan Persamaan reaksi berikut ini : a. Al + Fe 3 O 4 Al 2 O 3 + Fe b. Na 2 S 2 O 3 +I 2 Na. I + Na 2 S 4 O 6 www. themegallery. com

3. Sebanyak 4 g kalsium (Ca) direaksikan dengan 6, 3 g asam nitrat (HNO 3) sesuai reaksi berikut : Ca(s) + HNO 3 (aq) Ca. NO 3 (aq) + H 2(g) a. Setaran persamaan reaksi nya b. Tentukan pereaksi pembatasnya c. Hitung massa zat sisa nya dan zat hasil reaksi



Latihan… 1. Diketahui volum suatu campuran antara dua gas propana dan butana adalah 8 liter (pada STP) direaksikan dengan oksigen menghasilkan karbon dioksida dan air. Tentukan komposisi persentase volum kedua gas tersebut !
- Slides: 34