STOIKIOMETRI KIMIA M NURISSALAM STOIKIOMETRI Adalah cabang ilmu

STOIKIOMETRI KIMIA M. NURISSALAM

STOIKIOMETRI Adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya.

HUKUM KEKEKALAN MASSA (HUKUM LAVOISIER) �Massa zat-zat sebelum dan sesudah reaksi adalah tetap �Contoh: hidrogen + oksigen oksida (4 g) (32 g) hidrogen (36 g)

HUKUM PERBANDINGAN TETAP (HUKUM PROUST) �Perbandingan massa unsur dalam tiap-tiap senyawa adalah tetap �Contoh: Pada senyawa NH 3 : massa N : massa H = 1 Ar. N : 3 Ar. H = 1 (14) : 3 (1) = 14 : 3

Contoh: Berapa kadar C dalam 50 gram Ca. CO 3 ? (Ar: C = 12; 0 = 16; Ca=40) Massa C = (Ar C / Mr Ca. CO 3) x massa Ca. CO 3 = 12/100 x 50 gram = 6 g Kadar C = massa C/massa Ca. CO 3 x 100% = 6/50 x 100 % = 12%

Berapa perbandingan atom H dan O pada H 2 O

HUKUM PERBANDINGAN BERGANDA (HUKUM DALTON) �Bila dua buah unsur dapat membentuk dua atau lebih senyawa untuk massa salah satu unsur yang sama banyaknya maka perbandingan massa unsur kedua akan berbanding sebagai bilangan bulat dan sederhana

�Contoh: Bila unsur Nitrogen den oksigen disenyawakan dapat terbentuk, NO dimana massa N : 0 = 14 : 16 = 7 : 8 NO 2 dimana massa N : 0 =14 : 32 = 7 : 16 �Untuk massa Nitrogen yang sama banyaknya maka perbandingan massa Oksigen pada senyawa NO : NO 2 = 8 : 16 = 1 : 2


SATUAN INTERNASIONAL METER LITER Menentukan jumlah dengan kesepakatan internasionail misalkan 1 Lusin : 1 kodi : 1 Gross : 12 buah 20 buah 144 buah

Konsep mol Karena atom begitu kecil bahkan sangat kecil, maka satu tetes air akan mengandung trilyunan partikel H 2 O, Bahkan jika tiap molekul air dibagikan pada seluruh penduduk bumi, satu orang mendapatkan 6 juta buah partikel

�sehingga kesepakatan internasional menggunakan penyederhanan penentuan jumlah zat dengan Mol

Berapa kah 1 mol itu? Menurut Avogadro dalam laporan penelitan bahwa 1 mol zat apapun, senyawa apapun adalah 602. 000 buah atom/partikel yang kemudian di sederhanakan penulisanya menjadi 1 mol = 6, 02 x 10 23 partikel/atom
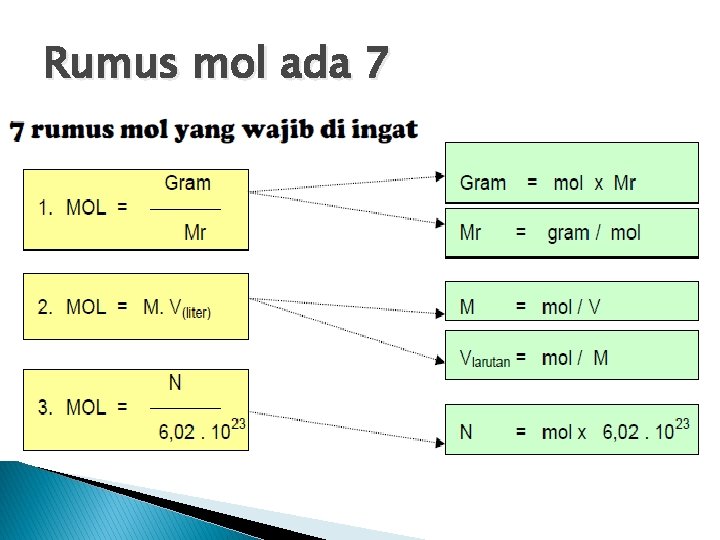
Rumus mol ada 7

keterangan Mol Gram Mr N M V = = = Jumlah Zat massa zat dalam (gram) Massa relatif senyawa Jumlah partikel/atom Molaritas (M) Volume (Liter) 1 Kg 1 L = 1. 000 gram = 1. 000 m. L

Contoh soal Hitunglah mol masing zat berikut: 1. 72 gram air (H 2 O) (diketahui Ar H=1, Ar O=16) 2. 9 gram Glukosa C 6 H 12 O 6 (diketahui Ar C=12) 3. Na. OH 2 M sebanyak 500 m. L

Contoh soal 4. Berapakah jumlah partikel/atom Na. OH 4 gram (diketahui Ar Na=23, Ar 0= 16, Ar H =1) 5. Berapa gram dari 12, 04 x 1023 partikel Oksigen (O 2 ).
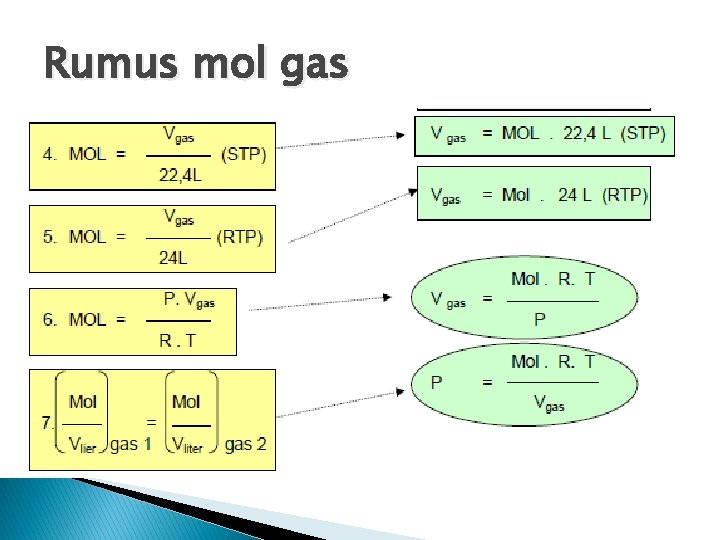
Rumus mol gas
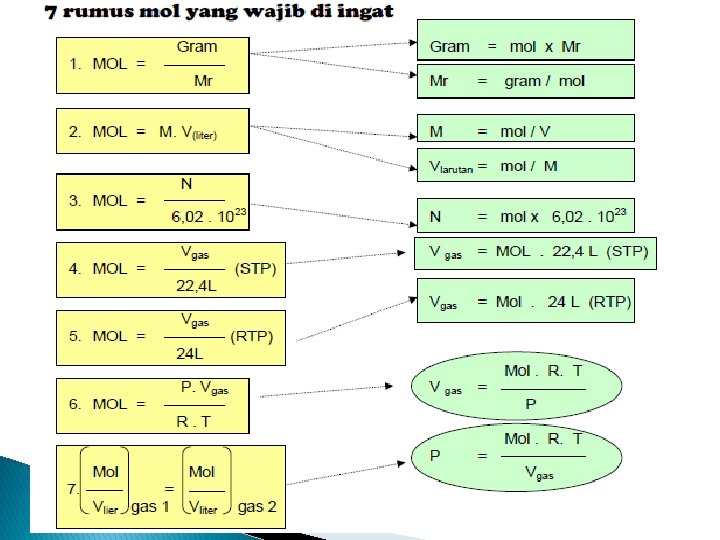

keterangan

keterangan

Contoh soal 1. Sebanyak 4, 4 gram CO 2 (Ar C=12, O=16). Hitunglah volume gas pada a. STP b. RTP c. Pada tekanan 2 atm suhu 270 C d. Pada keadaan 4 mol N 2 bervolume 2 L e. Pada keadaan 16 gram O 2 bervolume 2 L

Soal pengayaan 2. LPG mengandung gas propana (C 3 H 8 ). (diketahui Ar C= 12, Ar H= 1). Hitunglah volume gas LPG 3 Kg jika diukur pada tekanan udara 1 atm pada suhu 33 o. C.

Stoikiometri pada persamaan reaksi Pada persamaan reaksi , perbandingan koefisien reaksi adalah merupakan perbandingan harga mol masing zat yang terlibat. Contoh: Reaksi belum setara Mg + HCl Mg. Cl 2 + H 2

Setelah disetarakan 1 Mg + 2 HCl 1 Mg. Cl 2 + 1 H 2 2 mol 4 mol Misalkan mol Mg sebesar 2 mol, maka mol HCl sebesar 4 mol, mol Mg. Cl 2 sebesar 2 mol, dan H 2 sebesar……

contoh Sebanyak 6 gram Mg (Ar=24) direaksikan dengan HCl sesuai reaksi Mg + HCl Mg. Cl 2 + H 2 Hitunglah volume H 2 pada STP Jawab: Mol Mg di cari dengan rumus no 1, kemudian dengan perbandingan koefisien di dapatkan mol H 2 , setelah mol H 2 di dapat dari perbandingan koefisien, volume H 2 dapat di hitung

Mol Mg = gram / Mr = 6/24 = 0, 25 mol Mol H 2 = 0, 25 (karena koefisien nya sama dengan Mg) V gas STP = mol x 22, 4 L = 0, 25 x 22, 4 L = 5, 6 L

soal Sebanyak 2, 7 gram Al (Ar= 27) di reaksikan dengan HCl sesuai reaksi belum setara Al + HCl Al. Cl 3 + H 2 Hitunglah Volume gas H 2 pada tekanan udara 2 atm pada suhu 370 C.

soal Volume gas Hidrogen yang diukur pada suhu kamar sebesar 4, 8 L, pada reaksi antara Na dengan H 2 SO 4 pada reaksi belum setara berikut: Na + H 2 SO 4 Na 2 SO 4 + H 2 Jika Ar Na= 23, Hitunglah massa (gram) Na yang direaksikan?

soal Sebanyak 2, 3 gram etanol (C 2 H 5 OH )di bakar sesuai reaksi: Belum setara C 2 H 5 OH + O 2 CO 2 + H 2 O a. Setarakan reaksi di atas b. Hitunglah mol etanol c. Tentukan mol oksigen, CO 2 , H 2 O (dengan perbandingan mol) d. Hitunglah volume gas Oksigen pada RTP e. Hitunglah volume gas CO 2 pada tekanan 1 atm dan suhu 270 C f. Hitunglah Volume gas H 2 O pada keadaan dimana 4 mol NO bervolume 2 L?

soal Ke dalam 100 ml HCl 0, 2 M dimasukkan logam Zn sebanyak 1300 mg (Ar Zn= 65) sehingga terjadi reaksi : Zn (s) + 2 HCl (aq) → Zn. Cl 2 (aq) + H 2 (g) Hitunglah… a. Volume gas H 2 yang dihasilkan dalam keadaan standar b. Massa Zn yang tersisa

Soal UN 2013 � Sebanyak 10, 8 gram logam aluminium habis bereaksi dengan 9, 6 gram oksigen dalam ruang tertutup membentuk aluminium oksida menurut persamaan reaksi: � 4 Al(s) + 3 O 2(g) 2 Al 2 O 3(s) � Massa aluminium oksida yang dapat terbentuk sebanyak. . . ( Ar: Al = 27; O = 16) � A. 3, 6 gram � B. 10, 8 gram � C. 13, 0 gram � D. 20, 4 gram � E. 102, 0 gram

Soal UN 2012 Batu kapur sebanyak 30 gram dicampur dengan asam klorida 6, 72 L (STP), sesuai persamaan reaksi berikut: Ca. CO 3 (s)+2 HCl(g) Ca. Cl 2 (aq)+H 2 O (l)+CO 2(g) Volume gas yang dihasilkan jika diukur dalam keadaan standar sebanyak…. . (Ar C=12, O=16, Ca=40, H=1, Cl = 35, 5) a. 1, 12 L b. 2, 24 L c. 3, 36 L d. 6, 72 L e. 10, 08 L

Latihan soal di kumpulkan soal nomor 1 Magnesium sebanyak 4, 80 gram dimasukkan ke dalam 350 m. L larutan HCl 1 M. Diketahui massa atom Mg =24, H=1, Cl=35, 5. Mg + HCl Mg. Cl 2 + H 2 (blm setara) a. Hitunglah mol Mg b. Hitung mol HCl c. Setarakan persamaan reaksi tersebut d. Hitunglah Mr Mg. Cl 2 e. Hitunglah massa Mg. Cl 2 yang dihasilkan f. Hitunglah Volume gas yang dihasilkan pada keadaan STP g. Hitunglah massa zat yang tersisa

Soal nomor 2 Reduksi besi (III) oksida dengan CO menghasilkan besi menurut persamaan reaksi belum setara Fe 2 O 3 + CO Fe + CO 2 a. Untuk menghasilkan 11, 2 Kg besi (Ar Fe= 56) berapa Kg dibutuhkan besi (III) oksida (Mr=160). b. Berapa volume gas CO 2 yag dihasilkan jika diukur pada tekanan udara 1, 2 atm pada suhu 100 0 C jika 160 Kg Fe 2 O 3 yang digunakan
- Slides: 35