STOIKIOMETRI Hubungan Mol Massa Jumlah dalam Sistem Kimia

STOIKIOMETRI Hubungan Mol – Massa – Jumlah dalam Sistem Kimia

Konsep Mol • Konsep mol diperkenalkan sebagai jembatan bagi kimiawan untuk menghitung entitas kimia dengan menimbangnya • Mol didefinisikan sebagai jumlah zat yang mengandung sejumlah entitas yang sama dengan jumlah atom dalam 12 gram karbon-12 • Jumlah ini dinamakan Avogadro (ilmuwan Italia abad 19) dengan nilai numeris 6, 022 x 1023

Definisi Mol • • 1 mol karbon-12 mengandung 6, 022 x 1023 atom 1 mol H 2 O mengandung 6, 022 x 1023 molekul 1 mol Na. Cl mengandung 6, 022 x 1023 unit rumus Mol tidak hanya menghitung unit tetapi 1 mol zat merepresentasikan sejumlah tertentu entitas kimia yang memiliki massa yang tertentu • Atom-atom memiliki massa tertentu dan konsep mol memungkinkan kita menentukan jumlah atom, molekul dan unit rumus hanya dengan menimbangnya. • Massa atom suatu unsur yang tercantum pada tabel periodik adalah berat rata-rata massanya dari isotop yang ada dialam

Definisi Mol • 1 atom Fe memiliki massa 55, 85 amu • 1 atom S memiliki massa 32, 07 amu • 1 atom O memiliki massa 16, 00 amu • 1 molekul O 2 memiliki massa 32, 00 amu [ 1 mol atom Fe memiliki massa 55, 85 g [ 1 mol atom S memiliki massa 32, 07 g [ 1 mol atom O memiliki massa 16, 00 g [ 1 molekul O 2 memiliki massa 32, 00 g

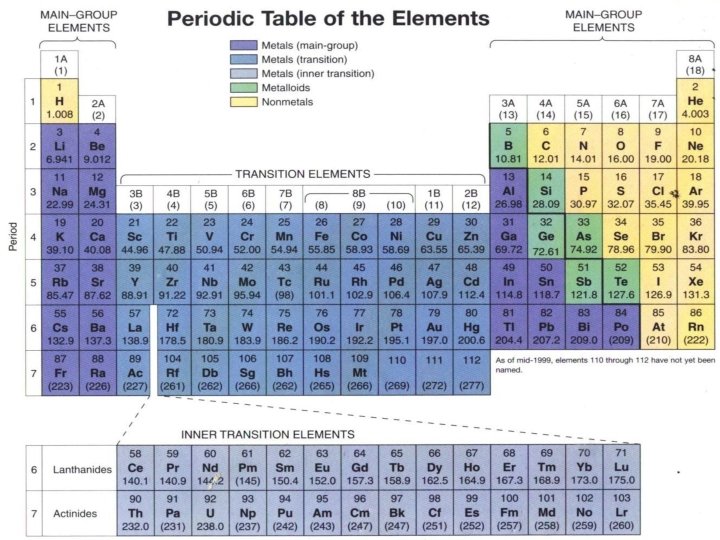
Massa Molar • Massa molar suatu zat adalah massa per mol dari entitasnya (atom, molekul atau unit rumus) • Massa molar memiliki satuan gram per mol (g/mol) • Rujukan utama massa molar adalah tabel periodik dalam menentukan massa molar suatu zat (unsur atau senyawa)

Massa Molar Unsur dan Senyawa • Massa molar unsur dihitung dengan melihat nilai yang tertera pada tabel periodik, kecuali untuk unsur molekular yang terbentuk dialam. Misal O 2 dan S 8 • Massa molar senyawa dihitung dari jumlah massa molar unsur yang ada menurut rumus. Misal SO 2 (1 x S dan 2 x O) • Subskrip dalam rumus merujuk ke atom-atom individual (atau ion) atau mol atom-atom

Interkonversi Mol, Massa dan Jumlah • Massa molar yang juga mengekspresikan hubungan ekivalen antara 1 mol zat dengan massanya dalam gram dapat digunakan sebagai faktor konversi Massa (g) = jumlah mol x jumlah gram/1 mol Atau Jumlah Mol = Massa (g) x 1 mol/jumlah gram • Demikian juga dengan bilangan Avogadro yang menghubungkan 1 mol zat dengan jumlah entitas Jumlah entitas = jumlah mol x 6, 022 x 1023/1 mol Atau Jumlah Mol = jumlah entitas x 1 mol/6, 022 x 1023
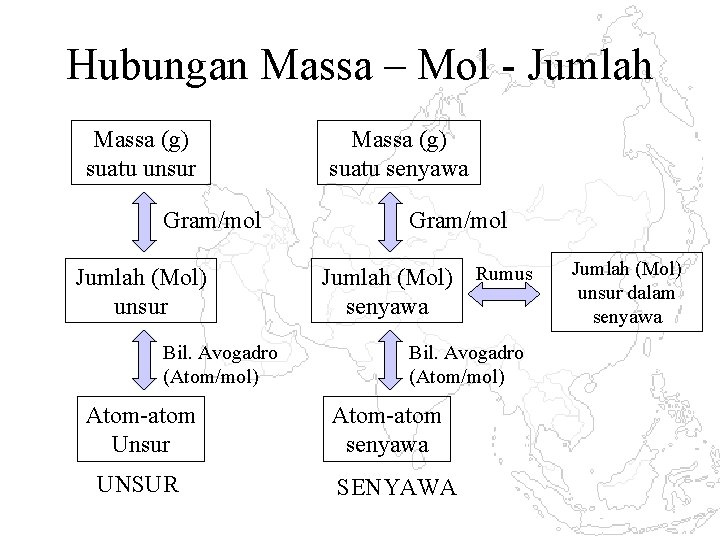
Hubungan Massa – Mol - Jumlah Massa (g) suatu unsur Gram/mol Jumlah (Mol) unsur Bil. Avogadro (Atom/mol) Atom-atom Unsur UNSUR Massa (g) suatu senyawa Gram/mol Jumlah (Mol) Rumus senyawa Bil. Avogadro (Atom/mol) Atom-atom senyawa SENYAWA Jumlah (Mol) unsur dalam senyawa

Soal Latihan • Perak (Ag) sering dipakai pada perhiasan dan alat makan, berapa gram Ag dalam 0, 0342 mol Ag? (Ar : 107, 9) • Besi adalah komponen utama dalam baja dan merupakan logam terpenting dalam struktur bangunan, berapa banyak atom Fe dalam 95, 8 g Fe? (Ar Fe : 55, 85) v Salah satu bentuk kristal karbon bernama grafit sering digunakan sebagai bahan pensil. Didalam 315 mg grafit terdapat berapa mol karbon? (Ar C 12, 01) v Tetraphosporus dekaoksida (P 4 O 10) bereaksi dengan air membentuk asam phospat, dalam skala lab asam ini digunakan sebagai drying agent (Ar P = 30, 97 O = 16) – Berapa massa (dalam g) 4, 65 x 1022 molekul tetraphosporus dekaoksida? – Berapa atom P yang ada dalam sampel diatas?

Persen Massa Berdasarkan Rumus Kimia • Masing-masing unsur dalam yang membentuk senyawa memiliki porsi tertentu yang merupakan bagian dari massa senyawa tsb • Jika ada unsur X dalam suatu senyawa; % Massa X = Mol X rumus x Massa molar X x 100 Massa 1 mol senyawa

Contoh Soal • Glukosa (C 6 H 12 O 6) adalah nutrien penting dalam sel makhluk hidup sebagai sumber energi. – Berapa persen massa masing-masing unsur penyusun glukosa tsb? – Berapa gram karbon yang terdapat pada 16, 55 gram glukosa?

Rumus Empiris • Analis kimia mengetahui suatu senyawa kimia dengan mendekomposisinya menjadi zat sederhana, menentukan massa unsur penyusun, merubah massa menjadi mol kemudian secara matematis merubah mol menjadi bilangan bulat • Prosedur ini akan menghasilkan rumus empiris suatu senyawa • Contoh: suatu senyawa tak dikenal diteliti mengandung 0, 21 mol seng, 0, 14 mol phospor dan 0, 56 mol oksigen. Karena mol mewakili proporsi unsur dalam senyawa kita dapat menulis • Zn 0, 21 P 0, 14 O 0, 56 jika bilangan subskrip ini kita bagi dengan kelipatan terkecil secara matematis akan diperoleh rumus empiris senyawa ini adalah Zn 3 P 2 O 8 atau Zn 3(PO 4)2.

Soal Latihan • Analisis unsur suatu sampel menunjukkan kandungan 2, 82 g Na; 4, 35 g Cl dan 7, 83 g O. Apa rumus empiris senyawa ini? v. Suatu logam tak dikenal M bereaksi dengan sulfur membentuk senyawa M 2 S 3. jika 3, 12 g M bereaksi tepat dengan 2, 88 g S. Logam apakah M dan senyawa apa M 2 S 3?

Rumus Molekul • Jika kita mengetahui massa molar senyawa maka kita dapat menggunakan rumus empiris untuk menentukan rumus molekul (jumlah aktual mol unsur yang menyusun senyawa) • Beberapa senyawa memiliki rumus empiris dan rumus molekul identik namun sebagian besar senyawa memiliki rumus molekul yang kelipatan bilangan bulat dari rumus emipris • Misal H 2 O 2 memiliki massa 34, 02 g/mol dengan rumus empiris HO (massa 17, 01 g/mol) maka kelipatan bilangan bulatnya adalah 34, 02/17, 01 = 2

Penentuan Rumus Molekul • Laboratorium analitis komersil biasanya menyediakan data senyawa dalam bentuk persen massa unsur penyusun. Berdasarkan ini kita dapat menentukan rumus molekul dengan cara: 1. Asumsi 100 g senyawa menjadikan persen massa langsung sebagai massa unsur 2. Konversi massa menjadi jumlah mol 3. Menyusun rumus empiris dan jika massa molar senyawa tersedia maka kita dapat menentukan rumus molekulnya

Soal Latihan • Selama aktifitas fisik, asam laktat (Mr = 90, 08 g/mol) terbentuk dijaringan otot dan menyebabkan pegal-pegal. Analisis unsur menunjukkan asam ini mengandung 40, 0% massa C, 6, 71% massa H dan 53, 3% massa O 1. Tentukan rumus empiris asam laktat 2. Tentukan juga rumus molekul asam ini v Salah satu senyawa penyebab kanker yang berbahaya adalah benzo[a]piren (Mr = 252, 30 g/mol) dan ditemukan pada debu batubara dan asap rokok. Analisis menunjukkan kandungan 95, 21% massa C, 4, 79% massa H. Bagaimana rumus molekul benzo[a]piren ini?

Beberapa senyawa dengan RE sama Nama RM F Mr Kegunaan Formaldehid As. Asetat As. Laktat Eritrosa Ribosa Glukosa CH 2 O C 2 H 4 O 2 C 3 H 6 O 3 C 4 H 8 O 4 C 5 H 10 O 5 C 6 H 12 O 6 1 2 3 4 5 6 30, 03 60, 05 90, 08 120, 10 150, 13 180, 16 Disinfektan Polimer asetat Penyebab otot pegal Hasil metabolisme gula Komponen as. nukleat Sumber energi sel

Menyeimbangkan Persamaan Reaksi • Magnesium bereaksi dengan oksigen membentuk magnesium oksida • Oktana (C 8 H 18) bereaksi dengan oksigen didalam mesin kendaraan menghasilkan karbon dioksida dan uap air • Reaksi khas logam alkali diantaranya adalah natrium bereaksi cepat dengan air membentuk gas hidrogen dan larutan natrium hidroksida v Larutan asam nitrat dapat merusak patung melalui reaksi dengan kalsium karbonat membentuk karbon dioksida, air dan larutan kalsium nitrat

Rules for Assigning an Oxidation Number • • • Aturan Umum Atom dalam bentuk unsur ON = 0 Ion monoatomik; ON = muatan ion Jumlah ON atom-atom dalam senyawa = 0 dan jumlah ON atom-atom dalam ion poliatomik = muatan ion Aturan Spesifik Gol 1 A ON = +1 dalam semua senyawa Gol 2 A ON = +2 dalam semua senyawa Hidrogen ON = +1 kombinasi dg non logam -1 kombinasi dg logam dan Boron Fluorin ON = -1 dalam semua senyawa Okisgen ON = -1 dalam peroksida -2 dalam semua senyawa lainnya kecuali dg F Gol 7 A ON = -1 dalam kombinasi dg logam, non logam (kecuali O) dan halogen lainnya yg lebih rendah dalam golongan

Rasio Molar Ekivalen Stoikiometris dalam Persamaan Reaksi Seimbang • Dalam persamaan seimbang, jumlah mol suatu zat ekivalen stoikiometris dengan jumlah mol zat yang lain C 3 H 8(g) + 5 O 2(g) 3 CO 2(g) + 4 H 2 O(g) • 1 mol C 3 H 8 bereaksi dengan 5 mol O 2 • 1 mol C 3 H 8 menghasilkan 3 mol CO 2 • 1 mol C 3 H 8 menghasilkan 4 mol H 2 O atau • 1 mol C 3 H 8 ekivalen stoikimetris dengan 5 mol O 2 • 1 mol C 3 H 8 ekivalen stoikimetris dengan 3 mol CO 2 • 1 mol C 3 H 8 ekivalen stoikimetris dengan 4 mol H 2 O

Contoh Soal • Tembaga banyak diperoleh melalui proses bertahap tembaga(I) sulfida dengan pembakaran (dengan gas oksigen) untuk membentuk serbuk tembaga(I) oksida dan gas sulfur dioksida 1. Berapa mol oksigen dibutuhkan untuk membakar 10 mol tembaga(I) sulfida? 2. Berapa gram sulfur dioksida terbentuk saat 10 mol tembaga(I) sulfida dibakar? 3. Berapa kilogram oksigen dibutuhkan untuk membentuk 2, 86 kg tembaga(I) oksida?

Tugas Mandiri - 1 • Campuran thermite adalah campuran antara besi (III) oksida dan serbuk aluminum yang dulu pernah digunakan dalam pembuatan rel kereta api, reaksi keduanya menghasilkan padatan aluminum oksida dan lelehan besi. 1. 2. 3. Berapa mol besi (III) oksida dibutuhkan untuk membentuk 3, 60 x 103 mol besi? Berapa mol besi terbentuk saat 1, 85 x 1025 molekul besi (III) oksida bereaksi? Berapa banyak atom Al bereaksi untuk setiap 1 gram aluminum oksida yang terbentuk?

Reaksi Kimia yang terjadi secara Berurutan/sekuensial • Tembaga(I) sulfida dibakar dengan gas O 2 menghasilkan tembaga(I) oksida: Cu 2 S(s) + 3 O 2(g) 2 Cu 2 O(s) + 2 SO 2(g) • Cu 2 O produk kemudian direaksikan lebih lanjut dengan karbon untuk mendapatkan logam Cu dengan reaksi Cu 2 O(s) + C(s) 2 Cu(s) + CO(g) • Kedua reaksi ini terjadi secara berurutan dengan reaksi overall : 2 Cu 2 S(s) + 3 O 2(g) + 2 C(s) 2 SO 2(g) + 4 Cu(s) + 2 CO(g)

Soal Latihan v. SO 2 yang dihasilkan dalam pengolahan tembaga, diudara bereaksi dengan oksigen membentuk gas sulfur trioksida. Gas ini jika terkena hujan akan bereaksi dengan air membentuk larutan asam sulfat yang kemudian jatuh kebumi sebagai hujan asam. Tuliskan reaksi individual dan overall dari peristiwa diatas!

Reaksi Berurutan dalam Organisme • Reaksi multi-tahap yang terjadi secara berurutan dikenal sebagai metabolic pathways dalam system biologis • Sebagai ilustrasi, pada sebagian besar sel, energi kimia dalam glukosa dilepaskan melalui urutan mencapai 30 reaksi individual • Produk dari satu reaksi menjadi reaktan reaksi berikutnya sehingga reaksi akhir dapat ditulis • C 6 H 12 O 6(aq) + 6 O 2(g) 6 CO 2(g) + 6 H 2 O(l)
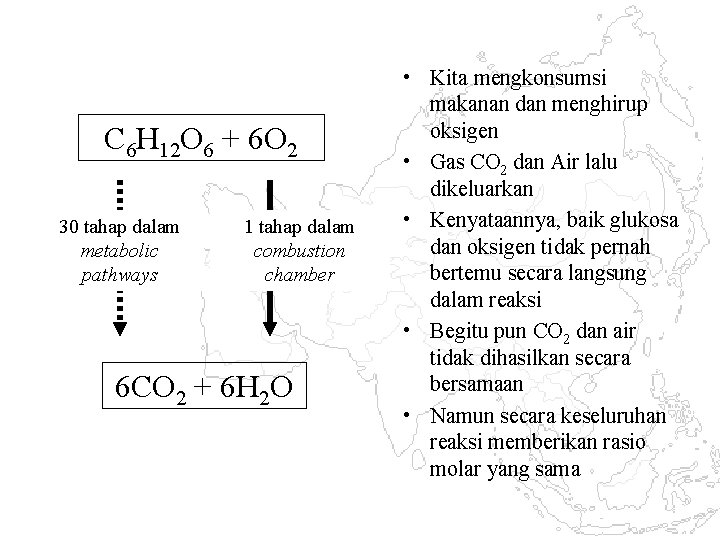
C 6 H 12 O 6 + 6 O 2 30 tahap dalam metabolic pathways 1 tahap dalam combustion chamber 6 CO 2 + 6 H 2 O • Kita mengkonsumsi makanan dan menghirup oksigen • Gas CO 2 dan Air lalu dikeluarkan • Kenyataannya, baik glukosa dan oksigen tidak pernah bertemu secara langsung dalam reaksi • Begitu pun CO 2 dan air tidak dihasilkan secara bersamaan • Namun secara keseluruhan reaksi memberikan rasio molar yang sama

Reaksi Kimia yang Melibatkan Pereaksi Pembatas • Pereaksi pembatas adalah satu reaktan didalam reaksi yang habis duluan sebelum pereaksi yang lain bereaksi semua • Suatu campuran bahan bakar terdiri dari hidrazin (N 2 H 4) dan dinitrogen tetraoksida (N 2 O 4) yang jika di-ignite akan menghasilkan gas nitrogen dan uap air. Berapa gram gas N 2 terbentuk saat 1, 00 x 102 g N 2 H 4 dicampur dengan 2, 00 x 102 g N 2 O 4 ? N 2 H 4 + N 2 O 4 N 2 + H 2 O

2 N 2 H 4(l) + N 2 O 4(l) 3 N 2(g) + 4 H 2 O(g) •


Alternative Approach •

Soal Latihan • How many grams of solid aluminum sulfide can be prepared by the reaction of 10. 0 g of aluminum and 15. 0 g of sulfur? How many grams of the nonlimiting reactants are in excess?

Tugas Mandiri - 2 • Butane gas (C 4 H 10) is used as the fuel in disposable lighters. It burns in oxygen to form carbon dioxide gas and water vapor. What mass of carbon dioxide is produced when 4. 65 g of butane is burned in 10. 0 g of oxygen? How many grams of the excess reactant remain unreacted when the reaction is over?

Theoretical, Actual, and percent reaction Yields • Up until now, we’ve assumed that 100% of the limiting reactant becomes product, that • Ideal methods exist for isolating the product, and that • We have perfect lab technique and collect all the product. • In theory, this may happen, but in reality, it doesn’t, and chemists recognize three types of reaction yield:

Theoretical Yield • The amount of product calculated from the molar ratio in the balanced equation is theoretical yield. • But, there are several reasons why theoretical yield is never obtained – Reactant mixtures often proceed through side reactions that form different products. In the rocket fuel reaction in Sample Problem, for example, the reactants might form some NO in the following side reaction: N 2 H 4(l) + 2 N 2 O 4(l) 6 NO(g) + 2 H 2 O(g) – This reaction decreases the amounts of reactants available for N 2 production.

• Even more important, many reactions seem to stop before they are complete, so some limiting reactant is unused. • Physical losses occur in every step of a separation some solid clings to filter paper, some distillate evaporates, and so forth. With careful technique, you can minimize, but never eliminate, such losses.

Actual Yield • Given these reasons for obtaining less than theoretical yield, the amount of product actually obtained is the actual yield. • Theoretical and actual yields are expressed in units of amount (moles) or mass (grams).

Percent Yield •
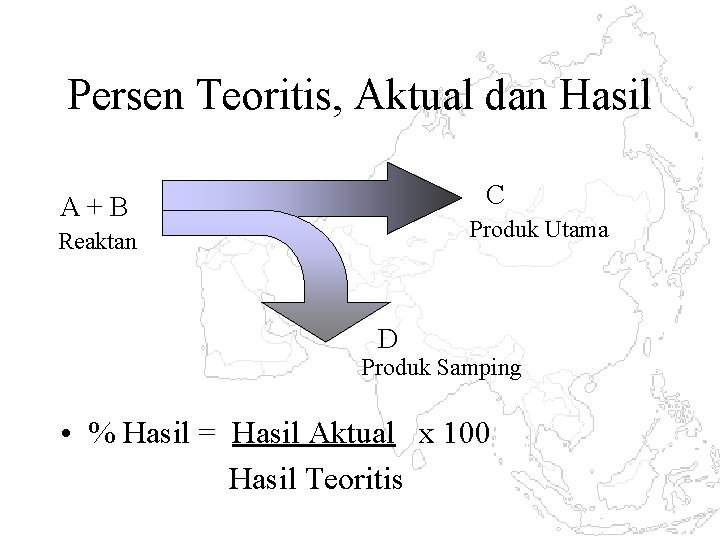
Persen Teoritis, Aktual dan Hasil C A + B Produk Utama Reaktan D Produk Samping • % Hasil = Hasil Aktual x 100 Hasil Teoritis

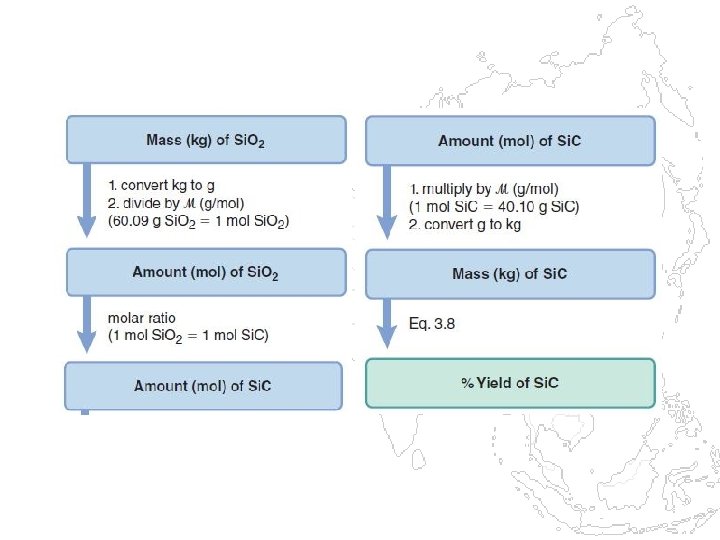
Sample Problem • Silicon carbide (Si. C) adalah material penting untuk keramik yang dibuat dengan mereaksikan pasir (silicon dioxide, Si. O 2) dengan serbuk karbon pada suhu tinggi. Dalam proses ini Carbon monoxide juga terbentuk. • Saat 100. 0 kg pasir diproses, diperoleh 51. 4 kg Si. C. • Berapa percent yield Si. C dari proses ini?


Tugas Mandiri - 3 v. Marbel (kalsium karbonat) bereaksi dengan asam klorida membentuk larutan kalsium klorida, air dan karbon dioksida. Berapa persen hasil karbon dioksida jika 3, 65 g gas ini berhasil dikumpulkan dari 10, 0 g marbel yang direaksikan?

Yields in multistep syntheses • In the multistep synthesis of a complex compound, the overall yield can be surprisingly low, even if the yield of each step is high. • For example, suppose a six-step synthesis has a 90. 0% yield for each step. • To find the overall percent yield, express the yield of each step as a decimal, multiply all the decimal amounts together, and then convert back to a percentage. • The overall recovery is only slightly more than 50%:

• Misalkan ada reaksi berurutan dengan persen yield masing-masing 90%, maka: Overall % yield = (0, 900 0, 900) 100 = 53, 1% • Such multistep sequences are common in laboratory syntheses of medicines, dyes, pesticides, and many other organic compounds.
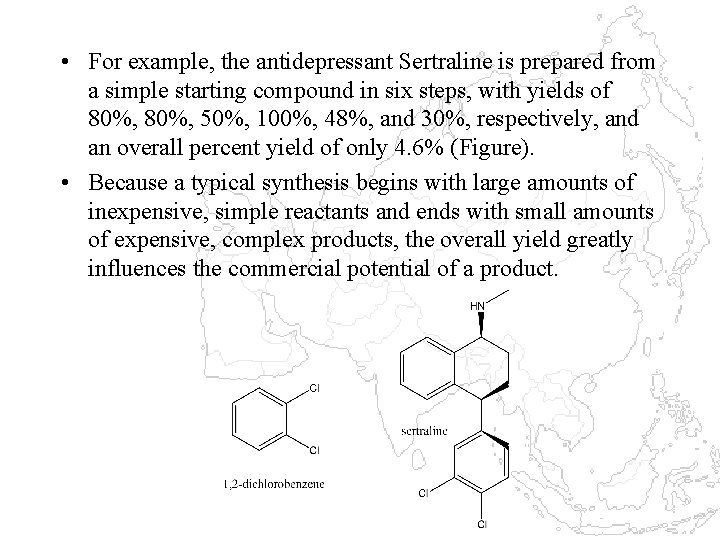
• For example, the antidepressant Sertraline is prepared from a simple starting compound in six steps, with yields of 80%, 50%, 100%, 48%, and 30%, respectively, and an overall percent yield of only 4. 6% (Figure). • Because a typical synthesis begins with large amounts of inexpensive, simple reactants and ends with small amounts of expensive, complex products, the overall yield greatly influences the commercial potential of a product.

Atom Economy: A Green Chemistry perspective on Yield • Dalam bidang yang relatif baru yakni green chemistry, kimiawan dari kalangan akademisi, pelaku industri, dan pemerintahan mengembangkan metode untuk mengurangi atau mencegah pelepasan harmful substances ke lingkungan dan membuang energy resources. • Salah satu cara yang dilakukan oleh kimiawan hijau adalah mengevaluasi synthetic route dengan titik tekan pada atom economy, yakni proporsi atom reaktan yang berakhir sebagai desired product. • Efisiensi sintesis dikuantifikasi dalam terminology the percent atom economy:


Comparing Routes

• From the perspective of atom economy, route 2 is preferable because a larger percentage of reactant atoms end up in the desired product. • It is also a “greener” approach than route 1 because it avoids the use of the toxic reactant benzene and does not produce CO 2, a gas that contributes to global warming.
- Slides: 50