Stoichiometry Oleh Sri wilda albeta stoichiometry RUANG LINGKUP
Stoichiometry Oleh: Sri wilda albeta

stoichiometry RUANG LINGKUP MATERI § RUMUS MOLEKUL q RUMUS EMPIRIS q Ar dan Mr q PERSAMAAN KIMIA § ARTI KUALITATIF DALAM RUMUS KIMIA

RUMUS MOLEKUL home Jumlah atom-atom unsur yang menyusun satu molekul suatu senyawa Ex : E X : Molekul glukosa: C 6 H 12 O 6 6 atom C, 12 atom H, 6 atom O
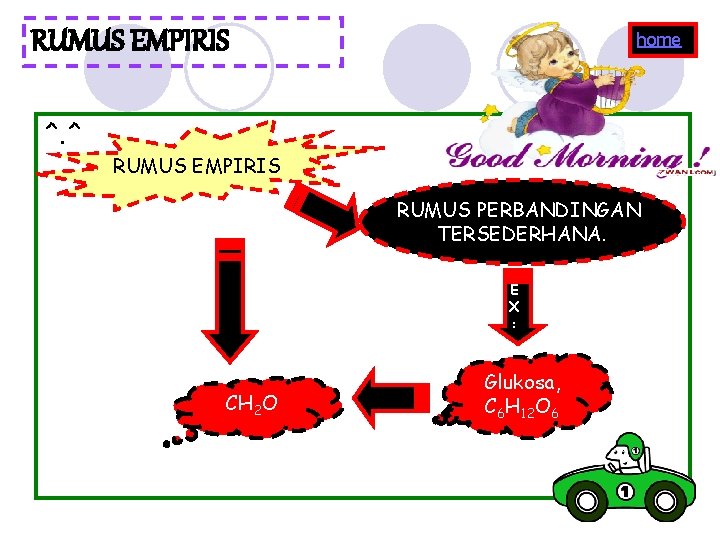
RUMUS EMPIRIS ^. ^ home RUMUS EMPIRIS RUMUS PERBANDINGAN TERSEDERHANA. E X : CH 2 O Glukosa, C 6 H 12 O 6

Contoh soal: Manakah rumus-rumus kimia di bawah ini yang merupakan rumus empiris? A. C 12 H 22 O 11 B. C 2 H 4 O C. N 2 H 4 D. C 4 H 8 O 2

JAWABAN SALAH

JAWABAN BENAR
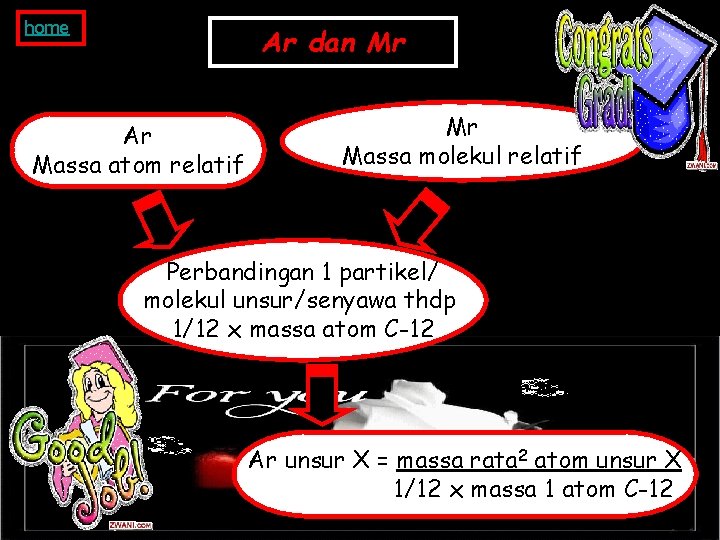
home Ar dan Mr Ar Massa atom relatif Mr Massa molekul relatif Perbandingan 1 partikel/ molekul unsur/senyawa thdp 1/12 x massa atom C-12 Ar unsur X = massa rata 2 atom unsur X 1/12 x massa 1 atom C-12

Lanjutan Ar dan Mr Contoh soal Ar: Massa rata-rata 1 atom unsur X = 4, 037 x 10 -23 gram sedangkan massa 1 atom C-12= 1, 199268 x 10 -23 gram. Tentukanlah massa atom relatif (Ar) unsur X tsb: Ar unsur X = massa rata 2 atom unsur X 1/12 x massa 1 atom C-12 = 4, 037 x 10 -23 gram 1/12 x 1, 199268 x 10 -23 gram = 24, 311

Lanjutan Ar dan Mr Contoh soal Ar: Khlor di alam terdiri atas dua macam isotop: a. Yang meliputi 75% dari seluruh atom 35 Cl b. Yang meliputi 25% dari seluruh atom 37 Cl c. Hitunglah massa atom (Ar) khlor! Ar Cl = (35 x 75)+(37 x 25) 100 = 35, 5 sma

Lanjutan Ar dan Mr Contoh soal Mr: Diketahui massa atom relatif (Ar) untuk H = 1, C = 12, O = 16, Ca = 40. Tentukalah massa molekul relatif (Mr) Ca(OH)2 dan H 2 C 2 O 4. 2 H 2 O ! Mr Ca(OH)2 = Ar. Ca+ (2 x. Ar. O) + (2 x. Ar. H) = 40 + (2 x 16) + (2 x 1) = 74 Mr H 2 C 2 O 4. 2 H 2 O = (2 x. Ar. H) + (2 x. Ar. C) + (4 x. Ar. O) + 2 x [(2 x. Ar. H)+Ar. O] = (2 x 1)+(2 x 12)+(4 x 16)+ 2 x [(2 x 1)+16] = 126
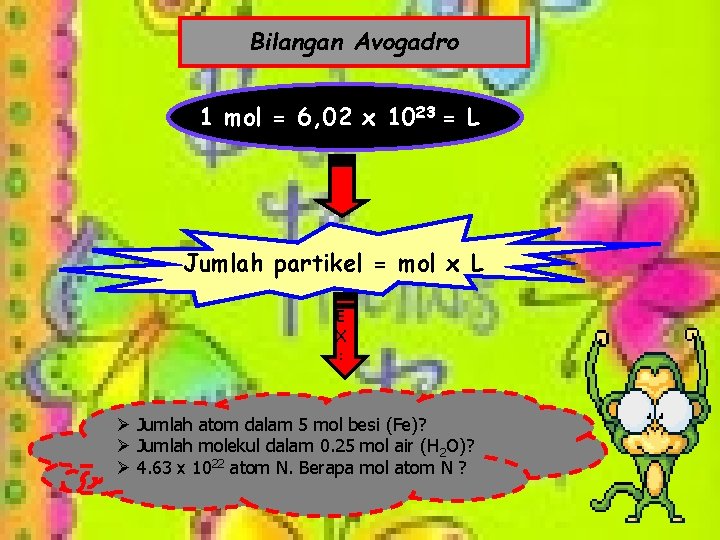
Bilangan Avogadro 1 mol = 6, 02 x 1023 = L Jumlah partikel = mol x L E X : Ø Jumlah atom dalam 5 mol besi (Fe)? Ø Jumlah molekul dalam 0. 25 mol air (H 2 O)? Ø 4. 63 x 1022 atom N. Berapa mol atom N ?
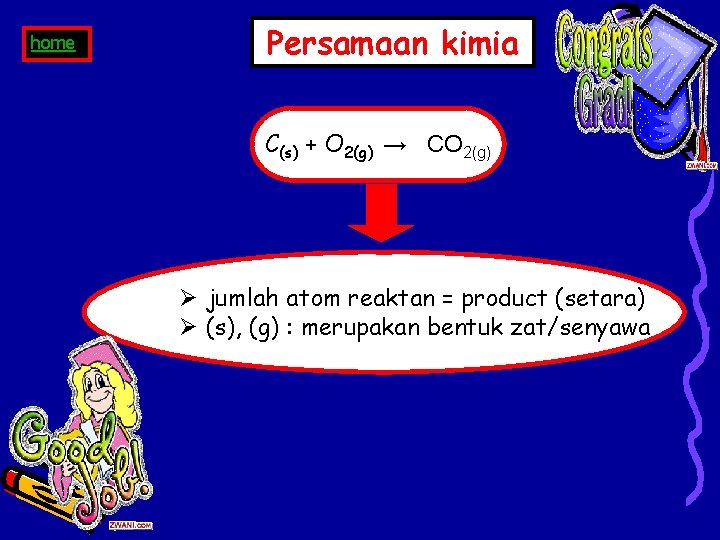
home Persamaan kimia C(s) + O 2(g) → CO 2(g) Ø jumlah atom reaktan = product (setara) Ø (s), (g) : merupakan bentuk zat/senyawa
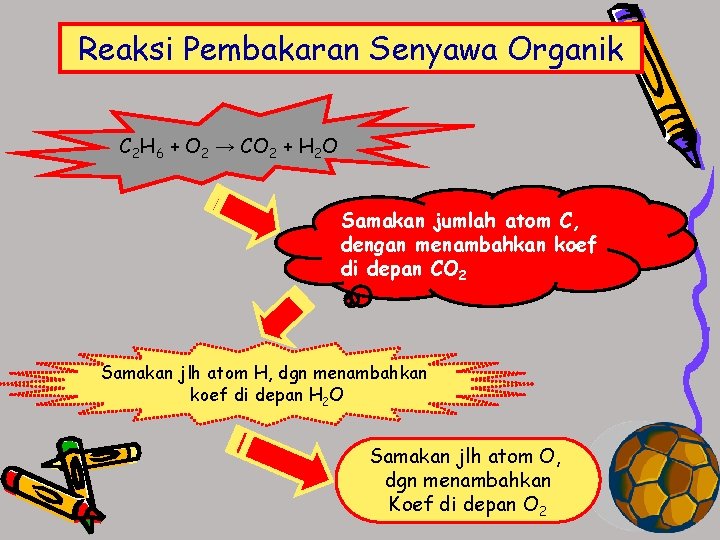
Reaksi Pembakaran Senyawa Organik C 2 H 6 + O 2 → CO 2 + H 2 O Samakan jumlah atom C, dengan menambahkan koef di depan CO 2 Samakan jlh atom H, dgn menambahkan koef di depan H 2 O Samakan jlh atom O, dgn menambahkan Koef di depan O 2

Ex: hub kuatitatif zat dalam reaksi RUMUS: Mol A = koef A = x Mol B koef B y C 2 H 6 + 7/2 O 2 → 2 CO 2 + 3 H 2 O. Dicampurkan 2 mol C 2 H 6. berapa mol CO 2 , H 2 O dan O 2? Dicampurkan 2 mol C 2 H 6, 3 mol O 2. Berapa mol CO 2 dan H 2 O yang dihasilkan?

ARTI KUALITATIF DALAM RUMUS KIMIA home RUMUS: UNSUR DALAM SENYAWA Berat unsur A : Berat unsur B = Jlh Ar A : Jlh Ar B Berat unsur = Berat senyawa jlh Ar unsur Mr senyawa % unsur senyawa = jlh Ar unsur x 100% Mr senyawa

ARTI KUALITATIF DALAM RUMUS KIMIA Ex : Jika diketahui Ar untuk H=1, C=12, O=16 Hitung perbandingan berat unsur-unsur dalam C 6 H 12 O 6! Ex : Hitunglah persentase berat besi dan oksigen dalam Fe 2 O 3! Ar Fe=56, O=16 Ex : Hitunglah berat Mg dalam 30 gr Mg. SO 4! (Mg=24, S=32, O=16)

PENENTUAN RUMUS KIMIA (RE & RM) RUMUS: MOL = Mol = indeks atom Senyawa yang mengandung atom C dan H dibakar sempurna menghasilkan 0. 325 g CO 2 dan 0. 0998 g H 2 O. Tentukan RE. Dan Tentukan RM (Mr=54)

Glossary

- Slides: 20