Stoffen moleculen Om te kunnen verklaren dat stoffen









- Slides: 17

Stoffen moleculen • Om te kunnen verklaren dat stoffen bepaalde stofeigenschappen hebben gebruiken we een modelvoorstelling • De molecuultheorie: stoffen bestaan uit een heleboel super kleine deeltjes van dezelfde soort • Deze deeltjes noemen we moleculen • Definitie: Een molecuul is het kleinste deeltje van een stof dat nog de eigenschappen heeft 1 van die stof

Moleculen • Opgebouwd uit atomen • Verschillende atomen (verbinding) ontleedbaar • Dezelfde atomen (element) niet-ontleedbaar 2

Ontleden • Uit één stof worden meerdere stoffen gemaakt. • Ontleden is een chemische reactie. Bij een chemische reactie veranderen de moleculen (stoffen) 3

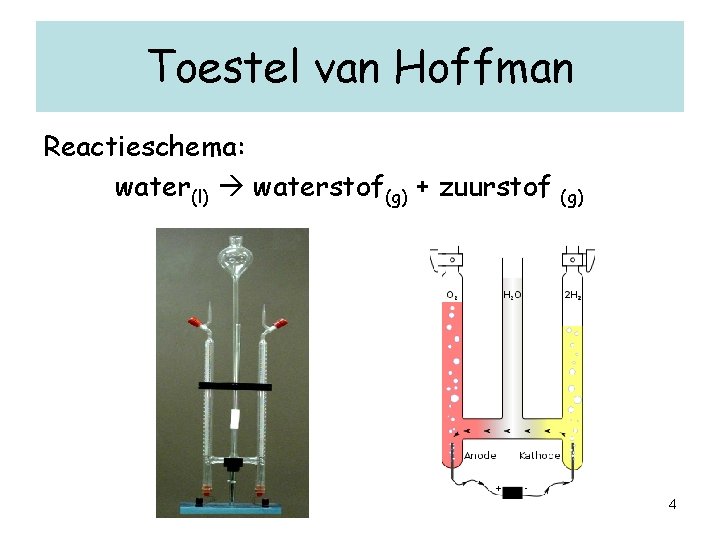
Toestel van Hoffman Reactieschema: water(l) waterstof(g) + zuurstof (g) 4

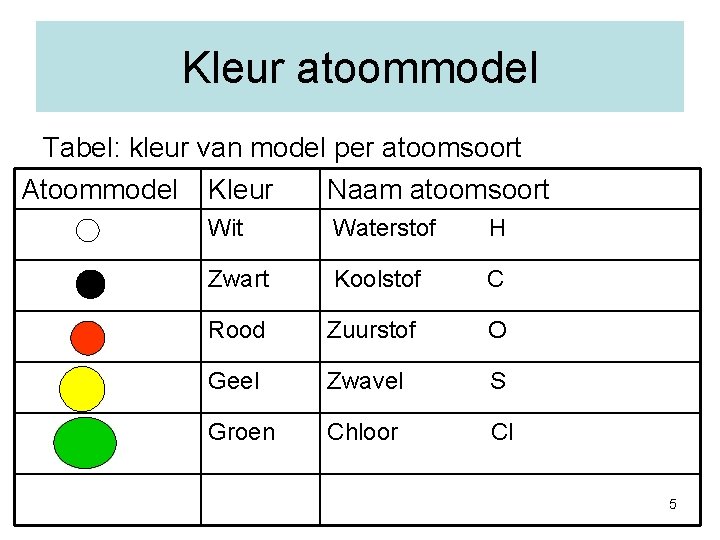
Kleur atoommodel Tabel: kleur van model per atoomsoort Atoommodel Kleur Naam atoomsoort Wit Waterstof H Zwart Koolstof C Rood Zuurstof O Geel Zwavel S Groen Chloor Cl 5

Atoommassa • Atomaire massa eenheid (u) 1 u = 1. 6 • 10 -24 gram Diameter 1 nm = 10 -9 meter ( 1/ miljoenste mm) 6

(Molecuul)model Definitie: Voorstelling van de werkelijkheid hoe wij denken dat hij is Een model geldt net zo lang tot het tegendeel is bewezen. 7

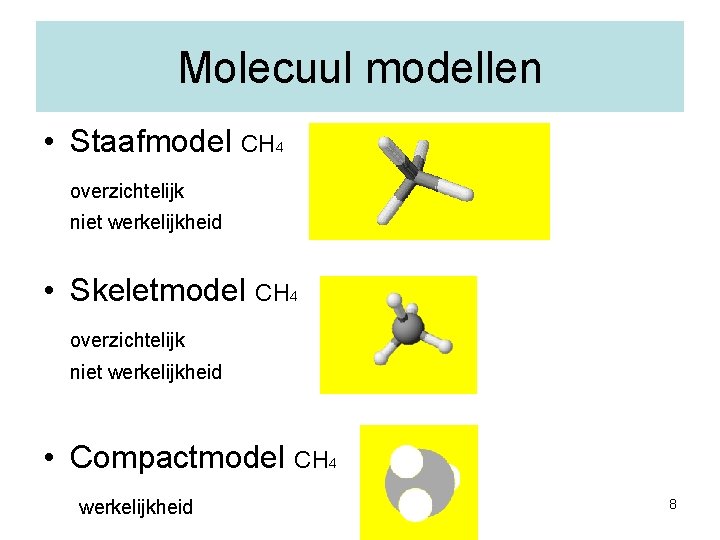
Molecuul modellen • Staafmodel CH 4 overzichtelijk niet werkelijkheid • Skeletmodel CH 4 overzichtelijk niet werkelijkheid • Compactmodel CH 4 werkelijkheid 8

Molecuulformule • Met behulp van een molecuulformule kun je zien welke atoomsoorten en hoeveel atomen er in een molecuul zitten. 9

Index en coëfficient Index (rechtsonder) Aantal atomen Coëfficient (getal vóór de molecuulformule) Aantal deeltjes (moleculen) 10

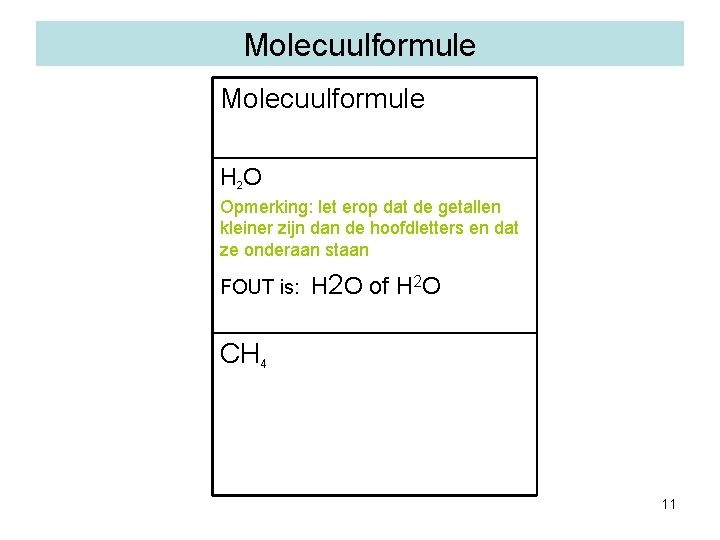
Molecuulformule H 2 O Opmerking: let erop dat de getallen kleiner zijn dan de hoofdletters en dat ze onderaan staan FOUT is: H 2 O of H 2 O CH 4 11

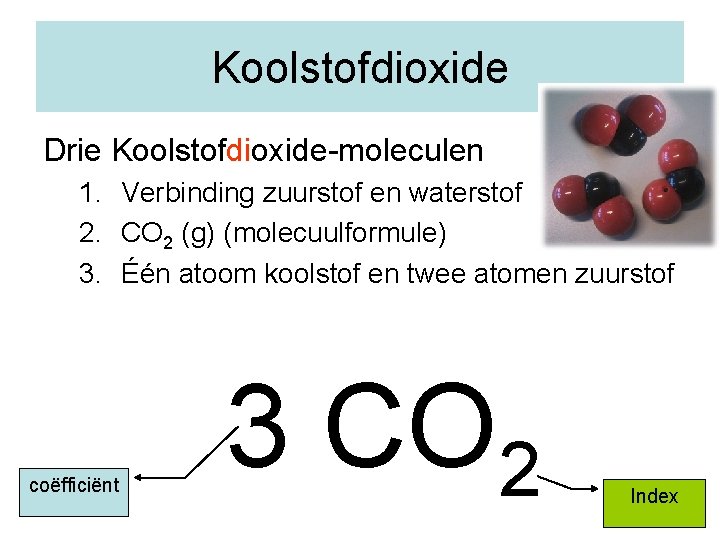
Koolstofdioxide Drie Koolstofdioxide-moleculen 1. Verbinding zuurstof en waterstof 2. CO 2 (g) (molecuulformule) 3. Één atoom koolstof en twee atomen zuurstof coëfficiënt 3 CO 2 Index 12

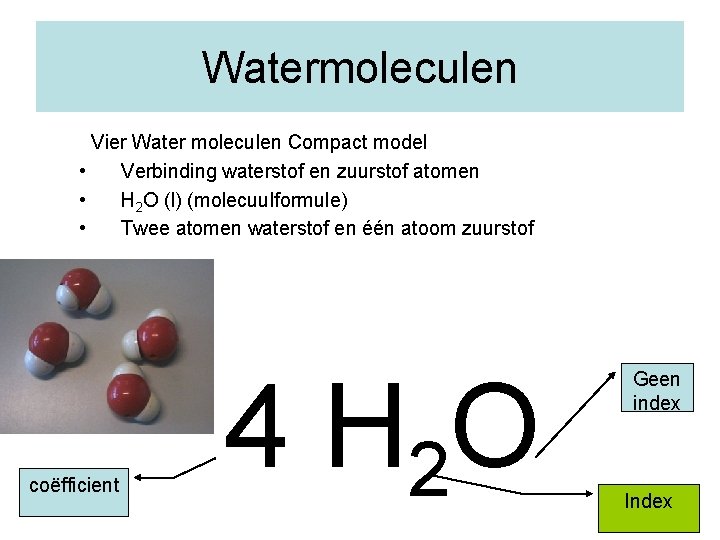
Watermoleculen Vier Water moleculen Compact model • Verbinding waterstof en zuurstof atomen • H 2 O (l) (molecuulformule) • Twee atomen waterstof en één atoom zuurstof coëfficient 4 H 2 O Geen index Index 13

Ontleedbare stoffen • Moleculen (verbindingen) die bestaan uit 2 of meer atoomsoorten • Voorbeelden – – Water (H 2 O) Alcohol (C 2 H 6 O) Koolstofdioxide (CO 2) Methaan (CH 4) 14

Niet ontleedbare stoffen (elementen) • Bestaan uit 1 atoomsoort (enkel) – Alle elementen uit het periodiek systeem behoren hiertoe Bijvoorbeeld: Fe = ijzer Au=goud Al = aluminium Edelgassen: He= helium Ne= Neon Ar=argon Xe= Xenon • Bestaan uit 1 atoomsoort maar dan dubbel – Alle stoffen in het rijtje van Brutus Br 2 N 2 H 2 F 2 Cl 2 I 2 O 2 15

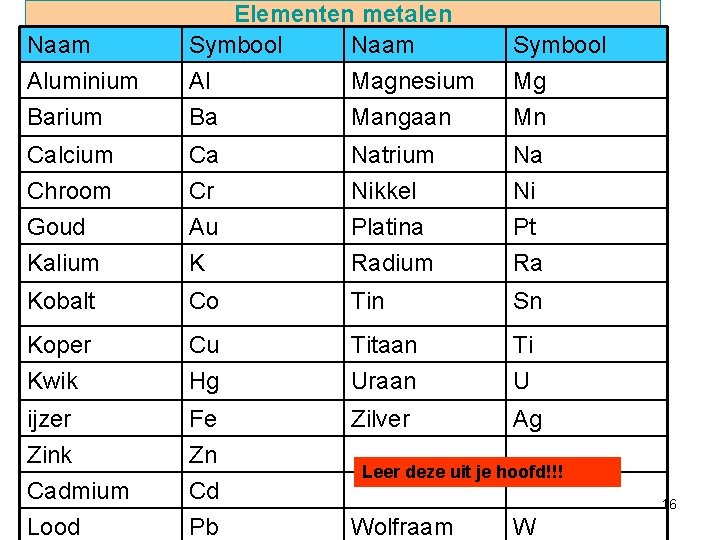
Naam Aluminium Barium Elementen metalen Symbool Naam Al Magnesium Ba Mangaan Symbool Mg Mn Calcium Ca Natrium Na Chroom Goud Kalium Cr Au K Nikkel Platina Radium Ni Pt Ra Kobalt Co Tin Sn Koper Kwik Cu Hg Titaan Uraan Ti U ijzer Zink Cadmium Lood Fe Zn Cd Pb Zilver Ag Leer deze uit je hoofd!!! 16 Wolfraam W

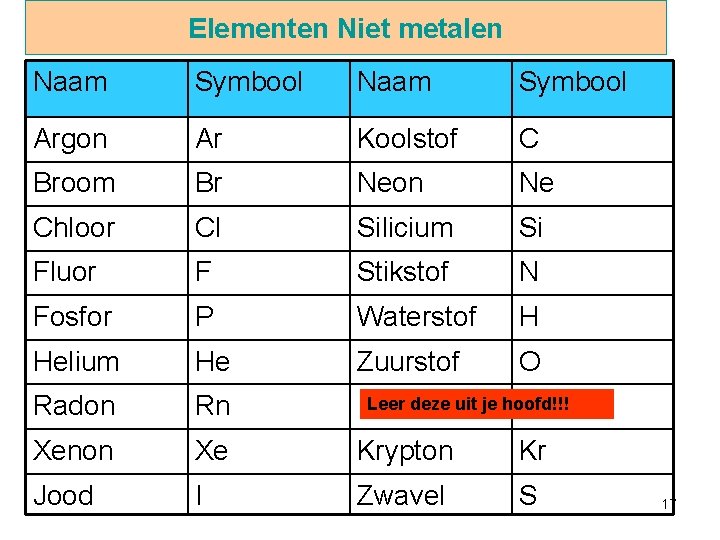
Elementen Niet metalen Naam Symbool Argon Ar Koolstof C Broom Br Neon Ne Chloor Cl Silicium Si Fluor F Stikstof N Fosfor P Waterstof H Helium He Zuurstof O Radon Rn Xenon Xe Krypton Kr Jood I Zwavel S Leer deze uit je hoofd!!! 17