Stoffen en Bindingen Tutor voor de vierde klassen

Stoffen en Bindingen Tutor voor de vierde klassen Hyperlinks zijn groen gekleurd en geven extra informatie 25 -5 -2021 1

Indeling van de Stoffen Bij de indeling van de stoffen in overzichtelijke groepen, maken we gebruik van een theoretische en een praktische benadering. * Theoretische benadering: We kijken naar het type atoom dat in de stof voorkomt (metaal en/of niet-metaal atoom) * Praktische benadering: We kijken naar de geleiding van de elektrische stroom in de vaste en vloeibare fase 25 -5 -2021 Copyright Bogerman 2

Schema Indeling van de Stoffen Beide benaderingen leiden tot de volgende indeling 25 -5 -2021 Copyright Bogerman 3

Molekulaire Stoffen Voor het bespreken van de bindingen die een rol spelen, wordt de groep van de molekulaire stoffen, in tweeën gesplitst 25 -5 -2021 * Hydrofiele Stoffen: stoffen die goed mengbaar zijn met water. * Hydrofobe stoffen: stoffen die slecht mengbaar zijn met water. Copyright Bogerman 4

Overzichtsschema Bindingen Samenvattend treffen we de volgende bindingen aan De bindingen worden in het vervolg per groep besproken 25 -5 -2021 Copyright Bogerman 5

Bindingen bij molekulaire stoffen Molekulaire stoffen bestaan uit molekulen. Molekulen zijn de kleinste eenheden van een stof, waaraan die stof nog herkenbaar is. Een molekuul is een groep atomen met een vaste samenstelling en structuur. Daarom maken we onderscheid tussen: bindingen in het molekuul (sterke binding) * bindingen tussen molekulen (zwakke bindingen) * 25 -5 -2021 Copyright Bogerman 6

Bindingen in het molekuul Een molekuul is opgebouwd uit (een of) meerdere (soorten) atomen. De atomen zitten aan elkaar met een atoombinding. De atoombinding is een sterke binding, die pas bij hoge temperatuur verbroken wordt. 25 -5 -2021 Copyright Bogerman 7

Bindingen tussen molekulen Tussen molekulen komen twee typen bindingen voor. We maken onderscheid tussen de vanderwaalsbinding die bij alle molekulen voorkomt en de waterstofbrug (H-brug) die slechts bij een deel van de molekulen voorkomt. Beide bindingen worden verbroken bij het kookpunt van een stof 25 -5 -2021 8

De binding bij de Zouten Bij de zouten treffen we slechts één binding aan. Dit is een sterke binding. Zouten zijn stoffen die zijn opgebouwd uit ionen. Ionen zijn deeltjes met een permanente positieve of negatieve lading. De aantrekkingskracht tussen deze positieve en negatieve ionen noemen we de ionbinding. meer informatie 25 -5 -2021 9

De binding bij de metalen Bij de metalen treffen we slechts één binding aan. Dit is een sterke binding. Metalen zijn stoffen die zijn opgebouwd uit ‘vrije elektronen’ en metaalatoomresten. De aantrekkingskracht tussen deze positieve metaalatoomresten en negatieve ‘vrije elektronen’ noemen we de metaalbinding. meer informatie 25 -5 -2021 10

Het verbreken van een binding Het verbreken van bindingen kost energie. Naarmate een binding sterker is, kost het meer energie om die binding te verbreken. De temperatuur waarbij voldoende energie aanwezig is om het ‘voorkomen’ van een stof te veranderen, noemen we het smelt- of kookpunt van een stof. Bij een fase-overgang is er zoveel beweging in een stof, dat daarbij een binding wordt verbroken. meer informatie 25 -5 -2021 11

De vanderwaalsbinding (1) In de vaste en vloeibare fase liggen de molekulen tegen elkaar aan. Door de beweging van de elektronen in een molekuul zitten er aan de oppervlakte van het molekuul afwisselend kleine positief en negatief geladen gebiedjes. Tegengesteld geladen gebiedjes van verschillende molekulen trekken elkaar aan. Deze aantrekking noemen we de vanderwaalsbinding meer informatie 25 -5 -2021 8. 1. A

De vanderwaalsbinding (2) Naarmate molekulen groter worden, zal het contactoppervlak tussen die molekulen ook groter worden. Een groter contactoppervlak betekent een sterkere aantrekkingskracht tussen die molekulen. Een sterkere aantrekkingskracht resulteert in een hoger kookpunt voor die stoffen. Hoe groter (zwaarder) het molekuul, hoe sterker de vanderwaalsbinding zal zijn. 25 -5 -2021 8. 1. B

De waterstofbrug (1) Sommige molekulen zijn in het bezit van OH- en/of NHgroepen in hun structuur. Deze groepen hebben een polair karakter. Dat wil zeggen het H-atoom is een beetje positief geladen (δ+) en het O- òf N-atoom is een beetje negatief geladen (δ-) voorbeeld bij een watermolekuul: meer informatie 25 -5 -2021 8. 2. A

De waterstofbrug (2) Deze OH- en NH-groepen kunnen elkaar als kleine magneetjes aantrekken. Daardoor ontstaat er een extra binding tussen molekulen met zo’n groep in hun structuur. Deze binding noemen we de H-brug voorbeeld: (H-brug = - - -) meer informatie 25 -5 -2021 8. 2. B

De waterstofbrug (3) Naast waterstofbrug vormende groepen, zoals OH- en NHgroepen, zijn er ook zogenaamde waterstofbrug ontvangende groepen. Voorbeelden van dat soort groepen zijn bijvoorbeeld de C=O en de C N groep. Het O- en het N-atoom in deze groepen kunnen een H-brug ontvangen. Voorbeeld: 25 -5 -2021 (– – – = H-brug) 8. 2. C

De atoombinding (1) Bij de vorming van een atoombinding, levert elk atoom één elektron voor de vorming van een bindend elektronenpaar. Een atoom kan meerdere bindende elektronenparen hebben. meer informatie 25 -5 -2021 7. A

De atoombinding (2) Het aantal bindende elektronenparen dat een element normaal gesproken vormt, kan bepaald worden met behulp van binas T 103. Rechts onderin elk blokje is de zogenaamde elektronenconfiguratie weergegeven. Het laatste getalletje geeft het aantal elektronen in de ‘buitenwolk’ aan. Niet-metaalatomen streven ernaar om acht elektronen in hun ‘buitenwolk’ te hebben. (uitgezonderd waterstof (2) en boor (6)) meer informatie 25 -5 -2021 7. B

De atoombinding (3) Het aantal bindende elektronenparen dat een atoom is aangegaan in een molekuul, noemen we de covalentie van dat atoom. Met behulp van T 103 is dus te voorspellen hoeveel bindende elektronenparen een atoomsoort meestal zal hebben in een molekuul. Als de atoombinding wordt verbroken, zal het molekuul uiteen vallen. Dit gebeurt alleen bij reacties van stoffen (alleen of met andere stoffen) 25 -5 -2021 7. C

Hydrofobe stoffen zijn herkenbaar aan het ontbreken van OHen NH-groepen. Deze stoffen bevatten vooral CH-groepen Voorbeeld: (butaan) òf meer informatie 25 -5 -2021 Copyright Bogerman 4. 2. A

Hydrofiele stoffen hebben in hun structuurformule één of meer OH- en/of NH-groepen Deze groepen voegen hydrofiel karakter toe aan de stof Voorbeeld: (2 -propanol) òf meer informatie 25 -5 -2021 Copyright Bogerman 4. 1. A

Hydrofiel- en hydrofoob karakter Vooral CH-groepen dragen bij aan hydrofoob karakter. OH- en NH-groepen dragen bij aan hydrofiel karakter. Bij stoffen met beide groepen in hun structuur is het dus van belang welk karakter overheerst. Daardoor wordt bepaald of de stof al dan niet goed met water kan mengen. Als het hydrofobe karakter overheerst, lost de stof niet of slecht op in water. (maar wel goed in bijv. benzine) Als het hydrofiele karakter overheerst, lost de stof goed op in water. (maar slecht in bijv. benzine) meer informatie 25 -5 -2021 4. B

Hydrofiel- en hydrofoob karakter De overgang tussen wel en niet mengbaar wordt dus bepaald door welk karakter overheerst. Overwegend hydrofoob of overwegend hydrofiel karakter. Voorbeeld: 1 -propanol is nog in alle verhoudingen mengbaar met water terwijl 1 -butanol nog slechts beperkt mengbaar is met water. 1 -propanol 25 -5 -2021 1 -butanol 4. C

De ionbinding (1) De metaalionen zijn allemaal enkelvoudige positieve ionen. De lading varieert meestal van 1+ tot 3+. De niet-metaalionen zijn allemaal enkelvoudige negatieve ionen. Zij krijgen allemaal de uitgang -ide. De lading varieert meestal van 1– tot 3 –. Naast enkelvoudige ionen kennen we ook zogenaamde samengestelde ionen. Samengestelde ionen hebben altijd twee of meer symbolen in hun ionformule staan. Je moet één samengesteld positief ion kennen, en een veelvoud aan samengestelde negatieve ionen. meer informatie 25 -5 -2021 9. A

De ionbinding (2) De aantrekkingskracht tussen positief geladen en negatief geladen ionen noemen we de ionbinding. Naarmate de lading van een ion groter wordt, zal de aantrekkingskracht ook groter worden. Naarmate de straal van een ion kleiner wordt, wordt de aantrekkingskracht ook groter. meer informatie 25 -5 -2021 9. B
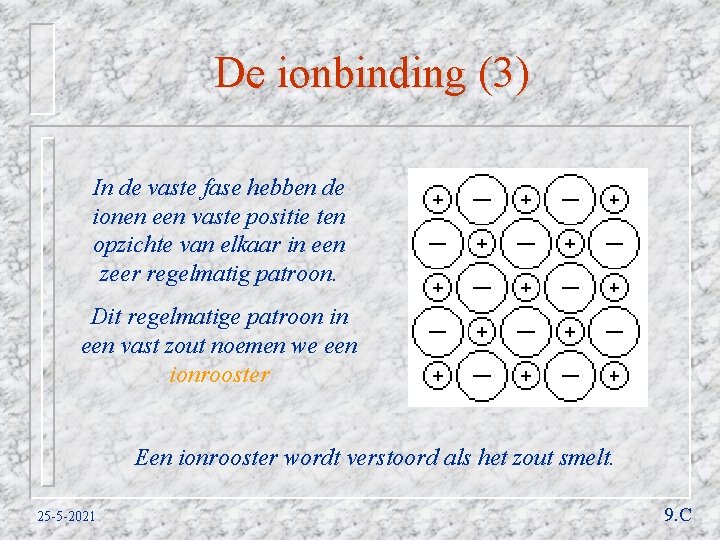
De ionbinding (3) In de vaste fase hebben de ionen een vaste positie ten opzichte van elkaar in een zeer regelmatig patroon. Dit regelmatige patroon in een vast zout noemen we een ionrooster Een ionrooster wordt verstoord als het zout smelt. 25 -5 -2021 9. C

De metaalbinding (1) Bij een metaalatoom is de buitenwolk erg dun bevolkt met elektronen. Daardoor kunnen de wolken van twee naast elkaar liggende metaalatomen makkelijk in elkaar doordringen. Er ontstaat een ‘overlapgebied’. meer informatie 25 -5 -2021 10. A

De metaalbinding (2) Elektronen die terecht komen in het ‘overlapgebied’ zitten dus eigenlijk tegelijkertijd in de elektronenwolk van twee atomen. Dan hangt het van het toeval af om welk atoom ze verder zullen gaan bewegen. Zo kan een elektron van een metaalatoom zich al ‘springend’ dwars door het hele metaal heen bewegen. De elektronen die dit kunnen, worden daarom wel ‘vrije elektronen’ genoemd meer informatie 25 -5 -2021 10. B

De metaalbinding (3) De vrije elektronen vormen als het ware een negatief vangnet rondom de positieve resten van de metaalatomen. De aantrekking tussen dit negatieve ‘vangnet’ en de positieve atoomresten noemen we de metaalbinding. De regelmatige rangschikking van de metaalatomen in de vaste fase noemen we het metaalrooster. 25 -5 -2021 10. C

Overzichtsschema Bij een chemische reactie worden alle bindingen verbroken. meer informatie 25 -5 -2021 11. A

Oplossen van stoffen Bij het oplossen van stoffen worden zowel bindingen verbroken, als nieuwe bindingen gevormd. Bij het oplossen van molekulaire stoffen worden de bindingen tussen de molekulen deels verbroken en er worden nieuwe bindingen gevormd tussen molekulen van het oplosmiddel en de opgeloste stof. Bij het oplossen van zouten wordt de ionbinding verbroken. De ionen worden vervolgens in de oplossing gehydrateerd. Dit hydrateren mag je beschouwen als het vormen van een nieuwe binding. 25 -5 -2021 11. B
- Slides: 31