Stille Oxidation Korrosion Eine chemische Reaktion bei der
![Stille Oxidation Korrosion Eine chemische Reaktion bei der ein Atom, Ion oder Molekül [A] Stille Oxidation Korrosion Eine chemische Reaktion bei der ein Atom, Ion oder Molekül [A]](https://slidetodoc.com/presentation_image_h2/f6f1b868425b9cd171366a82594607ec/image-1.jpg)
Stille Oxidation Korrosion Eine chemische Reaktion bei der ein Atom, Ion oder Molekül [A] ein Elektron abgibt, ist eine Oxidation. [Früher → Reaktion eines Stoffs mit Sauerstoff…] Oxidation: A → An+ + ne. Bsp. : Mg → Mg 2+ + 2 e- Reduktion: B + ne- → Bn+ Bsp. : O 2 + 4 e- → 2 O 2 Ein anderer Stoff [B] nimmt Elektronen auf und wird reduziert. Beide Reaktionen bilden als Teilreaktionen eine Redoxreaktion: 2 Mg + O 2 → 2 Mg. O Mg 2+ O 2 -
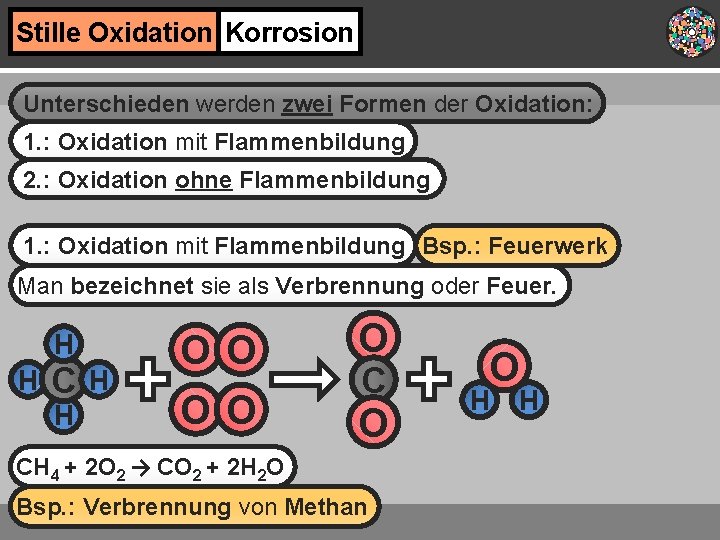
Stille Oxidation Korrosion Unterschieden werden zwei Formen der Oxidation: 1. : Oxidation mit Flammenbildung 2. : Oxidation ohne Flammenbildung 1. : Oxidation mit Flammenbildung Bsp. : Feuerwerk Man bezeichnet sie als Verbrennung oder Feuer. H H C H H OO OO O CH 4 + 2 O 2 → CO 2 + 2 H 2 O Bsp. : Verbrennung von Methan O H H

Stille Oxidation Korrosion 2. : Oxidation ohne Flammenbildung Die stille Oxidation ist eine Oxidation ohne Flammenbildung, bei der die Energie nur langsam abgegeben wird. Bsp. : Oxidation von Traubenzucker im Körper C 6 H 12 O 6 + 6 O 2 → 6 CO 2 + 6 H 2 O
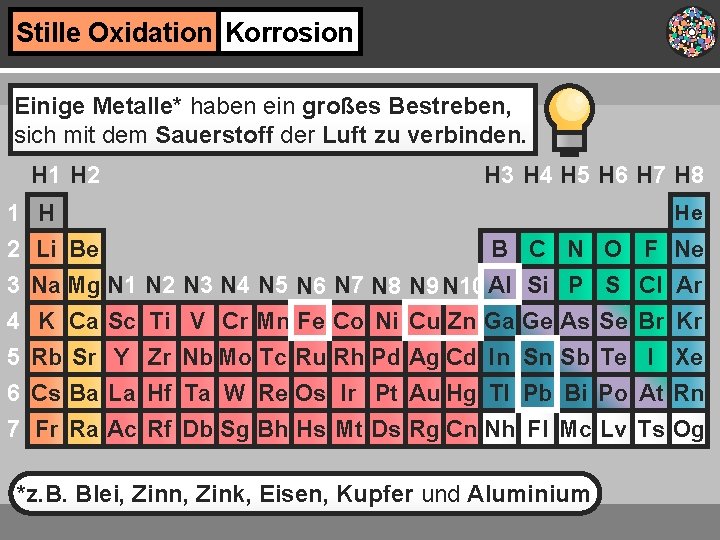
Stille Oxidation Korrosion Einige Metalle* haben ein großes Bestreben, sich mit dem Sauerstoff der Luft zu verbinden. H 1 H 2 H 3 H 4 H 5 H 6 H 7 H 8 1 H 2 Li Be He B C N O F Ne 3 Na Mg N 1 N 2 N 3 N 4 N 5 N 6 N 7 N 8 N 9 N 10 Al Si P S Cl Ar 4 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 6 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg TI Pb Bi Po At Rn 7 Fr Ra Ac Rf Db Sg Bh Hs Mt Ds Rg Cn Nh Fl Mc Lv Ts Og *z. B. Blei, Zinn, Zink, Eisen, Kupfer und Aluminium
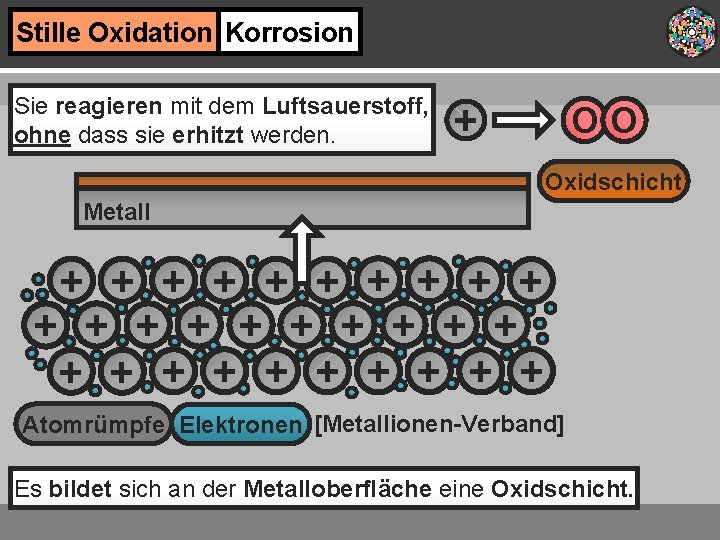
Stille Oxidation Korrosion Sie reagieren mit dem Luftsauerstoff, ohne dass sie erhitzt werden. + OO Oxidschicht Metall + + + + + + + + Atomrümpfe Elektronen [Metallionen-Verband] Es bildet sich an der Metalloberfläche eine Oxidschicht.
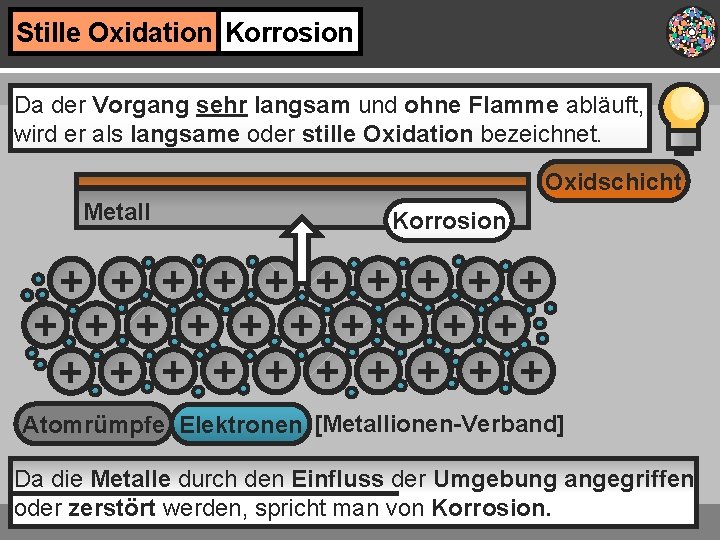
Stille Oxidation Korrosion Da der Vorgang sehr langsam und ohne Flamme abläuft, wird er als langsame oder stille Oxidation bezeichnet. Oxidschicht Metall Korrosion + + + + + + + + Atomrümpfe Elektronen [Metallionen-Verband] Da die Metalle durch den Einfluss der Umgebung angegriffen oder zerstört werden, spricht man von Korrosion.
Stille Oxidation Korrosion Die bedeutendste Korrosion und bekannteste Form der stillen Oxidation ist das Rosten von Eisen oder Stahl. Rost, chemisch gesehen, setzt sich aus Eisen(II)-oxid, Eisen(III)-oxid und Kristallwasser zusammen. Rost x. Fe. IIO �y. Fe 2 IIIO 3 � z. H 2 O [x, y, z positive Verhältniszahlen] An Eisen beginnt die Rostbildung [Korrosion] durch den Angriff einer Säure* oder von Sauerstoff** und Wasser. [*Säurekorrosion; ** Sauerstoffkorrosion] Die Korrosion ist eine chemische Reaktion und beruht auf Redoxreaktionen.
![Stille Oxidation Säurekorrosion Bei einer Säurekorrosion entziehen die Wasserstoffionen [Protonen] der Säure, dem Metall Stille Oxidation Säurekorrosion Bei einer Säurekorrosion entziehen die Wasserstoffionen [Protonen] der Säure, dem Metall](http://slidetodoc.com/presentation_image_h2/f6f1b868425b9cd171366a82594607ec/image-8.jpg)
Stille Oxidation Säurekorrosion Bei einer Säurekorrosion entziehen die Wasserstoffionen [Protonen] der Säure, dem Metall Elektronen. HCl + H 2 O → H 3 O+ + Cl. HCl → H+ + Cl- H Cl Im Wasser reagiert Eisen mit Wasserstoffionen zu Eisen-II-Kationen. Fe ⇌ Fe 2+ + 2 e[Oxidation] 2 H+ + 2 e- ⇌ H 2 [Reduktion] Fe + 2 H+ ⇌ Fe 2+ + H 2 Die Wasserstoffionen nehmen die Elektronen des Metalls auf und reagieren zu Wasserstoffgas.
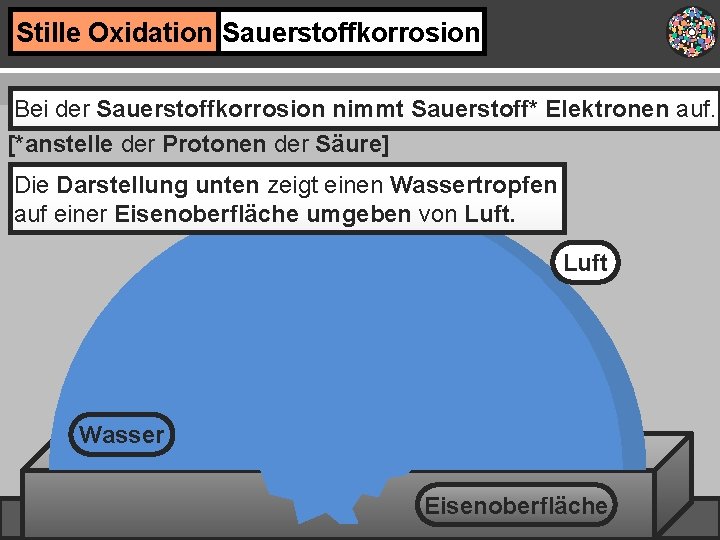
Stille Oxidation Sauerstoffkorrosion Bei der Sauerstoffkorrosion nimmt Sauerstoff* Elektronen auf. [*anstelle der Protonen der Säure] Die Darstellung unten zeigt einen Wassertropfen auf einer Eisenoberfläche umgeben von Luft Wasser Eisenoberfläche
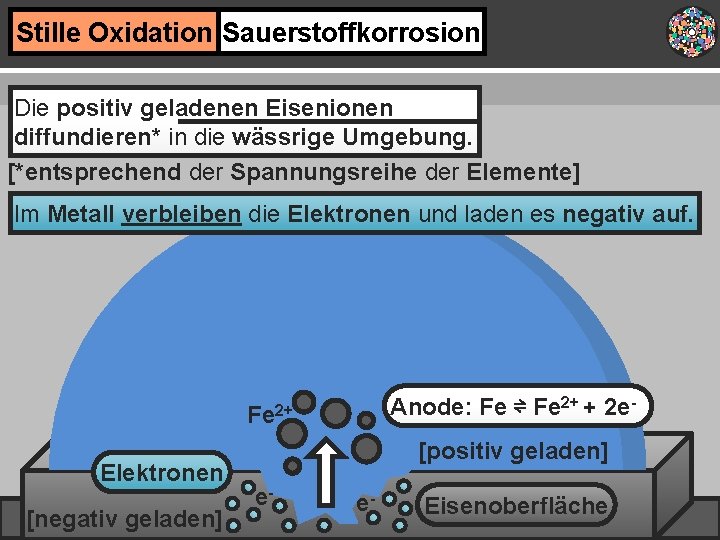
Stille Oxidation Sauerstoffkorrosion Die positiv geladenen Eisenionen diffundieren* in die wässrige Umgebung. [*entsprechend der Spannungsreihe der Elemente] Im Metall verbleiben die Elektronen und laden es negativ auf. Anode: Fe ⇌ Fe 2+ + 2 e- Fe 2+ Elektronen [negativ geladen] [positiv geladen] e- e- Eisenoberfläche
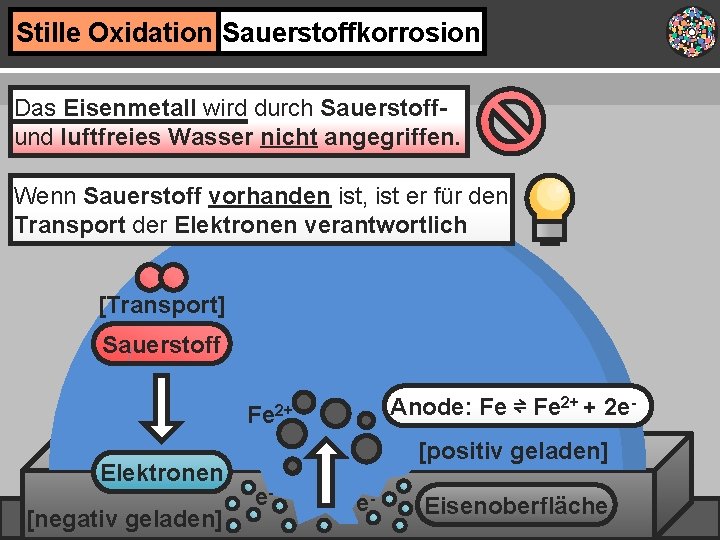
Stille Oxidation Sauerstoffkorrosion Das Eisenmetall wird durch Sauerstoffund luftfreies Wasser nicht angegriffen. Wenn Sauerstoff vorhanden ist, ist er für den Transport der Elektronen verantwortlich [Transport] Sauerstoff Anode: Fe ⇌ Fe 2+ + 2 e- Fe 2+ Elektronen [negativ geladen] [positiv geladen] e- e- Eisenoberfläche
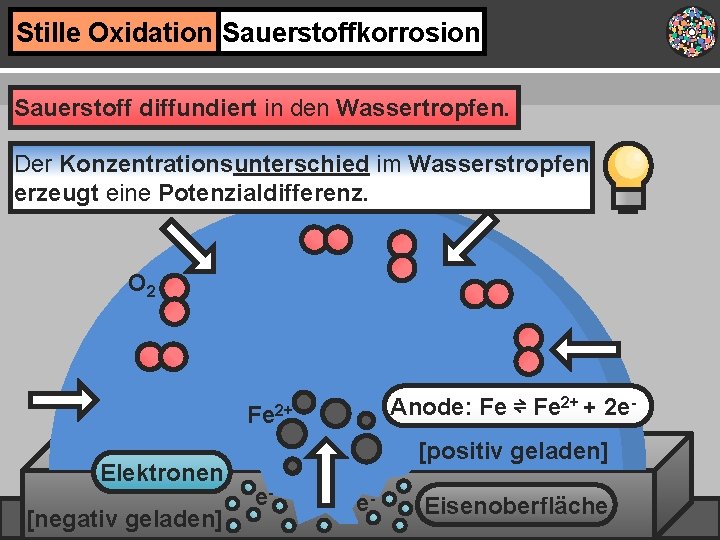
Stille Oxidation Sauerstoffkorrosion Sauerstoff diffundiert in den Wassertropfen. Der Konzentrationsunterschied im Wasserstropfen erzeugt eine Potenzialdifferenz. O 2 Anode: Fe ⇌ Fe 2+ + 2 e- Fe 2+ Elektronen [negativ geladen] [positiv geladen] e- e- Eisenoberfläche
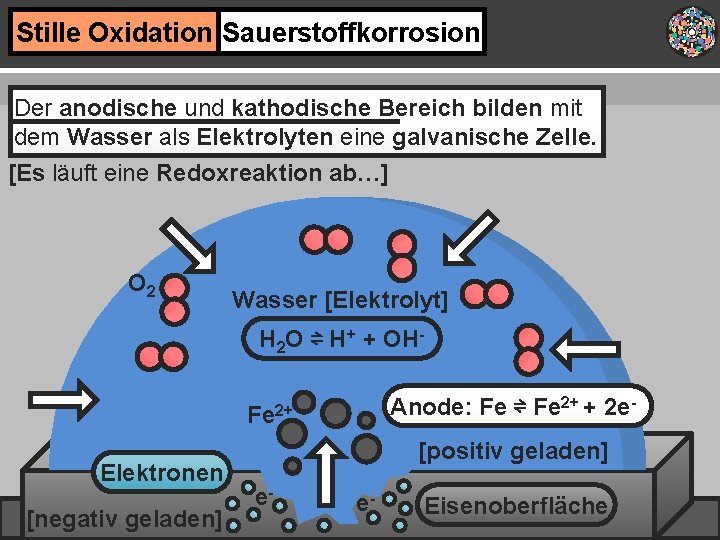
Stille Oxidation Sauerstoffkorrosion Der anodische und kathodische Bereich bilden mit dem Wasser als Elektrolyten eine galvanische Zelle. [Es läuft eine Redoxreaktion ab…] O 2 Wasser [Elektrolyt] H 2 O ⇌ H+ + OHAnode: Fe ⇌ Fe 2+ + 2 e- Fe 2+ Elektronen [negativ geladen] [positiv geladen] e- e- Eisenoberfläche
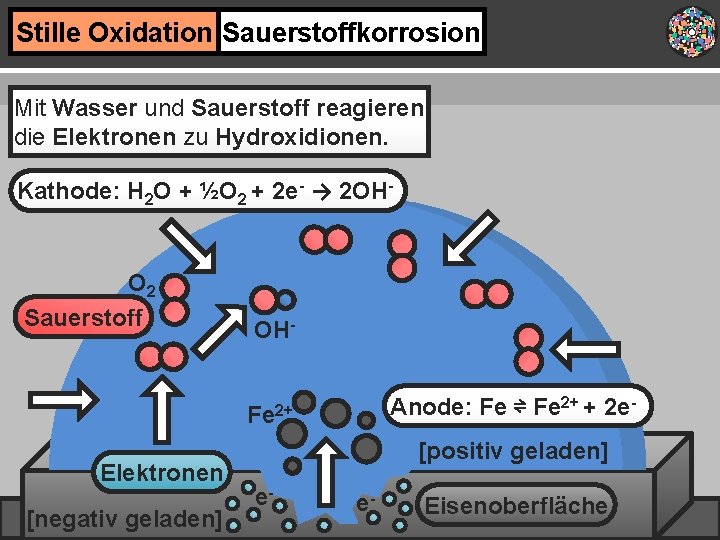
Stille Oxidation Sauerstoffkorrosion Mit Wasser und Sauerstoff reagieren die Elektronen zu Hydroxidionen. Kathode: H 2 O + ½O 2 + 2 e- → 2 OH- O 2 Sauerstoff OHAnode: Fe ⇌ Fe 2+ + 2 e- Fe 2+ Elektronen [negativ geladen] [positiv geladen] e- e- Eisenoberfläche
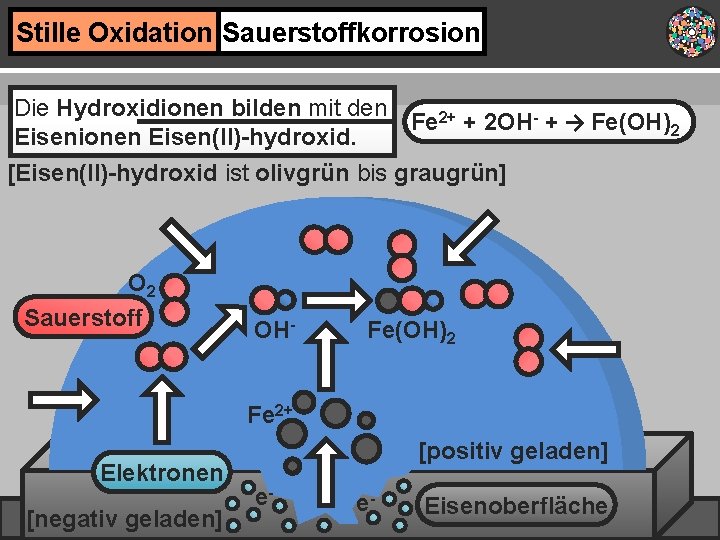
Stille Oxidation Sauerstoffkorrosion Die Hydroxidionen bilden mit den Fe 2+ + 2 OH- + → Fe(OH)2 Eisenionen Eisen(II)-hydroxid. [Eisen(II)-hydroxid ist olivgrün bis graugrün] O 2 Sauerstoff OH- Fe(OH)2 Fe 2+ Elektronen [negativ geladen] [positiv geladen] e- e- Eisenoberfläche

Stille Oxidation Sauerstoffkorrosion In Gegenwart von Wasser und Luft wird Eisen(II)-hydroxid zu Eisen-III-Ionen umgesetzt. Fe(OH)2 → Fe 2+ + 2 OH 2 Fe 2+ + 4(OH)- + ½O 2 + H 2 O → 2 Fe(OH)3 Eisen-III-Ionen bilden zusammen mit Hydroxidionen in einer zweiten Redoxreaktion rostbraunes Eisen(III)-hydroxid.
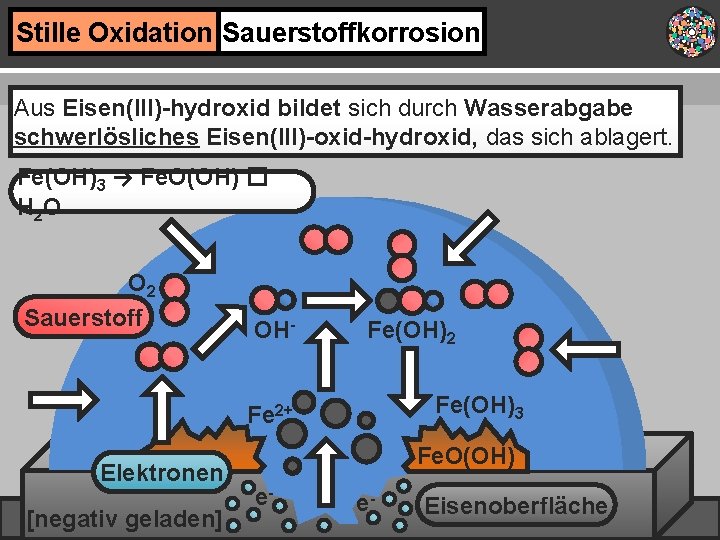
Stille Oxidation Sauerstoffkorrosion Aus Eisen(III)-hydroxid bildet sich durch Wasserabgabe schwerlösliches Eisen(III)-oxid-hydroxid, das sich ablagert. Fe(OH)3 → Fe. O(OH) � H 2 O O 2 Sauerstoff OH- Fe(OH)2 Fe(OH)3 Fe 2+ Elektronen [negativ geladen] Fe. O(OH) e- e- Eisenoberfläche
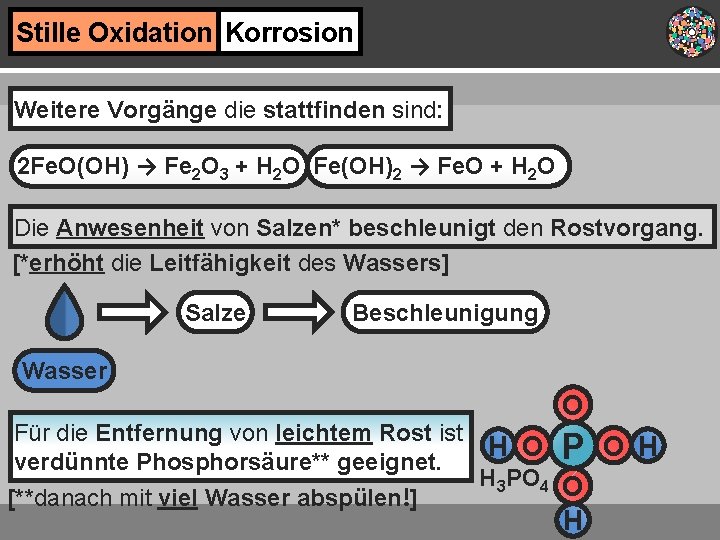
Stille Oxidation Korrosion Weitere Vorgänge die stattfinden sind: 2 Fe. O(OH) → Fe 2 O 3 + H 2 O Fe(OH)2 → Fe. O + H 2 O Die Anwesenheit von Salzen* beschleunigt den Rostvorgang. [*erhöht die Leitfähigkeit des Wassers] Salze Beschleunigung Wasser Für die Entfernung von leichtem Rost ist verdünnte Phosphorsäure** geeignet. [**danach mit viel Wasser abspülen!] O H O P H 3 PO 4 O H
Stille Oxidation Korrosion Weitere Strategien für einen wirksamen Korrosionsschutz: 1. : Abbau der Potentialdifferenz in Lokalelementen 2. : Fernhalten von Feuchtigkeit 3. : Fernhalten von Sauerstoff
Stille Oxidation Zusammenfassung: Die stille Oxidation ist eine Oxidation ohne Flammenbildung, bei der die Energie nur langsam abgegeben wird. Das bekannteste Beispiel für eine stille Oxidation ist das Rosten (Korrosion) von Eisen bzw. Stahl. Für diese Reaktion ist Sauerstoff und Wasser erforderlich.
- Slides: 20