Stedn prmyslov kola elektrotechnick a informanch technologi Brno

Střední průmyslová škola elektrotechnická a informačních technologií Brno Číslo a název projektu: CZ. 1. 07/1. 5. 00/34. 0521 – Investice do vzdělání nesou nejvyšší úrok Autor: Mgr. Nina Nováková Tematická sada: Aplikační matematické úlohy v hodinách chemie Téma: Výpočet p. H silných zásad Číslo materiálu: VY_42_INOVACE_06_03_NONI

Anotace: Tato prezentace slouží k výkladu nové látky v hodinách chemie na éma výpočet p. H silných zásad. Pro pochopení látky je předpokládaná znalost počítání s logaritmy z hodin matematiky. Protože logaritmické funkce se probírají až ve 2. ročníku, je toto učivo zařazeno do hodin chemie ve 3. a 4. ročníku při probírání učiva karboxylových kyselin. Tuto prezentaci je možné využít ve 3. a 4. ročnících oboru Průmyslová ekologie v hodinách chemie a pro zopakování látky v hodinách monitorování životního prostředí.

Výpočet p. H silných zásad 1. jednosytné zásady • silné zásady ( Na. OH, KOH ) jsou ve vodě zcela disociovány na hydroxidové anionty • obdobně jako p. H se vypočítá p. OH • vzorce pro výpočet: • p. OH = - log c (OH- ) p. H = 14 - p. OH

Př. 1. Vypočítejte p. H vodného roztoku hydroxidu sodného o koncentraci 0, 001 mol. dm-3. řešení: p. OH = - log c (OH) p. H = 14 – p. OH = - log c (Na. OH) p. H = 14 - 3 p. OH = - log 0, 001 p. H = 11 p. OH = - (log 10 10 -3) p. OH = - (-3) p. OH = 3 odpověď: PH roztoku Na. OH je 11.

Př. 2. Vypočítejte p. H vodného roztoku hydroxidu amonného o koncentraci 0, 003 mol. dm-3. řešení: p. OH = - log c (OH) p. H = 14 – p. OH = - log c (Na. OH) p. H = 14 – 2, 52 p. OH = - log 0, 003 kalkulačka! p. H = 11, 48 p. OH = - (-2, 52) p. OH = 2, 52 odpověď: p. H roztoku NH 4 OH je 11, 48.

Př. 3. Roztok hydroxidu draselného má p. H 8, 15. Vypočítejte, jaká je koncentrace tohoto hydroxidu. řešení: p. H +p. OH =14 – p. H p. OH = 14 – 8, 15 p. OH = 5, 85
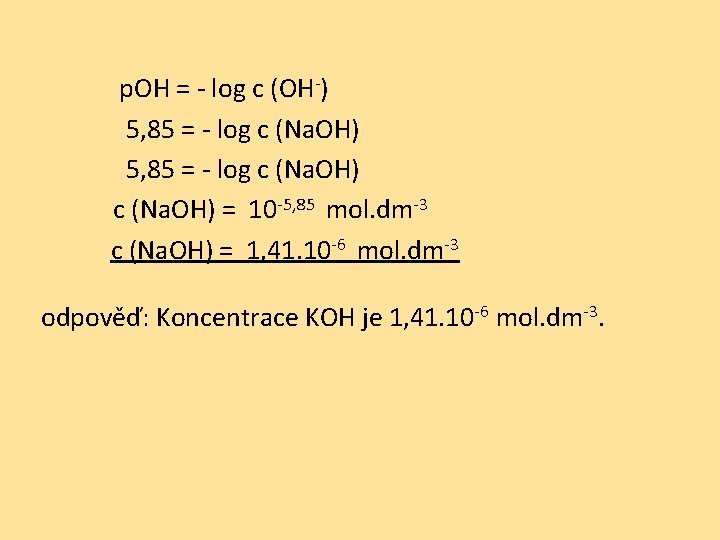
p. OH = - log c (OH-) 5, 85 = - log c (Na. OH) = 10 -5, 85 mol. dm-3 c (Na. OH) = 1, 41. 10 -6 mol. dm-3 odpověď: Koncentrace KOH je 1, 41. 10 -6 mol. dm-3.

2. vícesytné zásady • silné hydroxidy B(OH)x jsou také ve vodě zcela disociovány, ale koncentrace hydroxidových aniontů je x krát větší než koncentrace hydroxidu

Př. 1. Jaké je p. H roztoku Ba(OH)2 o koncentraci 0, 00017 M (mol. dm-3 ) ? řešení: p. OH = - log c (OH-) p. H = 14 – p. OH = - log 2. c [Ba(OH)2] p. H = 14 – 3, 47 p. OH = - log 2. 0, 00017 p. H = 10. 53 p. OH = - log 0, 00034 kalkulačka! p. OH = 3, 47 odpověď: p. H roztoku Ba(OH)2 je 10, 53.

Př. 2. Roztok hydroxidu vápenatého má p. H 11, 5. Vypočítejte, jaká je koncentrace tohoto hydroxidu. řešení: p. H +p. OH =14 – p. H p. OH = 14 – 11, 5 p. OH = 2, 5

p. OH = - log c (OH-) 2, 5 = - log 2. c [Ca(OH)2] = 10 -2. 5 mol. dm-3 2. c [Ca(OH)2] = 0. 0032 mol. dm-3 c [Ca(OH)2] = 0, 0015 mol. dm-3 c [Ca(OH) ] = 1, 5. 10 -3 mol. dm-3 odpověď: Koncentrace Ca(OH)2 je 1, 5. 10 -3 mol. dm-3.

Zdroje: VACÍK, Jiří. Přehled středoškolské chemie. Praha: SPN, 1995, ISBN 80 -7235 -108 -7. KOTLÍK, Bohumír; RŮŽIČKOVÁ, Květoslava. Chemie v kostce: pro střední školy. Obecná a anorganická chemie, výpočty v oboru chemie. I. Praha: Fragment, 1999, ISBN 8072003194. WIKIPEDIA. p. H [online]. [cit. 27. 9. 2013]. Dostupný na WWW: http: //cs. wikipedia. org/wiki/PH
- Slides: 12