Stedn prmyslov kola elektrotechnick a informanch technologi Brno

Střední průmyslová škola elektrotechnická a informačních technologií Brno Číslo a název projektu: CZ. 1. 07/1. 5. 00/34. 0521 – Investice do vzdělání nesou nejvyšší úrok Autor: Mgr. Kateřina Fialová Tematická sada: Aplikační matematické úlohy v hodinách chemie Téma: Názvosloví anorganických sloučenin – oxidační číslo, pravidla pro určování oxidačních čísel, názvosloví oxidů, názvosloví hydroxidů Číslo materiálu: VY_42_INOVACE_06_17_FIKA

Anotace: Prezentace je určena pro studenty středních škol. Obsahuje pojmy: oxidační číslo, elektronegativita, pravidla pro určování oxidačních čísel, názvosloví oxidů, názvosloví hydroxidů. Je určena pro výuku názvosloví oxidů a hydroxidů v hodinách chemie či základů přírodních věd. A dále procvičuje poměr, krácení největším společným celočíselným dělitelem a lineární rovnice v předmětu matematika. Zdroj: 1) Blažek J. , Melichar M. : Přehled chemického názvosloví, SPN Praha 1986, 1. vydání, 160 stran. 2) Vacík J. , Barthová J. : Přehled středoškolské chemie, SPN Praha 1996, 3. vydání, 368 stran.

Názvosloví

Elektronegativita je schopnost atomu přitahovat vazebné elektrony. Oxidační číslo je rovno výslednému náboji, který by atom získal přiřazením všech vazebných elektronů atomu, který má větší elektronegativitu.

Oxidační číslo (dále jen ox. č. ) I I Na Cl se zapisuje vpravo nahoře za značkou prvku značí se římskými číslicemi nabývá hodnot od – IV do VIII (včetně 0) u kladných ox. č. se obvykle znaménko + nezapisuje.

Pravidla pro určení ox. čísel 1) Ox. č. izolovaného atomu je „ 0“. 0 Ag 2) Ox. č. molekuly složené ze stejných atomů je „ 0“. 0 O 2

Pravidla pro určení ox. čísel 3) Ox. č. alkalických kovů (Li, Na, K, Rb, Cs) ve sloučeninách je „I“. I Li Cl chlorid lithný 4) Ox. č. kovů alkalických zemin (Be, Mg, Ca, Sr, Ba) ve sloučeninách je „II“. II Be O oxid beryllnatý Be O

Pravidla pro určení ox. čísel 5) Ox. č. vodíku v kyselinách je „I“. I H Cl kyselina chlorovodíková 6) Ox. č. vodíku v hydridech je „-I“. - I Li. H hydrid lithný

Pravidla pro určení ox. čísel 7) Ox. č. kyslíku oxidech je „- II“. - II CO oxid uhelnatý 8) Ox. č. kyslíku v peroxidu vodíku je „-I“. I - I H 2 O 2 peroxid vodíku

Pravidla pro určení ox. čísel 9) Ox. č. halogenidu (fluorid F-I, -I -I -I chlorid Cl , bromid Br , jodid I ) ve sloučeninách je „- I“. - I I Na Cl chlorid sodný

Pravidla pro určení ox. čísel 10) Ox. č. hydroxidové skupiny je „- I“. II Ca (OH)2 - I hydroxid vápenatý 11) Součet oxidačních čísel všech atomů v molekule se rovná „ 0“. I - I H 2 O 2 2 * I + 2 *(-I) = 0 0 = 0
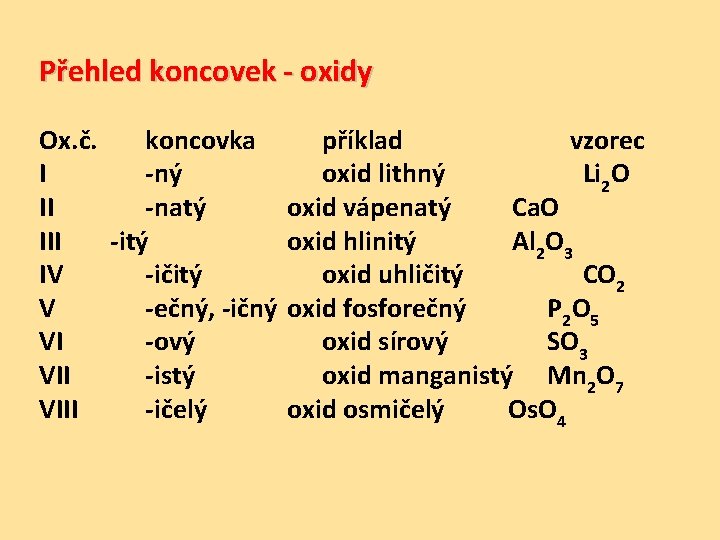
Přehled koncovek - oxidy Ox. č. koncovka I -ný II -natý III -itý IV -ičitý V -ečný, -ičný VI -ový VII -istý VIII -ičelý příklad vzorec oxid lithný Li 2 O oxid vápenatý Ca. O oxid hlinitý Al 2 O 3 oxid uhličitý CO 2 oxid fosforečný P 2 O 5 oxid sírový SO 3 oxid manganistý Mn 2 O 7 oxid osmičelý Os. O 4

Názvosloví oxidů Název oxidu se skládá: oxid uhelnatý z podstatného jména oxid z přídavného jména uhelnatý, jehož koncovka určuje ox. číslo uhlíku „II“.
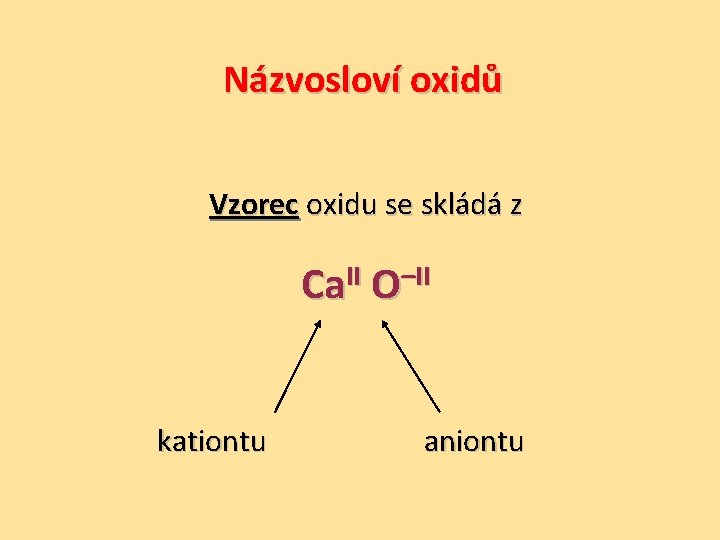
Názvosloví oxidů Vzorec oxidu se skládá z Ca. II O–II kationtu aniontu
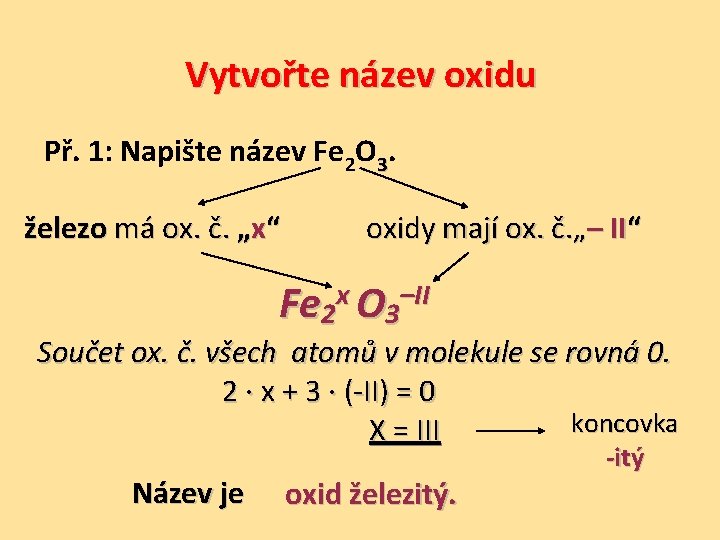
Vytvořte název oxidu Př. 1: Napište název Fe 2 O 3. železo má ox. č. „x“ oxidy mají ox. č. „– II“ x –II Fe 2 O 3 Součet ox. č. všech atomů v molekule se rovná 0. 2 ∙ x + 3 ∙ (-II) = 0 X = III Název je oxid železitý. koncovka -itý
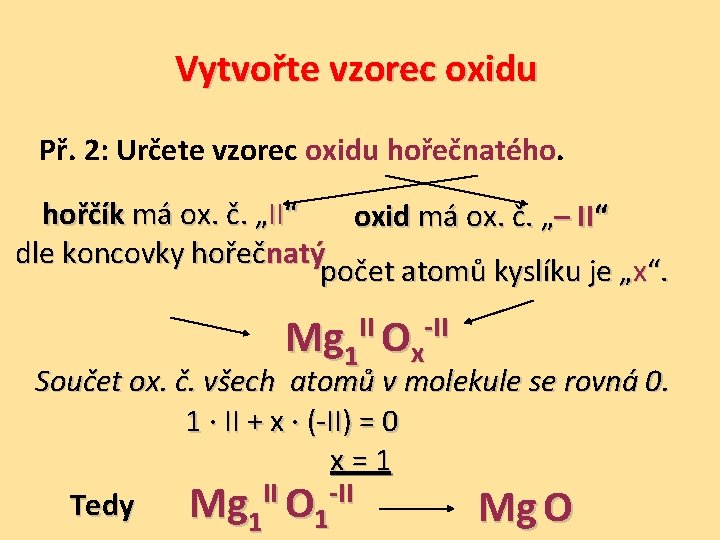
Vytvořte vzorec oxidu Př. 2: Určete vzorec oxidu hořečnatého. hořčík má ox. č. „II“ oxid má ox. č. „– II“ dle koncovky hořeč natý počet atomů kyslíku je „x“. Mg 1 II Ox-II Součet ox. č. všech atomů v molekule se rovná 0. 1 ∙ II + x ∙ (-II) = 0 x = 1 Tedy Mg II O 1 -II Mg O 1
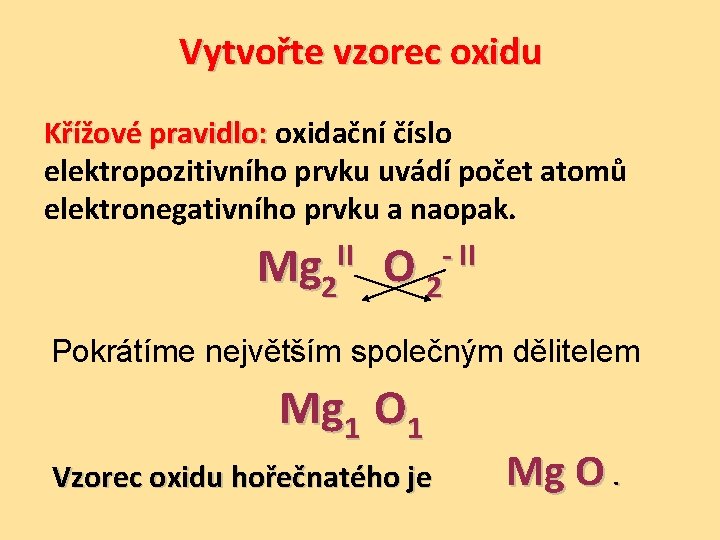
Vytvořte vzorec oxidu Křížové pravidlo: oxidační číslo Křížové pravidlo: elektropozitivního prvku uvádí počet atomů elektronegativního prvku a naopak. II - II Mg 2 O 2 Pokrátíme největším společným dělitelem Mg 1 O 1 Mg O. Vzorec oxidu hořečnatého je

Názvosloví hydroxidů Název hydroxidu se skládá: hydroxid draselný z podstatného jména hydroxid z přídavného jména draselný, jehož koncovka určuje ox. číslo draslíku „I“.
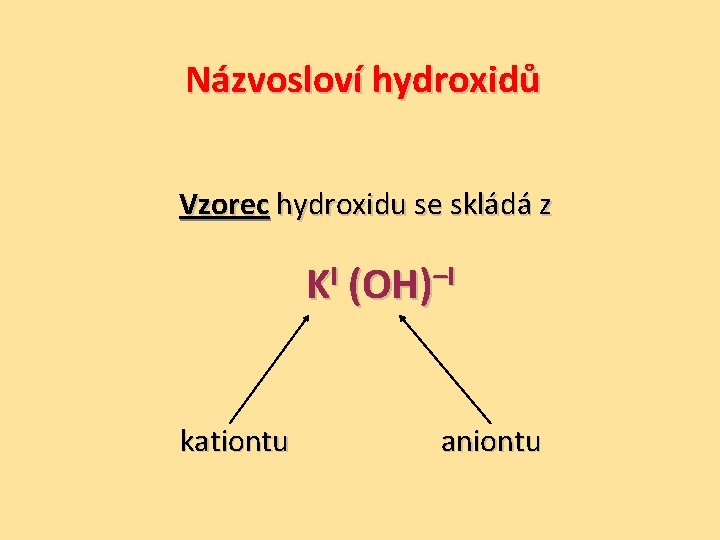
Názvosloví hydroxidů Vzorec hydroxidu se skládá z KI (OH)–I kationtu aniontu
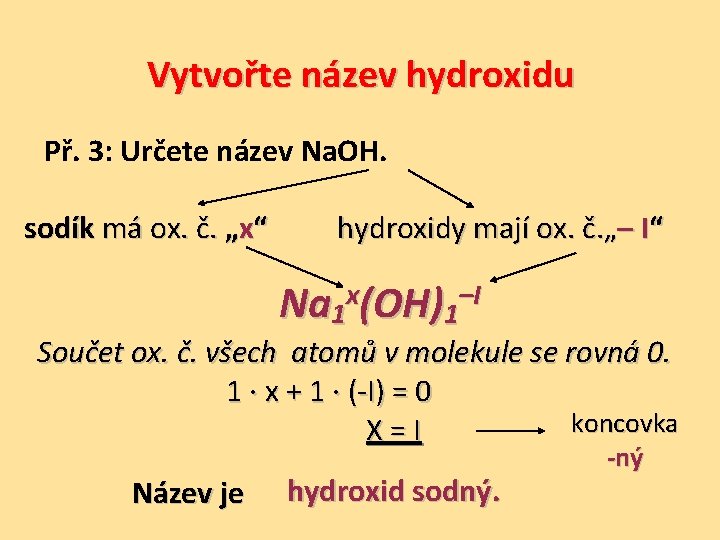
Vytvořte název hydroxidu Př. 3: Určete název Na. OH. sodík má ox. č. „x“ hydroxidy mají ox. č. „– I“ x –I Na 1 (OH)1 Součet ox. č. všech atomů v molekule se rovná 0. 1 ∙ x + 1 ∙ (-I) = 0 X = I Název je hydroxid sodný. koncovka -ný
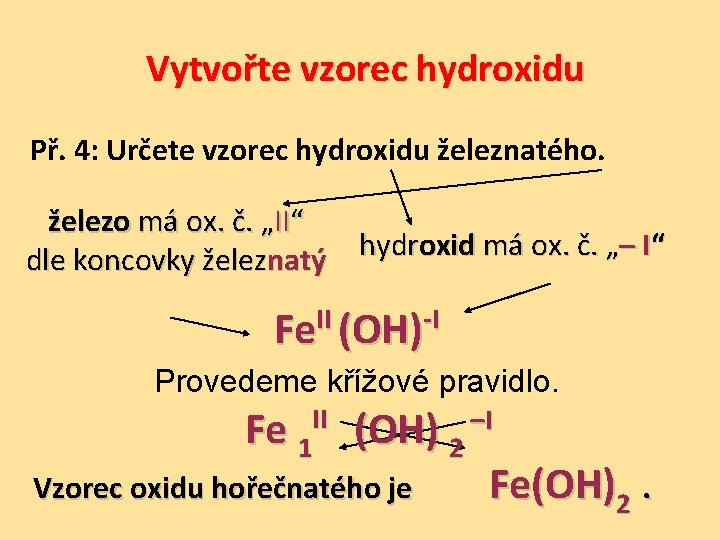
Vytvořte vzorec hydroxidu Př. 4: Určete vzorec hydroxidu železnatého. železo má ox. č. „II“ dle koncovky železnatý hydroxid má ox. č. „– I“ Fe. II (OH)-I Provedeme křížové pravidlo. Fe 1 II (OH) 2 –I Fe(OH)2. Vzorec oxidu hořečnatého je
- Slides: 21