Stappenplan berekeningen zuren en basen Voor de p

Stappenplan berekeningen zuren en basen

Voor de p. H-berekeningen moet je deze formules kennen! (binastabel 38 A) p. H = - log [H 3 O+] = 10 -p. H p. OH = - log [OH-] = 10 -p. OH Natuurlijk is het mogelijk dat je in een opgave meer rekenstappen nodig hebt, bv van mol gram of gram molariteit. Onthoud: Het aantal decimalen van de p. H = het aantal significantie cijfers

Als je moet rekenen aan een oplossing van een zuur en/of base, dan moet je eerst bekijken of je te maken hebt met een oplossing van: • • • Een sterk zuur Een zwak zuur Een sterke base Een zwakke base Een buffer, dus een oplossing van zwak zuur en de geconjugeerde base (de base die bij het zuur hoort, deze ontstaat als het zuur één H+ afstaat, deze base staat naast het zuur in tabel 49) • Op de volgende dia’s staan de stappenplannen.

Is het een oplossing van een sterk of zwak zuur? (tabel 49) Een sterk zuur: • Deze geeft alle H+-ionen af aan H 2 O-moleculen. Bijvoorbeeld 1, 0 M zoutzuur, alle HCl-moleculen hebben hun H+-ionen afgegeven, dus [H 3 O+] = 1, 0 M p. H=-log[H 3 O+] Een oplossing van zwak zuur: bv CH 3 COOH 1. Noteer de vergelijking van het evenwicht van het zuur met watermoleculen in de oplossing. 2. Noteer hieronder B(begin) R (reactie) en E (evenwicht) (of B O E) 3. Noteer onder de B, R en E wat je al weet of kunt berekenen, schrijf altijd aantal mol per liter op. Bedenk hierbij dat [CH 3 COO-] =[H 3 O+] 4. Schrijf de evenwichtsvoorwaarde op ( Kz = concentratiebreuk) 5. Kijk wat je in deze evenwichtsvoorwaarde kunt invullen. Welke molariteiten weet je, is de Kz bekend (tabel 49)? Vul voor onbekenden een x in. 6. Bereken x (en bedenk nu goed wat je hebt uitgerekend!) 7. Bekijk of je x mocht verwaarlozen. (Denk aan de 10%)
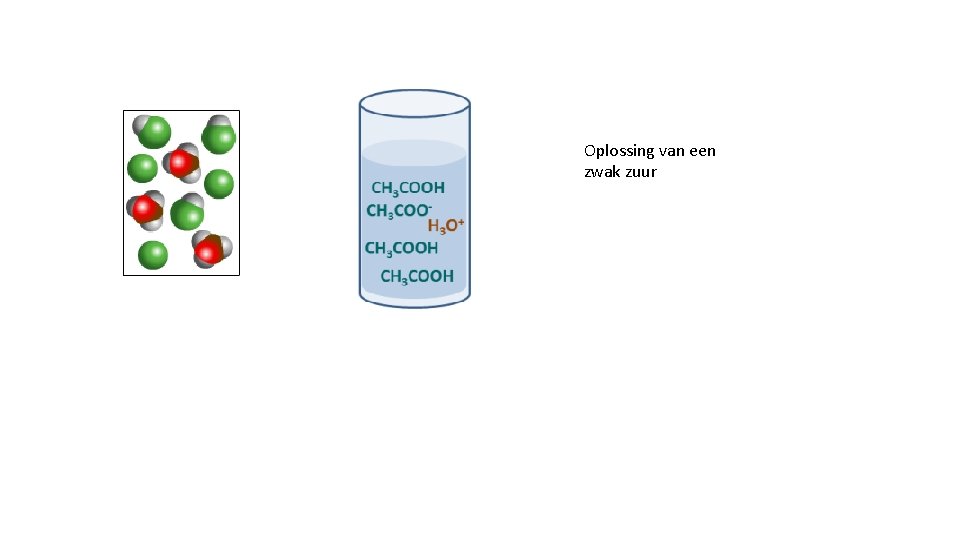
Oplossing van een zwak zuur

Is het een oplossing van een sterke of zwakke base? (tabel 49) Een sterke base: Bijvoorbeeld 1, 0 M natronloog, oplosvergelijking: Na. OH (s) Na+ (aq) + OH- (aq), [OH-] = 1, 0 M p. OH=-log[OH-] , p. H = 14, 00 - p. OH Een oplossing van zwakke base: bv Na. CH 3 COO (natriumacetaat) 1. Noteer (zo nodig) de oplosvergelijking. Noteer daarna de vergelijking van het evenwicht van de base met watermoleculen in de oplossing. 2. Noteer hieronder B(begin) R (reactie) en E (evenwicht) 3. Noteer onder de B, R en E wat je al weet of kunt berekenen, schrijf altijd aantal mol per liter op. Bedenk hierbij dat [CH 3 COO-] =[OH-] 4. Schrijf de evenwichtsvoorwaarde op ( Kb = concentratiebreuk) 5. Kijk wat je in deze evenwichtsvoorwaarde kunt invullen. Welke molariteiten weet je, is de K b bekend (tabel 49)? Vul voor onbekenden een x in. 6. Bereken x (en bedenk nu goed wat je hebt uitgerekend!) 7. Bekijk of je x mocht verwaarlozen. (Denk aan de 10%) 8. Als het wordt gevraagd: Bereken de p. H met 14, 00 – POH (let op significantie)


Extra voor 6 vwo: Een bufferoplossing (Een zwak zuur: bv CH 3 COOH en de geconjugeerde base CH 3 COO-) 1. Noteer de vergelijking van het evenwicht van het zwakke zuur met watermoleculen in de oplossing. (Bij buffers mag je ook de zwakke base 2. Schrijf de evenwichtsvoorwaarde op ( Kz = concentratiebreuk) 3. Bedenk hierbij dat [CH 3 COO-] nu niet gelijk is aan [H 3 O+]. Je lost het zwakke zuur en de zwakke base op 4. Kijk wat je in deze evenwichtsvoorwaarde kunt invullen. 5. Er wordt meestal gevraagd naar: • de p. H bij bekende verhouding zwak zuur: geconjugeerde base of het omgekeerde, • de verhouding zwak zuur: geconjugeerde base bij een gegeven p. H. Bij buffers een verschillende molariteit! [CH 3 COO-]. [H 3 O+] p. H Kz = -------------[CH 3 COOH] Tabel 49 De verhouding zuur: base (of base: zuur)
- Slides: 8