Standar Mikrobiologi dan Uji Mikrobiologi untuk Bahan dan

Standar Mikrobiologi dan Uji Mikrobiologi untuk Bahan dan Produk Farmasi Marlia Singgih Wibowo 1

Bahan Farmasi • • Bahan baku Air murni (Purified Water) Produk Farmasi Steril (Sterile Pharmaceuticals) Produk Farmasi Non-Steril (Non-Sterile Pharmaceuticals) 2

3

BAHAN BAKU FARMASI • Bahan baku untuk produk farmasi dapat berupa bahan kimia atau bahan yang berasal dari alam • Bahan yang berasal dari alam lebih cenderung terkontaminasi mikroorganisme lebih berat dibandingkan bahan sintetik kimia 4

Kategori Bahan Baku Alam (Grigo, 1976) 1. Bahan baku hasil sintesis atau ekstrak bahan alam yang sudah dimurnikan (rata-rata 10 cfu/g atau m. L) 2. Bahan baku hasil sintesis dan dari bahan alam (rata-rata 102 cfu/g atau m. L) 3. Ekstrak tanaman (rata-rata 103 cfu/g atau m. L) 4. Produk hewan atau tanaman yang sedikit mengalami proses (rata-rata 104 cfu/g atau m. L) 5. Produk hewan atau tanaman yang tidak mengalami proses (rata-rata 105 cfu/g atau m. L) 5
• • Mikroorganisme kontaminan yang sering dijumpai dalam bahan baku alam Bacillus Enterobacteriaceae Staphylococcus Aspergillus Penicillium Mucor Rhizopus E. coli Salmonella 6

AIR • • Air minum (potable water) : tidak boleh ada Coliform bacilli per 100 ml Air untuk injeksi : – < 0, 25 endotoksin unit (EU) per ml. – Batas mikroba < 10 cfu per 100 ml – Tidak ada Pseudomonas • Air untuk sediaan non-steril : o Kisaran dari <10 sampai < 100 cfu per 100 ml o Tidak ada Pseudomonas 7

Produk Farmasi Steril • Untuk produk parenteral, sediaan obat mata, termasuk larutan lensa kontak , dan produk-produk yang diberikan pada luka terbuka atau untuk proses irigasi rongga tubuh. • Uji sterilitas perlu dilakukan • Syarat Steril : Sterility Assurance Level dengan probabilitas sama atau lebih baik dari 10 -6, artinya dalam satu juta sediaan steril hanya boleh maksimum 1 yang tidak steril. • Analisis sterilitas adalah berdasarkan tidak adanya pertumbuhan mikroba pada media Fluid Thioglycollate (FTM) dan Soyabean Casein Digest (SCD)pada 30 -35°C (bakteri) dan 20 -25°C (fungi) selama 7 dan 14 hari. 8

Produk Farmasi Non-Steril • Tidak ada aturan tunggal yang mengatur, tergantung pada farmakope negara masing • Tidak mengandung mikroba yang dapat menyebabkan infeksi akibat penggunaan obat tersebut (medication-borne infection) • TVC (Total Viable Count) dalam jumlah tertentu dan tidak adanya patogen enterik dalam bahan baku nya. 9

Persyaratan Kualitas Mikrobiologi Sediaan Farmasi versi FIP (1976) Gol. Jenis Sediaan Persyaratan 1 a 1 b Injeksi Steril – Farmakope Obat mata, sed. utk bgn tubuh Bebas mikroba yang memp. daya hidup/g atau yg bebas mikroba, sed. utk luka m. L bakar, tukak berat 2 Sed. topikal pada lesi kulit, hidung, tenggorokan (resiko tinggi) Mikroba yg memp. daya hidup maks 102 /g atau m. L, dan tidak mengandung Enterobacteriaceae, P. aeruginosa, S. aureus 3 Sediaan lain Mikroba yg memp. daya hidup maks 103 – 104 bakteri anaerob, 102 ragi dan kapang /g atau m. L, Batas mikroba spesifik : tdk ada E. coli, dan tidak mengandung Salmonella, P. aeruginosa, S. aureus, Enterobacteriaceae lain maks. 102 /g atau 10 m. L
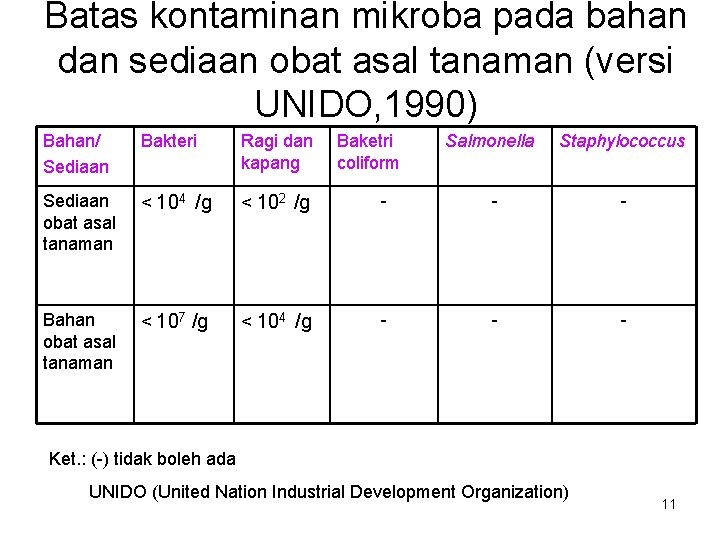
Batas kontaminan mikroba pada bahan dan sediaan obat asal tanaman (versi UNIDO, 1990) Bahan/ Sediaan Bakteri Ragi dan kapang Sediaan obat asal tanaman < 104 /g < 102 /g Bahan obat asal tanaman < 107 /g < 104 /g Baketri coliform Salmonella Staphylococcus - - - Ket. : (-) tidak boleh ada UNIDO (United Nation Industrial Development Organization) 11

Uji Mikrobiologi yang Tercantum pada Farmakope Indonesia edisi IV • Uji secara Mikrobiologi <51> Uji Batas Mikroba <61> Uji Efektivitas Pengawet <71> Uji Sterilitas • Uji dan Penetapan secara Biologi <91> Penetapan Aktivitas Vitamin B 12 <121> Penetapan Kadar Kalsium Pantotenat <131> Penetapan Potensi Antibiotik secara Mikrobiologi 12

<51> Uji Batas Mikroba • Dilakukan untuk memperkirakan jumlah mikroba aerob viabel di dalam semua jenia perbekalan farmasi, mulai dari bahan baku hinga sediaan jadi • Untuk menyatakan bahwa perbekalan farmasi tersebut bebas dari spesies mikroba tertentu • Pengerjaan harus dilakukan secara aseptik • Jika tidak dinyatakan lain, “inkubasi” adalah menempatkan wadah di dalam ruang terkendali secara termostatik pada suhu antara 30 – 35°C selama 24 – 48 jam • Istilah “tumbuh” ditujukan untuk pengertian adanya dan kemungkinan adanya perkembangan mikroba viabel 13

<61> Uji Efektivitas Pengawet • Pengertian Pengawet Antimikroba : zat yang ditambahkan pada sediaan obat untuk melindungi sediaan terhadap kontaminasi mikroba. • Pengawet terutama digunakan pada wadah dosis ganda • Pengawet tidak boleh digunakan semata-mata untuk menurunkan jumlah mikroba viabel sebagai pengganti cara produksi yang tidak baik • Kadar yang digunakan harus serendah mungkin • Pengujian dalam farmakope dimaksudkan untuk menguji efektivitas pengawet yang ditambahkan pada sediaan dosis ganda yang dibuat dengan dasar atau bahan pembawa cairan • Pengujian dan persyaratan hanya berlaku pada produk di dalam wadah asli yang belum dibuka , yang didistribusikan oleh produsen 14

<71> Uji Sterilitas • Digunakan untuk menetapkan apakah bahan atau produk farmasi yang harus steril memenuhi syarat berkenaan dengan uji sterilitas seperti yang tertera pada masing-masing monografi bahan atau produk • Untuk penggunaan prosedur uji sterilitas sebagai bagian dari pengawasan mutu di industri, tertera pada <1371> Sterilisasi dan Jaminan Sterilitas Bahan Kompendia • Mengingat kemungkinan hasil positif dapat disebabkan oleh pengerjaan yang salah atau kontaminasi lingkungan, diberlakukan pengujian 2 tahap seperti yang tertera pada bagian : Penafsiran Hasil Uji Sterilitas 15

• Prosedur alternatif dapat digunakan asal hasil yang diperoleh sekurang-kurangnya setara keandalannya → Lihat Prosedur pada Uji dan Penetapan dalam Ketentuan Umum • Jika timbul perbedaan, dan adanya kontaminasi terdapat pada hasil dari prosedur Farmakope, maka hasil harus dinyatakan sebagai tidak memenuhi syarat. 16

<91> Penetapan Aktivitas Vitamin B 12 • Dilakukan menggunakan bakteri uji Lactobacillus leichmanii dengan metode turbidimetri • Pembanding larutan baku Sianokobalamin BPFI berkisar antara 0, 01 – 0, 04 ng per m. L. Blanko menggunakan air. • Metode spektrofotometri pada panjang gelombang 530 nm. • Penetapan kadar dihitung melalui kurva baku 17

<121> Penetapan Kadar Kalsium Pantotenat • Dilakukan menggunakan bakteri uji Lactobacillus plantarum dengan metode turbidimetri • Pembanding larutan baku Kalsium pantotenat BPFI berkisar antara 0, 01 – 0, 04 µg per m. L. Blanko menggunakan air. • Metode spektrofotometri pada panjang gelombang 660 nm. • Penetapan kadar dihitung melalui kurva baku 18

<131> Penetapan Potensi Antibiotik secara Mikrobiologi • Aktivitas (potensi) suatu antibiotik dapat ditunjukkan pada kondisi sesuai dengan efek daya hambatnya terhadap mikroba uji • Perbedaan kadar dan potensi • Dua metode umum : cara lempeng dan cara tabung • Cara lempeng : menggunakan kertas cakram atau selinder baja, efek difusi antibiotik pada medium agar. • Cara tabung : turbidimetri, efek larutan antibiotik terhadap turbiditas mikroba 19
- Slides: 19