STANDAR KOMPETENSI 3 Memahami kinetika reaksi kesetimbangan kimia

STANDAR KOMPETENSI: 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang mempengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri. KOMPETENSI DASAR 3. 2. Memahami teori tumbukan (tabrakan) untuk menjelaskan faktor-faktor penentu laju dan orde reaksi serta terapannya dalam kehidupan sehari-hari. By Farid Qim Iya szazza 1

Indikator : 1) menentukan orde / tingkat reaksi zat 2) Menentukan persamaan laju reaksi 3) Menentukan nilai tetapan laju reaksi Indikator Tambahan (pengayaan) 1) Menentukan laju sesaat ( laju saat waktu tertentu) jika diketahui persamaan laju reaksinya By Farid Qim Iya szazza 2

HUKUM LAJU REAKSI / PERSAMAAN LAJU REAKSI Hukum laju reaksi atau persamaan laju reaksi menyatakan hubungan antara konsentrasi dan laju reaksi. Reaksi : a. A + b. B c. C + d. D Persamaan laju reaksi adalah V = k [A]m [B]n Persamaan laju reaksi menunjukkan laju awal reaksi V (velocity) = laju reaksi k = tetapan laju reaksi m = orde atau tingkat reaksi [A] n = orde atau tingkat reaksi [B] Orde reaksi adalah banyaknya faktor konsentrasi zat reaktan yang mempengaruhi kecepatan reaksi. By Farid Qim Iya szazza 3

Konsentrasi Orde Reaksi Pangkat perubahan konsentrasi terhadap perubahan laju disebut orde reaksi Ada reaksi berorde O, dimana tidak terjadi perubahan laju reaksi berapapun perubahan konsentrasi pereaksi. Ada reaksi berorde 1, dimana perubahan konsentrasi pereaksi 2 kali menyebabkan laju reaksi lebih cepat 2 kali. Ada reaksi berorde 2, dimana laju perubahan konsentrasi pereaksi 2 kali menyebabkan laju reaksi lebih cepat 4 kali, dst. By Farid Qim Iya szazza 4

Konsentrasi Grafik hubungan perubahan konsentrasi terhadap laju reaksi Reaksi Orde 1 Reaksi Orde 2 Laju reaksi Reaksi Orde 0 Konsentrasi By Farid Qim Iya szazza 5

Konsentrasi Grafik hubungan perubahan konsentrasi terhadap laju reaksi Reaksi Orde 1 Reaksi Orde 2 Laju reaksi Reaksi Orde 0 Konsentrasi By Farid Qim Iya szazza 6
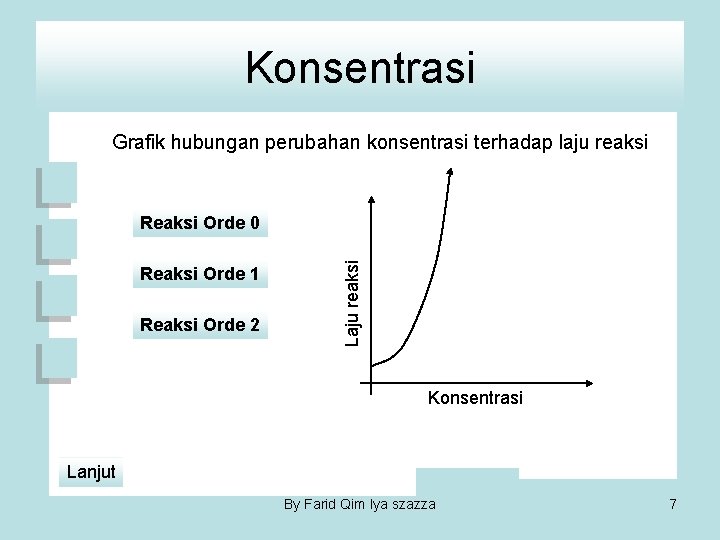
Konsentrasi Grafik hubungan perubahan konsentrasi terhadap laju reaksi Reaksi Orde 1 Reaksi Orde 2 Laju reaksi Reaksi Orde 0 Konsentrasi Lanjut By Farid Qim Iya szazza 7

Konsentrasi Untuk reaksi A + B C Rumusan laju reaksi adalah : V =k. [A]m. [B]n Dimana : k = tetapan laju reaksi Orde reakasi total = m + n m = orde reaksi untuk A n = orde reaksi untuk B By Farid Qim Iya szazza 8

Konsentrasi Rumusan laju reaksi tersebut diperoleh dari percobaan. Misalkan diperoleh data percobaan untuk reaksi : NO(g) + Cl 2(g) NOCl 2(g) Diperoleh data sebagai berikut : Perc [NO] M [Cl 2] M V M/s 1 2 3 4 0, 1 0, 2 0, 3 0, 1 0, 2 0, 1 0, 3 4 16 8 X Maka nilai X adalah ? By Farid Qim Iya szazza 9

langkah penyelesaian: 1. Menentukan persamaan umum laju reaksi berdasar persamaan reaksinya. 2. Menentukan orde reaksi zat NO dan Cl 2 3. Membandingan data percobaan 4 dengan 1 atau percobaan 4 dengan 2 atau percobaan 4 dengan 3 1. Persamaan umum laju reaksi v = k [NO]m [Cl 2]n 2. Menentukan orde m pilih [Cl 2] yang sama , berarti konsentrasi zat Cl 2 tidak mempengaruhi laju reaksi data 1 dan 3 By Farid Qim Iya szazza 10
![Persamaan umum laju reaksi v = k [NO]m [Cl 2]n Menentukan orde m [NO] Persamaan umum laju reaksi v = k [NO]m [Cl 2]n Menentukan orde m [NO]](http://slidetodoc.com/presentation_image/4139ba658dfec3d82a591e293ad30dfd/image-11.jpg)
Persamaan umum laju reaksi v = k [NO]m [Cl 2]n Menentukan orde m [NO] pilih [Cl 2] yang sama , berarti konsentrasi zat Cl 2 tidak mempengaruhi laju reaksi data 1 dan 3 By Farid Qim Iya szazza 11
![Menentukan orde zat Cl 2 pilih [NO] yang sama (berarti konsentrasi zat NO tidak Menentukan orde zat Cl 2 pilih [NO] yang sama (berarti konsentrasi zat NO tidak](http://slidetodoc.com/presentation_image/4139ba658dfec3d82a591e293ad30dfd/image-12.jpg)
Menentukan orde zat Cl 2 pilih [NO] yang sama (berarti konsentrasi zat NO tidak mempengaruhi laju reaksi) pilih data 1 dan 2 By Farid Qim Iya szazza 12
![Sehingga persamaan laju reaksinya : v = k[NO]. [Cl 2]2 Untuk mencari laju percobaan Sehingga persamaan laju reaksinya : v = k[NO]. [Cl 2]2 Untuk mencari laju percobaan](http://slidetodoc.com/presentation_image/4139ba658dfec3d82a591e293ad30dfd/image-13.jpg)
Sehingga persamaan laju reaksinya : v = k[NO]. [Cl 2]2 Untuk mencari laju percobaan 4 dapat dengan cara menghitung nilai k lebih dahulu atau dengan membandingkan data 4 dengan 1 atau membandingkan data 4 dengan 2 atau membandingkan data 4 dengan 3. Misal dengan membandingkan data 4 dengan 1 By Farid Qim Iya szazza 13

Atau dengan menghitung nilai k terlebih dahulu, dapat menggunakan salah satu nomor data percobaan. Misal menggunakan data percobaan 1 v = k[NO]1. [Cl 2]12 4 = k [0, 1]2 4 = k. 0, 001 k = 4000 Mencari satuan k : satuan v = M/s , satuan konsentrasi =M By Farid Qim Iya szazza 14

Setelah nilai k didapat kemudian masukkan data percobaan 4, sehingga nilai laju reaksi percobaan 4 dapat diketahui v = 4000[NO]4. [Cl 2]42 v = 4000. [0, 3]2 = 4000. 0, 027 = 108 M/s By Farid Qim Iya szazza 15
![Rumusan laju reaksi untuk reaksi tersebut adalah : V = k. [NO]m. [Cl 2]n Rumusan laju reaksi untuk reaksi tersebut adalah : V = k. [NO]m. [Cl 2]n](http://slidetodoc.com/presentation_image/4139ba658dfec3d82a591e293ad30dfd/image-16.jpg)
Rumusan laju reaksi untuk reaksi tersebut adalah : V = k. [NO]m. [Cl 2]n Orde NO = m Percobaan 1 dan 3 Orde Cl 2 = n Percobaan 1 dan 2 By Farid Qim Iya szazza 16
![Konsentrasi Maka rumusan laju reaksinya adalah : V=k. [NO]1. [Cl 2]2 Harga k diperoleh Konsentrasi Maka rumusan laju reaksinya adalah : V=k. [NO]1. [Cl 2]2 Harga k diperoleh](http://slidetodoc.com/presentation_image/4139ba658dfec3d82a591e293ad30dfd/image-17.jpg)
Konsentrasi Maka rumusan laju reaksinya adalah : V=k. [NO]1. [Cl 2]2 Harga k diperoleh dengan memasukan salah satu data percobaan, misal menggunakan data 1 By Farid Qim Iya szazza 17
![Konsentrasi Maka laju reaksi pada percobaan 4 adalah : V= k. [NO]. [Cl 2]2 Konsentrasi Maka laju reaksi pada percobaan 4 adalah : V= k. [NO]. [Cl 2]2](http://slidetodoc.com/presentation_image/4139ba658dfec3d82a591e293ad30dfd/image-18.jpg)
Konsentrasi Maka laju reaksi pada percobaan 4 adalah : V= k. [NO]. [Cl 2]2 V= 4. 103. [0, 3]2 V= 108 Ms-1 By Farid Qim Iya szazza 18

Suatu reaksi 2 A + 2 B C + 2 D, diperoleh data percobaan sebagai berikut. No Percobaan 1 2 3 [ A ] M [ B ] M (M/s) 2 4 6 3 3 6 5 20 90 Tentukan : [a] orde reaksi terhadap A [b] orde reaksi terhadap B [c] nilai konstanta reaksi ( k ), dan satuan k [d] persamaan laju reaksinya [e] nilai jika [ A ] = 1 M dan [ B ] = 1. 5 M By Farid Qim Iya szazza 19

Bila diketahui data untuk reaksi : A + B AB adalah sebagai berikut : [A], M [B], M r, Mdet-1 0, 3 0, 2 0, 05 0, 10 0, 20 2 36 32 Tentukan orde zat A Tentukan orde zat B Tentukan nilai K dan satuan K Tuliskan persamaan laju reaksinya Hitung laju reaksi ketika [A] = 0, 5 M dan [B] = 0, 5 M By Farid Qim Iya szazza 20

Evaluasi 1 2 3 Diketahui reaksi A + B + C D. Jika persamaan laju reaksi tersebut v = k. [B]2. [C]1, berapa kali perubahan laju reaksinya bila konsentrasi masing-masing komponen pereaksi diperbesar 2 kali semula? 4 5 By Farid Qim Iya szazza 21

Satuan V selalu = M/s Satuan K ditentukan oleh orde reaksi total 1. Tentukan satuan k untuk reaksi : a. Reaksi berorde total 1 persamaan laju v = k[A] atau v=k[A] [B]o a. Berorde 4 2. Tentukan orde reaksi total jika -1/2. S-1 a. satuan k = mol 1/2. �� 1/2. S-1 b. satuan k = mol-1/2. �� By Farid Qim Iya szazza 22

Satuan V selalu = M/s Satuan K ditentukan oleh orde reaksi total 2. Tentukan orde reaksi total jika -1/2. S-1 a. satuan k = mol 1/2. �� 1/2. S-1 b. satuan k = mol-1/2. �� By Farid Qim Iya szazza 23
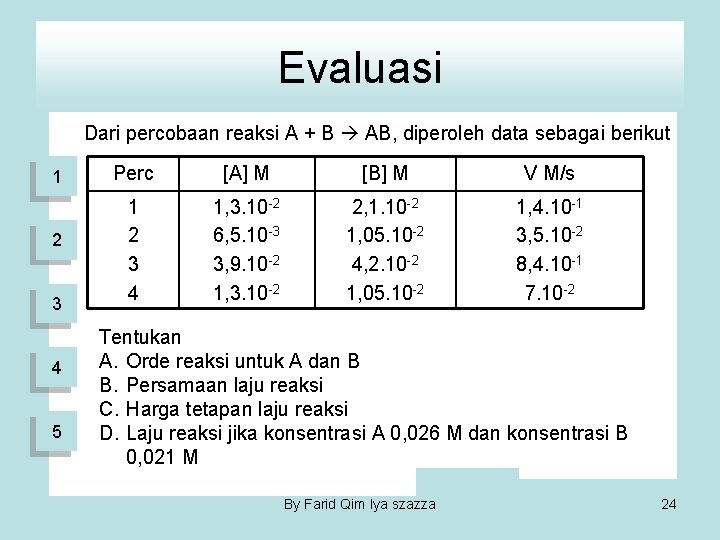
Evaluasi Dari percobaan reaksi A + B AB, diperoleh data sebagai berikut 1 2 3 4 5 Perc [A] M [B] M V M/s 1 2 3 4 1, 3. 10 -2 6, 5. 10 -3 3, 9. 10 -2 1, 3. 10 -2 2, 1. 10 -2 1, 05. 10 -2 4, 2. 10 -2 1, 05. 10 -2 1, 4. 10 -1 3, 5. 10 -2 8, 4. 10 -1 7. 10 -2 Tentukan A. Orde reaksi untuk A dan B B. Persamaan laju reaksi C. Harga tetapan laju reaksi D. Laju reaksi jika konsentrasi A 0, 026 M dan konsentrasi B 0, 021 M By Farid Qim Iya szazza 24
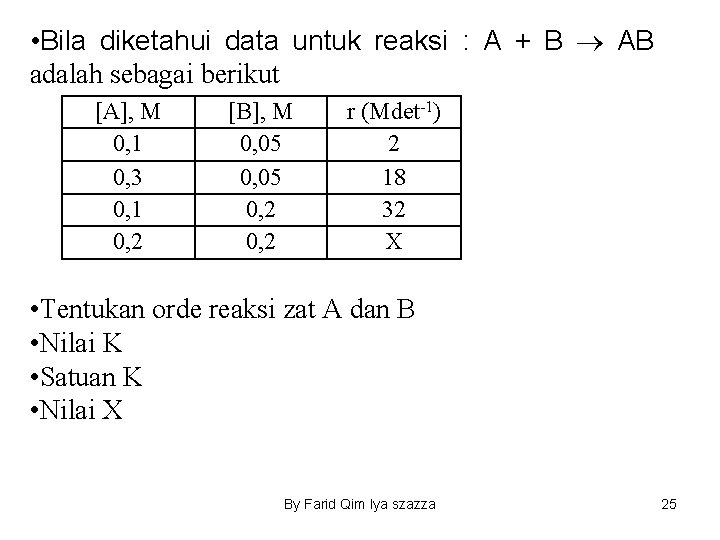
• Bila diketahui data untuk reaksi : A + B AB adalah sebagai berikut [A], M 0, 1 0, 3 0, 1 0, 2 [B], M 0, 05 0, 2 r (Mdet-1) 2 18 32 X • Tentukan orde reaksi zat A dan B • Nilai K • Satuan K • Nilai X By Farid Qim Iya szazza 25

• Suatu reaksi X + Y XY diperoleh data sebagai berikut : No [X] M [Y] M 1 0, 05 Waktu (detik) 12 2 0, 1 0, 2 3 3 0, 05 4 Tentukan a. Orde zat X b. Orde zat Y c. Persamaan laju reaksi d. satuan K dalam reaksi tersebut adalah : Nilai K tidak dapat ditentukan karena data yang ada By Farid Qim Iya szazza 26 waktu bukan laju reaksi
![Waktu (detik) V ≈ 1 / waktu No [X] M [Y] M 1 0, Waktu (detik) V ≈ 1 / waktu No [X] M [Y] M 1 0,](http://slidetodoc.com/presentation_image/4139ba658dfec3d82a591e293ad30dfd/image-27.jpg)
Waktu (detik) V ≈ 1 / waktu No [X] M [Y] M 1 0, 05 12 1 / 12 2 0, 1 0, 2 3 1/3 3 0, 05 4 1/4 Laju reaksi berbanding terbalik dengan waktu Satuan V = Molar / waktu V ≈ 1 / waktu By Farid Qim Iya szazza 27

1. Bila dalam wadah bervolum 1 dm 3 dicampurkan masing 3 mol gas-gas NO dan Cl 2 sehingga bereaksi menjadi gas NOCl, dan diketahui bahwa orde reaksi untuk NO adalah dua dan Cl 2 adalah satu, serta tetapan laju reaksi adalah 0, 4 M-2 det-1, maka setelah 30% gas NO bereaksi akan memiliki laju reaksi sebesar . . Mdet-1. 2. Persamaan laju reaksi untuk P + 2 Q R adalah v = k[P][Q]2. Jika konsentrasi P dan Q semula masing 1 molar, maka pada saat konsentrasi P tinggal ¾ molar laju reaksinya adalah . . . M/ By Farid Qim Iya szazza 28

1. Bila dalam wadah bervolum 1 dm 3 dicampurkan masing 3 mol gas-gas NO dan Cl 2 sehingga bereaksi menjadi gas NOCl, dan diketahui bahwa orde reaksi untuk NO adalah dua dan Cl 2 adalah satu, serta tetapan laju reaksi adalah 0, 4 M-2 det-1, maka setelah (saat) 30% gas NO bereaksi akan memiliki laju reaksi sebesar . . Mdet-1. (v = 4, 4982 M/s) Laju reaksi selalu ditentukan dari konsentrasi pereaksi yang masih ada (yang tinggal) Laju reaksi dalam soal sperti tersebut menunjukkan laju reaksi saat itu (laju sesaat) Penjelasan : Jika saat NO yang bereaksi 100% maka NO yang tinggal = 0 Atau setelah Cl 2 yang bereaksi 50 % maka NO yang tiggal = 0 By Farid Qim Iya szazza 29 berarti reaksi telah berhenti

1. Bila dalam wadah bervolum 1 dm 3 dicampurkan masing 3 mol gas-gas NO dan Cl 2 sehingga bereaksi menjadi gas NOCl, dan diketahui bahwa orde reaksi untuk NO adalah dua dan Cl 2 adalah satu, serta tetapan laju reaksi adalah 0, 4 M-2 det-1, maka setelah (saat) 30% gas NO bereaksi akan memiliki laju reaksi sebesar . . Mdet-1. 2 NO + Cl 2 2 NOCl m 3 mol b 30% x 3 0, 9 0, 45 s 2, 1 2, 55 Molaritas NO yang ada 2, 1 mol / 1 liter = 2, 1 M Molaritas Cl 2 yang ada 2, 55 mol / 1 liter = 2, 55 M Maka : V = 0, 4 [NO]2 [Cl 2] V = 4, 4. [2, 1]. [2, 55] = 4, 4982 M/s By Farid Qim Iya szazza 30

Bila dalam wadah bervolum 1 dm 3 dicampurkan masing 3 M gas-gas NO dan Cl 2 sehingga bereaksi menjadi gas NOCl, dan diketahui bahwa orde reaksi untuk NO adalah dua dan Cl 2 adalah satu, serta tetapan laju reaksi adalah 0, 4 M-2 det-1, maka saat 100% gas NO bereaksi akan memiliki laju reaksi sebesar . . Mdet-1. 2 NO + Cl 2 2 NOCl m 3 M b 100% x 3 1, 5 s 0 1, 5 Saat gas NO yang bereaksi 100% berarti gas NO sudah habis maka reaksi sudah berhenti. maka V = 0, 4 [0]2 [Cl 2] V = 0 By Farid Qim Iya szazza 31

5. Diketahui reaksi : 2 P + 3 Q P 2 Q 3 , Mula-mula terdapat P sebanyak 1, 25 M. Setelah 250 detik ternyata P tinggal 0, 50 M, maka : a. Laju berkurangnya zat Q adalah. . M / detik b. Laju pembentukan zat P 2 Q 3 adalah . . M / detik. By Farid Qim Iya szazza 32

5. Diketahui reaksi : 2 P + 3 Q P 2 Q 3 , Mula-mula terdapat P sebanyak 1, 25 M. Setelah 250 detik ternyata P tinggal 0, 50 M, maka : a. Laju berkurangnya zat Q adalah. . M / detik b. Laju pembentukan zat P 2 Q 3 adalah . . M / detik. 2 P + 3 Q P 2 Q 3 m 1, 25 M b 0, 75 M 3/2 x 0, 75 ½ x 0, 75 1, 125 M 0, 375 M s 0, 50 M VQ = 1, 125 M / 250 dt VP 2 Q 3 = 0, 375 M / 250 dt By Farid Qim Iya szazza 33

By Farid Qim Iya szazza 34

By Farid Qim Iya szazza 35

By Farid Qim Iya szazza 36
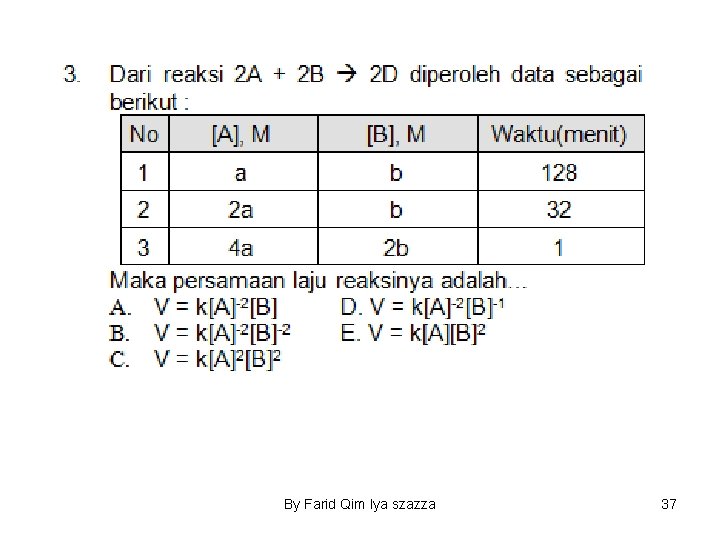
By Farid Qim Iya szazza 37
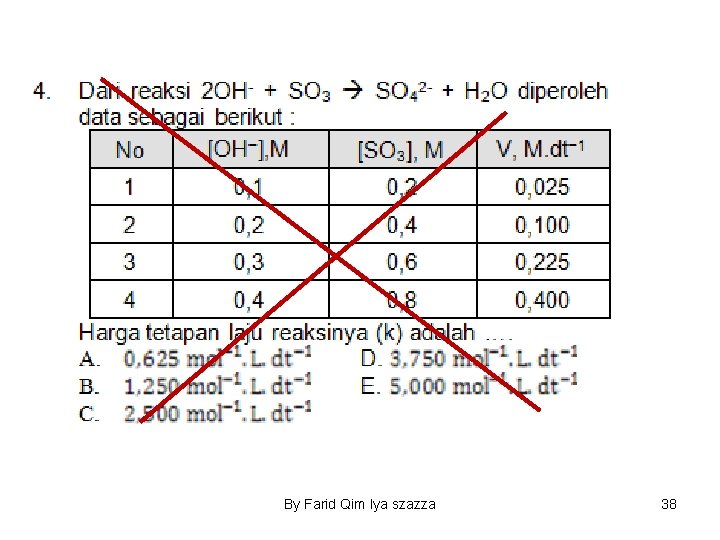
By Farid Qim Iya szazza 38
- Slides: 38