Stabiln izotopy Izotopy Stejn atomov slo rzn hmotov

Stabilní izotopy
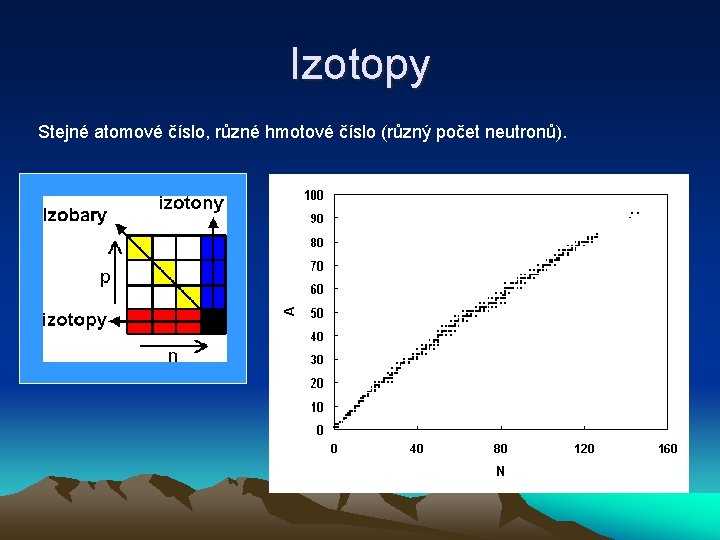
Izotopy Stejné atomové číslo, různé hmotové číslo (různý počet neutronů).
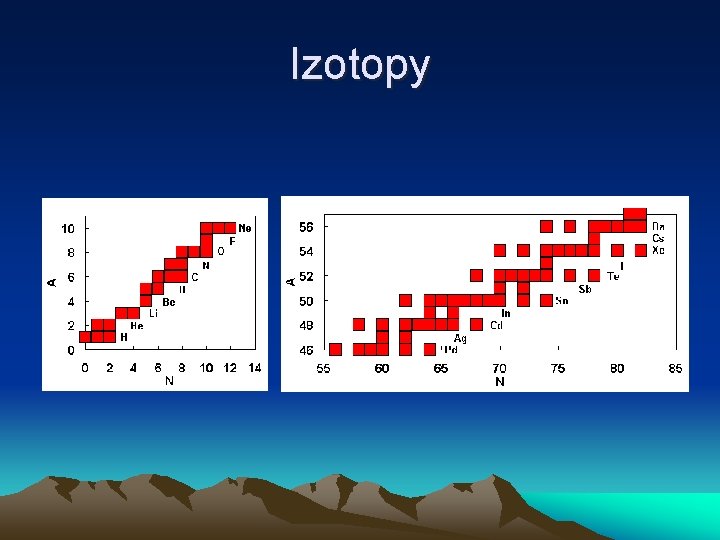
Izotopy

Vlastnosti důležité pro využití (fyzikální) • • • nízká hmotnost relativně velký rozdíl hmotnosti mezi izotopy vysoký stupeň kovalentní vazby více oxidačních stavů relativně vysoká koncentrace méně zastoupeného izotopu (nejméně desetiny %)
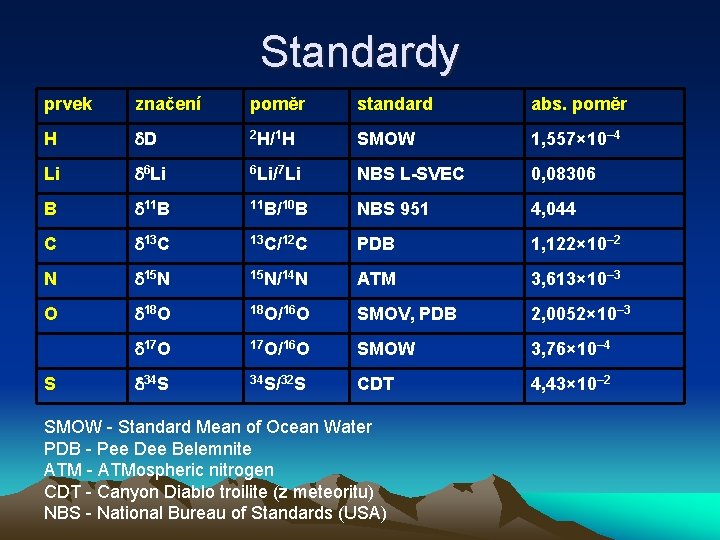
Standardy prvek značení poměr standard abs. poměr H D 2 H/1 H SMOW 1, 557× 10– 4 Li 6 Li/7 Li NBS L-SVEC 0, 08306 B 11 B/10 B NBS 951 4, 044 C 13 C/12 C PDB 1, 122× 10– 2 N 15 N/14 N ATM 3, 613× 10– 3 O 18 O/16 O SMOV, PDB 2, 0052× 10– 3 17 O/16 O SMOW 3, 76× 10– 4 34 S/32 S CDT 4, 43× 10– 2 S SMOW - Standard Mean of Ocean Water PDB - Pee Dee Belemnite ATM - ATMospheric nitrogen CDT - Canyon Diablo troilite (z meteoritu) NBS - National Bureau of Standards (USA)

Frakcionace izotopů - vyjádření frakcionace vyjádřená jako (‰) 18 O = { [(18 O/16 O)vz – (18 O/16 O)SMOW] / (18 O/16 O)SMOW} × 103 koeficient frakcionace A-B = RA/RB A-B = A – B = 103 ln frakcionace – translační, rotační a vibrační pohyb 1/2 C 16 O 2 + H 218 O 1/2 C 18 O 2 + H 216 O K = 1, 04 (25°C)
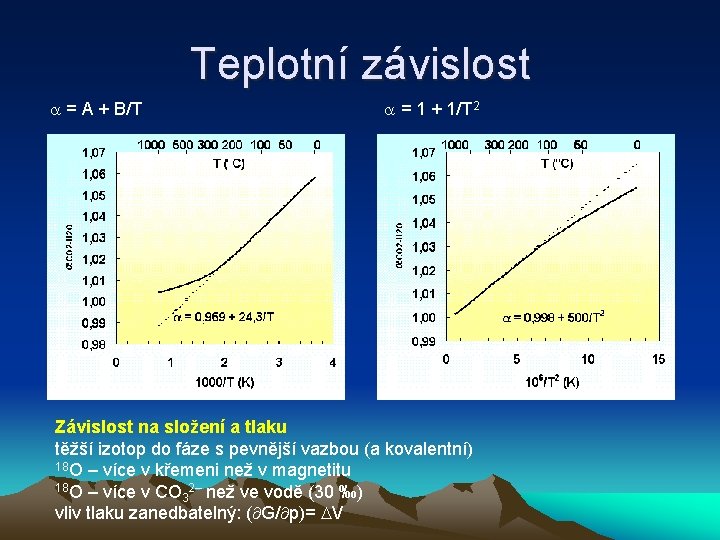
Teplotní závislost = A + B/T = 1 + 1/T 2 Závislost na složení a tlaku těžší izotop do fáze s pevnější vazbou (a kovalentní) 18 O – více v křemeni než v magnetitu 18 O – více v CO 2– než ve vodě (30 ‰) 3 vliv tlaku zanedbatelný: ( G/ p)= V

Kinetika difuze, odpařování pokud není dosaženo rovnováhy v reakci, reakční produkty nabohaceny lehčím izotopem (fotosyntéza, bakteriální redukce) Frakcionace A H 216 O, B H 218 O d. A = k. AA, d. B = k. BB koeficient frakcionace: = k. B / k. A po integraci: ln B/B°= ln A/A° B/B°= (A/A°) (B/A) /(B°/A°) = f – 1 [(B/A) – (B°/A°)]/(B°/A°) = f – 1– 1 = 1000(f – 1– 1) kde je rozdíl původního izotopického složení a izotopického složení po tom, kdy zkondenzovala (vykrystalizovala) část f

Frakcionace Izotopické složení zbývající páry po kondenzaci (f – 1) množství vody ve srovnání s původním izotopickým složením páry. Znázorněna je nerovnovážná a rovnovážná kondenzace.
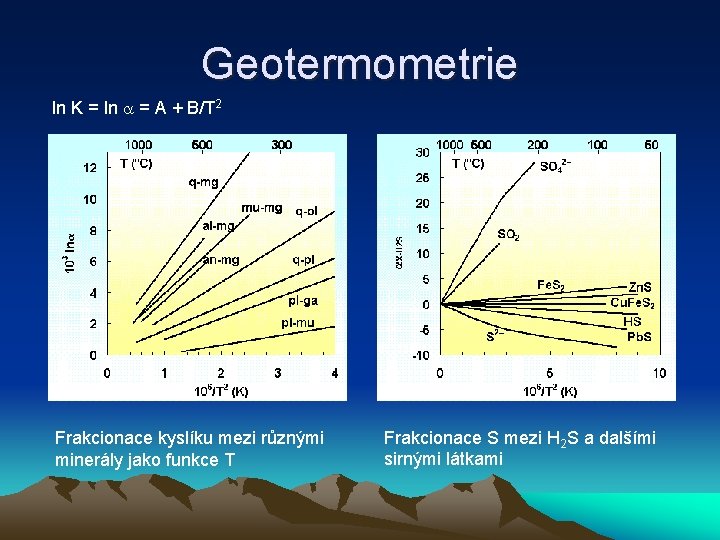
Geotermometrie ln K = ln = A + B/T 2 Frakcionace kyslíku mezi různými minerály jako funkce T Frakcionace S mezi H 2 S a dalšími sirnými látkami
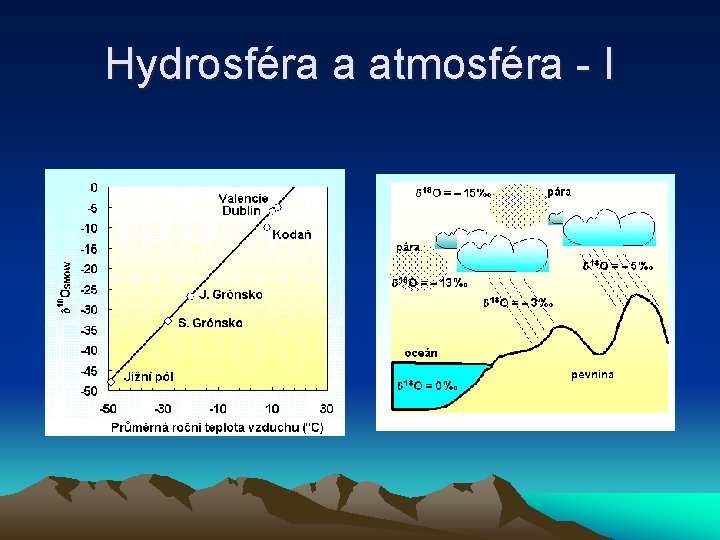
Hydrosféra a atmosféra - I
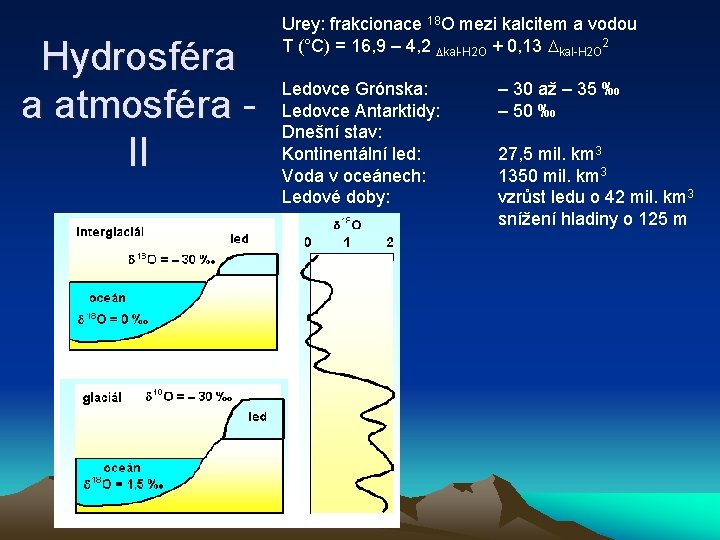
Hydrosféra a atmosféra II Urey: frakcionace 18 O mezi kalcitem a vodou T (°C) = 16, 9 – 4, 2 kal-H 2 O + 0, 13 kal-H 2 O 2 Ledovce Grónska: Ledovce Antarktidy: Dnešní stav: Kontinentální led: Voda v oceánech: Ledové doby: – 30 až – 35 ‰ – 50 ‰ 27, 5 mil. km 3 1350 mil. km 3 vzrůst ledu o 42 mil. km 3 snížení hladiny o 125 m
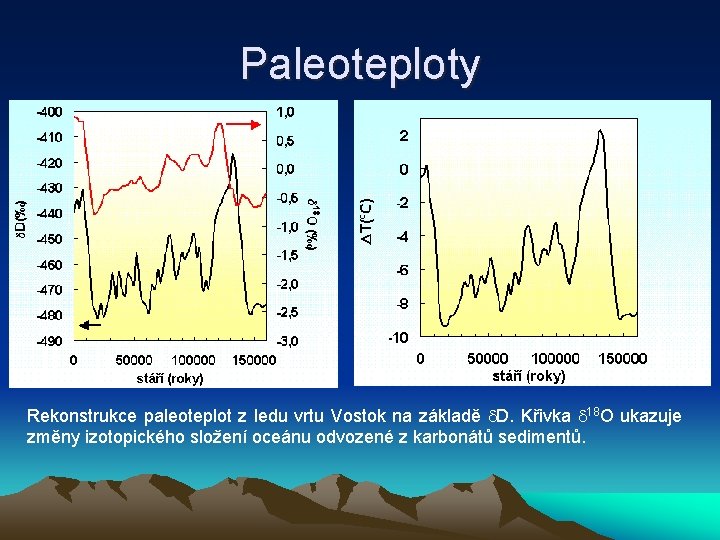
Paleoteploty Rekonstrukce paleoteplot z ledu vrtu Vostok na základě D. Křivka 18 O ukazuje změny izotopického složení oceánu odvozené z karbonátů sedimentů.
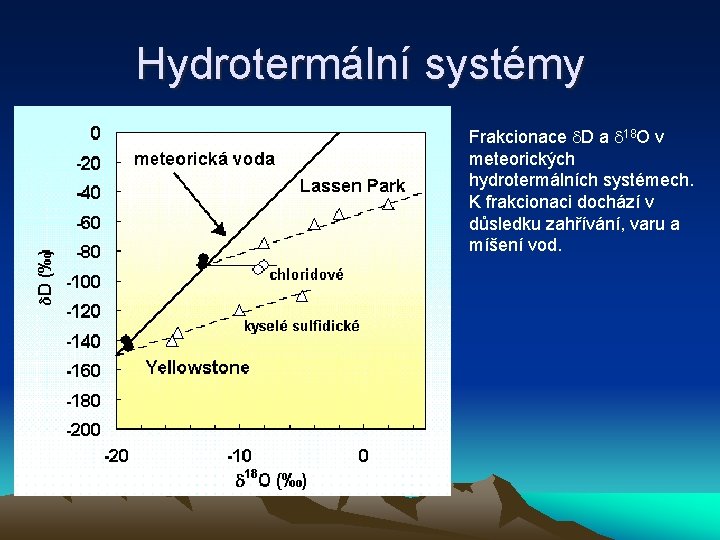
Hydrotermální systémy Frakcionace D a 18 O v meteorických hydrotermálních systémech. K frakcionaci dochází v důsledku zahřívání, varu a míšení vod.
![Krystalizace magmatu Frakční krystalizace Rl / Ro = 1/ [f + (1 -f)] = Krystalizace magmatu Frakční krystalizace Rl / Ro = 1/ [f + (1 -f)] =](http://slidetodoc.com/presentation_image_h2/aa573a487564bb5944fc746041837ed3/image-15.jpg)
Krystalizace magmatu Frakční krystalizace Rl / Ro = 1/ [f + (1 -f)] = Rs / Rl = tav – o = [Rl/Ro – 1] × 1000 = 1000 (f – 1) frakční krystalizace: pro kyslík velmi blízké 1 Frakční krystalizace a asimilace (AFC) l – o = [ ( a – o) + ×R] (1 – f(1/(R– 1)) l – magma o - původní magma, a - asimilovaný materiál, = l – kryst R - poměr mezi krystalizovaným a asimilovaným materiálem
- Slides: 15