SS 2002 Experimentalvortrag Wasserstoffperoxid 19 06 02 Gliederung























- Slides: 36

SS 2002 Experimentalvortrag Wasserstoffperoxid 19. 06. 02

Gliederung 1. Allgemeine Eigenschaften 2. Vorkommen 3. Physiologische Wirkung 4. Historie 5. Darstellung 6. Verwendung

1. Allgemeine Eigenschaften • Summenformel H 2 O 2 • farb- und geruchlose Flüssigkeit • im wasserfreiem Zustand: sirupartig • mit Wasser in allen Mengenverhältnissen mischbar • 30%iges H 2 O 2 kommt als „Perhydrol“ in den Handel • sehr schwache Säure H 2 O 2 (aq) + H 2 O HO 2 - (aq) + H 3 O+ (aq)

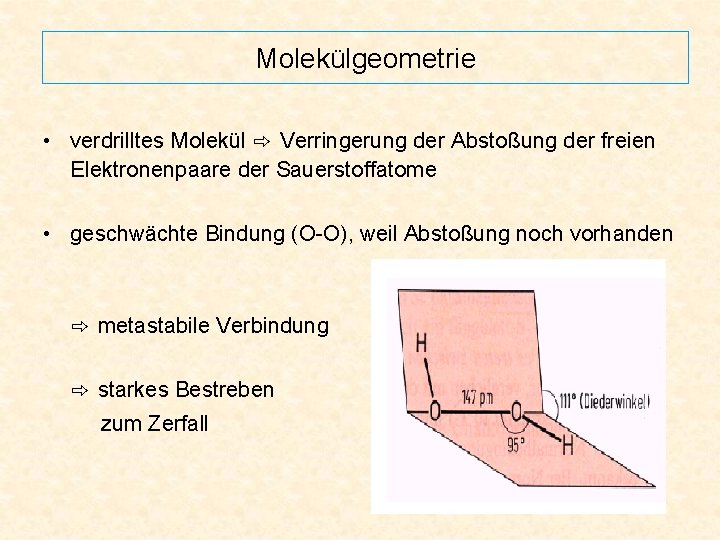
Molekülgeometrie • verdrilltes Molekül ⇨ Verringerung der Abstoßung der freien Elektronenpaare der Sauerstoffatome • geschwächte Bindung (O-O), weil Abstoßung noch vorhanden ⇨ metastabile Verbindung ⇨ starkes Bestreben zum Zerfall

Allgemeine Eigenschaften • hohes Zerfallsbestreben unter großer Wärmeentwicklung: -1 -2 0 2 H 2 O 2 (aq) → 2 H 2 O + O 2 (g) ↑ ∆H° = - 98 k. J/mol • Zerfall wird initiiert durch Bildung von OH-Radikalen: HOOH → 2 HO∙ ∆H° = 211 k. J/mol HO∙ + H 2 O 2 → H 2 O + HO 2∙ + H 2 O 2 → H 2 O + O 2 + HO∙ • jedoch sehr langsam bei Zimmertemperatur

Allgemeine Eigenschaften • Erhöhung der Zersetzungsgeschwindigkeit durch Katalysatoren (z. B. Schwermetalle, Alkalien oder andere Verunreinigungen) ⇨ Versuch 1 • Deshalb: Zugabe geringer Mengen (ca. 100 - 1000 ppm) an Stabilisatoren z. B. Chelatbildner, Stannate oder Phosphate, die Metallionen komplexieren

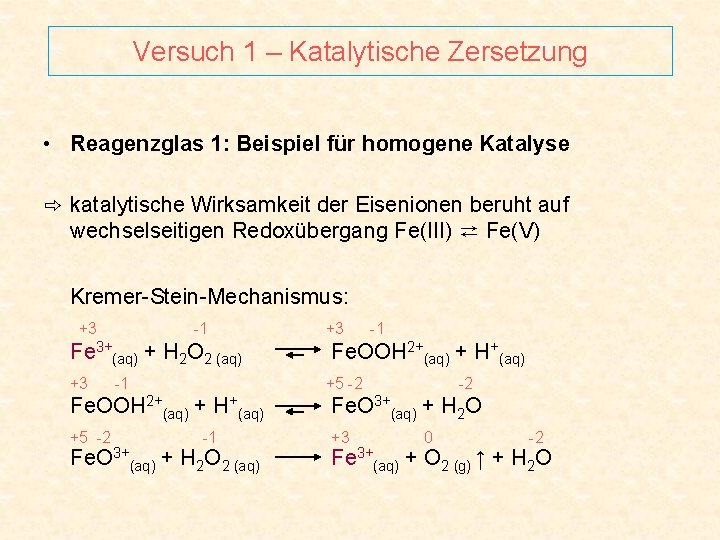
Versuch 1 – Katalytische Zersetzung • Reagenzglas 1: Beispiel für homogene Katalyse ⇨ katalytische Wirksamkeit der Eisenionen beruht auf wechselseitigen Redoxübergang Fe(III) ⇄ Fe(V) Kremer-Stein-Mechanismus: +3 -1 Fe 3+(aq) + H 2 O 2 (aq) +3 -1 Fe. OOH 2+(aq) + H+(aq) +5 -2 -2 Fe. OOH 2+(aq) + H+(aq) Fe. O 3+(aq) + H 2 O +5 -2 +3 -1 Fe. O 3+(aq) + H 2 O 2 (aq) 0 -2 Fe 3+(aq) + O 2 (g) ↑ + H 2 O

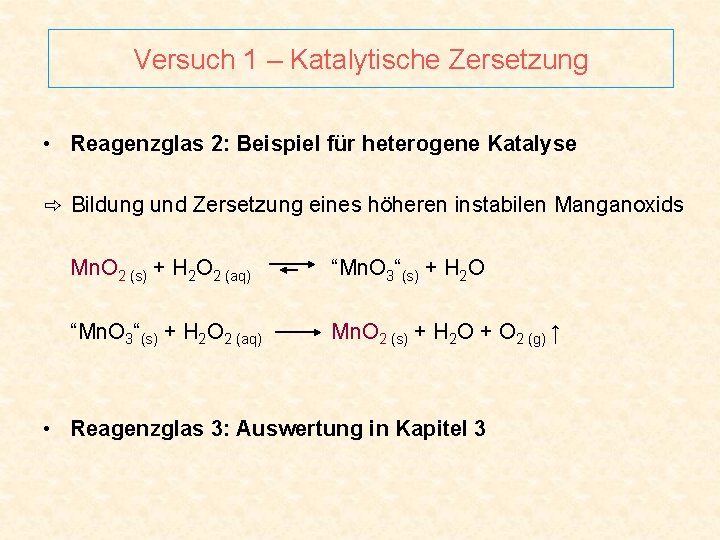
Versuch 1 – Katalytische Zersetzung • Reagenzglas 2: Beispiel für heterogene Katalyse ⇨ Bildung und Zersetzung eines höheren instabilen Manganoxids Mn. O 2 (s) + H 2 O 2 (aq) “Mn. O 3“(s) + H 2 O 2 (aq) Mn. O 2 (s) + H 2 O + O 2 (g) ↑ • Reagenzglas 3: Auswertung in Kapitel 3

2. Vorkommen In sehr niedrigen Konzentrationen natürlich vorkommende Substanz: • im Wasser (1 – 30 μg/L) • in der Atmosphäre (0, 1 – 1 ppm) • in allen aerob lebenden Zellen (z. B. menschliche Atemluft 300 - 1000 μg/m 3) • Kuriosität: Bombardierkäfer (Brachinus crepitans / Brachinus explodens)

Bombardierkäfer • Käfer produziert mit seinen Drüsen Hydrochinon und Wasserstoffperoxid (bis zu einer Konzentration von 28, 5 %) • Substanzen dienen als Abwehrstoffe gegen Freßfeinde

3. Physiologische Wirkung Wie kommt H 2 O 2 in den Organismus? • Endreaktion der Atmungskette ⇨ aus Sauerstoff kann das toxische Superoxid-Ion O 2 - gebildet werden: 2 O 2 -(aq) + 2 H+(aq) Superoxid. Dismutase H 2 O 2 (aq) + O 2 (g) Folgen? • in höheren Konzentrationen: Zellgift Deshalb: Schutzmechanismen, in Form von H 2 O 2 -zersetzenden Enzymen (Katalase / H 2 O 2 -Oxidoreduktase) ⇨ Versuch 2

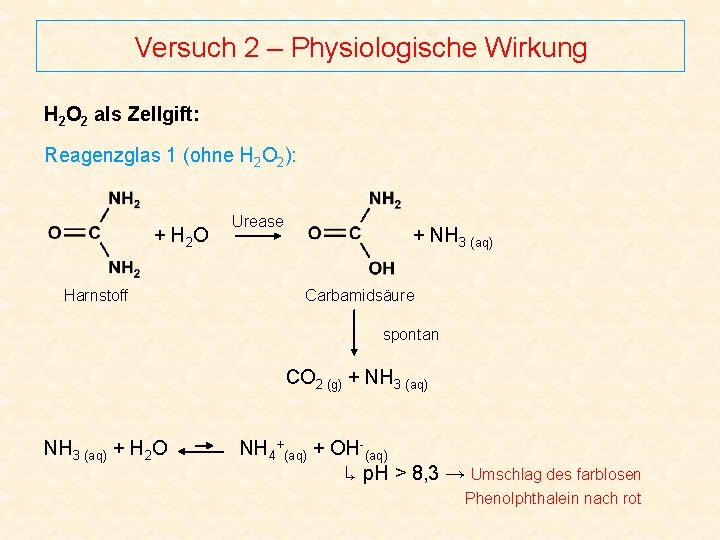
Versuch 2 – Physiologische Wirkung H 2 O 2 als Zellgift: Reagenzglas 1 (ohne H 2 O 2): + H 2 O Harnstoff Urease + NH 3 (aq) Carbamidsäure spontan CO 2 (g) + NH 3 (aq) + H 2 O NH 4+(aq) + OH-(aq) ↳ p. H > 8, 3 → Umschlag des farblosen Phenolphthalein nach rot

Versuch 2 – Physiologische Wirkung Reagenzglas 2 (mit H 2 O 2): Urease wird durch H 2 O 2 irreversibel geschädigt, deshalb kein Umschlag des farblosen Phenolphthaleins + H 2 O

Physiologische Wirkung Schutzmechanismen: Reagenzglas 3 (von Versuch 1): Katalysator im Blut ist das Enzym Katalase, welches in der Lage ist H 2 O 2 sehr schnell zu zersetzen Katalase: ∙ eines der effektivsten Enzyme (ein Katalasemolekül zerlegt in einer Sekunde 3· 1011 H 2 O 2 -Moleküle) ∙ enthält 4 Hämgruppen mit Fe(III) ∙ Hauptaufgabe ist Zerstörung des Zellgifts H 2 O 2

4. Historie • 1818 erstmalige Darstellung durch Thenard mit Bariumperoxid als Ausgangssubstanz ⇨Versuch 3

Versuch 3 a – Darstellung Reaktion ist mit einem Fällungsvorgang und einer Säure-Base-Reaktion nach Brønsted verknüpft: Ba. O 2 (s) + H 2 SO 4 (aq) Ba. SO 4 (s) ↓ + H 2 O 2 (aq) O 22 -(aq) + 2 H 3 O+(aq) H 2 O 2 (aq) + 2 H 2 O weiß Abstumpfen des Reaktionsmilieus: Ba. CO 3 (s) + 2 H 3 O+(aq) + SO 42 -(aq) Ba. SO 4 (s) ↓ + CO 2 (g) ↑ + 3 H 2 O weiß

Versuch 3 b – Nachweis mit Titanoxidsulfat Reaktion ist mit einer Ligandenaustauschreaktion verknüpft: formal: -2 -1 [Ti. O]SO 4 (aq) + H 2 O 2 (aq) H 3 O + -1 -1 -2 [Ti. O-O]SO 4 (aq) + H 2 O gelb genauer: -2 -1 [Ti(OH)2(H 2 O)4]2+(aq) + H 2 O 2 (aq) -1 -2 [Ti(O 2) · aq]2+(aq) + 6 H 2 O gelb

Historie • 1818 erstmalige Darstellung durch Thenard mit Bariumperoxid als Ausgangssubstanz • bleichende und desinfizierende Wirkung wurde erkannt • 1873 erste Anlage zur fabrikmäßigen Herstellung von 3%igen H 2 O 2 aus Ba. O 2 bei Schering in Berlin • 1896 technische Produktion von 3 -8%igen H 2 O 2 bei Merck in Darmstadt • 1905 industrieller Durchbruch mit einem Deutschen Reichspatent zur Herstellung auf elektrolytischem Weg über die Peroxodischwefelsäure (ca. 28%ige Lösungen) • 1953 erste großtechnische Anthrachinon-Autoxidations-Anlage in Memphis/Tennessee

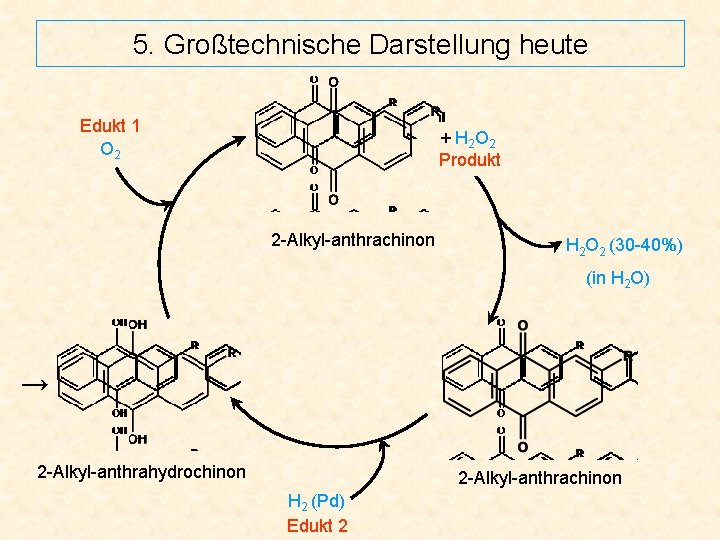
5. Großtechnische Darstellung heute Edukt 1 O 2 + H 2 O 2 Produkt 2 -Alkyl-anthrachinon H 2 O 2 (30 -40%) (in H 2 O) → 2 -Alkyl-anthrahydrochinon 2 -Alkyl-anthrachinon H 2 (Pd) Edukt 2

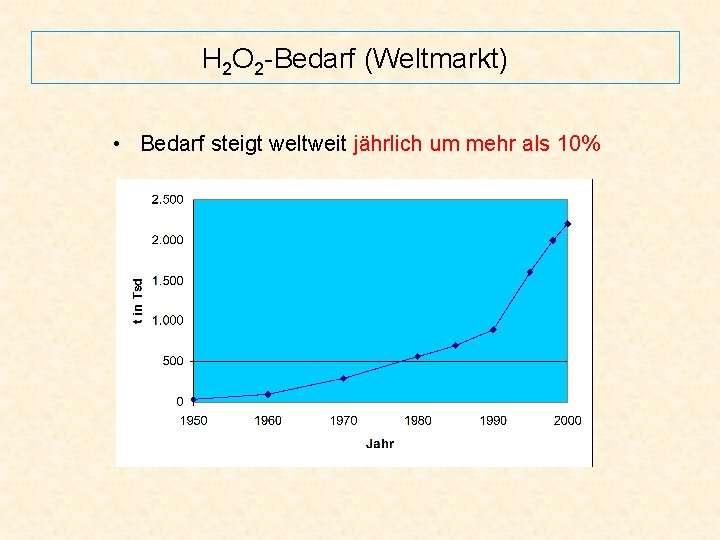
H 2 O 2 -Bedarf (Weltmarkt) • Bedarf steigt weltweit jährlich um mehr als 10%

6. Verwendung 1831 Publikation von Heinrich Wilhelm Kurrer: „ Diese Flüssigkeit [. . . ] wird, wenn man es erst in großem wohlfeil zubereiten gelernt hat, zur Vervollkommnung der Bleichkunst wesentlich beitragen. “

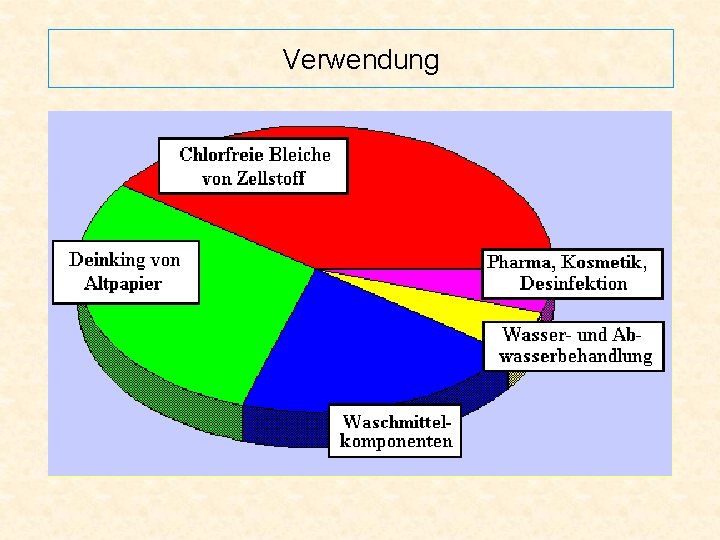
Verwendung • Lösung als Bleichmittel in der Papier- und Zellstoffindustrie und in der Textilindustrie • 3 -8%ige Lösung für medizinische und kosmetische Zwecke ⇨Versuch 4 • in gebundener Form als Waschmittelkomponente (“festes“ H 2 O 2) ⇨Versuch 5 • chemische Abwasserbehandlung • in der chemischen Industrie zur Synthese von organischen Peroxiden und Epoxyverbindungen • 85 -90%ige Lösung für militärische Anwendungen und als Treibstoff für Satellitenantriebe

Verwendung

Verwendung als Desinfektionsmittel • antimikrobielle Wirksamkeit von H 2 O 2 seit etwa 100 Jahren bekannt • abtötende Wirkung beruht auf oxidativen Zerstörung wichtiger Zellkomponenten durch hochaktiven Sauerstoff • Sauerstoff in statu nascendi entsteht beim Zerfall • Vorteil: Verzicht auf Konservierungsstoffe ⇨ Versuch 4

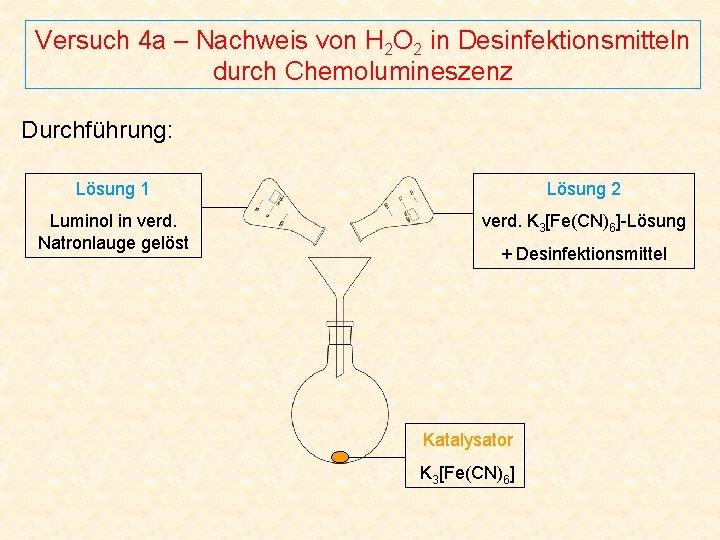
Versuch 4 a – Nachweis von H 2 O 2 in Desinfektionsmitteln durch Chemolumineszenz Durchführung: Lösung 1 Lösung 2 Luminol in verd. Natronlauge gelöst verd. K 3[Fe(CN)6]-Lösung + Desinfektionsmittel Katalysator K 3[Fe(CN)6]

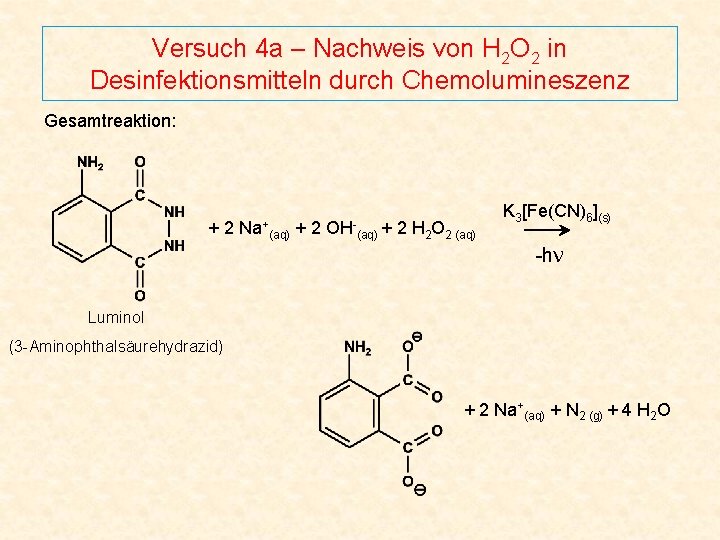
Versuch 4 a – Nachweis von H 2 O 2 in Desinfektionsmitteln durch Chemolumineszenz Gesamtreaktion: +2 Na+ (aq) +2 OH- (aq) + 2 H 2 O 2 (aq) K 3[Fe(CN)6](s) -hν Luminol (3 -Aminophthalsäurehydrazid) + 2 Na+(aq) + N 2 (g) + 4 H 2 O

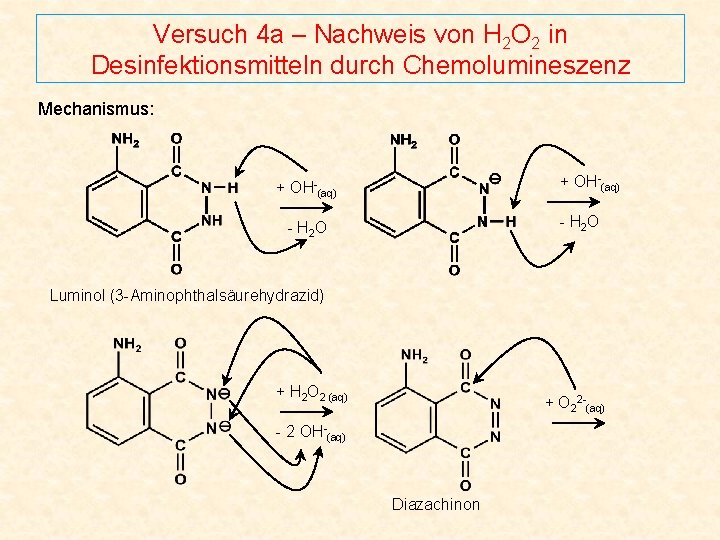
Versuch 4 a – Nachweis von H 2 O 2 in Desinfektionsmitteln durch Chemolumineszenz Mechanismus: + OH-(aq) - H 2 O Luminol (3 -Aminophthalsäurehydrazid) + H 2 O 2 (aq) + O 22 -(aq) - 2 OH-(aq) Diazachinon

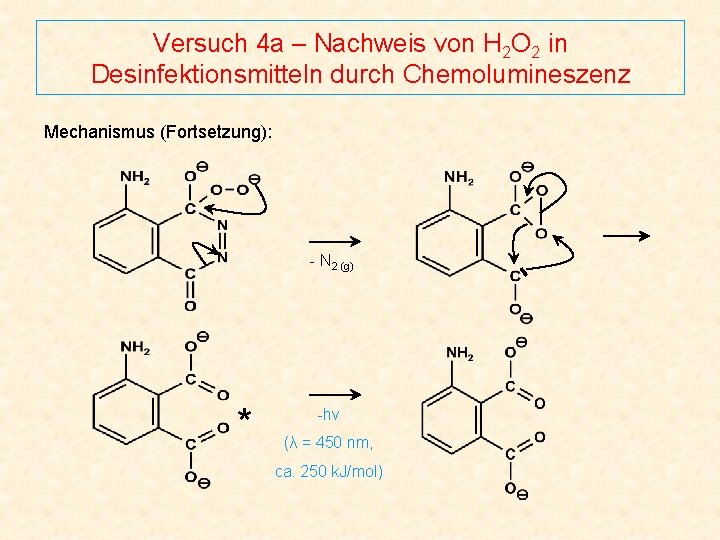
Versuch 4 a – Nachweis von H 2 O 2 in Desinfektionsmitteln durch Chemolumineszenz Mechanismus (Fortsetzung): - N 2 (g) * -hν (λ = 450 nm, ca. 250 k. J/mol)

Versuch 4 b – Quantitative Bestimmung von H 2 O 2 in Desinfektionsmitteln Bestimmung mit Hilfe der Permanganometrie: Durchführung: • • Einwaage: 5 g Desinfektionslösung Maßlösung: KMn. O 4 -Lösung (c = 0, 02 mol/L) Milieu: schwefelsauer Endpunktsbestimmung: bleibende blaßrosa Färbung der Lösung (mind. ½ Minute) Reaktionsgleichung: 2 +7 Mn. O 4 -(aq) + violett -1 5 H 2 O 2 (aq) + 6 H 3 O+ (aq) 2 +2 Mn 2+ blaßrosa 0 (aq) + 5 O 2 (g)↑ + 14 H 2 O

Versuch 4 b – Quantitative Bestimmung von H 2 O 2 in Desinfektionsmitteln Berechnung: 1 m. L KMn. O 4 -Lösung (c = 0, 02 mol/L) enthält 3, 16 mg KMn. O 4 (M(KMn. O 4) = 158 g/mol) Somit ergibt sich: m(H 2 O 2) = 3, 16 mg · 5 mol · 34 g/mol 2 mol · 158 g/mol = 1, 7 mg Also entsprechen. . . . m. L KMn. O 4 -Lösung. . mg H 2 O 2. Für den Massenanteil ergibt sich somit: w(H 2 O 2) = m(H 2 O 2) m(Desinfektionsmittel) = . . . g = 5 g Literaturwert (Kontaktlinsendesinfektionsmittel): w = 0, 6% . . . . %

Verwendung in Waschmitteln • z. B. im Fleckensalz 15 -30% Bleichmittel in Form von Natriumcarbonat-Peroxohydrat 2 Na 2 CO 3 · 3 H 2 O 2 oder als Natriumperoxoborat “Na. BO 2 · H 2 O 2 · 3 H 2 O” • freigesetztes H 2 O 2 zerstört Schmutz durch Oxidation → farbige Anschmutzungen werden in nicht farbige Verbindungen überführt • Bleichwirkung geht von atomaren Sauerstoff aus (statu nascendi) ⇨ Versuch 5

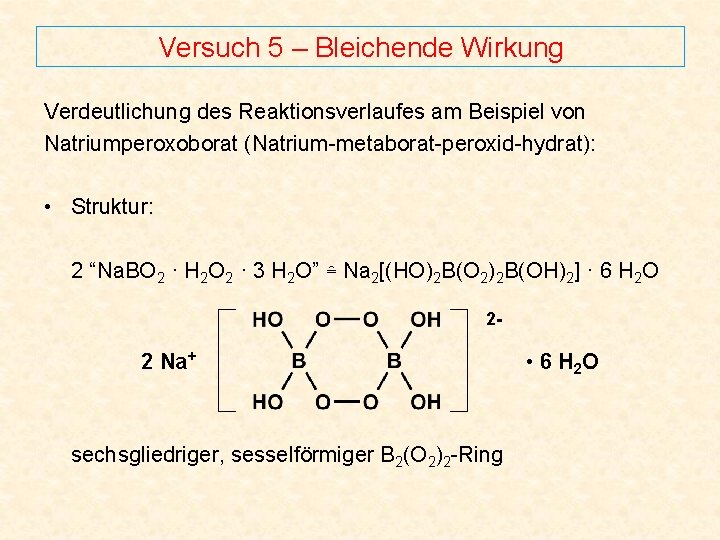
Versuch 5 – Bleichende Wirkung Verdeutlichung des Reaktionsverlaufes am Beispiel von Natriumperoxoborat (Natrium-metaborat-peroxid-hydrat): • Struktur: 2 “Na. BO 2 · H 2 O 2 · 3 H 2 O” ≙ Na 2[(HO)2 B(O 2)2 B(OH)2] · 6 H 2 O 2 - 2 Na+ sechsgliedriger, sesselförmiger B 2(O 2)2 -Ring • 6 H 2 O

Versuch 5 – Bleichende Wirkung (1) Freisetzung von H 2 O 2: Na 2[B 2(O 2)2(OH)4] (s) + 2 H 2 O 2 H 2 BO 3 - (aq) + 2 H 2 O ∆ 2 H 2 O 2 (aq) + 2 Na+(aq) + 2 H 2 BO 3 -(aq) 2 H 3 BO 3 (aq) + 2 OH-(aq) (2) Zerfall von H 2 O 2 mit Bleichwirkung: H 2 O 2 (aq) + OH-(aq) H 2 O + HO 2 -(aq) OH-(aq) + [O] ↓ statu nascendi → Bleichwirkung unerwünschte Reaktion: 2 H 2 O 2 (aq) ∆ 2 H 2 O + O 2 (g) ↑

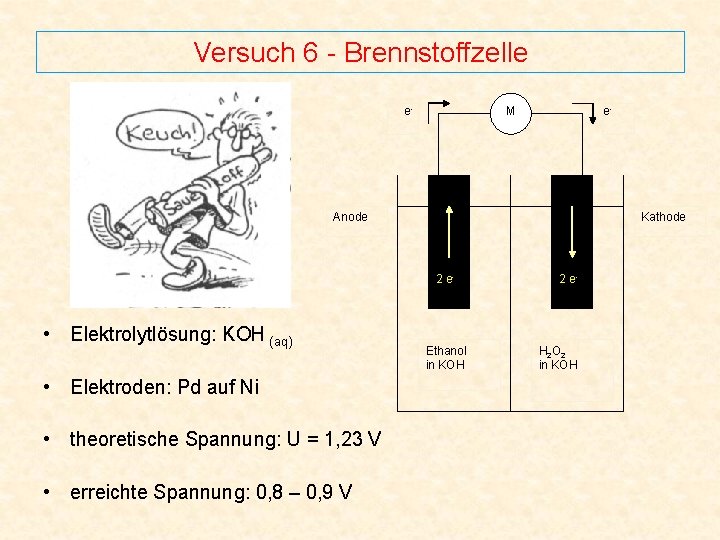
Versuch 6 - Brennstoffzelle e- M e- Anode Kathode 2 e- • Elektrolytlösung: KOH (aq) • Elektroden: Pd auf Ni • theoretische Spannung: U = 1, 23 V • erreichte Spannung: 0, 8 – 0, 9 V Ethanol in KOH 2 e- H 2 O 2 in KOH

Versuch 6 - Brennstoffzelle Kohlenstoffoxidation an der Anode: -3 -1 H 3 C―CH 2―OH (aq) + 12 OH- +4 2 CO 2 (g) + 9 H 2 O + 12 e- (aq) Sauerstoffreduktion an der Kathode: -1 direkte Reaktion: 6 H 2 O 2 (aq) + 12 e- -2 12 OH-(aq) oder Zersetzung unter katalytischen Einfluß des Elektrodenmaterials: -1 6 H 2 O 2 (aq) 0 Pd -2 0 6 H 2 O + 3 O 2 (g) + 6 H 2 O + 12 e- -2 12 OH-(aq) Also: Pro Mol H 2 O 2 werden 2 Mol Elektronen verbraucht.

Schlussbetrachtung ⇨ ideales Oxidationsmittel, da es keine belastenden Nebenprodukte bildet ⇨ keine Anreicherung in der Natur (weder durch natürliche, noch durch industrielle Prozesse) ⇨ immer mehr Anwendungen als umweltfreundliche Alternative zu Chlor und dessen Derivaten