SPOZNVAME CHEMICK REAKCIE V NAOM OKOL CHMIA PRE























- Slides: 26

SPOZNÁVAME CHEMICKÉ REAKCIE V NAŠOM OKOLÍ CHÉMIA PRE VII. ROČNÍK

FYZIKÁLNE A CHEMICKÉ DEJE

Chémia je prírodná veda. Jej cieľom je skúmať látky a ich premeny na iné látky. Fyzikálny dej – látka sa nezmení, len sa zmení jej tvar, veľkosť, skupenstvo. Chemická premena – látka sa premení na inú látku.

Chemický dej • • • horenie dreva hrdzavenie železa dýchanie fotosyntéza hnitie ovocia Fyzikálny dej • • • fúkanie vetra topenie ľadu dážď rozbitie skla pílenie dreva

CHEMICKÉ REAKCIE

ČO SÚ CHEMICKÉ REAKCIE? Chemické reakcie sú deje, pri ktorých sa látky menia /z určitých chem. látok vznikajú iné chem. látky/. Reaktanty sú látky, ktoré vstupujú do chem. reakcie, navzájom reagujú. Produkty sú látky, vznikajú chem. reakciou. Pri chem. reakcii sa reaktanty menia na produkty. Schéma zápisu: reaktanty produkty

Chem. reakcia horčíka s kyslíkom Kúsok horčíkovej pásky vložíme do plameňa kahana. Horčík horí oslnivým plameňom. Po skončení horenia vznikne biela prášková látka – oxid horečnatý. Schéma zápisu: reaktanty produkty horčík + kyslík oxid horečnatý

ZÁKON ZACHOVANIA HMOTNOSTI PRI CHEMICKÝCH REAKCIÁCH Celková hmotnosť všetkých rektantov sa rovná celkovej hmotnosti všetkých produktov. Pri chem. reakcii zreagovalo 8 g vodíka a 64 g kyslíka. Koľko gramov vody vzniklo? Schéma zápisu: reaktanty produkty vodík + kyslík voda 8 g + 64 g = Chem. reakciou vzniklo 72 g vody. 72 g

ZÁKON ZACHOVANIA HMOTNOSTI produkty reaktanty hmotnosť reaktantov = hmotnosť produktov

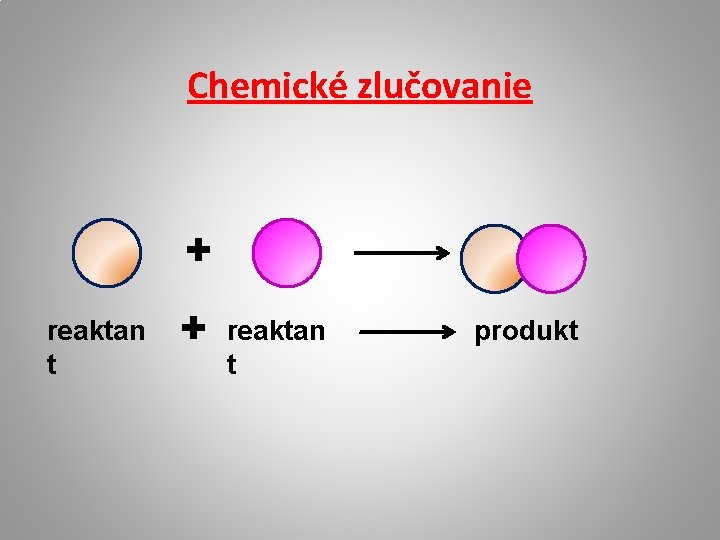
CHEMICKÉ ZLUČOVANIE Chemické zlučovanie je chemická reakcia, pri ktorej z dvoch jednoduchších reaktantov vzniká jeden zložitejší produkt. Reakcia síry a železa Zahriatím síry a železa vznikne nová látka sulfid železnatý. síra + železo sulfid železnatý R 1 + R 2 P reaktanty produkt

Chemické zlučovanie + reaktan t produkt

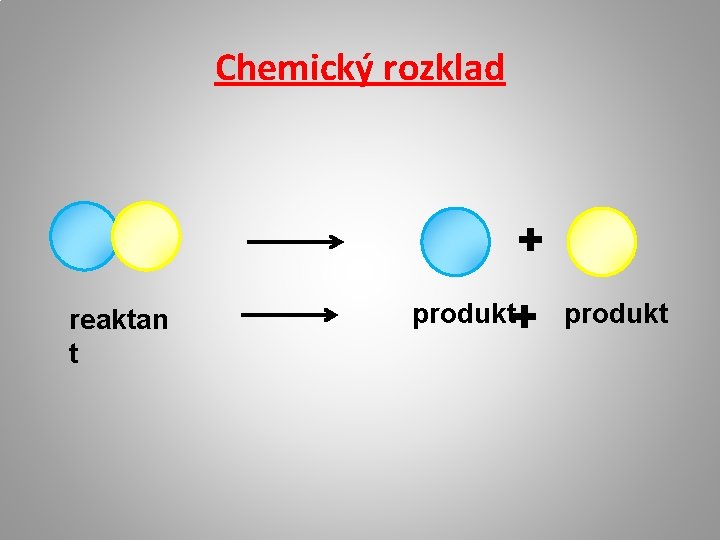
CHEMICKÝ ROZKLAD Chemický rozklad je chemická reakcia, pri ktorej z jedného zložitejšieho reaktantu vznikajú dva alebo viac jednoduchších produktov. Reakcia rozkladu oxidu ortuťnatého Oxid ortuťnatý sa teplom rozkladá na ortuť a kyslík. Oxid ortuťnatý ortuť + kyslík R P 1 + P 2 Reaktant produkty

Chemický rozklad + reaktan t produkt+ produkt

HORENIE

ČO JE HORENIE? Horenie je chemická reakcia, pri ktorej sa uvoľňuje svetlo a teplo. Látky sa pri horení zlučujú so vzdušným kyslíkom.

Podmienky horenia 1. Prítomnosť horľavej látky 2. Prítomnosť kyslíka 3. Zahriatie látky na zápalnú teplotu

1. Prítomnosť horľavej látky Horľavá látka je látka, ktorá reaguje s kyslíkom, pričom vzniká plameň. Plameň je stĺpec horiacich, väčšinou plynných látok. .

2. Prítomnosť kyslíka Kyslík reaguje s horľavými látkami, pričom vzniká svetlo a teplo. Látka horí vtedy, ak má k nej prístup kyslík, ktorý je vo vzduchu.

3. Zahriatie látky na zápalnú teplotu Zápalná teplota je teplota, pri ktorej sa látka zapáli. Možno ju dosiahnuť plameňom, iskrou, teplom z chemických reakcií, alebo z trenia. Čím je zápalná teplota nižšia, tým je látka nebezpečnejšia z hľadiska vzniku požiaru.

Skladovanie a práca s horľavinami Horľaviny musia byť výrazne označené Horľavé sú aj pary horľavín, so vzduchom tvoria výbušnú zmes. Skladovanie horľavín: § uzavreté v malých nádobách § vo vetraných miestnostiach § v prítomnosti horľavín sa nesmie pracovať s otvoreným ohňom § prísny zákaz fajčenia § v miestnosti musí byť hasiaci prístroj

Oheň je dobrý sluha, ale zlý pán !

POŽIAR A JEHO HASENIE Podmienky hasenia 1. Odstránenie horľavej látky. 2. Zabránenie vzdušného kyslíka. 3. Ochladenie látky pod zápalnú teplotu. • Aby sme uhasili požiar, stačí odstrániť jednu z podmienok hasenia.

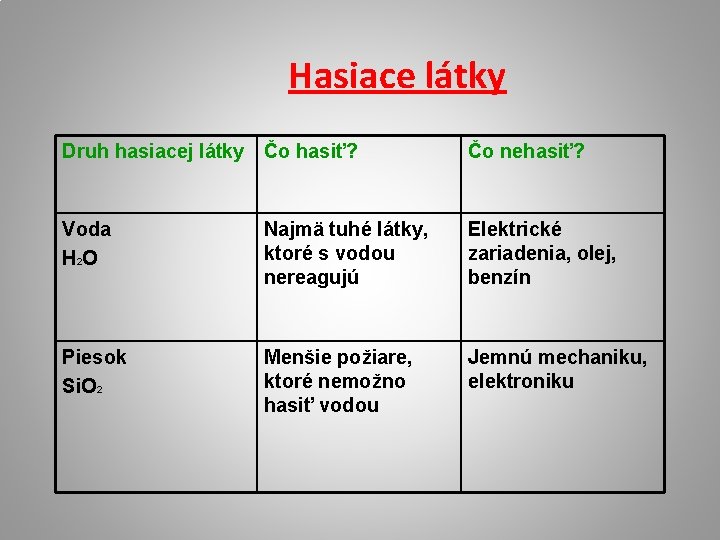
Hasiace látky Druh hasiacej látky Čo hasiť? Čo nehasiť? Voda H 2 O Najmä tuhé látky, ktoré s vodou nereagujú Elektrické zariadenia, olej, benzín Piesok Si. O 2 Menšie požiare, ktoré nemožno hasiť vodou Jemnú mechaniku, elektroniku

Hasiace prístroje Hasiaca látka Oxid uhličitý CO 2 Snehový hasiaci prístroj Oxid uhličitý a voda CO 2 a H 2 O Penový hasiaci prístroj Oxid hlinitý Al 203 Práškový hasiaci prístroj Čo hasiť? Čo nehasiť? Tuhé, kvapalné a plynné látky, elektrické zariadenia Práškové látky Tuhé a kvapalné látky Elektrické zariadenia pod napätím Tuhé, kvapalné, plynné látky, elektrické zariadenia Jemnú mechaniku a elektroniku

Čo treba robiť v prípade požiaru? Nepodliehať panike, zachovať pokoj! V prípade, že je požiar veľký a jeho hasenie nezvládneme, ihneď zavoláme hasičov. Volajte 150 alebo 112

ZDROIE: http: //thumbs. dreamstime. com/thumb_580/12968329626 a. Hr 9 n. jpg http: //photo. sistek. name/images/20070807004548_20070731_1512 -plamen. jpg http: //www. zborovna. sk CHÉMIA pre 7. ročník základných škôl a 2. ročník gymnázií a osemročným štúdiom ING. JANA KOTÚNOVÁ ZÁKLADNÁ ŠKOLA SADOVÁ 620, SENICA 2013