Spettroscopia spettroscopia Infrarosso spettroscopia UVVisibile spettroscopia NMR Spettrometria

Spettroscopia spettroscopia Infrarosso spettroscopia UV-Visibile spettroscopia NMR Spettrometria di Massa

Principi di Spettroscopia Molecolare Radiazione Elettromagnetica

Radiazione Elettromagnetica Si propaga alla velocità della luce Ha proprietà di particella ed onda L’energia di un fotone è proporzionale alla sua frequenza
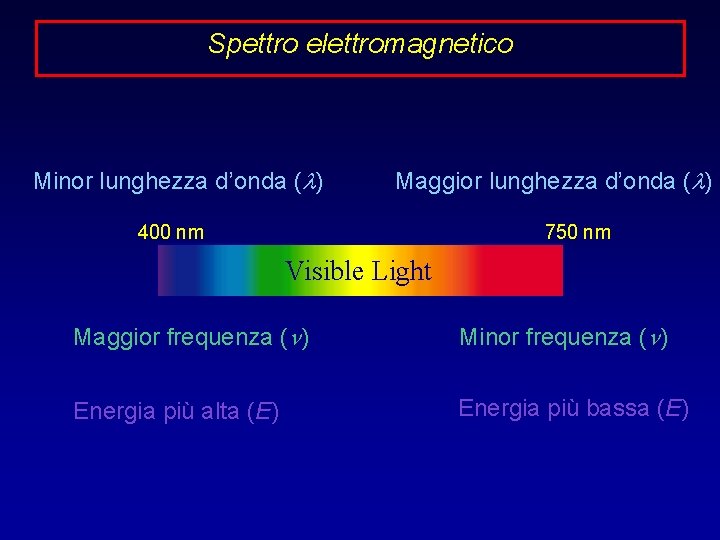
Spettro elettromagnetico Minor lunghezza d’onda (l) Maggior lunghezza d’onda (l) 400 nm 750 nm Visible Light Maggior frequenza (n) Minor frequenza (n) Energia più alta (E) Energia più bassa (E)

Spettro elettromagnetico Minor lunghezza d’onda (l) Ultravioletto Maggior lunghezza d’onda (l) Infrarosso Maggior frequenza (n) Minor frequenza (n) Energia più alta (E) Energia più bassa (E)

Spettro elettromagnetico Raggi cosmici Raggi g Raggi X Energy Luce ultravioletta Luce visibile Radiazioni infrarosso Microonde Onde radio

Principi di Spettroscopia Molecolare Stati energetici
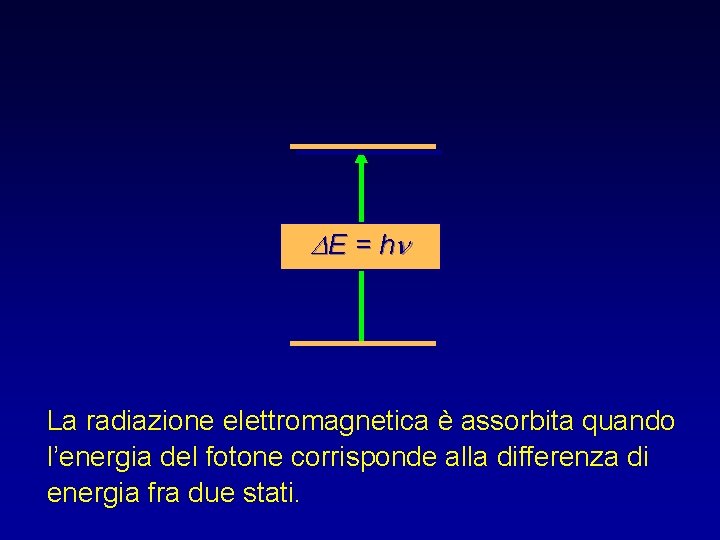
D E = hn La radiazione elettromagnetica è assorbita quando l’energia del fotone corrisponde alla differenza di energia fra due stati.

Quali stati? elettronico UV-Vis vibrazionale infrarosso rotazionale microonde spin nucleare radiofrequenze

Introduzione alla Spettroscopia 1 H NMR

I nuclei più utili al chimico organico 1 H and 13 C Entambi hanno spin = ± 1/2 1 H ha il 99% di abbondanza natuale 13 C ha l’ 1. 1% di abbondanza natuale
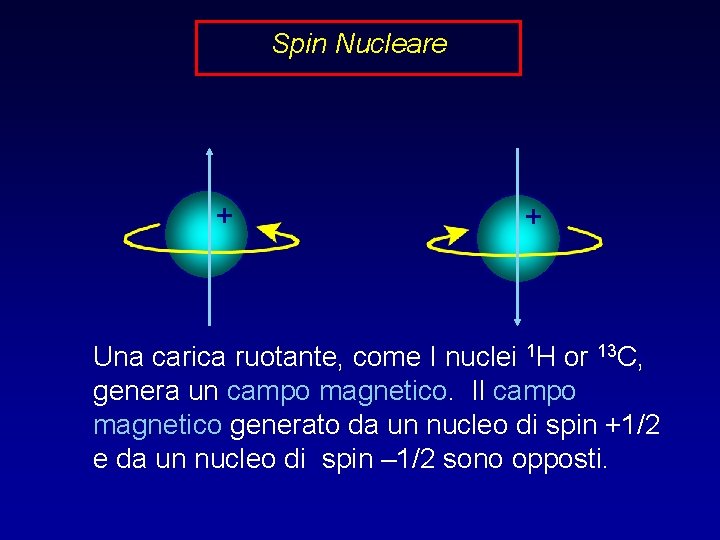
Spin Nucleare + + Una carica ruotante, come I nuclei 1 H or 13 C, genera un campo magnetico. Il campo magnetico generato da un nucleo di spin +1/2 e da un nucleo di spin – 1/2 sono opposti.
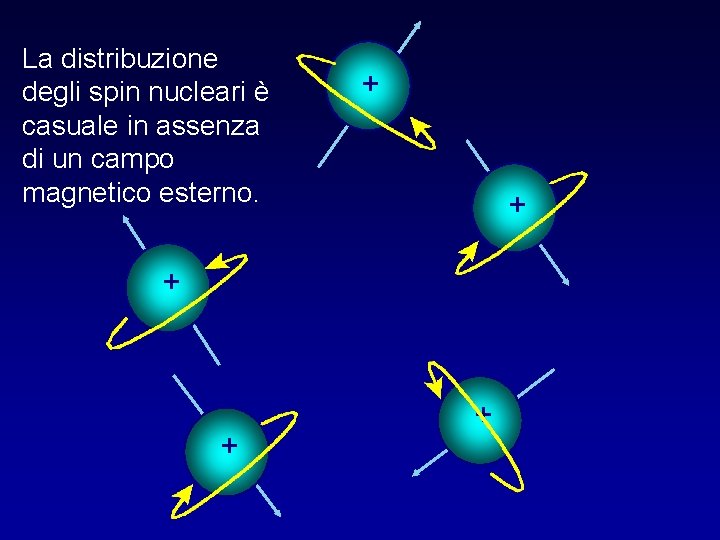
La distribuzione degli spin nucleari è casuale in assenza di un campo magnetico esterno. + + +
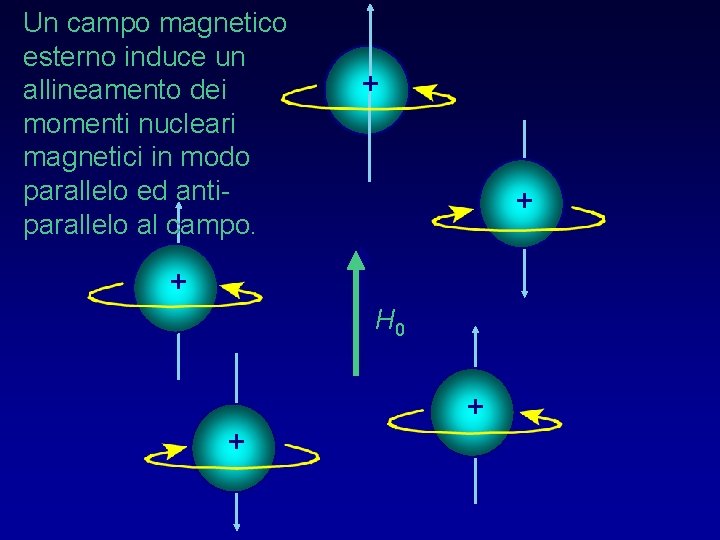
Un campo magnetico esterno induce un allineamento dei momenti nucleari magnetici in modo parallelo ed antiparallelo al campo. + + + H 0 + +
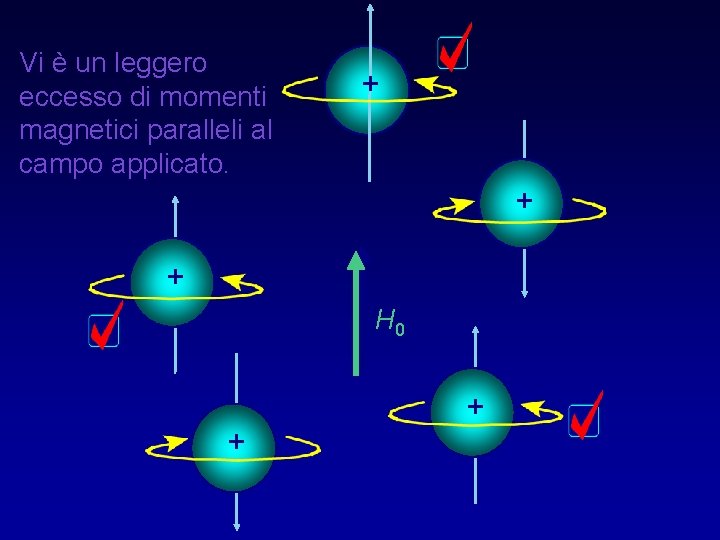
Vi è un leggero eccesso di momenti magnetici paralleli al campo applicato. + + + H 0 + +
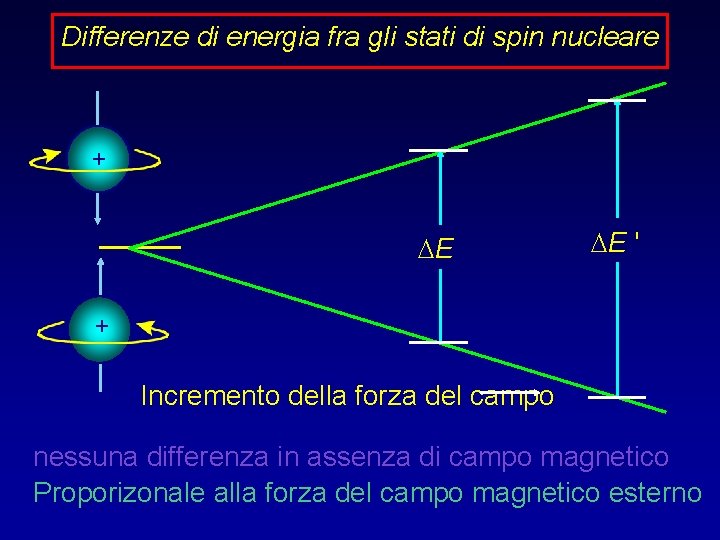
Differenze di energia fra gli stati di spin nucleare + DE DE ' + Incremento della forza del campo nessuna differenza in assenza di campo magnetico Proporizonale alla forza del campo magnetico esterno

Relazioni in NMR Unità La frequenza della radiazione elettromagnetica assorbita è proporzionale a: differenza di energia fra i due stati nucleari che a sua volta è proporzional al: campo magnetico applicato Hz k. J/mol (kcal/mol) tesla (T)

La frequenza della radiazione elettromagnetica assorbita varia con gli elementi o con i vari isotopi dello stesso elemento. Per un campo di forza 4. 7 T: 1 H assorbe radiazioni con una frequenza di 200 MHz (200 x 106 s-1) 13 C assorbe radiazioni con una frequenza di of 50. 4 MHz (50. 4 x 106 s-1) La frequenza della radiazione elettromagnetica assorbita da un particolare nucleo dipende dal suo intorno molecolare Questo è il motivo per cui l’NMR è una tecnica potentissima per la caratterizzazione stuttuale di una molecola.

1 H Chemical Shifts
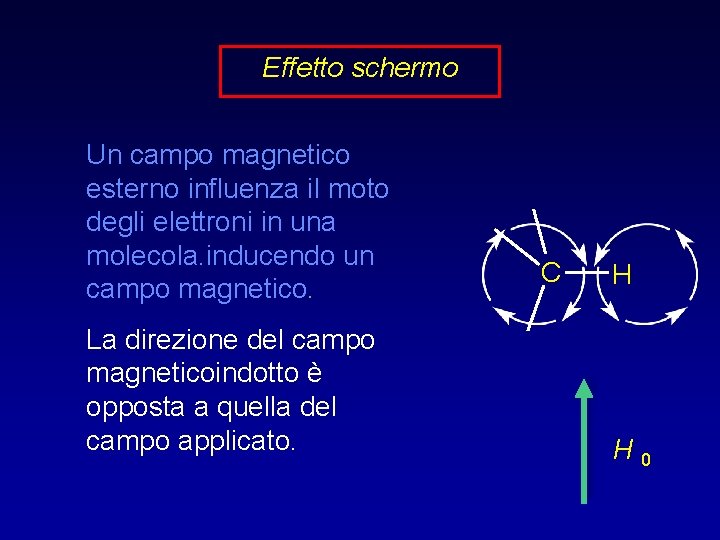
Effetto schermo Un campo magnetico esterno influenza il moto degli elettroni in una molecola. inducendo un campo magnetico. La direzione del campo magneticoindotto è opposta a quella del campo applicato. C H H 0
Il campo indotto scherma I nuclei dal campo applicato. E’ necessario un campo esterno più forte affinchè la differenza di energia fra gli stati di spin eguagli l’energia della radiazione rf. per raggiungere l’energia rf della radiazione. C H H 0
Chemical Shift Il Chemical shift è una misura del grado in cui un nucleo in una moleocla è schermato. Poichè I protoni in differenti intorni sono schermati in modo diifferente, essi hanno chemical shifts differenti. C H H 0

Campi bassi Diminuzione dell’effetto schermo Campi alti Aumento dell’effetto schemo (CH 3)4 Si (TMS) 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 Chemical shift (d, ppm) rispetto al TMS 2. 0 1. 0 0
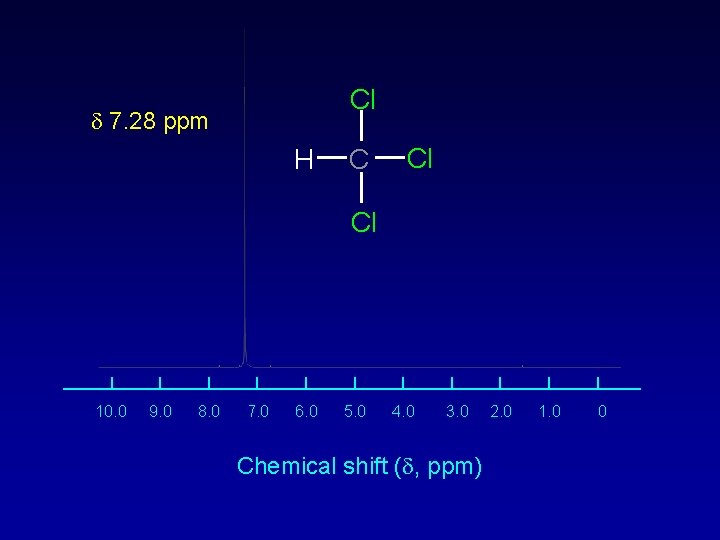
Cl d 7. 28 ppm H C Cl Cl 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 Chemical shift (d, ppm) 2. 0 1. 0 0

Effetti della Struttura Molecolare sull’ 1 H Chemical Shifts
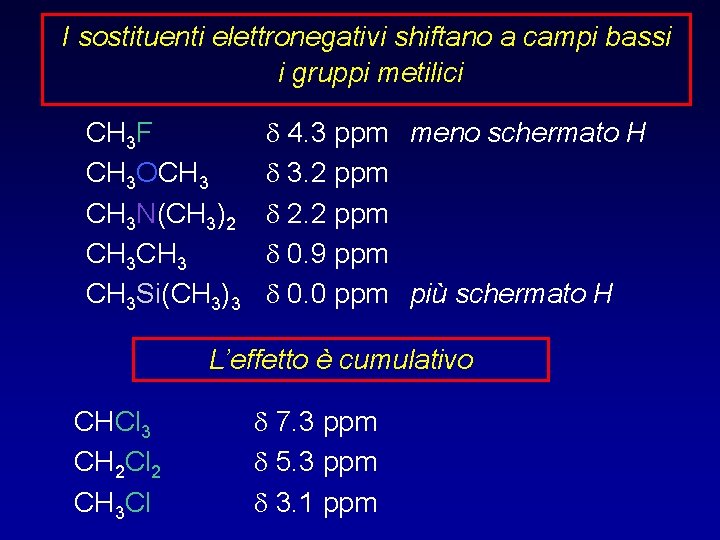
I sostituenti elettronegativi shiftano a campi bassi i gruppi metilici CH 3 F CH 3 OCH 3 N(CH 3)2 CH 3 Si(CH 3)3 d 4. 3 ppm meno schermato H d 3. 2 ppm d 2. 2 ppm d 0. 9 ppm d 0. 0 ppm più schermato H L’effetto è cumulativo CHCl 3 CH 2 Cl 2 CH 3 Cl d 7. 3 ppm d 5. 3 ppm d 3. 1 ppm
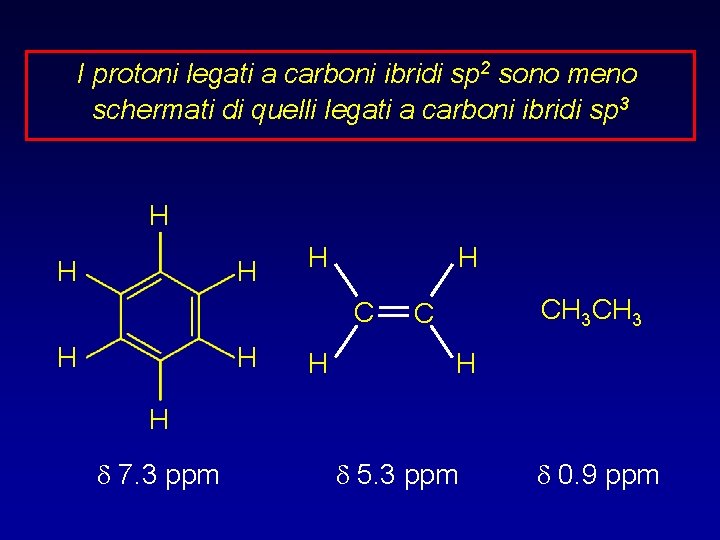
I protoni legati a carboni ibridi sp 2 sono meno schermati di quelli legati a carboni ibridi sp 3 H H H CH 3 C H H d 7. 3 ppm d 5. 3 ppm d 0. 9 ppm

Tipo di protone Chemical shift (d), Tipo di protone ppm H C R 0. 9 -1. 8 H C C C 1. 6 -2. 6 H C Ar C C C 2. 5 2. 3 -2. 8 H O H Chemical shift (d), ppm 2. 1 -2. 5 C C 4. 5 -6. 5
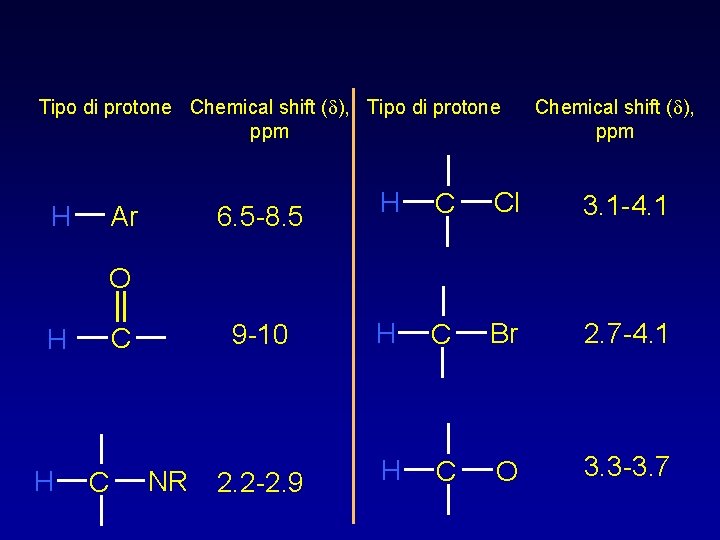
Tipo di protone Chemical shift (d), Tipo di protone ppm H Ar Chemical shift (d), ppm 6. 5 -8. 5 H C Cl 3. 1 -4. 1 9 -10 H C Br 2. 7 -4. 1 H C O 3. 3 -3. 7 O C H H C NR 2. 2 -2. 9
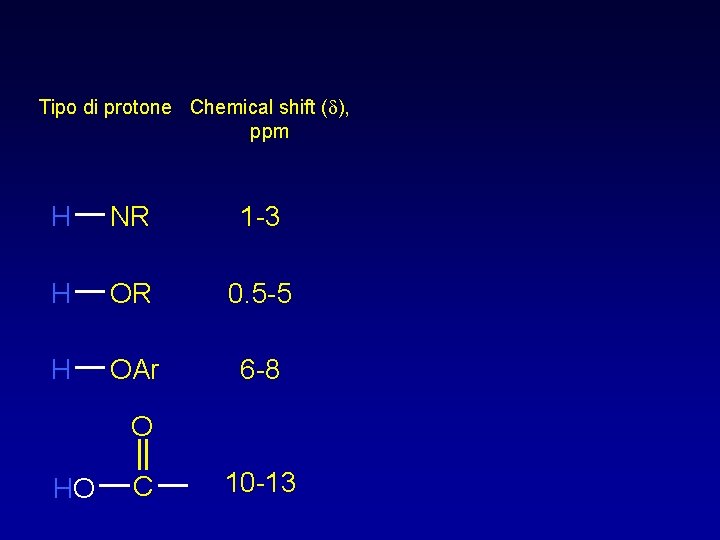
Tipo di protone Chemical shift (d), ppm H NR 1 -3 H OR 0. 5 -5 H OAr 6 -8 O HO C 10 -13

Informazioni ottenibili da uno spettro NMR 1. Numero di segnali 2. Intensità relativa 3. Molteplicità

Numero di segnali I protoni che hanno differenti chemical shifts sono chimicamente non equivalenti, cioè sono in intorni molecolari differenti
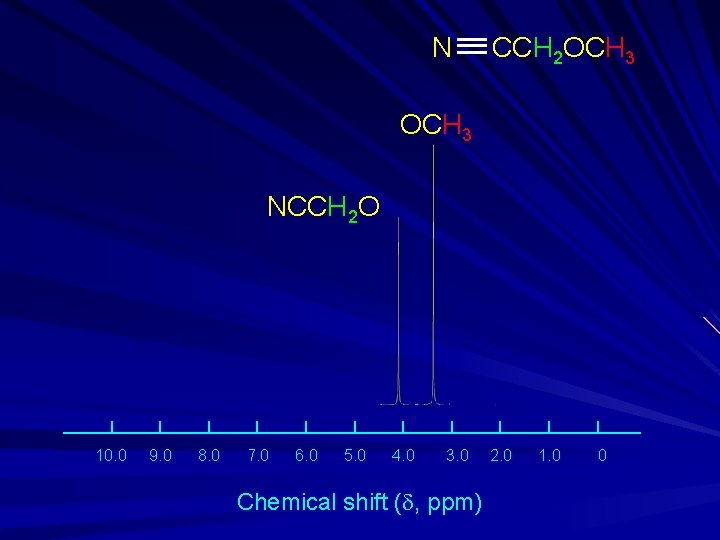
N CCH 2 OCH 3 NCCH 2 O 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 Chemical shift (d, ppm) 2. 0 1. 0 0

Protoni Diastereotopici e Enantiotopici I protoni diastereotopici possono avere t chemical shifts differenti Br H d 5. 3 ppm C H 3 C C H d 5. 5 ppm I protoni enantiotopici hanno lo stesso chemical shift
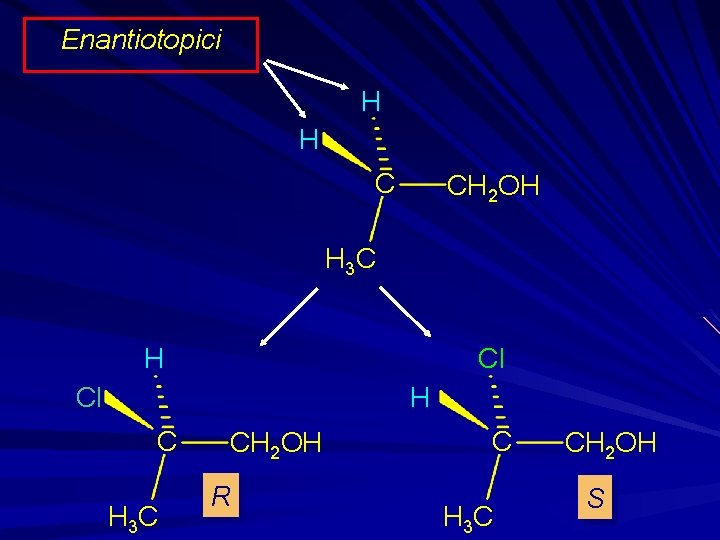
Enantiotopici H H C CH 2 OH H 3 C H Cl Cl H C H 3 C CH 2 OH R C H 3 C CH 2 OH S
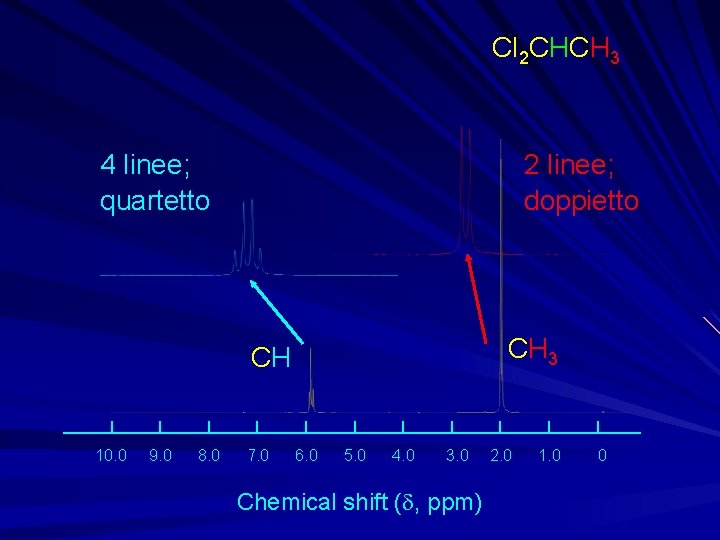
Cl 2 CHCH 3 4 linee; quartetto 2 linee; doppietto CH 3 CH 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 Chemical shift (d, ppm) 2. 0 1. 0 0
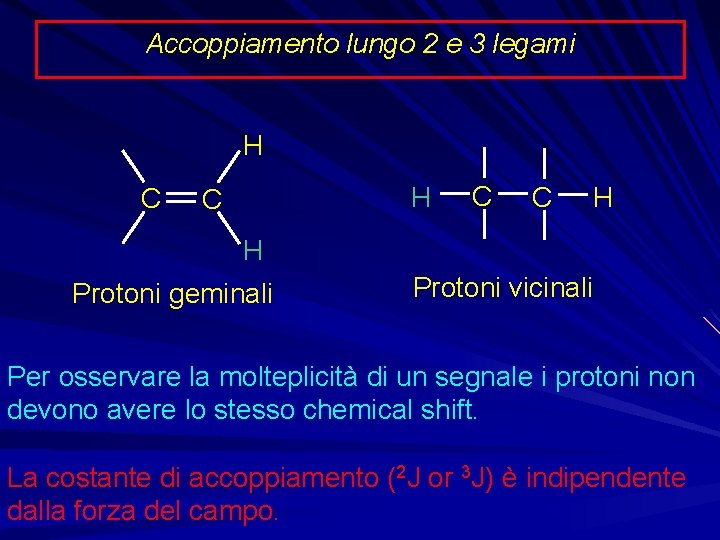
Accoppiamento lungo 2 e 3 legami H C C H Protoni geminali H C C H Protoni vicinali Per osservare la molteplicità di un segnale i protoni non devono avere lo stesso chemical shift. La costante di accoppiamento (2 J or 3 J) è indipendente dalla forza del campo.
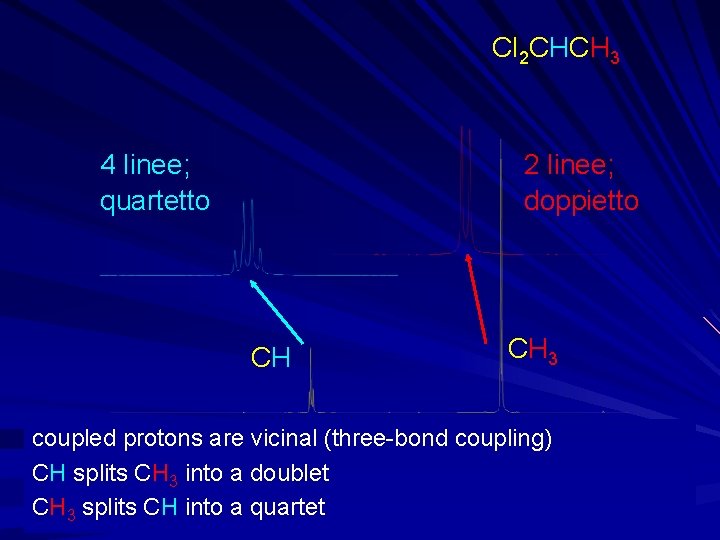
Cl 2 CHCH 3 4 linee; quartetto 2 linee; doppietto CH CH 3 coupled protons are vicinal (three-bond coupling) 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 2. 0 1. 0 CH splits CH 3 into a doublet CH 3 splits CH into a. Chemical quartet shift (d, ppm) 0

Why do the methyl protons of 1, 1 -dichloroethane appear as a doublet? H Cl H C C Cl H signal for methyl H protons is split into a doublet To explain the splitting of the protons at C-2, we first focus on the two possible spin orientations of the proton at C-1

Why do the methyl protons of 1, 1 -dichloroethane appear as a doublet? H Cl H C C Cl H signal for methyl H protons is split into a doublet There are two orientations of the nuclear spin for the proton at C-1. One orientation shields the protons at C-2; the other deshields the C 2 protons.

Why do the methyl protons of 1, 1 -dichloroethane appear as a doublet? H Cl H C C Cl H signal for methyl H protons is split into a doublet The protons at C-2 "feel" the effect of both the applied magnetic field and the local field resulting from the spin of the C-1 proton.
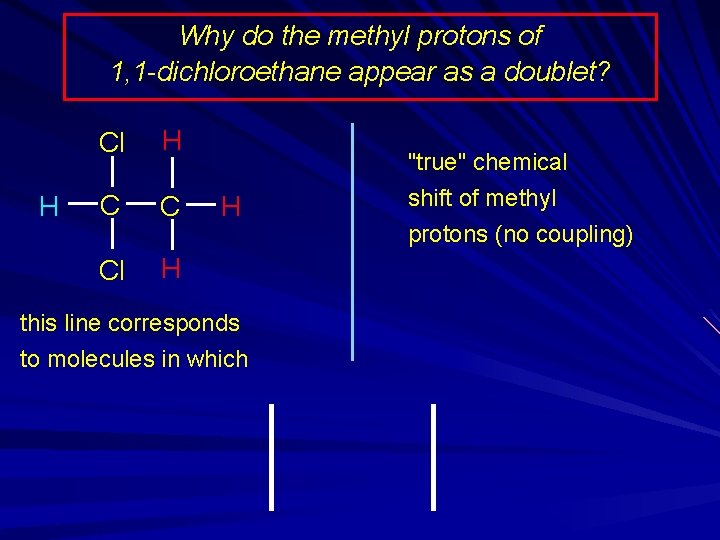
Why do the methyl protons of 1, 1 -dichloroethane appear as a doublet? H Cl H C C Cl H H this line corresponds to molecules in which "true" chemical shift of methyl protons (no coupling)
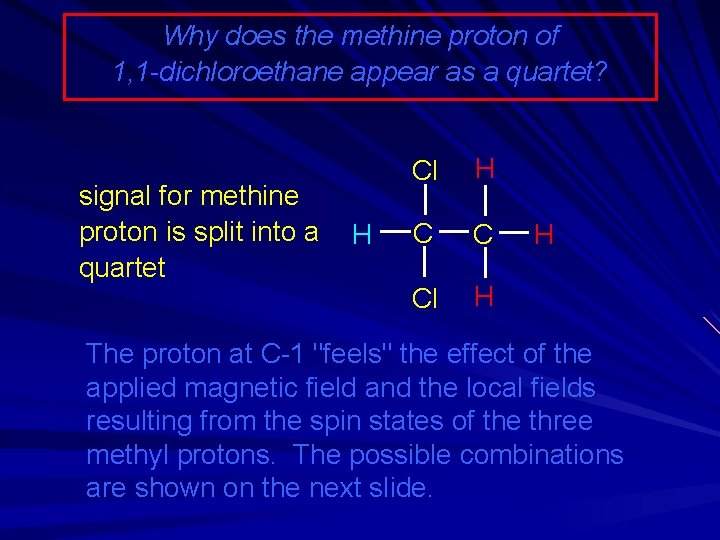
Why does the methine proton of 1, 1 -dichloroethane appear as a quartet? signal for methine proton is split into a quartet H Cl H C C Cl H H The proton at C-1 "feels" the effect of the applied magnetic field and the local fields resulting from the spin states of the three methyl protons. The possible combinations are shown on the next slide.
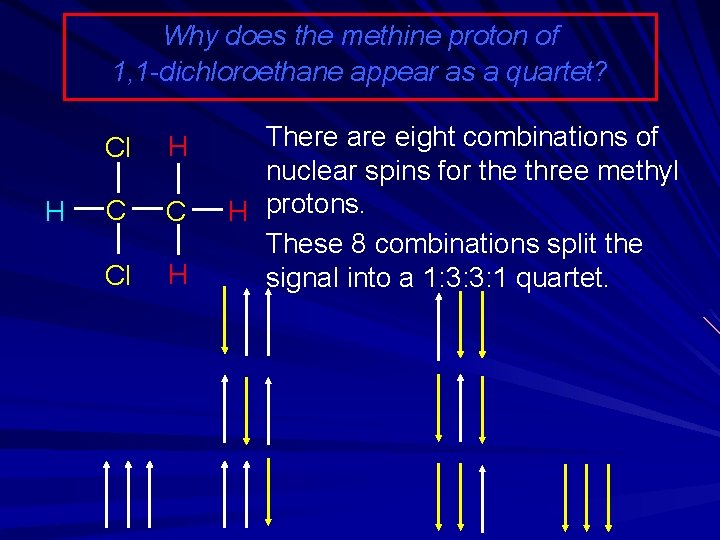
Why does the methine proton of 1, 1 -dichloroethane appear as a quartet? H Cl H C C Cl H There are eight combinations of nuclear spins for the three methyl H protons. These 8 combinations split the signal into a 1: 3: 3: 1 quartet.

The splitting rule for 1 H NMR For simple cases, the multiplicity of a signal for a particular proton is equal to the number of equivalent vicinal protons + 1.

Table 13. 2 (page 504) Splitting Patterns of Common Multiplets Number of equivalent protons to which H is coupled 1 2 3 4 5 6 Appearance Intensities of lines of multiplet in multiplet Doublet Triplet Quartet Pentet Sextet Septet 1: 1 1: 2: 1 1: 3: 3: 1 1: 4: 6: 4: 1 1: 5: 10: 5: 1 1: 6: 15: 20: 15: 6: 1

13. 8 Splitting Patterns: The Ethyl Group CH 3 CH 2 X is characterized by a triplet-quartet pattern (quartet at lower field than the triplet)
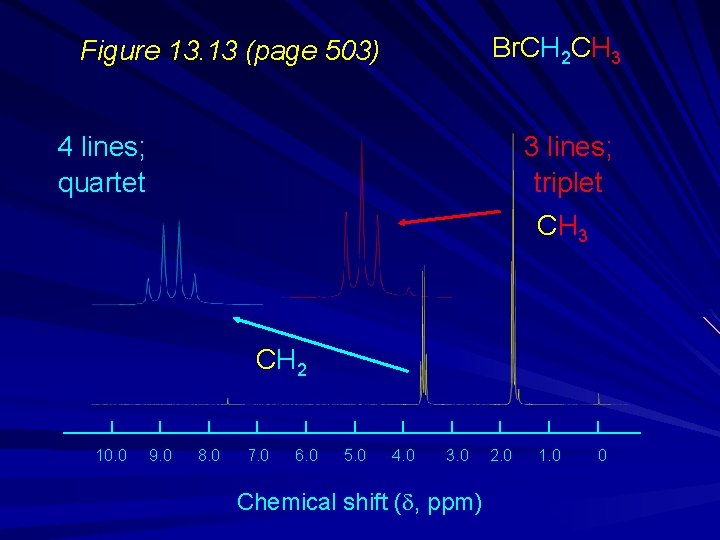
Br. CH 2 CH 3 Figure 13. 13 (page 503) 4 lines; quartet 3 lines; triplet CH 3 CH 2 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 Chemical shift (d, ppm) 2. 0 1. 0 0

13. 9 Splitting Patterns: The Isopropyl Group (CH 3)2 CHX is characterized by a doublet-septet pattern (septet at lower field than the doublet)
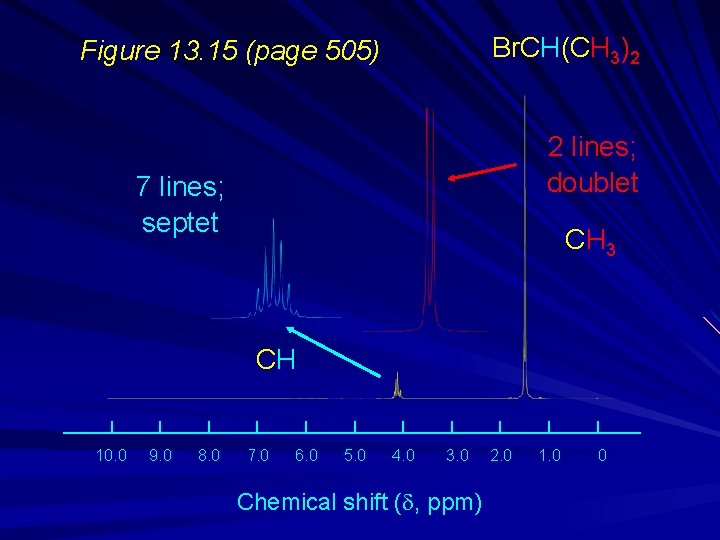
Br. CH(CH 3)2 Figure 13. 15 (page 505) 2 lines; doublet 7 lines; septet CH 3 CH 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 Chemical shift (d, ppm) 2. 0 1. 0 0

13. 10 Splitting Patterns: Pairs of Doublets Splitting patterns are not always symmetrical, but lean in one direction or the other.

Pairs of Doublets H C C H Consider coupling between two vicinal protons. If the protons have different chemical shifts, each will split the signal of the other into a doublet.

Pairs of Doublets H C C H Let Dn be the difference in chemical shift in Hz between the two hydrogens. Let J be the coupling constant between them in Hz.
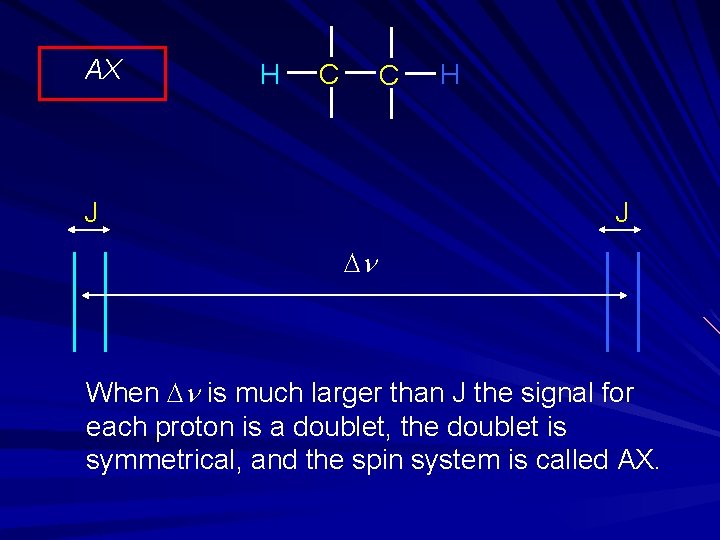
AX H C C J H J Dn When Dn is much larger than J the signal for each proton is a doublet, the doublet is symmetrical, and the spin system is called AX.
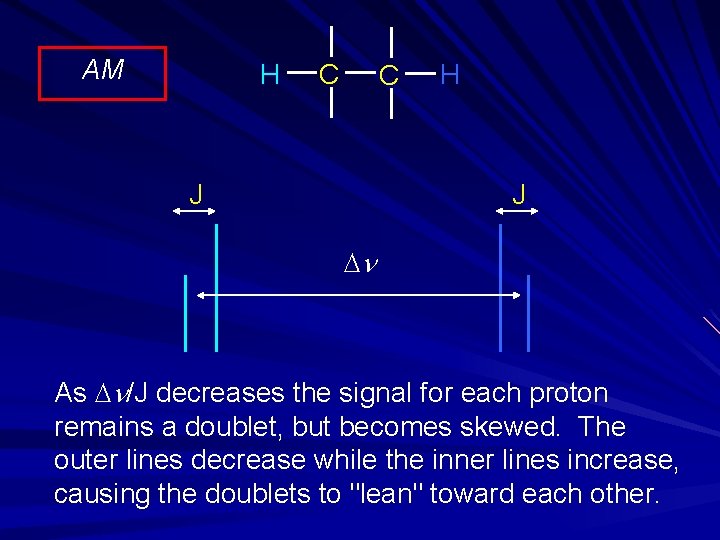
AM H C C J H J Dn As Dn/J decreases the signal for each proton remains a doublet, but becomes skewed. The outer lines decrease while the inner lines increase, causing the doublets to "lean" toward each other.
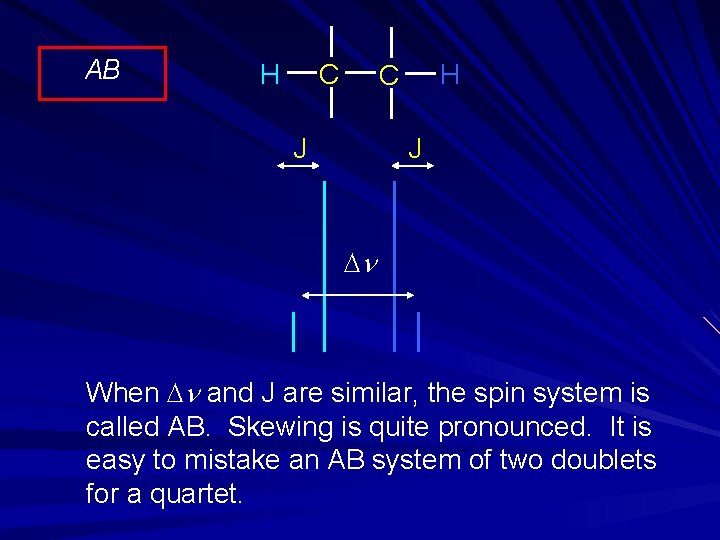
AB H C J J Dn When Dn and J are similar, the spin system is called AB. Skewing is quite pronounced. It is easy to mistake an AB system of two doublets for a quartet.

A 2 H C C H When Dn = 0, the two protons have the same chemical shift and don't split each other. A single line is observed. The two doublets have collapsed to a singlet.

H Figure 13. 17 (page 507) skewed doublets H OCH 3 Cl H H OCH 3 10. 0 9. 0 8. 0 7. 0 6. 0 5. 0 4. 0 3. 0 Chemical shift (d, ppm) 2. 0 1. 0 0

13. 11 Complex Splitting Patterns Multiplets of multiplets
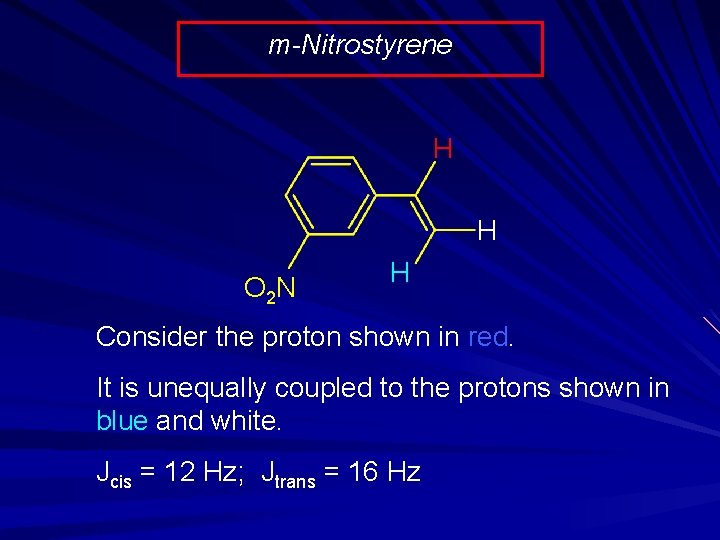
m-Nitrostyrene H H O 2 N H Consider the proton shown in red. It is unequally coupled to the protons shown in blue and white. Jcis = 12 Hz; Jtrans = 16 Hz
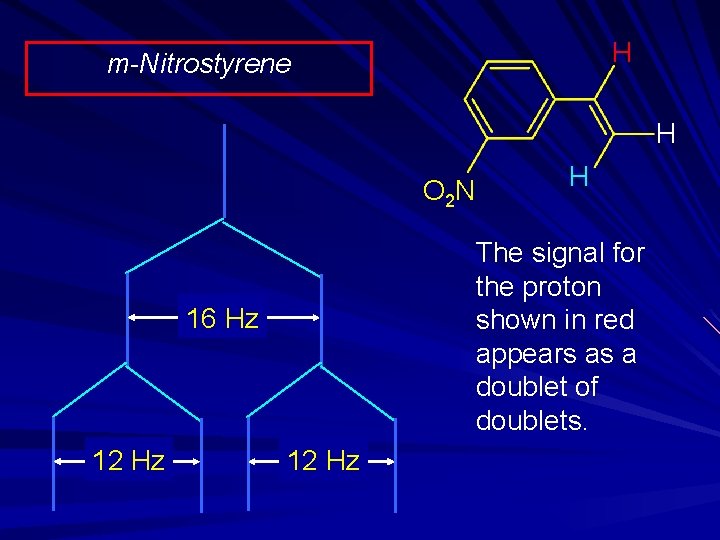
H m-Nitrostyrene H O 2 N The signal for the proton shown in red appears as a doublet of doublets. 16 Hz 12 Hz H 12 Hz
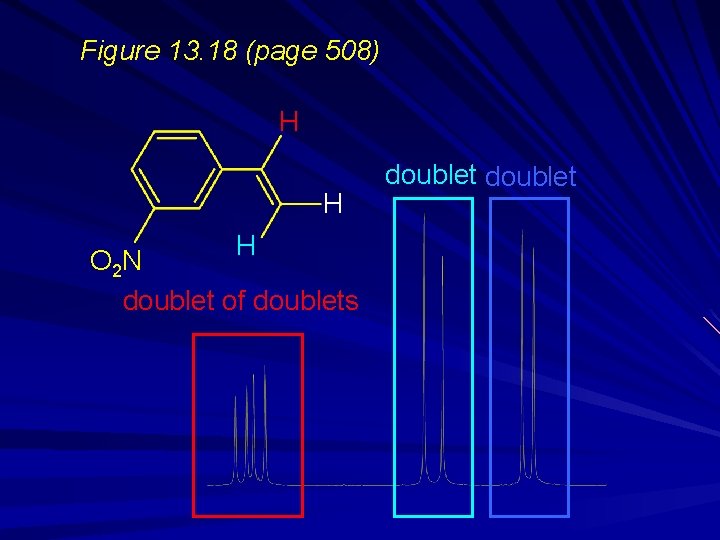
Figure 13. 18 (page 508) H H H O 2 N doublet of doublets doublet

13. 12 1 H NMR Spectra of Alcohols What about H bonded to O?

O—H H C O H The chemical shift for O—H is variable (d 0. 55 ppm) and depends on temperature and concentration. Splitting of the O—H proton is sometimes observed, but often is not. It usually appears as a broad peak. Adding D 2 O converts O—H to O—D. The O —H peak disappears.

13. 13 NMR and Conformations

NMR is "slow" Most conformational changes occur faster than NMR can detect them. An NMR spectrum is the weighted average of the conformations. For example: Cyclohexane gives a single peak for its H atoms in NMR. Half of the time a single proton is axial and half of the time it is equatorial. The observed chemical shift is half way between the axial chemical shift and the equatorial chemical shift.
- Slides: 66