Spettroscopia Molecolare Vibrazionale IR Teoria e applicazioni Spettroscopia

Spettroscopia Molecolare Vibrazionale - IR Teoria e applicazioni

Spettroscopia Molecolare • Assorbimento: FTIR • Un campione va messo in un fascio di radiazione IR • L’assorbimento del campione in funzione del lunghezza d’onda (wavenumber) viene calcolato e riportato in un grafico
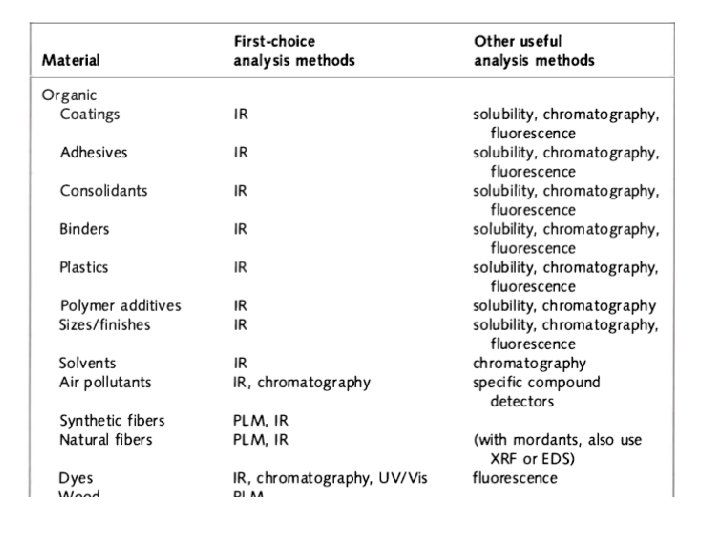



Introduzione • • Vibrazioni – che cosa sono? Molecole – quali proprietà? Come mai assorbono la radiazione? Applicazioni
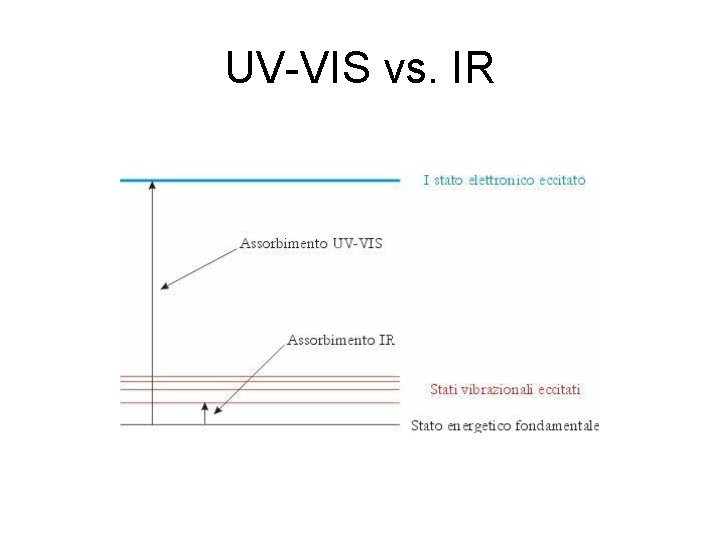
UV-VIS vs. IR

Spettroscopia IR • Definizione – Per avere lo spettro infrarosso (IR) di un materiale è necessario che il materiale assorba una certa quantità di radiazione IR. Si ricorda che la parte di spettro elettromagnetico corrispondente all’IR è compresa fra λ ≈ 800 nm e λ ≈ 1 mm ovvero fra ν ≈ 12500 cm− 1 e ν ≈ 10 cm− 1. • Esempi: FTIR oppure IRTF • Fourier Transform Infra. Red – Infrarosso con la trasformazione di Fourier
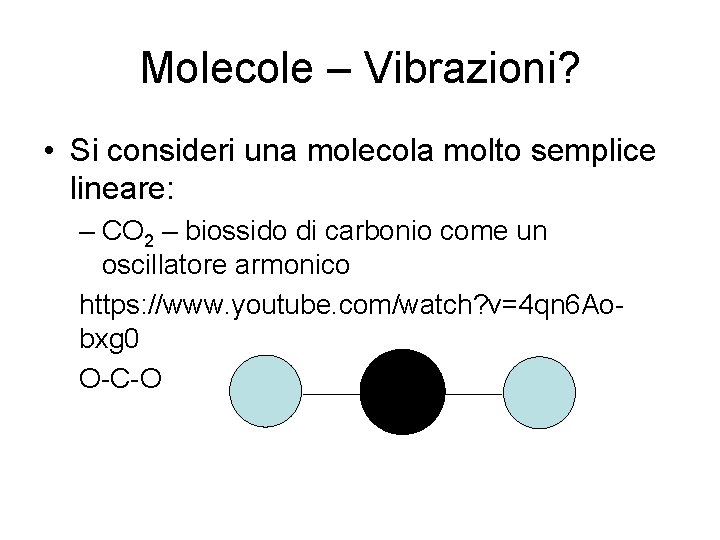
Molecole – Vibrazioni? • Si consideri una molecola molto semplice lineare: – CO 2 – biossido di carbonio come un oscillatore armonico https: //www. youtube. com/watch? v=4 qn 6 Aobxg 0 O-C-O

Molecular vibrations • How many vibrations are possible (=fundamental vibrations)? A molecule has as many degrees of freedom as the total degree of freedom of its individual atoms. Each atom has three degrees of freedom (corresponding to the Cartesian coordinates), thus in an N-atom molecule there will be 3 N degree of freedom. In molecules, movements of the atoms are constrained by interactions through chemical bonds. Translation - the movement of the entire molecule while the positions of the atoms relative to each other remain fixed: 3 degrees of translational freedom. Rotational transitions – interatomic distances remain constant but the entire molecule rotates with respect to three mutually perpendicular axes: 3 rotational freedom (nonlinear), 2 rotational freedom (linear).

Vibrations – relative positions of the atoms change while the average position and orientation of the molecule remain fixed. Fundamental Vibrations
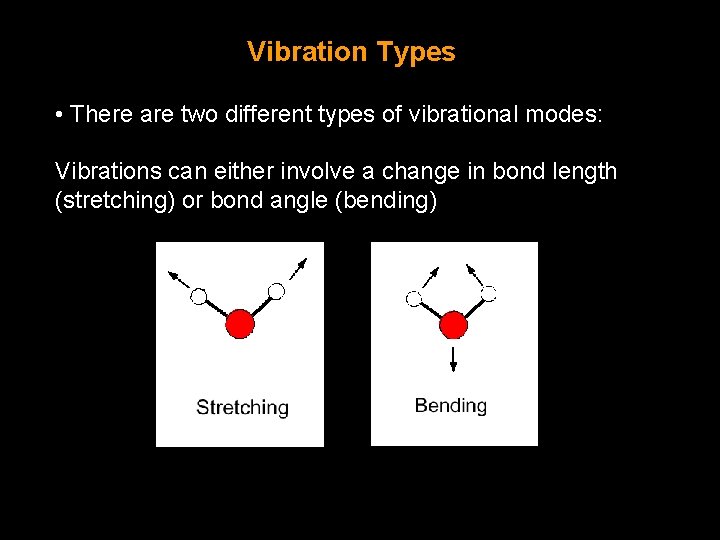
Vibration Types • There are two different types of vibrational modes: Vibrations can either involve a change in bond length (stretching) or bond angle (bending)

The bending vibrations are often subdivided into scissoring, rocking, wagging, and twisting.

Legge di Numero di Vibrazioni • Una molecola di N atomi può vibrare secondo 3 N-6 (3 N-5 se è lineare) modi normali di vibrazione, ciascuno caratterizzato da una frequenza ovvero un’energia fondamentale che può variare da 100 a 4000 cm− 1.
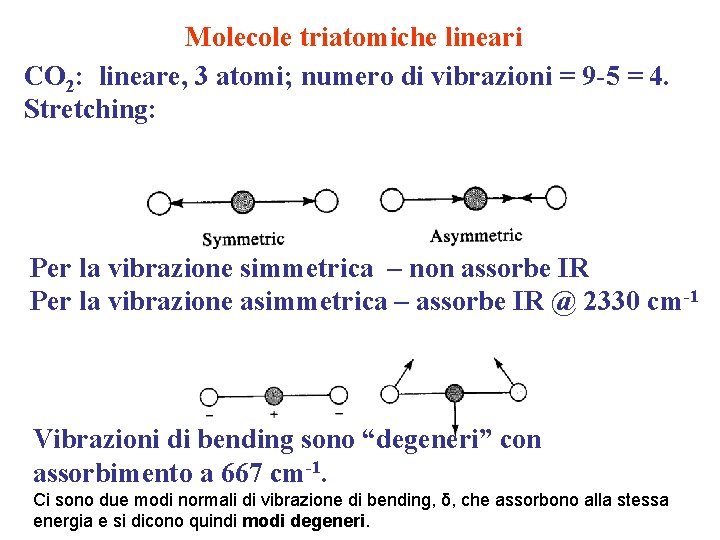
Molecole triatomiche lineari CO 2: lineare, 3 atomi; numero di vibrazioni = 9 -5 = 4. Stretching: Per la vibrazione simmetrica – non assorbe IR Per la vibrazione asimmetrica – assorbe IR @ 2330 cm-1 Vibrazioni di bending sono “degeneri” con assorbimento a 667 cm-1. Ci sono due modi normali di vibrazione di bending, δ, che assorbono alla stessa energia e si dicono quindi modi degeneri.
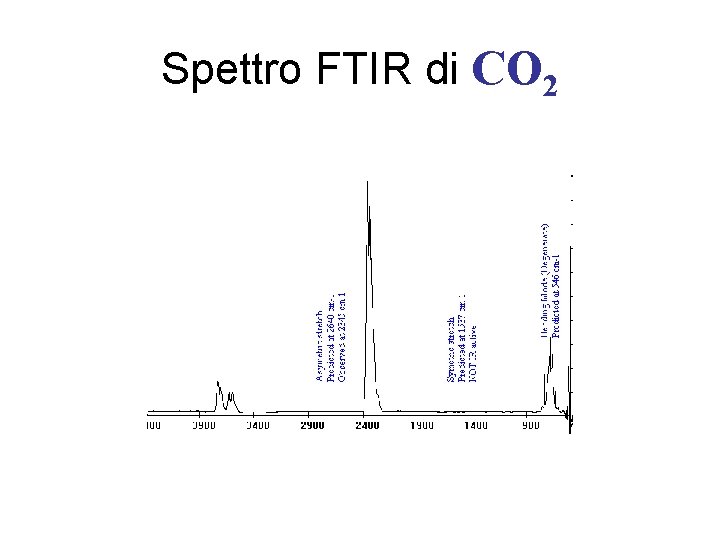
Spettro FTIR di CO 2
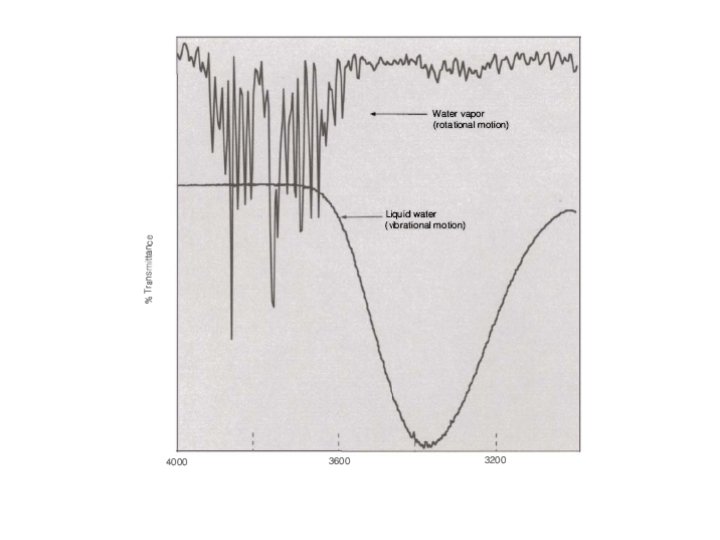
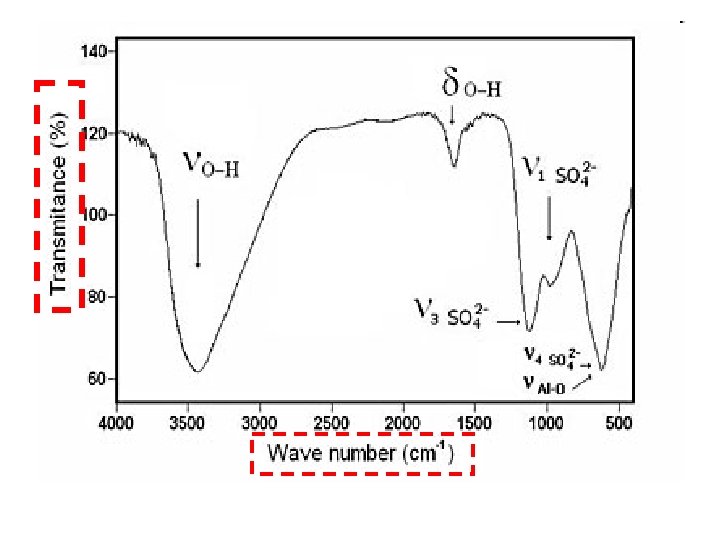

Contesto piu’ ampio Molecole poliatomiche Per molecole di più grosse dimensioni si introduce il concetto di vibrazione di gruppo. Aumentando le dimensioni delle molecole i metodi che abbiamo usato negli esempi precedenti rimangono sempre validi. Tuttavia con le dimensioni delle molecole aumenta anche il numero dei modi normali e in genere il numero delle bande infrarosse.

Quali molecole vi interessano nello specifico? Legno/Pietra/Tele/Tavole/ Gessi/Fotografie/Carte/ Metalli?

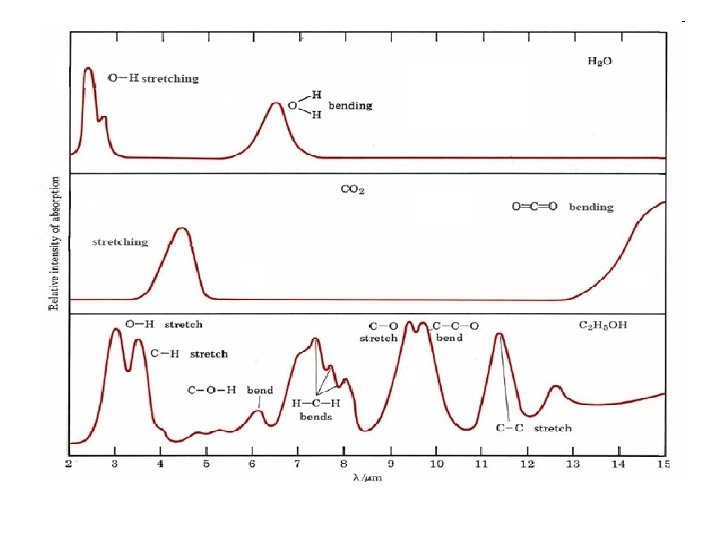
Approfondimenti • Uno spettro (e cioè la posizione delle bande e la loro intensità) è caratteristico di ogni sostanza molecolare e può praticamente costituire come un’impronta digitale della sostanza. • Se un materiale ignoto in esame ha lo stesso spettro di una sostanza precedentemente analizzata, deve sicuramente trattarsi dello stesso composto. • La determinazione può anche essere condotta in maniera quantitativa. • Nello spettro infrarosso ogni banda ha un’intensità caratteristica.
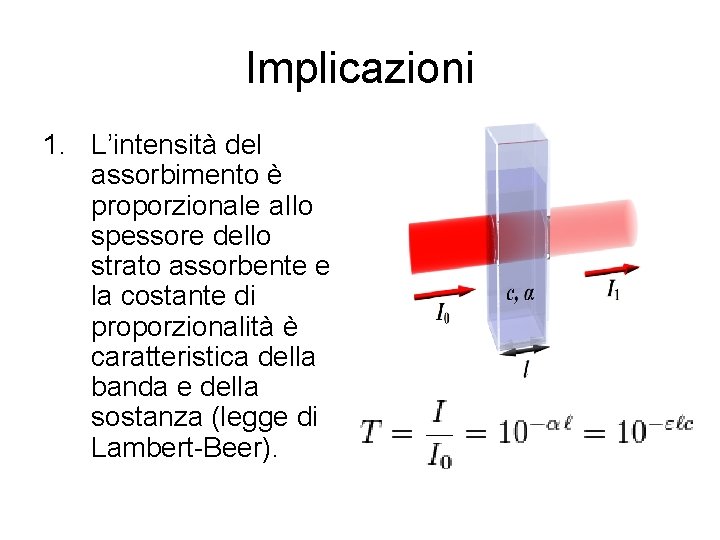
Implicazioni 1. L’intensità del assorbimento è proporzionale a. Ilo spessore dello strato assorbente e la costante di proporzionalità è caratteristica della banda e della sostanza (legge di Lambert-Beer).

Paragonare gli spettri 1. Se confrontiamo l’intensità delle bande in un campione contenente una quantità ignota di sostanza con l’intensità in un campione che ne contiene una quantità nota, possiamo risalire alla determinazione quantitativa nel campione in esame. 2. Questo metodo si presta quindi a essere usato per la determinazione qualitativa e quantitativa dei componenti di miscele di sostanze.

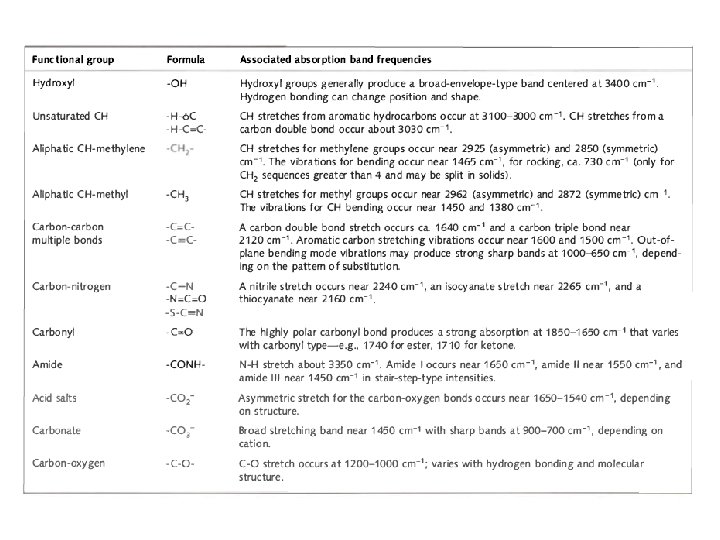
Come facciamo ad identifcare molecole? è stato constatato sperimentalmente che tutte le volte che in una molecola esiste un raggruppamento particolare di atomi si osserva un assorbimento infrarosso a una stessa frequenza e con la stessa intensità. Queste frequenze caratteristiche vengono dette frequenze di gruppo e la loro presenza o meno può essere presa come evidenza dell’esistenza o meno di quel gruppo nella molecola.

Lo spettro IR Si può suddividere in tre diverse zone: • zona dei gruppi funzionali, che si estende da 3800 a 1300 cm-1 e comprende bande dovute sia a stiramenti che a deformazioni di gruppi funzionali (per esempio legami N-H, O-H, C=C, C=O, N=O, ecc. ), con quest'ultimi compresi tra 1600 e 1300 cm-1; • zona delle impronte digitali, da 1300 a 650 cm-1 e che deve il suo nome alla presenza di bande strettamente caratteristiche di ciascuna singola molecola in quanto originate da vibrazioni corali dell'intero scheletro molecolare; • zona del lontano IR, che si estende da 650 a 200 cm-1 e presenta bande dovute a stiramenti di atomi pesanti, deformazioni di gruppi privi di idrogeno e vibrazioni di scheletro.
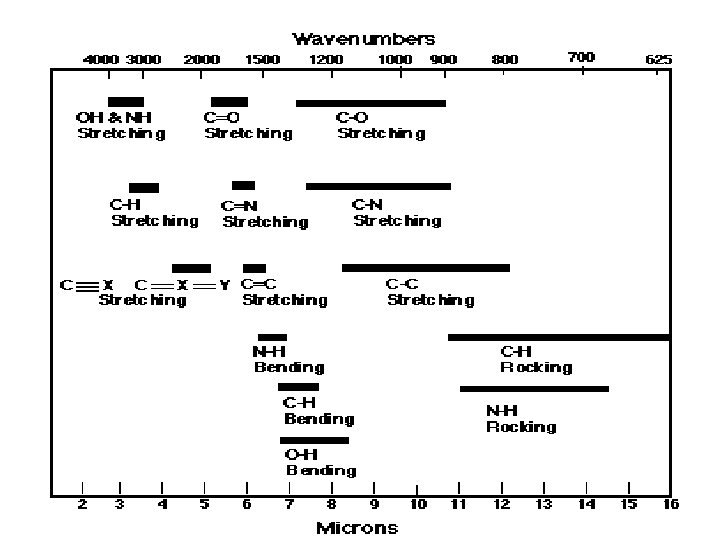

spiegazione La base teorica per l’esistenza di queste frequenze di gruppo è complessa ma comporta la localizzazione del movimento oscillatorio nel gruppo e la costanza delle costanti di forza associate con i vari legami chimici. Le costanti di forza in un legame tra due atomi dipendono dalla struttura elettronica della molecola (i legami) e, ad esempio, la costante di forza di stiramento di un certo legame misura la rigidità del legame.

Come si usa? Per un certo gruppo ci sono delle frequenze caratteristiche nello spettro che consentono di identificarne la presenza; però la frequenza caratteristica si sposterà leggermente a seconda della struttura elettronica del resto della molecola, e in base a questi piccoli spostamenti possiamo ottenere informazioni sulla struttura generale della molecola

Preparazione di un campione solida per analisi in trasmissione? • Schiaccia il campione per fare un film molto sottile – Questo puo essere effetuato se si mette un campione in una “cella di diamante” – Tra due facce di due diamanti che sono trasparente al IR • Implicazioni – Perdi una parte del integrità del campione – Se il campione si separa si può selezionare diverse zone del campione per analisi IR – Puoi usare il campione per altre analisi

Macinare il campione e disperdere il campione in una matrice di KBr • Si puo inoltre macinare il campione in una polvere pùu fine di 5 micrometri disperso in un sale che e’ trasparente nel IR • KBr e’ trasparente e utilizzato per tanti tipi di analisi IR • Dopo aver maccinato il campione, si deve pressare il campione in una pressa addatta ad oltre 1000 atmosfere di pressione

Altri metodi • Sciogliere o disperdere un campione in un solvente non attivo in IR • Depositare il campione su dischi di sale (KBr oppure Na. Cl) • Montare dischi in una porta campione • Mettere nell spettrometro

Lo strumento • • Sorgente: IR Campione: Varie geometrie Revelatore: Sensore CCD Presentazione: Elaborazione tramite computer • Interpretazione: complicato – normalmente tramite bancadati e paragoni visuali con campioni noti

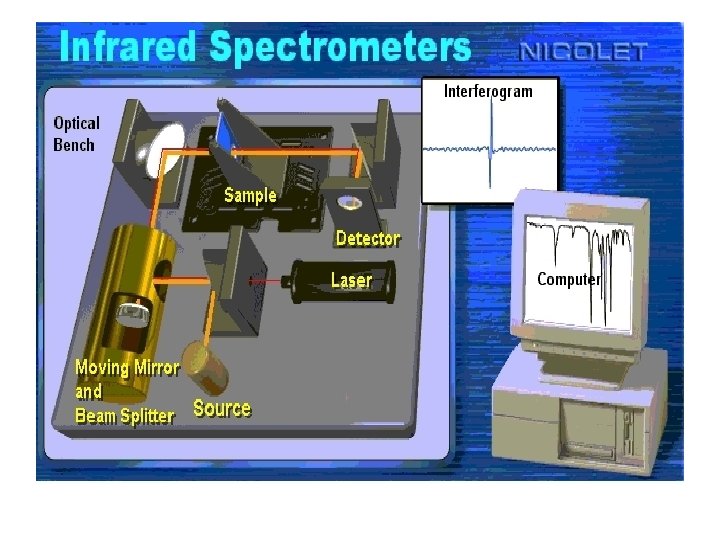


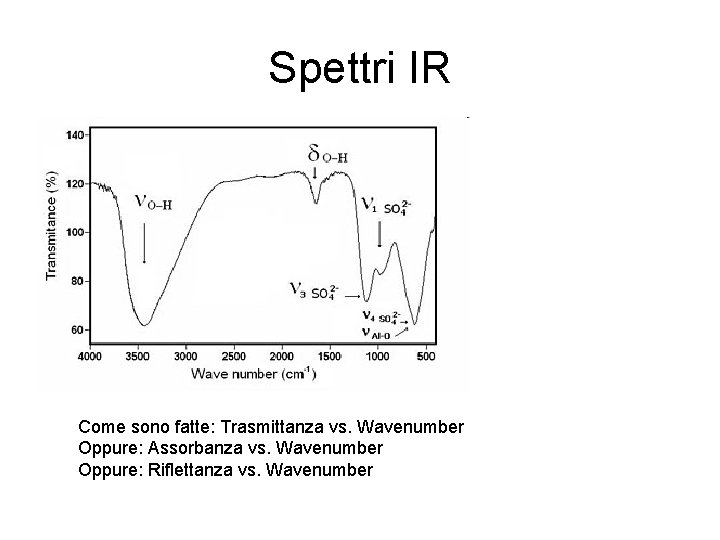
Spettri IR Come sono fatte: Trasmittanza vs. Wavenumber Oppure: Assorbanza vs. Wavenumber Oppure: Riflettanza vs. Wavenumber

Quali proprietà • Bande (non pichi) – Posizione-frequenza • Dipende dal tipo di legame molecolare – Forma • Riflette la purezza del campione e interferenze tra gruppi vicini – Intensità relativa • Numero di vibrazioni (concentrazione) • Cambiamenti di posizione, forma e intensità indica differenza in un campione – però delle volte puo’ essere legata alla preparazione oppure modo di acquisizione della misura e non al campione stesso

Come si interpreta? • Guardare lo spettro e meta data– noti range, tipo di spettro (trasmittanza, riflettanza), risoluzione – La risoluzione e’ normalmente 4 cm-1 – Informazioni importanti per l’interpretazione • Paragonare lo spettro con riferimenti • Identificare le bande e cercare di capire che gruppi rappresentono • Spiegare differenze
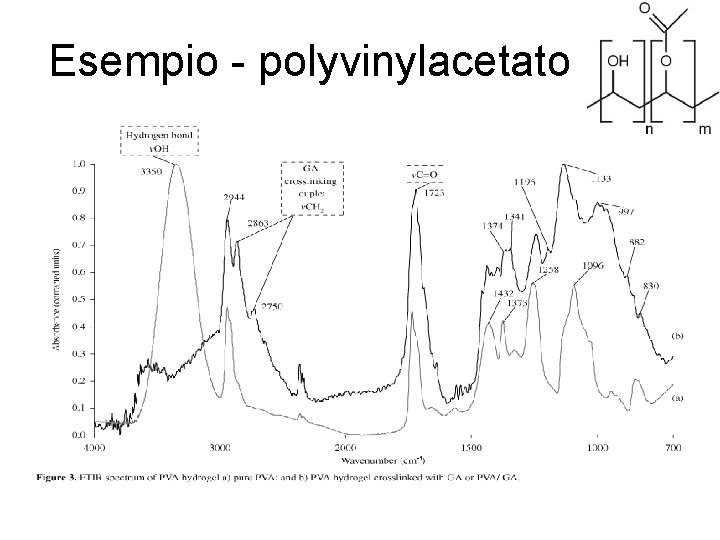
Esempio - polyvinylacetato

Utilizzo di (FTIR) spettri • • Acquisizione Buono spettro? Si riconosce? – paragonare con riferimento Se non e’ riconoscibile, cerca con scansione computer automatico tramite algoritmo • Cerca di identificare gruppi funzionali • Raramente si considera campioni puri – spettri sono sovrapposizione di segnali da diversi materiali – Grosso problema del FTIR – Analisi alternative spesso richieste
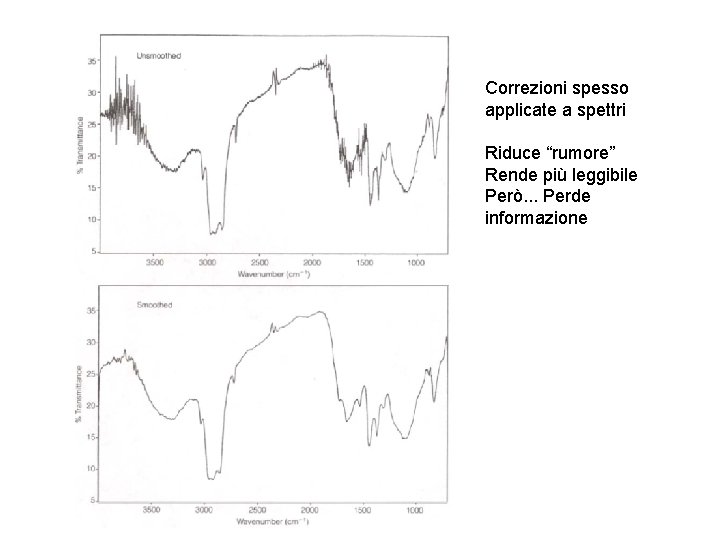
Correzioni spesso applicate a spettri Riduce “rumore” Rende più leggibile Però. . . Perde informazione
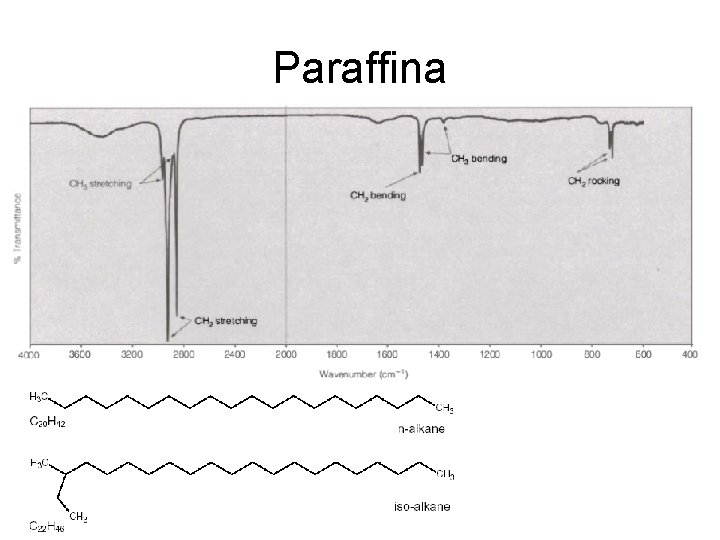
Paraffina
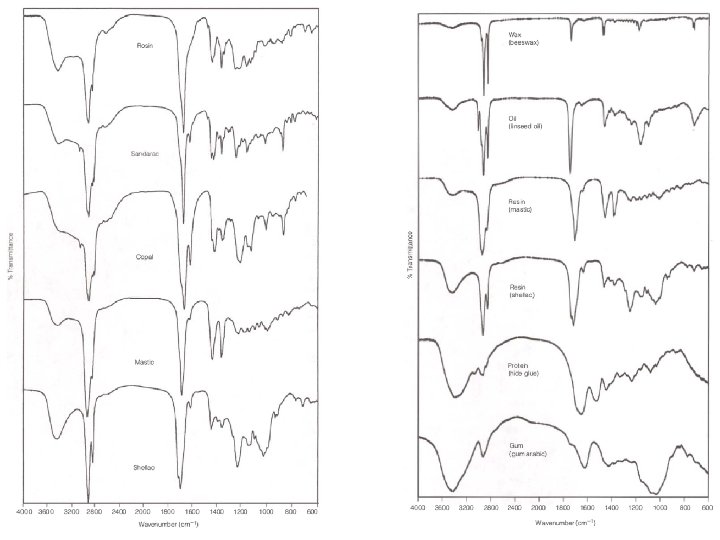
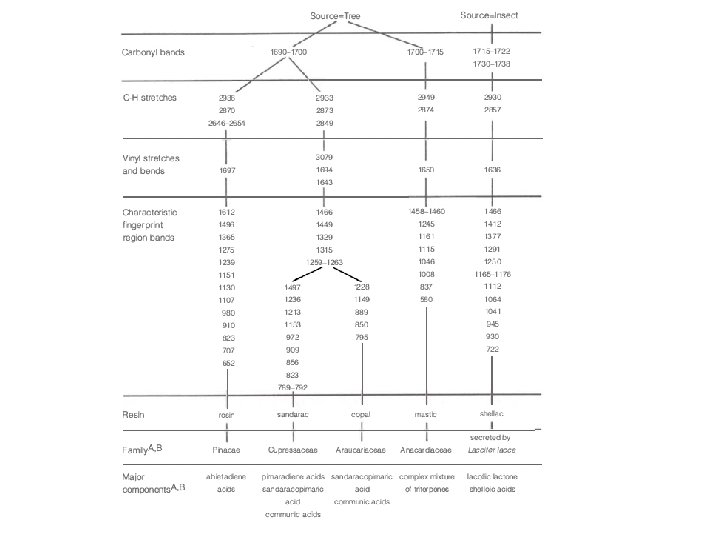
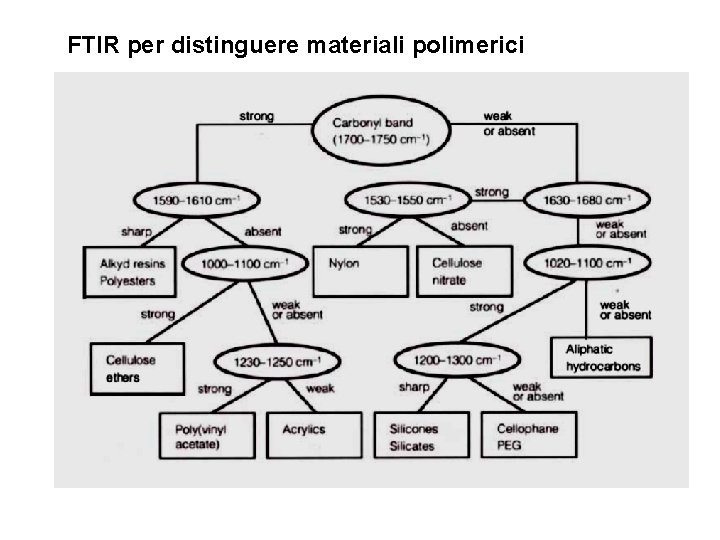
FTIR per distinguere materiali polimerici
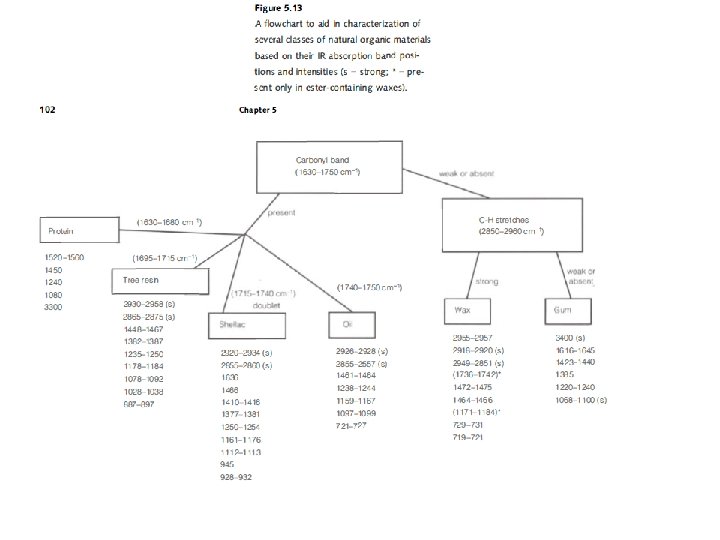

FTIR per Distinguere minerali Gesso, calcite, malachite, Barite, silicio, kaolina
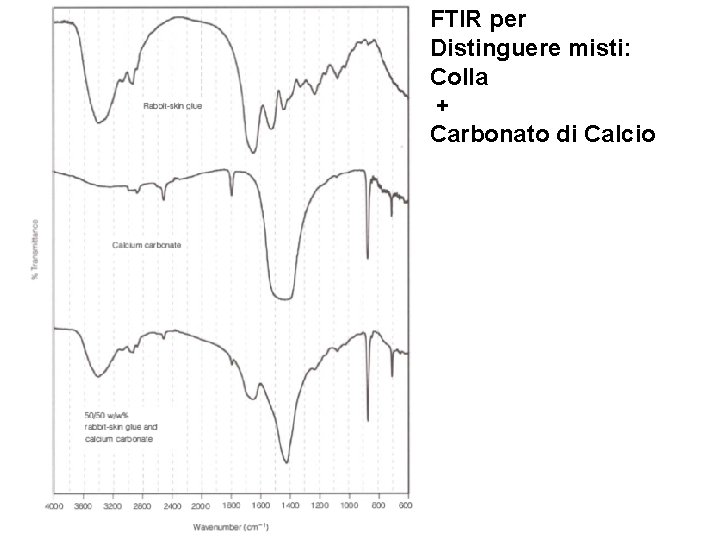
FTIR per Distinguere misti: Colla + Carbonato di Calcio
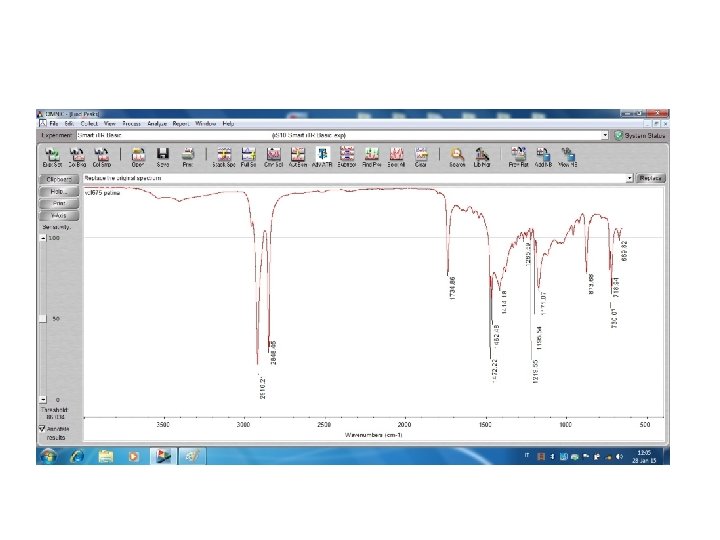
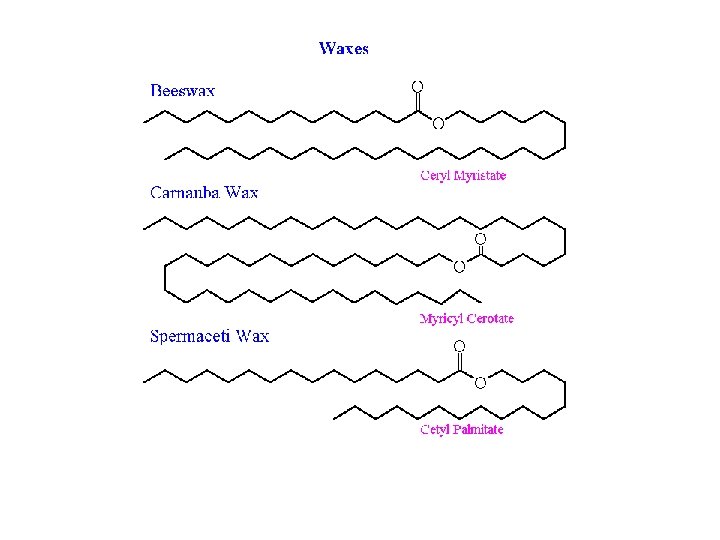
- Slides: 53