SPETTROSCOPIA di RISONANZA MAGNETICA del CARBONIO C13 NMR

SPETTROSCOPIA di RISONANZA MAGNETICA del CARBONIO: C-13 NMR

CARATTERISTICHE del 13 C NMR 12 C è non attivo all’ NMR I = 0 tuttavia…. 13 C ha I = 1/2 I segnali 13 C sono 6000 volte più deboli dell’ 1 H perchè: 1. L’abbondanza isotopica del 13 C è piccola 2. (1. 08%) 2. La costante giromagnetica del 13 C è ¼ di quella 3. del 1 H I 13 C assorbono in un range molto più elevato 0 - 200 ppm

SENSIBILITA’ v ABBONDANZA ISOTOPICA v g : la sensibilità dipende da g 3 poiché g compare in tre aspetti del fenomeno NMR § l’eccesso di popolazione nello stato a più bassa E § L’intensità dei momenti magnetici m= g. h. [I(I+1)]1/2 § La velocità di precessione e quindi il voltaggio prodotto v= g. B 0

CARATTERISTICHE 13 C NMR A causa della scarsa abbondanza isotopica (0. 0108) c’è una scarsa probabilità di trovare due atomi 13 C legati l’uno all’altro 13 C - 13 C coupling NO! IMPROBABILE I segnali osservati sono dovuti al contributo di molte molecole ciascuna delle quali contiene un solo 13 C. Tuttavia il 13 C dà accoppiamento con i protoni (I = 1/2) 13 C - 1 H coupling SI MOLTO COMUNE

ACCOPPIAMENTO CON I PROTONI
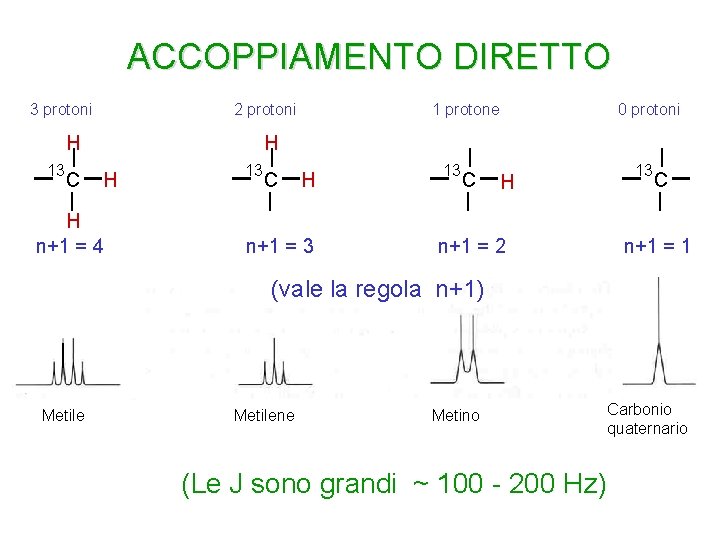
ACCOPPIAMENTO DIRETTO 3 protoni 2 protoni H 13 C H n+1 = 4 1 protone 0 protoni H H 13 C H n+1 = 3 13 C H n+1 = 2 13 C n+1 = 1 (vale la regola n+1) Metilene Metino (Le J sono grandi ~ 100 - 200 Hz) Carbonio quaternario
FENILACETATO di ETILE 13 C Accoppiato

SPETTRI DISACCOPPIATI
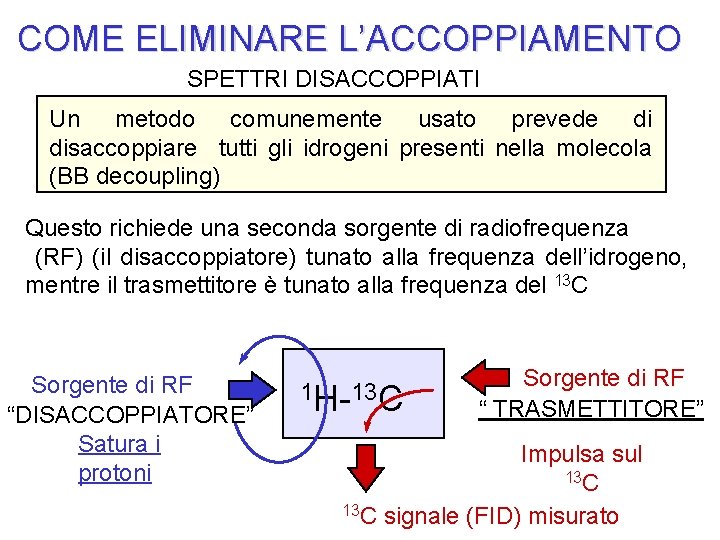
COME ELIMINARE L’ACCOPPIAMENTO SPETTRI DISACCOPPIATI Un metodo comunemente usato prevede di disaccoppiare tutti gli idrogeni presenti nella molecola (BB decoupling) Questo richiede una seconda sorgente di radiofrequenza (RF) (il disaccoppiatore) tunato alla frequenza dell’idrogeno, mentre il trasmettitore è tunato alla frequenza del 13 C Sorgente di RF “DISACCOPPIATORE” Satura i protoni 1 H-13 C Sorgente di RF “ TRASMETTITORE” Impulsa sul 13 C signale (FID) misurato

ETHYL PHENYLACETATE 13 C disaccoppiato dal protone
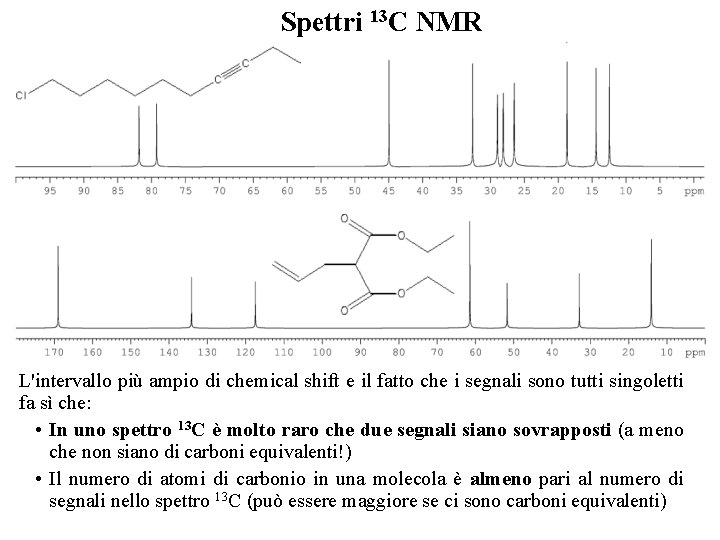
Spettri 13 C NMR L'intervallo più ampio di chemical shift e il fatto che i segnali sono tutti singoletti fa sì che: • In uno spettro 13 C è molto raro che due segnali siano sovrapposti (a meno che non siano di carboni equivalenti!) • Il numero di atomi di carbonio in una molecola è almeno pari al numero di segnali nello spettro 13 C (può essere maggiore se ci sono carboni equivalenti)

CHEMICAL SHIFTS dei NUCLEI 13 C

CARATTERISTICHE GENERALI Ø Il range di assorbimento è MOLTO più ampio (0 -230 ppm) Ø E’ molto improbabile trovare due carboni allo stesso c. s, per cui il numero di picchi osservati in uno spettro 13 C corrisponde al n° di C presenti nella molecola Ø I c. s influenzati soprattutto dalla elettronegatività dei sostituenti e dall’ibridizzazione Ø I sostuituenti legati direttamente (a), attraverso due atomi (b) e attraverso tre atomi (g) hanno effetti additivi sul c. s Ø L’intensità dei segnali non dipende rigorosamente dal numero di nuclei che li generano
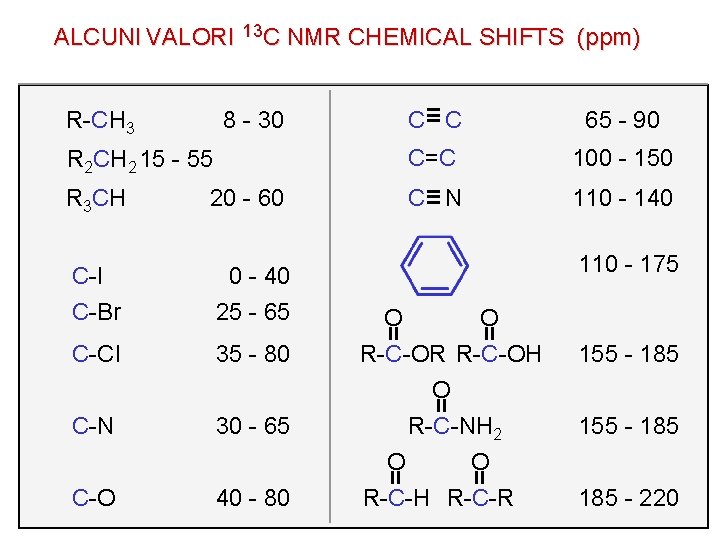
ALCUNI VALORI 13 C NMR CHEMICAL SHIFTS (ppm) R-CH 3 8 - 30 C C 65 - 90 R 2 CH 2 15 - 55 C=C 100 - 150 R 3 CH 20 - 60 C N 110 - 140 C-I C-Br 0 - 40 25 - 65 C-Cl 35 - 80 C-N 30 - 65 C-O 40 - 80 110 - 175 O O R-C-OR R-C-OH O R-C-NH 2 O O R-C-H R-C-R 155 - 185 185 - 220
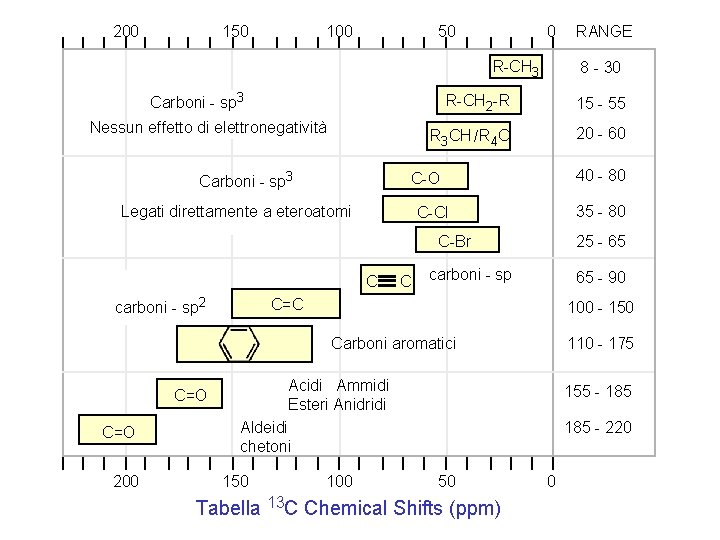
200 150 100 50 0 R-CH 3 Carboni - sp 3 Nessun effetto di elettronegatività Carboni - sp 3 8 - 30 R-CH 2 -R 15 - 55 R 3 CH / R 4 C 20 - 60 40 - 80 C-O Legati direttamente a eteroatomi 35 - 80 C-Cl C-Br C carboni - sp 2 C 25 - 65 carboni - sp 65 - 90 C=C 100 - 150 110 - 175 Carboni aromatici Acidi Ammidi Esteri Anidridi C=O 200 155 - 185 Aldeidi chetoni 150 RANGE 185 - 220 100 50 Tabella 13 C Chemical Shifts (ppm) 0
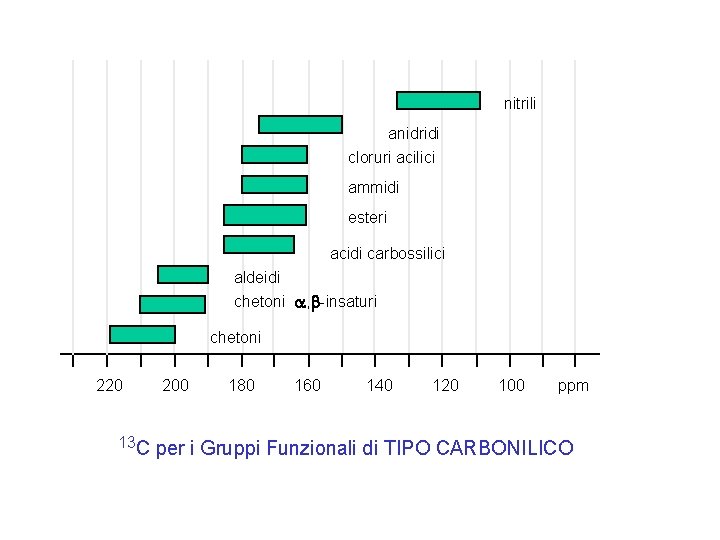
nitrili anidridi cloruri acilici ammidi esteri acidi carbossilici aldeidi chetoni a, b-insaturi chetoni 220 13 C 200 180 160 140 120 100 ppm per i Gruppi Funzionali di TIPO CARBONILICO
SPETTRI
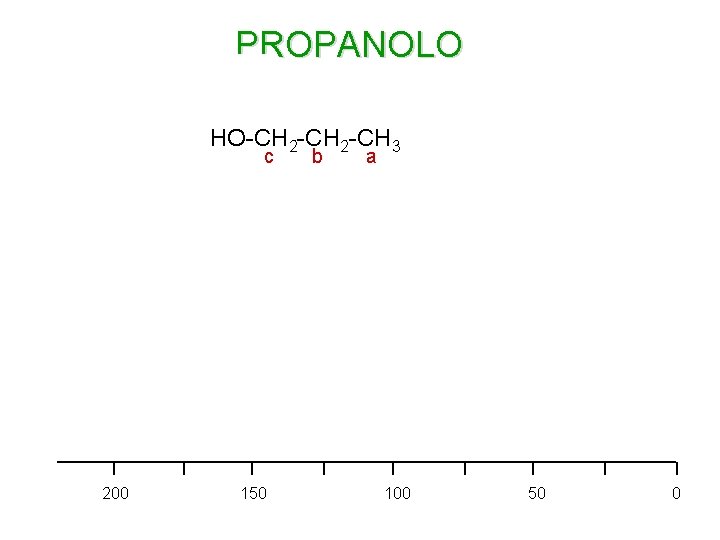
PROPANOLO HO-CH 2 -CH 3 c 200 150 b a 100 50 0

2, 2 -DIMETILBUTANO

BROMOCICLOESANO

CICLOESANOLO

TOLUENE

CICLOESENE

CICLOESANONE
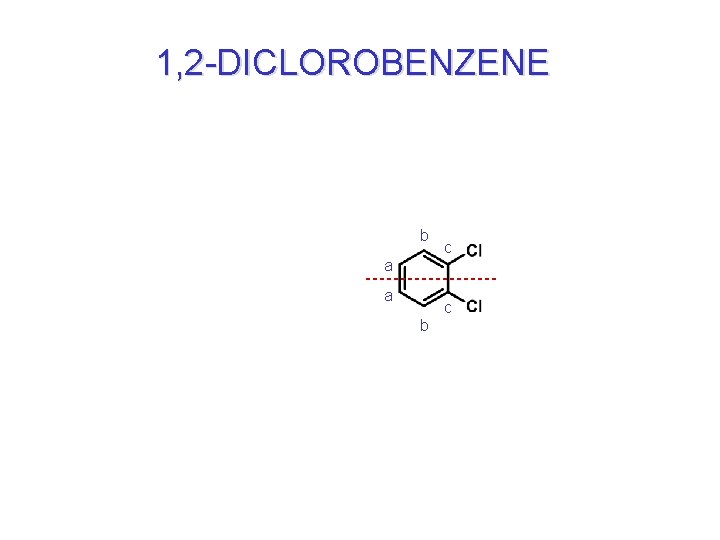
1, 2 -DICLOROBENZENE b c a a c b
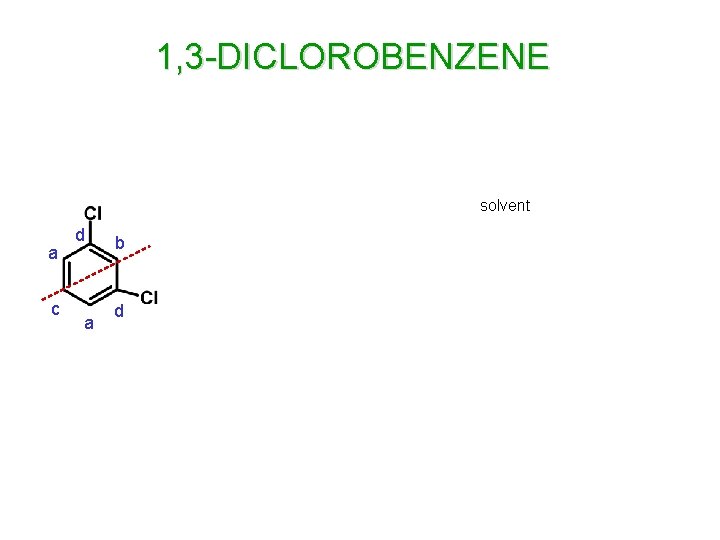
1, 3 -DICLOROBENZENE solvent a c d a b d

Esperimenti DEPT Dalla combinazione dei dati forniti da spettro 13 C disaccoppiato, DEPT 90 e DEPT 135 è possibile determinare con sicurezza se un carbonio è un CH 3, un CH 2, un CH o un C non protonato. Inoltre l’esperimento DEPT è addirittura più sensibile del normale spettro 13 C disaccoppiato.

Esperimenti DEPT Il disaccoppiamento a larga banda è molto utile, ma elimina una importante informazione: il numero dei protoni legati ad ogni carbonio. In sua assenza, infatti, e considerando solo le costanti grandi 1 JCH, i CH 3 sarebbero quartetti, i CH 2 sarebbero tripletti, i CH sarebbero doppietti, ed i C non protonati singoletti. Esiste un esperimento multiimpulso, detto DEPT, che permette di recuperare queste informazioni. In questi esperimenti i nuclei 13 C sono eccitati da una serie di impulsi sia a frequenza 13 C che 1 H, ed il risultato è che i CH 3, i CH 2, i CH ed i C non protonati sono eccitati in maniera diversa l’uno dall’altro. In particolare esistono due versioni di questo esperimento, che differiscono per la durata di uno degli impulsi e sono dette: DEPT 90: nello spettro appaiono esclusivamente i CH DEPT 135: Nello spettro appaiono i CH 3, ed i CH normalmente, mentre i CH 2 compaiono dalla parte opposta dello spettro (come se fossero segnali negativi; si dice che hanno fase opposta)
- Slides: 28