SPEKTROMETRIA MASOWA MS J J Thompson 1911 r










- Slides: 17

SPEKTROMETRIA MASOWA ( MS ) (J. J. Thompson – 1911 r. ) To komplementarna w stosunku do NMR i IR metoda analizy związków organicznych.

Spektrometria masowa pozwala określić: a). skład pierwiastkowy związku b). skład izotopowy analizowanych substancji c). masę cząsteczkową i wzór sumaryczny związku d). strukturę związku na podstawie identyfikacji jonów na jaki rozpadł się związek w czasie procesu fragmentacji MS pozwala identyfikować związki chemiczne i ich mieszaniny.

Metoda ta stosowana jest w chemii organicznej, chemii analitycznej, biochemii, farmacji, diagnostyce medycznej. Pozwala badać próbki nawet rzędu mikrogramów. Aparatem do otrzymywania widm masowych jest spektrometr masowy.

Widmo jest zbiorem pików przedstawiających zależność jonowego od stosunku m / z. prądu (m – masa jonu, z – ładunek jonu) pp Widmo zawiera informacje na jakie fragmenty rozpadł się związek w czasie fragmentacji i jaka jest względna wydajność dla poszczególnych fragmentów.

SPOSÓB OTRZYMYWANIA WIDMA a). badany związek doprowadza się do jonizacji i rozpadu na jony (fragmenty) b). naładowane fragmenty przyśpiesza się w polu elektrycznym c). strumień jonów rozdziela się wg. stosunku ich masy do ładunku d). mierzy się natężenie prądu jonowego odpowiadającego poszczególnym jonom

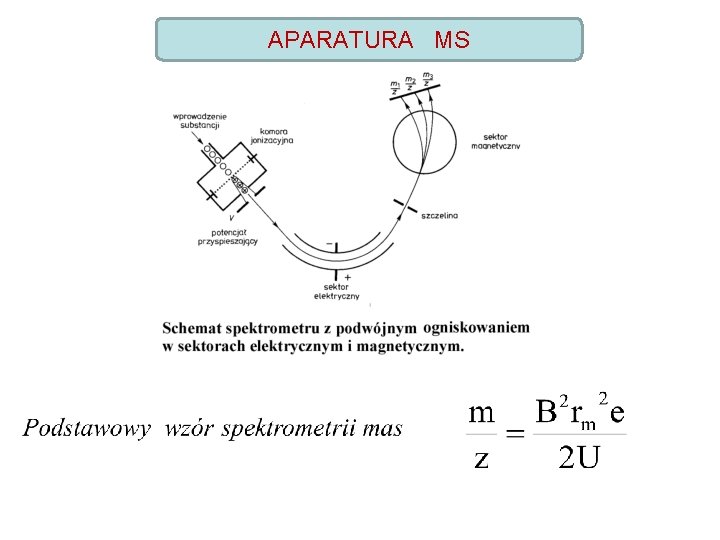
APARATURA MS

APARATURA składa się z: a). układu wprowadzania próbki b). komory jonizacyjnej i układu przyśpieszania jonów ( próbka musi być przeprowadzona w stan pary, prężność par nie może być mniejsza niż 10 -7 Tr ), to jest ograniczeniem tej metody ) c). analizatora – najpierw analizator elektrostatyczny, później magnetyczny, to tzw. Układ Niera – Johnsona (dwusektorowy) d). detektora

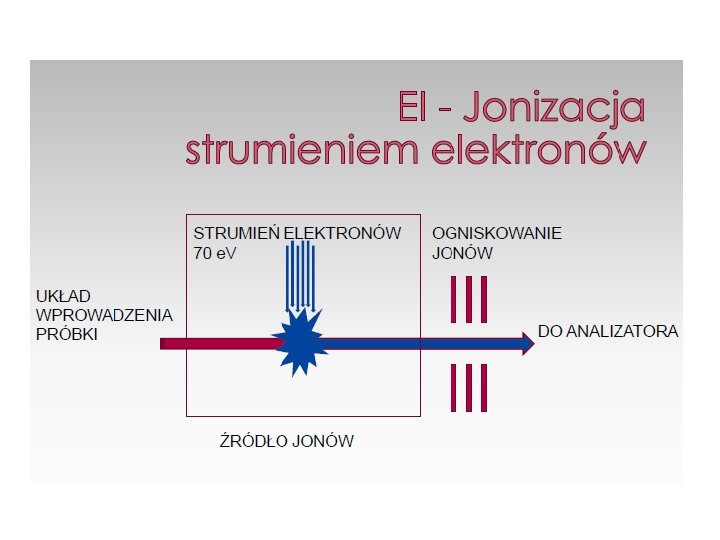
METODY JONIZACJI: a). metoda EI ( Electron Impact Ionization ) – tu jonizacja za pomocą elektronów o energii 10 - 70 e. V. ← to tzw. rodniko - kation ( jon molekularny) Ma odpowiednio dużą energię i rozpada się na jony – to tzw. fragmentacja związku.


b). metoda FAB ( Fast Atom Bombardment ) – tu jonizacja następuje przez bombardowanie dodatnimi jonami argonu i ksenonu. Stosuje się do badania substancji trudno lotnych np. peptydów rozpuszczonych w cieczach o dużej lepkości. c). Plazma wzbudzona indukcyjnie (ICP) – jonizowana substancja jest wprowadzana do plazmy płomienia palnika znajdującego się w kwarcowej rurce. Rurka otoczona jest cewką, w której płynie prąd zmienny o wysokiej częstotliwości. Plazma ogrzewa się do temperatury ok. 10 000 K ( wzbudzenie zmiennym polem magnetycznym wytworzonym przez prąd płynący w cewce). Metodę nadaje stosuje się do analizy pierwiastków metalicznych.

Podstawowe reguły procesu fragmentacji: Podstawowe • w czasie fragmentacji łańcucha węglowodorowego faworyzowane jest rozrywanie wiązań C-C • najłatwiej następuje rozrywanie wiązań C-C w miejscach rozgałęzienia łańcucha • łatwo rozerwaniu ulegają wiązania C-C odległe o dwa wiązania od wiązania podwójnego • w pochodnych węglowodorów elektron jest odrywany zwykle od heteroatomu co sprzyja rozrywaniu sąsiadującego z nim wiązania

RODZAJE PIKÓW W MS a). pik molekularny – odpowiada jonowi molekularnemu b). pik główny – najsilniejszy pik w widmie c). piki izotopowe – odpowiadają izotopom

OKREŚLANIE MASY MOLOWEJ ZWIĄZKU Polega na ustaleniu w widmie piku molekularnego M+·. Z reguły jest to pik o największej wartości m / z, jeżeli nie brać pod uwagę pików izotopowych. Uwaga: – w widmie może nie być piku molekularnego jeżeli fragmentacja prowadzona jest zbyt intensywnie, dlatego w metodzie EI robi się drugi pomiar przy mniejszej energii elektronów np. 15 e. V

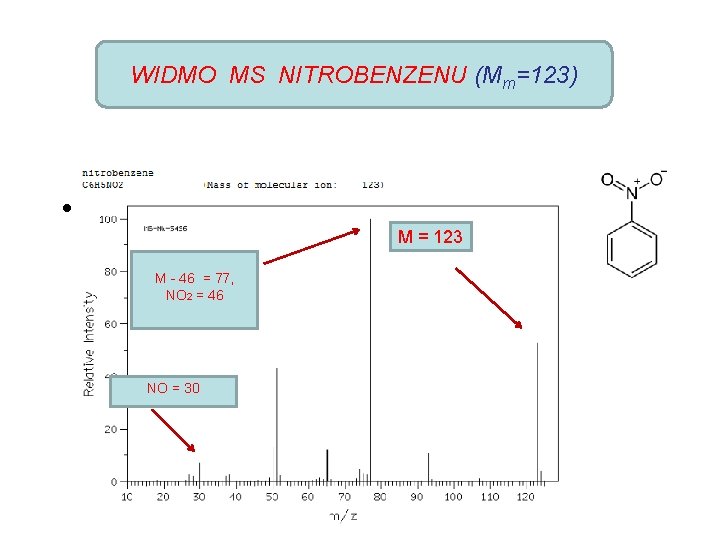
WIDMO MS NITROBENZENU (Mm=123) • M = 123 M - 46 = 77, NO 2 = 46 NO = 30

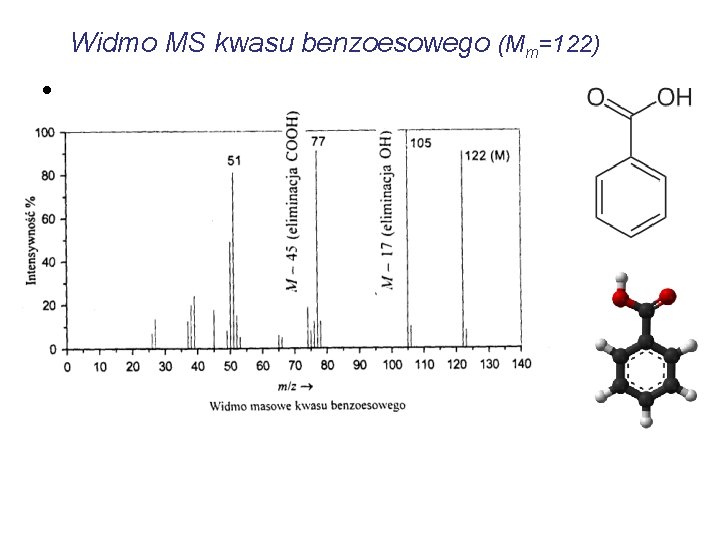
Widmo MS kwasu benzoesowego (Mm=122) •

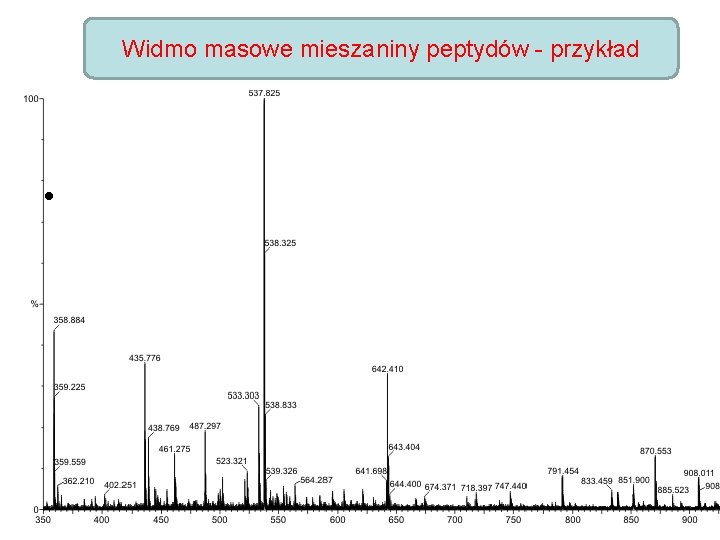
Widmo masowe mieszaniny peptydów - przykład •

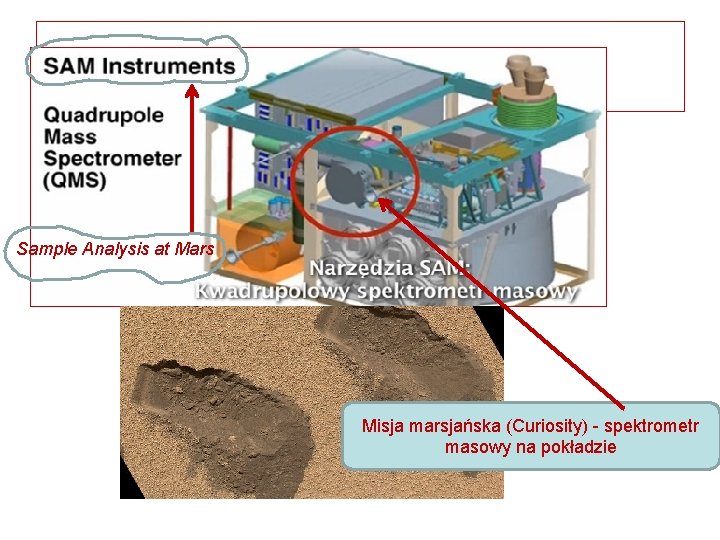
• Sample Analysis at Mars Misja marsjańska (Curiosity) - spektrometr masowy na pokładzie